Strukturelle Charakterisierung und dielektrische Eigenschaften von kugel- und stäbchenförmigen PbTiO3-Pulvern, die durch Synthese von geschmolzenem Salz synthetisiert wurden
Zusammenfassung
Durch Reaktion von PbC2 O4 und TiO2 in den eutektischen NaCl-KCl-Salzen sowohl kugel- als auch stäbchenförmiges PbTiO3 (PTO)-Pulver wurden mittels Schmelzsalzsynthese (MSS) bzw. Templat-MSS-Verfahren synthetisiert. Röntgenbeugungsmuster zeigen, dass alle PTO-Pulver in einer tetragonalen Phasenstruktur kristallisieren. Erhöhung des Molverhältnisses von PbC2 O4 :TiO2 :NaCl:KCl von 1:1:10:10 bis 1:1:60:60 im MSS-Verfahren hat wenig Einfluss auf die kugelförmige Morphologie der PTO-Pulver, die 5 Stunden lang bei 950 °C synthetisiert wurden. Polykristalline stäbchenförmige PTO-Pulver in großem Maßstab mit Durchmessern von 480 nm bis 1,50 µm und Längen bis zu 10 µm wurden bei 800 ° C für 5 h durch die MSS-Templatmethode synthetisiert, wobei der stäbchenförmige Anatas TiO2 Vorstufen wurden als Template verwendet und das Molverhältnis von PbC2 O4 :TiO2 :NaCl:KCl war gleich 1:1:60:60. Röntgenenergiedispersive Spektroskopie-Spektren zeigen, dass alle PTO-Pulver aus Pb-, Ti- und O-Elementen bestehen und die gemessenen Pb:Ti-Atomverhältnisse nahe 1:1 liegen. Beim Templat-MSS-Verfahren spielt der Gehalt an geschmolzenem Salz eine wichtige Rolle bei der Bildung der stabförmigen PTO-Pulver. Bei einem niedrigen Gehalt an geschmolzenem Salz können die stabförmigen PTO-Pulver nicht synthetisiert werden, selbst wenn das stabförmige TiO2 Vorlagen verwendet werden. Darüber hinaus unterdrückte eine Verlängerung der Reaktionszeit die Bildung von stäbchenförmigen PTO-Pulvern, förderte jedoch die Bildung von kugelförmigen PTO-Nanopartikeln. Die dielektrischen Eigenschaften der kugel- und stabförmigen PTO-Pulver wurden vergleichend untersucht. Bei Raumtemperatur die Dielektrizitätskonstante und der dielektrische Verlust der kugelförmigen PTO-Pulver, die durch das MSS-Verfahren mit dem Molverhältnis von PbC2 . synthetisiert wurden O4 :TiO2 :NaCl:KCl gleich 1:1:30:30 waren ~ 340 und 0,06 (gemessen bei 10 6 Hz) bzw. Die entsprechenden Werte für die stäbchenförmigen PTO-Pulver, synthetisiert durch die Templat-MSS-Methode mit dem Molverhältnis von PbC2 O4 :TiO2 :NaCl:KCl gleich 1:1:60:60 waren 140 bzw. 0,08. Die vorliegenden Ergebnisse zeigen, dass die kugelförmigen PTO-Pulver bessere dielektrische Eigenschaften haben, die vielversprechende Anwendungen in den Bereichen Mehrschichtkondensatoren und Resonatoren haben.
Einführung
Perowskitoxide mit der allgemeinen Formel ABO3 sind eine der wichtigsten Materialklassen in der Festkörperchemie, die in den Bereichen Ferroelektrizität, Magnetismus, Optoelektronik und Energieumwandlung weit verbreitet sind [1,2,3]. Unter allen Mitgliedern der Familie der Perowskitoxide ist PbTiO3 (PTO) hat die höchste tetragonale Verzerrung (c /a ~ 1.064), was es gegenüber anderen bemerkenswert macht. Diese große tetragonale Verzerrung entspricht der höchsten spontanen Polarisation unter allen ferroelektrischen Perowskitoxiden. Als Paradigma der ferroelektrischen Perowskit-Oxide besitzt PTO ausgezeichnete dielektrische, piezoelektrische und pyroelektrische Eigenschaften [4, 5]. Jedoch sind reine PTO-Keramiken aufgrund von Problemen wie der Fehlanpassung der Wärmeausdehnung, der mechanischen Streckkraft und Mikrorissen in der PTO-Keramik schwierig als hochdichte und monolithische Keramik herzustellen. In den letzten zehn Jahren wurde der Synthese von PTO-Pulvern auf verschiedenen Wegen wie Festkörperreaktion [6], Sol-Gel-Prozess [7, 8], Hydrothermalmethode [9, 10], die Pechini-Methode [11], Co-Präzipitation [12] und so weiter. Bei all diesen Verfahren ist jedoch eine Kalzinierung bei mehr oder weniger hoher Temperatur erforderlich, um reines kristallisiertes ferroelektrisches PTO zu erhalten. Leider erzeugt die Hochtemperatur-Kalzinierung normalerweise agglomerierte Pulver mit einer groben Teilchengröße, die einen zusätzlichen Mahlprozess erfordert. Verunreinigungen und andere unerwünschte Merkmale während des Fräsprozesses können zu Fehlern in den hergestellten Produkten führen und die elektrischen Eigenschaften der Zapfwellenkeramik beeinträchtigen.
Die Methode der Salzschmelzensynthese (MSS) ist ein effektiver Weg zur Herstellung elektronischer Keramikpulver aus Perowskitoxid, bei der geschmolzenes Salz als Medium zur Synthese reiner Perowskitoxide aus ihren Bestandteilen (Oxide und Carbonate) bei relativ niedriger Temperatur und in kürzerer Zeit verwendet wird Reaktionszeit im Vergleich zu herkömmlichen Festkörperreaktionen [13]. Kürzlich werden Perowskit-PTO-Pulver durch Schmelzflussreaktion unter Verwendung von NaCl und NaCl-KCl als Reaktionsmedien synthetisiert [14,15,16]. Die Bildung von kugelförmigen PTO-Pulvern wurde durch das Diffundieren des gelösten PbO auf das TiO2 . erreicht Oberfläche in den geschmolzenen Salzen und in-situ-Reaktion, um PTO-Nanopartikel zu bilden, und dann der Keimbildung und dem Wachstum von PTO-Nanopartikeln folgen. Im Vergleich zu den PTO-Pulvern ist die Synthese von PTO 1D-Nanomaterialien (z. B. Nanostäbe, Nanodrähte und Nanoröhren) durch die MSS-Methode weit zurückgeblieben. Der Hauptgrund liegt in den Herausforderungen bei der Synthese hochwertiger PTO 1D-Nanomaterialien, da die hohe Symmetrie der Perowskitstruktur leicht dazu führen kann, dass PTO zu einem kubischen Block wächst. Bisher sind in der Literatur nur wenige Arbeiten zur Synthese von PTO 1D-Nanomaterialien mittels MSS-Methode verfügbar. Deng et al. [17] synthetisierten PTO-Nanostäbe mit Durchmessern von 50–80 nm und Längen von wenigen Mikrometern bei 700 °C unter Verwendung eines Tensids (Polyoxyethylen (9) Nonylphenylether, NP-9)-unterstützter Ansatz in einem NaCl-Schmelzsalzmedium. Das Wachstum der PTO-Nanostäbchen wurde der Dispersion feiner PTO-Nanopartikel und deren erneuter Ablagerung auf größeren Partikeln zugeschrieben, was unter der Kombinationswirkung von NP-9-Tensid und NaCl-Fluss zur Bildung von Nanostäbchen in axialer Richtung führte. Cai et al. [15] berichteten über die Synthese von einkristallinen PTO-Nanostäbchen mit Durchmessern von 0.1–1.0 μm und Längen bis zu einigen Mikrometern nach der Templat-MSS-Methode, wobei NP-9 als Tensid und das stäbchenförmige TiO2 Vorläufer wurden als Template für Titanquellen verwendet. Die Größe und Morphologie des stäbchenförmigen TiO2 Matrizen wurden in den synthetisierten PTO-Partikeln zurückgehalten. In ähnlicher Weise wurden nadelartige PTO-Pulver auch über die Schablonen-MSS-Methode synthetisiert, bei der reines nadelartiges TiO2 Als Template wurden Partikel verwendet [18]. Die nadelförmigen PTO-Partikel, die durch die Schablonen-MSS-Methode bei 800 °C synthetisiert wurden, hatten eine Länge von 30–100 µm und einen Durchmesser von 500 nm–2,0 µm.
Trotz der obigen Berichte über die Synthese von PTO-Nanomaterialien durch die MSS-Methode und die Templat-MSS-Methode gibt es kaum Daten über die dielektrischen Eigenschaften der PTO-Pulver. Darüber hinaus ist der Bildungsmechanismus von PTO-Nanostäbchen durch die Templat-MSS-Methode nicht gut verstanden. In dieser Arbeit berichten wir über die Synthese von kugel- und stäbchenförmigen PTO-Pulvern mittels (Templat-)MSS-Methoden durch Reaktion von PbC2 O4 und TiO2 in den eutektischen NaCl-KCl-Salzen ohne Verwendung des Tensids NP-9. Der Einfluss der Verarbeitungsparameter des Templat-MSS-Verfahrens wie Reaktionszeit und Schmelzsalzgehalt auf die Bildung von stabförmigen PTO-Pulvern wurde detailliert untersucht. Die Ergebnisse zeigen, dass der Gehalt an geschmolzenem Salz eine entscheidende Rolle bei der Bildung des stabförmigen ABO3 . spielt Verbindungen mit kubischer oder pseudokubischer Kristallstruktur im Templat-MSS-Prozess. Bei niedrigem Gehalt an geschmolzenem Salz können die PTO-Nanostäbe nicht synthetisiert werden, obwohl das stabförmige TiO2 Vorlagen werden im Vorlagen-MSS-Prozess verwendet. Die dielektrischen Eigenschaften von kugel- und stabförmigen PTO-Pulvern, die durch das MSS-Verfahren und das Schablonen-MSS-Verfahren synthetisiert wurden, wurden ebenfalls vergleichend untersucht, und die Ergebnisse zeigten, dass die kugelförmigen PTO-Pulver bessere dielektrische Eigenschaften aufwiesen.
Methoden
Materialien
Reagenzien in analytischer Qualität von PbC2 O4 und TiO2 (mit kugelförmiger Morphologie und Mischphasenstruktur von Anatas und Rutil) wurden von Sigma-Aldrich (Shanghai) Trading Co., Ltd. bezogen. Reagenzien von NaCl- und KCl-Salzen in analytischer Qualität, K2 CO3 , AgNO3, und HCl-Lösungen wurden von Shanghai Chemical Reagent Co., Ltd. bezogen
Synthese von kugelförmigen Zapfwellenpulvern nach der MSS-Methode
Kugelförmige PTO-Pulver wurden über die MSS-Methode durch Reaktion von PbC2 . synthetisiert O4 und TiO2 in den eutektischen NaCl-KCl-Salzen. Die Molverhältnisse von PbC2 O4 :TiO2 :NaCl:KCl wurden als 1:1:10:10, 1:1:20:20, 1:1:30:30, 1:1:40:40 und 1:1:60:60 ausgewählt. Die Mischungen von PbC2 O4 , TiO2 , NaCl und KCl wurden 30 min in Mörser und Pistill gemahlen und dann 5 h in den Aluminiumoxidtiegeln auf 950 °C erhitzt. Schließlich wurden die Produkte im Ofen auf natürliche Weise auf Raumtemperatur abgekühlt und mehrmals mit entionisiertem Wasser gewaschen, bis keine freien Chloridionen von AgNO3 . nachgewiesen wurden Lösung, um eine vollständige Entfernung der Salze zu gewährleisten. Nach dem Waschen wurden die Produkte zur strukturellen Charakterisierung 4 Stunden lang bei 120°C getrocknet.
Synthese von stabförmigen Zapfwellenpulvern nach der Schablonen-MSS-Methode
Stäbchenförmige PTO-Pulver wurden über die Schablonen-MSS-Methode synthetisiert, bei der der stäbchenförmige Anatas TiO2 Als Titanquelle wurden Partikel verwendet. Das stabförmige TiO2 Schablonen wurden aus dem stabförmigen K2 . hergestellt Ti4 O9 , nach einem zuvor von Hayashi et al. [19]. Zuerst K2 CO3 Oxid wurde mit TiO2 . gemischt Oxid mit einem Molverhältnis von 1:3, und dann wurde die Mischung auf 1000 °C erhitzt und für 18 Stunden gehalten. Schließlich wurde das Produkt im Ofen auf natürliche Weise auf Raumtemperatur abgekühlt und mehrmals mit entionisiertem Wasser gewaschen, um restliches K2 . zu entfernen CO3 . Das erhaltene Hauptprodukt von K2 Ti4 O9 wurde in 70°C HCl-Lösung (Konzentration 1 M) 2 h lang gewaschen, um K2 . zu extrahieren O, und die resultierende Phase war TiO2 ·nH2 O, das 1 h bei 600°C, 700°C bzw. 800°C getempert wurde, um das stabförmige TiO2 . zu erhalten Verbindungen. Und dann PbC2 O4 wurde mit stäbchenförmigem TiO2 . vermischt Template und NaCl-KCl-Schmelzsalz mit Molverhältnissen von PbC2 O4 :TiO2 (Vorlagen):NaCl:KCl gleich 1:1:20:20 bzw. 1:1:60:60. Die beiden Mischungen wurden bei 800 °C für unterschiedliche Stunden getempert (z. B. 1 h, 5 h und 10 h). Die Endprodukte wurden in ähnlichen Schritten wie oben gewaschen und getrocknet.
Mikrostrukturelle Charakterisierung
Die Phasenstrukturen der hergestellten PTO-Pulver wurden durch Röntgenpulverbeugung (Rigaku D/Max-RA, Cu Kα-Strahlung) charakterisiert. Eine Schrittweite betrug 0,01° pro Sekunde, und der Bereich von 2θ betrug 15–70°. Die Oberflächenmorphologien der PTO-Produkte wurden mit Rasterelektronenmikroskopie (REM, Hitachi S-3400 N II, 30 kV) ausgestattet mit einer energiedispersiven Röntgenspektroskopie (EDS) (EX-250-Spektroskopie, HORIBA Corporation) auf Element . untersucht Erkennung. Die REM-Proben wurden durch Aufsprühen von Pulver auf Kohleband hergestellt und anschließend bei Bedarf mit Gold beschichtet.
Dielektrische Messungen
Für die Messungen der dielektrischen Eigenschaften wurden die getrockneten kugel- und stabförmigen PTO-Pulver zu Pellets von 12 mm Durchmesser und 1,0 mm Dicke unter einem Druck von 7 MPa gepresst, die bei 1150 °C für 2 h in Luft geglüht wurden. Anschließend wurden die Oberflächen der geglühten Pellets geschliffen und poliert, gefolgt von einem Auftragen von Silberpaste auf beide Oberflächen. Die Silberpasten wurden dann 60 Minuten bei 550 °C gebrannt. Die Dielektrizitätskonstanten und Dielektrizitätsverluste der getemperten PTO-Pulver wurden bei Raumtemperatur von 10 Hz bis 1 MHz unter Verwendung eines Agilent 4192 A Impedanzanalysators gemessen.
Ergebnisse und Diskussion
Phasenstruktur und Morphologie von PTO-Pulvern, synthetisiert nach der MSS-Methode
XRD-Muster der PTO-Pulver, die durch die MSS-Methode bei 950 °C für 5 Stunden unter verschiedenen Gehalten an geschmolzenem Salz synthetisiert wurden, sind in Abb. 1 gezeigt. 06–0452, P 4mm Raumgruppe, Gitterkonstante a = 0.390 nm und c = 0,415 nm) und es werden keine anderen Störstellenphasen detektiert. Normalerweise ist das XRD-Muster im Bereich von 2θ = 45° charakteristisch für das Vorliegen einer entweder kubischen oder tetragonalen Perowskitstruktur. In diesem Fall ist die Aufspaltung von kubischen (200) in tetragonale (200) und (002) Reflexe bei etwa 2θ = 45 ° wird deutlich beobachtet, was die Bildung einer reinen tetragonalen ferroelektrischen Phase anzeigt. Die Gitterparameter (a und c ) der tetragonalen PTO-Pulver kann durch die folgende Gleichung berechnet werden:
$$ \frac{1}{d^2}=\frac{h^2+{k}^2}{a^2}+\frac{l^2}{c^2} $$ (1)wo d ist der Interplanarabstand zwischen den benachbarten (hkl ) Flugzeuge und a und c sind die Gitterparameter in der tetragonalen Phasenstruktur. Die Gitterparameter a der aus XRD-Mustern berechneten PTO-Pulver lagen im Bereich von 0,3905–0,3911 nm und c im Bereich von 0,4077–0,4089 nm. Details sind in Tabelle 1 aufgeführt. Die c /a Verhältnis lag im Bereich von 1,043 bis 1,047 mit einem Durchschnittswert von 1,045, kleiner als 1,064 für PTO-Einkristall. Aus den in Fig. 1 gezeigten XRD-Mustern ist ersichtlich, dass die Phasenstruktur der PTO-Pulver nicht durch den Gehalt an geschmolzenem Salz beeinflusst wird. Alle PTO-Pulver kristallisierten in einer tetragonalen Phasenstruktur mit einer Raumgruppe von P 4mm . Kürzlich haben die theoretischen Studien zur strukturellen Evolution von Perowskit-PTO von einem 0D-Cluster zu einem 3D-Kristall durch die Struktursuchmethode CALYPSO (Crystal Structure AnaLYsis by Particle Swarm Optimization) in Verbindung mit Dichtefunktionaltheorie-Rechnungen gezeigt, dass die Grundzustandsstruktur von PTO bei Umgebungsdruck ist der P 4mm Phase und die quasiplanare Struktur des PTO-Clusters und der 2D-PTO-Doppelschicht sind auch bei Umgebungsdruck stabil [20]. Die REM-EDS-Untersuchungen der PTO-Pulver sind in Abb. 2 dargestellt. Die in Abb. 2a–e gezeigten REM-Aufnahmen zeigen, dass die PTO-Pulver hauptsächlich aus vielen kugelförmigen Nanopartikeln mit Ausnahme einiger stäbchenförmiger Partikel bestehen. Mit zunehmendem Molverhältnis von PbC2 O4 :TiO2 :NaCl:KCl von 1:1:10:10 bis 1:1:60:60 veränderte sich die Morphologie der PTO-Pulver offensichtlich nicht, wie in Abb. 2a–e gezeigt. Das heißt, unterschiedliche Mengen der gleichen Salzschmelzen wirken nur als Reaktionsmedium, sie beeinflussen lediglich die Diffusionsgeschwindigkeit der Reaktionsionen. Die eutektischen NaCl-KCl-geschmolzenen Salze (eutektischer Schmelzpunkt 650 °C) stellen eine Flüssigphasen-Reaktionsumgebung mit relativ niedriger Temperatur bereit, die den Transport der reaktanten Ionen während des MSS-Prozesses unterstützt. Es wird berichtet, dass die Löslichkeit der Reaktanten in der Salzschmelze eine wichtige Rolle im MSS-Prozess spielt, was die Reaktionsgeschwindigkeit und die Morphologie der synthetisierten Produkte entscheidend beeinflusst [13]. In der vorliegenden Arbeit wird PbO aus PbC2 . zerlegt O4 über die chemische Reaktion bei Temperaturen von 400–500 °C [14]
$$ {\mathrm{PbC}}_2{\mathrm{O}}_4\to \mathrm{PbO}+\mathrm{CO}\uparrow +{\mathrm{CO}}_2\uparrow $$ (2)welches eine höhere Löslichkeit im geschmolzenen Salz von NaCl-KCl hat (die Löslichkeit in NaCl-KCl-Salzen beträgt 30 μmol/g Chloride bei 900°C [21]) als TiO2 (das eine sehr geringe Löslichkeit in Alkalichloriden hat [22]). Daher kann das besser lösliche Reaktant PbO in der Salzschmelze auf die Oberfläche von kugelförmigem TiO2 . diffundieren Vorläufer und reagieren damit in situ, um kugelförmige PTO-Pulver durch das Lösungsfällungsverfahren zu bilden. Ein typisches EDS-Spektrum in Abb. 2f zeigt, dass die Probe aus Pb-, Ti- und O-Elementen besteht, und die EDS-Analyse bestätigt, dass die chemische Zusammensetzung der nominellen Zusammensetzung fast ähnlich ist.
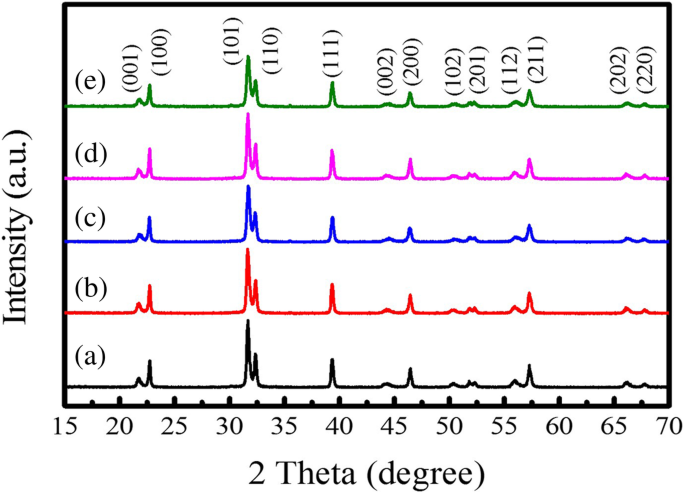
XRD-Muster der kugelförmigen PTO-Produkte, synthetisiert durch die MSS-Methode bei 950°C für 5 h mit den Molverhältnissen von PbC2 O4 :TiO2 :NaCl:KCl gleich (a) 1:1:10:10, (b) 1:1:20:20, (c) 1:1:30:30, (d) 1:1:40:40, und (e) 1:1:60:60

REM-Aufnahmen der kugelförmigen PTO-Produkte, synthetisiert durch die MSS-Methode bei 950°C für 5 h mit den Molverhältnissen von PbC2 O4 :TiO2 :NaCl:KCl gleich a 1:1:10:10, b 1:1:20:20, c 1:1:30:30, d 1:1:40:40 und e 1:1:60:60 bzw. f Typisches EDS-Spektrum, aufgenommen von kugelförmigen PTO-Produkten, die bei 950 °C für 5 h mit dem Molverhältnis von PbC2 . synthetisiert wurden O4 :TiO2 :NaCl:KCl gleich 1:1:10:10
Phasenstruktur und Morphologie von stabförmigen PTO-Pulvern, synthetisiert durch die Schablonen-MSS-Methode
Vor der Synthese der stäbchenförmigen PTO-Pulver durch die Schablonen-MSS-Methode, die Phasenstruktur und die Morphologie des TiO2 Schablonen wurden zuerst untersucht. Abbildung 3 zeigt die XRD-Muster von TiO2 Templates bei unterschiedlichen Temperaturen für 1 h getempert. Es wird beobachtet, dass die vorherrschende Anatas-Phase von TiO2 wurde in den Produkten nach dem Glühen bei 600°C (Abb. 3a) und 700°C (Abb. 3b) gebildet. Eine gewisse Menge an K2 Ti4 O9 noch in den Produkten enthalten. Die durch Sterne gekennzeichneten XRD-Beugungspeaks stammen vom K2 Ti4 O9 Phase (ICDD-Nr. 32-0861). Bei Erhöhung der Glühtemperatur auf 800°C (Abb. 3c) wird das unreine K2 Ti4 O9 Phase fast verschwunden. Alle in Abb. 3c gezeigten XRD-Beugungspeaks können gut auf den Anatas TiO2 . indiziert werden (JCPDS Nr. 021–1272), was auf die Bildung von reiner Anatas-Phase TiO2 . hinweist . Es wurde auch festgestellt, dass die kristalline Qualität des TiO2 Templat stark verbessert, da die Intensität des (101)-Hauptbeugungspeaks stark zugenommen hat. Abbildung 4 zeigt die REM-Bilder des TiO2 . Schablonen bei unterschiedlichen Temperaturen getempert. Das gesamte TiO2 Schablonen wiesen eine stabförmige Morphologie auf, und ihre durchschnittlichen Durchmesser variierten von 490 nm bis 570 nm und dann 500 nm, wenn die Glühtemperaturen anstiegen, während ihre durchschnittlichen Längen bei etwa 12,0 µm gehalten wurden. Die Seitenverhältnisse des TiO2 Templaten, die bei 600 °C, 700 °C und 800 °C getempert wurden, betrugen etwa 25, 23 bzw. 24. Die stabförmige Morphologie des geglühten TiO2 Templates wird dem anisotropen Wachstum der Anatas-Phasenstruktur im Annealing-Prozess zugeschrieben. Basierend auf den obigen experimentellen Ergebnissen kann geschlossen werden, dass das TiO2 Templates mit Anatas-Phase, die bei 800 °C für 1 h getempert wurden, haben eine hohe Kristallinität und eine stäbchenförmige Morphologie, die geeignet sind, die stäbchenförmigen PTO-Pulver über die Templat-MSS-Methode zu synthetisieren.
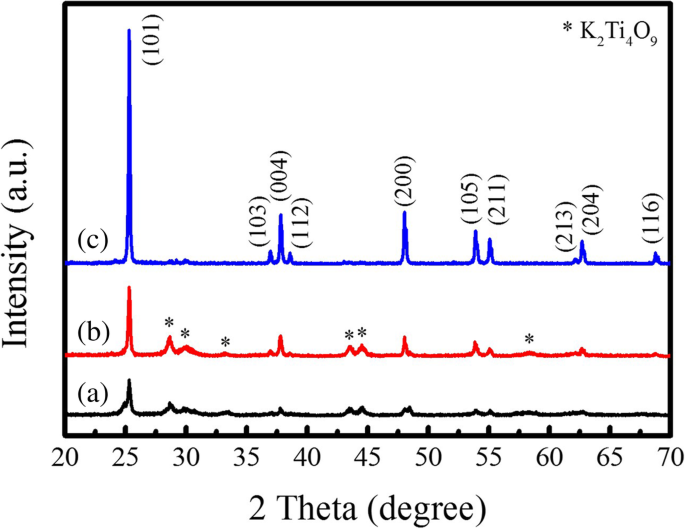
XRD-Muster des TiO2 Template getempert bei (a) 600°C, (b) 700°C und (c) 800°C für 1 h

REM-Aufnahmen des TiO2 Vorlagen getempert bei a , b 600°C; c , d 700°C; und e , f 800°C für 1 h
Abbildung 5 zeigt die XRD-Muster der PTO-Pulver, die mit der Schablonen-MSS-Methode bei 800°C für unterschiedliche Reaktionszeiten synthetisiert wurden, wobei das stäbchenförmige TiO2 Templates (Anatas-Phase getempert bei 800 °C für 1 h) wurden als Titanquelle verwendet und das Molverhältnis von PbC2 O4 :TiO2 (Vorlage):NaCl:KCl war gleich 1:1:20:20. Die XRD-Beugungsmuster zeigen, dass alle PTO-Pulver in einer tetragonalen Phasenstruktur (JCPDS Nr. 06-0452) kristallisieren und keine anderen Fremdphasen nachgewiesen werden, was die Bildung einer reinen tetragonalen Phasenstruktur veranschaulicht. Die Gitterparameter der PTO-Pulver wurden aus den XRD-Mustern abgeleitet, Details sind in Tabelle 2 dargestellt. Die entsprechenden REM-Bilder der PTO-Pulver sind in Fig. 6 gezeigt. Wie in Fig. 6a gezeigt, wurde die Morphologie der PTO-Pulver getempert bei 800 °C für 1 h ist eine Kombination aus wenigen stäbchenförmigen und großen Mengen kugelförmiger PTO-Partikel. Der qualitative Volumenanteil der stabförmigen PTO-Partikel betrug nur etwa 3%, und die stabförmigen PTO-Partikel hatten einen durchschnittlichen Durchmesser von etwa 860 nm und eine Länge von 4,50 µm. Mit Erhöhung der Reaktionszeit von 1 h auf 5 h wurde jedoch der Volumenanteil der stabförmigen PTO-Partikel auf ~ 2,4% reduziert (Abb. 6c), und die stabförmigen PTO-Partikel hatten einen durchschnittlichen Durchmesser von etwa 930 nm und Länge von 6.0 μm. Bei einer weiteren Erhöhung der Reaktionszeit auf 10 h (Abb. 6e) wurden die stabförmigen PTO-Partikel in den PTO-Produkten kaum beobachtet, während eine große Menge kugelförmiger PTO-Partikel gebildet wurde (siehe Abb. 6e-f). Das heißt, eine Verlängerung der Reaktionszeit fördert die Bildung von kugelförmigen PTO-Partikeln, während die Bildung von stäbchenförmigen PTO-Partikeln unterdrückt wird. Die durchschnittliche Partikelgröße der kugelförmigen PTO-Partikel, die 10 h bei 800 °C getempert wurden, betrug etwa 550 nm (Abb. 6e), etwas größer als der Durchmesser des stabförmigen TiO2 . Vorlage (480 nm) (Abb. 4e). Die Bildung großer Mengen kugelförmiger PTO-Partikel in den 10 h bei 800°C geglühten Produkten kann darauf zurückgeführt werden, dass das stabförmige TiO2 Template werden während des Template-MSS-Prozesses in kleine kugelförmige Partikel zerbrochen, die mit dem gelösten PbO (zersetzt aus PbC2 .) reagieren O4 ) in der NaCl-KCl-Salzschmelze und bildet über den Lösungs-Präzipitationsmechanismus kugelförmige PTO-Pulver. Die unterbrochene Spur des TiO2 Templat wurde in Fig. 6b und d beobachtet, wo einige kugelförmige PTO-Partikel miteinander verbunden waren, um die Form einer Zuckerkürbisschnur zu bilden. Es scheint, dass die stabförmigen PTO-Pulver nicht erfolgreich durch das Templat-MSS-Verfahren bei einem niedrigen Gehalt an geschmolzenem Salz synthetisiert werden.
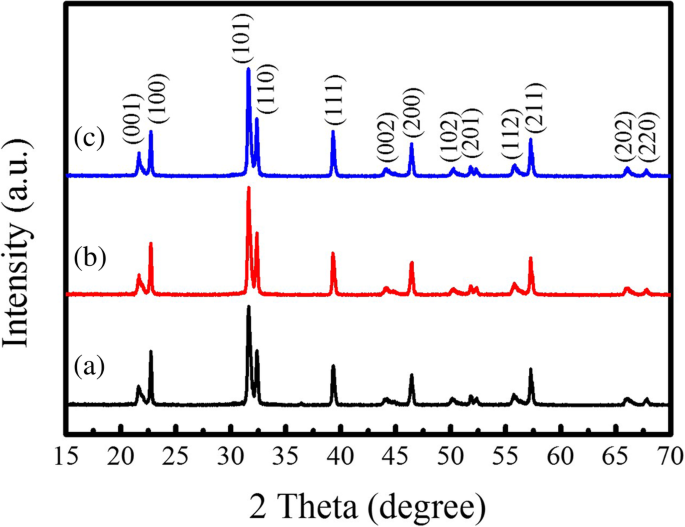
XRD-Muster der PTO-Pulver, synthetisiert über die Templat-MSS-Methode mit dem Molverhältnis von PbC2 O4 :TiO2 (Vorlage):NaCl:KCl gleich 1:1:20:20 und bei 800 °C für (a) 1 h, (b) 5 h und (c) 10 h

SEM-Bilder der PTO-Produkte, synthetisiert über die Schablonen-MSS-Methode mit dem Molverhältnis von PbC2 O4 :TiO2 (Vorlage):NaCl:KCl gleich 1:1:20:20 und bei 800°C für a . getempert , b 1 h; c , d 5 h; und e , f 10 h
Es ist bekannt, dass beim MSS-Verfahren das Korn bei hohen Temperaturen durch die Schmelzsalzflüsse wächst, der Schmelzsalzgehalt die Kornwachstumsrate und die Morphologie der Endprodukte steuert [23]. Mit zunehmendem Salzschmelzengehalt werden bei hoher Temperatur größere Mengen an geschmolzener Salzflüssigkeit gebildet. Somit werden die gelösten Reaktionsionen (z. B. Bleiionen) effektiv in der Salzschmelze abgetrennt, und ihre Konzentrationen benötigen eine längere Zeit, um die Sättigungskonzentration zu erreichen. Daher ist die Keimbildungsrate von PTO-Nanokristalliten an der Oberfläche von unlöslichem TiO2 Templatpartikel sollten reduziert werden. Die gebildeten PTO-Nanokristallite haben genug Zeit, um sie in der Umgebung mit hohem geschmolzenem Salzgehalt zu stabförmigen PTO-Partikeln wieder zu vereinen. Das bedeutet, dass eine Umgebung mit hohem geschmolzenem Salzgehalt hilfreich ist, um die stabförmigen PTO-Partikel im Templat-MSS-Verfahren zu synthetisieren. Daher haben wir das Molverhältnis von PbC2 . erhöht O4 :TiO2 (Vorlage):NaCl:KCl bis zu 1:1:60:60, und ihre Mischungen wurden bei 800 °C für verschiedene Stunden getempert. Abbildung 7 zeigt die XRD-Muster der PTO-Pulver, die bei 800°C nach der MSS-Templatmethode unter hohem Salzschmelzengehalt synthetisiert wurden. Es wurde festgestellt, dass die PTO-Pulver, die 5 h (Fig. 7b) und 10 h (Fig. 7c) bei 800 °C geglüht wurden, eine reine tetragonale Phase aufwiesen; jedoch hatten die PTO-Pulver, die bei 800 °C für 1½ h geglüht wurden (Abb. 7a), eine überwiegende tetragonale Phase mit Ausnahme der kleinen unreinen Phasen von Ti3 O5 und TiO2 . Die Gitterkonstanten a und c der PTO-Pulver, die für verschiedene Stunden bei 800°C geglüht wurden, wurden berechnet und in Tabelle 2 aufgeführt. Die c /a Das Verhältnis betrug etwa 1,050. Die Oberflächenmorphologien der entsprechenden PTO-Pulver sind in Fig. 8 gezeigt. In Fig. 8a ist zu sehen, dass die PTO-Pulver, die 1 h bei 800 °C getempert wurden, aus stab- und kugelförmigen Partikeln bestehen. Der qualitative Volumenanteil der stäbchenförmigen Partikel, geschätzt aus dem SEM-Bild, betrug etwa 70%. Die Durchmesser der stäbchenförmigen Partikel variierten von 480 nm bis 1,50 µm, während ihre Längen im Bereich von 3,0 bis 7,0 µm lagen. Das in Abb. 8b gezeigte lokal vergrößerte SEM-Bild zeigt, dass die stabförmigen PTO-Pulver aus sehr kleinen PTO-Nanokristalliten bestehen, was auf die unterbrochene Spur des stabförmigen TiO2 . hinweist Vorlagen während des Vorlagen-MSS-Prozesses. Mit Erhöhung der Reaktionszeit von 1 h auf 5 h konnte der Volumenanteil der stabförmigen PTO-Pulver im Endprodukt auf ~ 97% gesteigert werden (Abb. 8c). Die Länge der stabförmigen PTO-Pulver lag im Bereich von 7,0–10,0 µm. Bei einer weiteren Erhöhung der Reaktionszeit auf 10 h (Abb. 8e) betrug der Volumenanteil der stabförmigen PTO-Partikel im Endprodukt jedoch etwa 85% und die Länge der PTO-Stäbe lag im Bereich von 3,5– 6,5 µm. Der Durchmesser der stabförmigen PTO-Pulver lag im Bereich von 970 nm–1,50 μm.
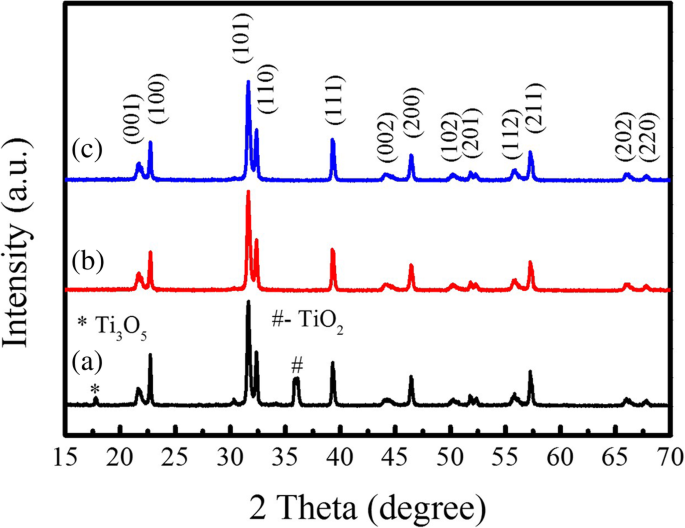
XRD-Muster der PTO-Pulver, synthetisiert über die Templat-MSS-Methode mit dem Molverhältnis von PbC2 O4 :TiO2 (Schablone):NaCl:KCl gleich 1:1:60:60 und bei 800 °C für (a) 1 h, (b) 5 h und (c) 10 h getempert

REM-Aufnahmen der PTO-Pulver, synthetisiert über die Templat-MSS-Methode mit dem Molverhältnis von PbC2 O4 :TiO2 (Vorlage):NaCl:KCl gleich 1:1:60:60 und bei 800°C für a , b 1 h; c , d 5 h; und e , f 10 h
Die Bildung von stabförmigen PTO-Pulvern unter einem hohen Gehalt an geschmolzenem Salz durch das Templat-MSS-Verfahren kann durch das folgende Verfahren verstanden werden. Im Vorlagen-MSS-Prozess PbC2 O4 wird zunächst in PbO, CO und CO2 . zerlegt im Temperaturbereich von 400–500 °C, und PbO wird bei 800 °C in der Salzschmelze gelöst (seine Löslichkeit in NaCl-KCl-Salzen beträgt 14 µmol/g Chloride bei 800 °C [21]). Das gelöste PbO diffundiert auf die Oberfläche des stabförmigen TiO2 Vorlage und reagiert mit TiO2 in situ zur Bildung von PTO-Nanokristalliten durch die chemische Reaktion bei 800°C
$$ \mathrm{PbO}+{\mathrm{TiO}}_2\to {\mathrm{PbTiO}}_3 $$ (3)Da der Gehalt an geschmolzenem Salz sehr hoch ist (das Molverhältnis von PbC2 O4 :TiO2 (Vorlage):NaCl:KCl gleich 1:1:60:60), damit die gelösten Bleiionen in der Salzschmelze effektiv abgeschieden werden, deren Konzentration eine längere Zeit benötigt, um die Sättigungskonzentration zu erreichen. Das stabförmige TiO2 Template haben eine sehr geringe Löslichkeit in NaCl-KCl-Salzen, die in kleine TiO2 . zerlegt werden kugelförmige Partikel bei einer hohen Temperatur in einer Umgebung mit hohem geschmolzenem Salzgehalt. Daher reagiert das gelöste PbO mit dem zerbrochenen TiO2 Partikel an ihren Oberflächen, um PTO-Nanokristallite zu bilden. Diese PTO-Nanokristallite haben genug Zeit, um sie in einer Umgebung mit hohem geschmolzenem Salzgehalt wieder zu den stabförmigen PTO-Partikeln zu vereinigen. Wie in Abb. 8c gezeigt, wurden großmaßstäbliche polykristalline stabförmige PTO-Pulver mit Durchmessern im Bereich von 480 nm bis 1,50 µm und Längen bis zu 10 µm synthetisiert. Sie bestehen aus kleinen Nanokristalliten, wie in Abb. 8d zu sehen ist. Die schematischen Diagramme, die die Bildung von PTO-Partikeln im MSS-Prozess und stabförmigen PTO-Pulvern im Templat-MSS-Prozess veranschaulichen, sind in Abb. 9 gezeigt. Unsere vorliegenden Arbeiten zeigen, dass der Gehalt an geschmolzenem Salz eine entscheidende Rolle bei der Bildung des stabförmigen ABO3 Verbindungen mit kubischer oder pseudokubischer Kristallstruktur im Templat-MSS-Prozess. Das heißt, bei einem niedrigen Gehalt an geschmolzenem Salz können die stabförmigen PTO-Pulver nicht synthetisiert werden, obwohl das stabförmige TiO2 Vorlagen werden im Vorlagen-MSS-Prozess verwendet. Die Bildung der polykristallinen stabförmigen PTO-Pulver in Form einer Zuckerkürbisschnur anstelle von einkristallinen PTO-Stäben bedarf noch weiterer Untersuchungen.
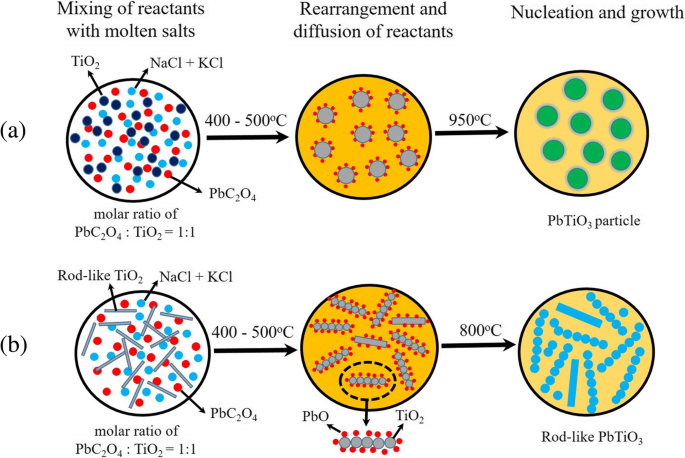
Schematische Darstellungen zur Veranschaulichung der Bildung von (a) PTO-Partikeln im MSS-Prozess und (b) stabförmigen PTO-Pulvern im Templat-MSS-Prozess
Dielektrische Eigenschaften von kugelförmigen und stabähnlichen Zapfwellenpulvern
Die Dielektrizitätskonstanten (εr ) and dielectric losses (tanδ ) of the spherical and rod-like PTO powders synthesized by MSS and template MSS methods are shown in Fig. 10, which are measured at room temperature as a function of the frequency. Similar frequency-dependent dielectric behaviors are observed in the spherical and rod-like PTO powders. As shown in Fig. 10a, the sphere-like PTO powders (a) and (b) synthesized by MSS method at 950 °C for 5 h with the molar ratios of PbC2 O4 :TiO2 :NaCl:KCl equal to (a) 1:1:30:30 and (b) 1:1:60:60, respectively, have much higher dielectric constants than the rod-like PTO powders (c) and (d) synthesized by template MSS method at 800 °C for (c) 5 h and (d) 10 h with the molar ratio of PbC2 O4 :TiO2 (template):NaCl:KCl equal to 1:1:60:60. It is noticed that the dielectric constants of the sphere-like PTO powders (a) and (b) have decreased fast (from ~ 3000 to ~ 700) in the frequency range below 10 3 Hz, then reduced slowly with further increasing the frequency over 10 3 Hz, and finally become a constant value of ~ 340 at a higher frequency over 10 5 Hz. The fast decrease of the dielectric constant at lower frequencies is ascribed to the space charge polarization effect, which is correlated to the non-uniform charge accumulation at grain boundaries within the sphere-like PTO powders. The slow reduction of the dielectric constant is due to that the dipoles present in the PTO powders could not reorient themselves as fast as the frequency of an alternating electric field, resulting in a decrease of the dielectric constants [24]. In contrast, the rod-like PTO powders (c) and (d) synthesized by template MSS method exhibit a slight frequency-dependent dielectric behavior, their dielectric constants are slightly reduced with increasing frequency below 10 3 Hz, and then become a constant value of ~ 140. It is observed in Fig. 10b that all the dielectric losses of the spherical and rod-like PTO powders are decreased with increasing frequency due to the existence of the space charge polarization in all the PTO powders. The dielectric loss of the PTO powder (b) has the highest value, which has reduced fast with increasing frequency below 10 5 Hz, and then it becomes constant. The dielectric losses of the PTO powder (a) are reduced slowly with increasing frequency, which has the lowest value as compared with the other three PTO samples. The dielectric losses of the spherical PTO powders (c) and (d) synthesized by template MSS method exhibit very similar dielectric behavior, their dielectric losses are reduced slowly as the frequency increases. At room temperature, the dielectric constant and dielectric loss of the spherical PTO powders (a) measured at 10 6 Hz were ~ 340 and 0.06, respectively. The corresponding values for the spherical PTO powders (b) were 155 and 0.12, 140 and 0.08 for the rod-like PTO powders (c), and 130 and 0.07 for the rod-like PTO powders (d). Therefore, the sphere-like PTO powders (a) have high dielectric constant and low dielectric loss, and these dielectric data are better than that reported previously for the PTO nanoparticles synthesized via sol-gel process and annealed at 600 °C for 6 h (the dielectric constant and dielectric loss at 10 6 Hz were about 15 and 0.40) [25], and for the PTO nanoparticles synthesized by stearic acid gel method and annealed at 400 °C for 1 h (the dielectric constant and dielectric loss at 10 6 Hz were about 50 and 0.002) [26]. Normally, to measure the dielectric properties of PbTiO3 ceramics prepared from the nanopowders synthesized by chemical methods such as the sol-gel method [27], hydrothermal method [28, 29], or by physical method such as high-energy ball milling technique [30], PbTiO3 powder samples are usually pressed into pellets under a hydraulic press (using 1 cm diameter die). For making dense PbTiO3 ceramics, the samples are needed to be sintered at high temperatures (e.g., 900 °C or 1000 °C for 2 h in air) followed by furnace cooling. Leonarska et al. [28] synthesized the PTO nanopowders at 490 K for 2 h by hydrothermal method and then prepared the PTO ceramics from the as-synthesized PTO nanopowders and sintered it at 1240 K for 1.5 h. They checked the impact of high-temperature process on the morphology or crystallization degree of the PTO ceramics by SEM observations and found that the PTO ceramics had slightly larger and rounded ceramic grains in comparison with the nanoparticles obtained directly from hydrothermal method. Similarly, Hu et al. [29] also reported the preparation of PTO nanoceramics (with grain sizes of ~ 200 nm) under sintering process (at 950 °C for 2 h in air) using the hydrothermal PTO nanopowders (with average grain size of ~ 100 nm) as the raw materials. This result indicates the sintering process of the hydrothermal PTO nanopowders can increase the grain size. Kong et al. [30] prepared the PTO nanopowders (with average grain size of ~ 10 nm) by high-energy ball milling technique, and pressed them directly into green pellets and sintered at 1100 °C for 1 h. Crack-free PTO ceramics with 95% of the theoretical density were successfully obtained. SEM images revealed that the average grain size of the sintered samples were < 1.5 μm. In the present work, we have prepared dense PbTiO3 ceramic samples under a sintering process (at 1150 °C for 2 h) by using the as-synthesized sphere-like PTO powders via MSS method and the as-synthesized rod-like PTO powders via template MSS method. The high-temperature process has improved the crystallized quality and the grain sizes of the PTO powders but has few effects on the morphology. The best dielectric properties of the PTO ceramics prepared the as-synthesized spherical PTO powders by MSS method are attributed to their larger average particle size (~ 2.0 μm).
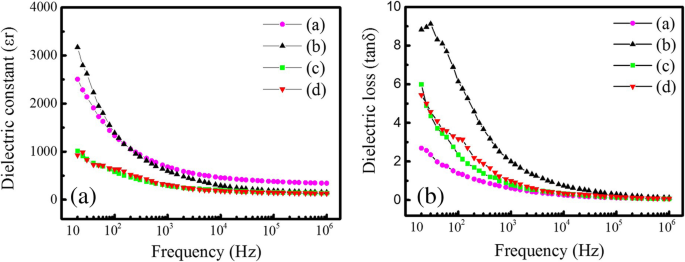
a Dielectric constants (εr ) and b dielectric losses (tanδ ) of the PTO powders synthesized by MSS method and template MSS method. Samples (a) and (b) were synthesized by MSS method at 950 °C for 5 h with the molar ratios of PbC2 O4 :TiO2 :NaCl:KCl equal to 1:1:30:30 and 1:1:60:60, respectively. Samples (c) and (d) were synthesized by template MSS method with the molar ratio of PbC2 O4 :TiO2 (rod-like template):NaCl:KCl equal to 1:1:60:60 and annealed 800 °C for 5 h and 10 h, respectively
Schlussfolgerungen
Both sphere- and rod-like PTO powders were synthesized by MSS and template MSS methods, respectively. XRD patterns reveal that all the PTO powders are crystallized in a tetragonal phase structure. SEM images demonstrated that increasing the molar ratio of PbC2 O4 :TiO2 :NaCl:KCl from 1:1:10:10 to 1:1:60:60 in the MSS process had little effect on the sphere-like morphology of the PTO powders synthesized by MSS method. Large-scale polycrystalline rod-like PTO powders with length up to 10 μm and diameters in the range of 480 nm–1.50 μm were successfully synthesized by template MSS method at 800 °C for 5 h, where the rod-like anatase TiO2 precursors were used as a titanium source and the molar ratio of PbC2 O4 :TiO2 :NaCl:KCl was equal to 1:1:60:60. It is found that under low molten salt content, extending the reaction time promoted the formation of sphere-like PTO particles whereas the formation of rod-like PTO particles was suppressed. In addition, the rod-like PTO powders cannot be synthesized even if the rod-like TiO2 templates are used. Dielectric measurements demonstrated that the dielectric constants of the sphere-like PTO powders synthesized by MSS method decreased fast from ~ 3000 to ~ 700 at low frequencies below 10 3 Hz, and at high frequencies over 10 5 Hz they became a constant value of ~ 340. The fast decrease of the dielectric constant at low frequencies is ascribed to the space charge polarization due to the non-uniform charges accumulated within the PTO powders. The rod-like PTO powders synthesized by template MSS method exhibited slight frequency-dependent dielectric behavior, their dielectric constants decreased slowly at the frequencies below 10 3 Hz and then remained a constant value of ~ 140 as the frequency increased up to 10 6 Hz. At room temperature, dielectric constant and dielectric loss (measured at 10 6 Hz) of the sphere-like PTO powders synthesized by MSS method at 950 °C for 5 h with low molten salt content (the molar ratio of PbC2 O4 :TiO2 :NaCl:KCl equal to 1:1:30:30) were 340 and 0.06, respectively, and the corresponding values were 155 and 0.12 for the sphere-like PTO powders synthesized by MSS method with high molten salt content (the molar ratio of PbC2 O4 :TiO2 :NaCl:KCl equal to 1:1:60:60). The dielectric constant and dielectric loss for the rod-like PTO powders synthesized by template MSS method at 800 °C for 5 h and 10 h under high molten salt content (the molar ratio of PbC2 O4 :TiO2 (rod-like template):NaCl:KCl equal to 1:1:60:60) were 140 and 0.08, and 130 and 0.07, respectively. The higher dielectric constant and lower dielectric loss of the sphere-like PTO powders synthesized at 950 °C for 5 h by MSS method with the molar ratio of PbC2 O4 :TiO2 :NaCl:KCl equal to 1:1:30:30 are ascribed to their large average particle size (~ 2.0 μm), which have promising applications in multilayer capacitors and resonators.
Abkürzungen
- CALYPSO:
-
Crystal Structure AnaLYsis by Particle Swarm Optimization
- EDS:
-
Energy Dispersive Spectroscopy
- MSS:
-
Molten Salt Synthesis
- NP-9:
-
Polyoxyethylene (9) Nonylphenyl Ether
- PTO:
-
PbTiO3
- SEM:
-
Scanning Electron Microscopy
- XRD:
-
X-ray Diffraction
Nanomaterialien
- Einfache Synthese und optische Eigenschaften kleiner Selen-Nanokristalle und -Nanostäbe
- Nanostrukturiertes Siliciumdioxid/Gold-Cellulose-gebundenes Amino-POSS-Hybrid-Komposit über den Sol-Gel-Prozess und seine Eigenschaften
- Strukturelle Besonderheiten ionenleitfähiger organisch-anorganischer Polymerverbundwerkstoffe auf Basis von aliphatischem Epoxidharz und Lithiumperchloratsalz
- Die Wirkung von Kontakt-Nichtgleichgewichtsplasma auf die strukturellen und magnetischen Eigenschaften von Mn Х Fe3 − X О4 Spinellen
- Einfluss von Wasser auf die Struktur und die dielektrischen Eigenschaften der mikrokristallinen und Nano-Cellulose
- Synthese und Lumineszenzeigenschaften wasserlöslicher α-NaGdF4/β-NaYF4:Yb,Er Kern-Schale-Nanopartikel
- Strukturelle und im sichtbaren Infrarotbereich sichtbare optische Eigenschaften von Cr-dotiertem TiO2 für farbige kühle Pigmente
- Synthese wasserlöslicher Antimonsulfid-Quantenpunkte und ihre photoelektrischen Eigenschaften
- Einfache Synthese von Wurmloch-ähnlichem mesoporösem Zinnoxid durch verdunstungsinduzierte Selbstorganisation und die verbesserten Gassensoreigenschaften
- Untersuchung der strukturellen, elektronischen und magnetischen Eigenschaften von Ag n V (n = 1–12)-Clustern



