Bildung monodisperser Kohlenstoffkugeln mit einstellbarer Größe durch Triblockcopolymer-unterstützte Synthese und ihre Kondensatoreigenschaften
Zusammenfassung
Zur Herstellung monodisperser Kohlenstoffkugeln (MCSs) wurde eine einfache hydrothermale Polymerisationsmethode unter Verwendung des Triblockcopolymers F108 als Tensid entwickelt. Die Synthese basiert auf der Ammoniak-katalysierten Polymerisationsreaktion zwischen Phenol und Formaldehyd (PF). Die resultierenden MCSs haben eine perfekte sphärische Morphologie, eine glatte Oberfläche und eine hohe Dispersität. Die Partikelgrößen können in einem weiten Bereich von 500-2400 nm eingestellt werden, indem die Dosierung des PF-Precursors angepasst wird. Die aktivierten MCSs mit geeigneten Heteroatomen (N und O) dotiert und einer großen spezifischen Oberfläche (960 m 2 g− 1 ) erhalten. Eine Hochleistungselektrode aus elektrischen Doppelschichtkondensatoren, die aus diesem aktiven Material hergestellt ist, hat eine ausgezeichnete spezifische Kapazität (310 F g −1 bei 0,5 A g −1 ) und hervorragende Zyklenstabilität (92% Kapazitätserhalt nach 10.000 Zyklen). Diese Arbeit bietet eine neue Möglichkeit für die Herstellung von MCSs mit potentiellen Anwendungen.
Einführung
In den letzten Jahrzehnten wurden poröse Kohlenstoffmaterialien häufig in den Bereichen Gasspeicher [1], Katalysatorträger [2], Superkondensatoren [3], Lithium-Ionen-Batterien [4], Solarzellen [5] und Elektronik eingesetzt Geräte [6] aufgrund ihrer Vorteile wie der hohen spezifischen Oberfläche, der guten elektrischen Leitfähigkeit und der hohen chemischen Stabilität. Aus Sicht der Materialchemie wurden poröse Kohlenstoffmaterialien mit unterschiedlicher Morphologie und Struktur wie Kohlenstoffaerogele [7], Fasern [8], Nanotubes [9], Nanosphären [10] und Aktivkohle [11] erfolgreich synthetisiert. In letzter Zeit haben monodisperse Kohlenstoffkugeln (MCSs) aufgrund ihrer einzigartigen Eigenschaften wie hoher Stapeldichte, inhärent kurzer Ionendiffusionspfade und guter struktureller Stabilität erhebliche Untersuchungen zu funktionellen Elektrodenmaterialien für Energiespeicher- und -umwandlungsvorrichtungen erhalten [12, 13]. Die genaue Kontrolle über Morphologie, Dispersität, glatte Oberfläche und Partikelgröße der MCSs war der Schlüssel zur Erfüllung der Anforderungen für einige spezielle praktische Anwendungen [14].
Die Carbonisierung von vorsynthetisierten Phenolharz-Polymerkugeln mit ausgezeichneter thermischer Stabilität hat sich als bevorzugter Ansatz für die Herstellung von MCS erwiesen. Die Gruppe von Zhao berichtete über eine hydrothermale Route mit niedriger Konzentration zur Synthese hochgradig einheitlich geordneter mesoporöser Kohlenstoffkugeln mit einer einstellbaren Größe von 20 bis 140 nm unter Verwendung von phenolischem Resol als Kohlenstoffvorstufe [15]. Durch die intelligente Verknüpfung des Hydrolyse-Polymerisations-Reaktionsmechanismus von Resorcin-Formaldehyd-Harzen mit den klassischen Stöber-Siliciumdioxid-Kugeln entwickelten Liu und seine Mitforscher erfolgreich eine Erweiterung der Stöber-Methode zur Synthese von MCS mit einheitlicher und kontrollierbarer Größe im Submikrometerbereich [16 ]. Basierend auf der Benzoxazin-Chemie etablierten Lu und Mitarbeiter einen neuen Weg zur Synthese von hochdispersen MCS mit maßgeschneiderten Größen im Bereich von 95~225 nm unter genau programmierten Reaktionstemperaturen [17]. Nach diesen bahnbrechenden Arbeiten wurde dem Design und der Synthese von MCSs große Aufmerksamkeit geschenkt [18,19,20,21]. Die meisten dieser Ansätze erfordern jedoch entweder langwierige hydrothermale Behandlungsverfahren oder können keine breite einstellbare Partikelgröße mit glatter Oberfläche und enger Größenverteilung herstellen. Daher bleibt die Synthese von weit abstimmbaren, sehr einheitlichen und morphologisch klar definierten MCSs immer noch eine große Herausforderung.
In dieser Arbeit schlagen wir eine einfache hydrothermale Methode zur Herstellung von MCSs unter Verwendung des Triblockcopolymers Pluronic F108 als Tensid basierend auf der Ammoniak-katalysierten Polymerisationsreaktion von Phenol und Formaldehyd (PF) vor. Der detaillierte Bildungsmechanismus von MCSs wurde diskutiert. Die so hergestellten MCS haben eine perfekte sphärische Morphologie und glatte Oberfläche und sind sehr einheitlich. Die Partikelgrößen von MCSs können in Abhängigkeit von der Konzentration des PF-Vorläufers in einem weiten Bereich von 500 bis 2400 nm eingestellt werden. Wenn sie als Elektrodenmaterialien für Superkondensatoren verwendet werden, weisen die aktivierten MCSs aufgrund der Stickstoff- und Sauerstoff-Codotierung und der hohen spezifischen Oberfläche eine hervorragende elektrochemische Leistung auf.
Methoden
Synthese von MCS
In einer typischen Synthese wurden 0,5 ml wässriges Ammoniak (25 Gew.-%) mit 30 ml Ethanol und 50 ml entionisiertem Wasser (H2 Ö). Dann 10 mg Triblock-Copolymer Pluronic F108 (Mw =14.600, PEO132 -PPO50 -PEO132 ) wurde in der Mischlösung gelöst. Als nächstes wurden 0,2 ml Phenol bzw. 0,2 ml Formaldehyd (37 Gew.-%) unter leichtem Rühren für 30 Minuten zugegeben. Schließlich wurde die resultierende Lösung in einen mit Teflon ausgekleideten 100-ml-Autoklaven überführt und die hydrothermale Reaktion wurde 3 h bei 160 °C reguliert. Die resultierenden PF-Harz-Polymerkugeln wurden durch Waschen mit H2 . erhalten O und Ethanol für mehrere Male. Dann wurden MCSs-x durch Tempern der PF-Harzkugeln unter N2 . erhalten Atmosphäre bei 600 °C für 3 h, „x“ bezeichnet die verwendete Phenol- und Formaldehyd-Dosierung (z. B. 0,2, 0,4, 0,6 und 0,8 beziehen sich auf 0,2, 0,4, 0,6 bzw. 0,8 ml Phenol und Formaldehyd). Die MCSs-x wurden durch KOH (in einem Massenverhältnis von 1:2) bei 700 °C für 1 h in einem N2 . chemisch aktiviert Atmosphäre zur Vorbereitung des aMCSs-x.
Charakterisierung
Rasterelektronenmikroskopie (SEM) wurde auf einem NovaNanoSEM230-Instrument durchgeführt. Transmissionselektronenmikroskopie (TEM) wurde auf einem Tecnai G2 F20 S-TWIX-Instrument durchgeführt. Röntgenbeugungsmuster (XRD) wurden mit einem SIEMENS D500 Diffraktometer mit Cu Kα-Strahlung (λ =0,15056 nm). Die Raman-Spektroskopie wurde auf einem LabRAMHR-800-System durchgeführt. Eine Röntgen-Photoelektronenspektroskopie (XPS)-Analyse wurde auf einem ESCALAB 250Xi-Instrument durchgeführt. Die Stickstoffadsorptions-Desorptions-Isothermen wurden bei 77 K auf einem ASAP 2020-Gerät gemessen.
Elektrochemische Messung
Der elektrochemische Test der zyklischen Voltammetrie (CV), der galvanostatischen Ladung/Entladung (GCD) und der elektrochemischen Impedanzspektroskopie (EIS) wurde auf der elektrochemischen Workstation CHI660E mit einem Drei-Elektroden-System in 6 M KOH-Elektrolytlösung durchgeführt. Die Platinfolie und Hg/HgO wurden als Gegenelektrode bzw. Referenzelektrode verwendet. Die Arbeitselektroden wurden durch Mischen von aMCSs-x, Polytetrafluorethylen (60 Gew.-%) und Acetylenruß mit einem Massenanteil von 8:1:1 hergestellt. Die gravimetrische spezifische Kapazität wurde nach folgender Gleichung berechnet:
$$ Cg=\frac{I\Delta t}{m\Delta V} $$ (1)wo ich (A), Δt (s), ΔV (V) und m (g) sind der angelegte Strom, die Entladezeit, das Potentialfenster bzw. die Masse des aktiven Materials der Elektroden.
Ergebnisse und Diskussion
In dieser Studie präsentieren wir einen möglichen Synthesemechanismus der MCSs in Schema 1. Schritt I ist der Sol-Gel-Prozess. In Weg a bildeten sich die Emulsionströpfchen durch die Wasserstoffbrücken-Wechselwirkung zwischen Phenol, Formaldehyd, Ammoniakmolekül, Ethanol und Wasser [16]. Ammoniakmoleküle katalysieren die Polymerisation von PF, die aus dem Inneren der Emulsionströpfchen stattfindet [22]. Außerdem wird eine große Zahl von PF-Hydroxymethyl-substituierten Einheiten durch schnelle Reaktion von Phenol und Formaldehyd erzeugt, die aufgrund der elektrostatischen Wechselwirkung mit Ammoniakionen an der äußeren Oberfläche der Emulsionströpfchen positioniert sind. Gleichzeitig zeigt Pfad b den Selbstbildungsprozess von F108-Mizellen, die aus Triblockcopolymer-F108-Monomeren gebildet werden, bei denen es sich um die hydrophoben PPO-Blöcke zur Bildung des Kerns im Inneren und die hydrophilen PEO-Segmente außerhalb handelt [23]. Dann können in Weg c reichlich Emulsionströpfchen/PF-hydroxymethylsubstituierte Spezies mit den hydrophilen PEO-Segmenten von F108-Micellen über Wasserstoffbrücken-Wechselwirkung wechselwirken, um die kolloidale Emulsion zu bilden [24]. In Schritt II dienen die Spezies unter milden hydrothermalen Behandlungsbedingungen der weiteren Vernetzungspolymerisation und führen zu gleichförmigen PF-Harz/F108-Copolymerkugeln. Schließlich folgt in Schritt III den Kugeln aus PF-Harz/F108-Copolymer eine Carbonisierung bei hoher Temperatur, um die MCSs zu erhalten.
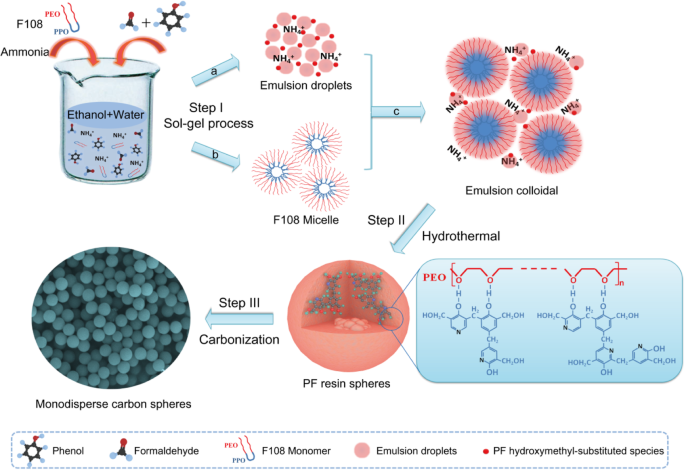
Der Syntheseprozess von MCSs
Die in Abb. 1a–d gezeigten REM-Bilder von MCSs, die mit unterschiedlichen PF-Dosierungen hergestellt wurden, zeigen, dass die MCSs eine perfekte sphärische Morphologie mit einheitlicher Größe aufweisen. TEM-Bilder in Abb. 1e–h bestätigen weiter, dass die MCSs sphärische Partikel, eine glatte Oberfläche und eine hohe Dispersität aufweisen. Der durchschnittliche Partikeldurchmesser stieg von 500 auf 2400 nm mit zunehmender Dosierung der PF-Vorstufe von 0,2 auf 0,8 ml, wie in Abb. 1i–1 gezeigt. Dies liegt daran, dass die zunehmende Konzentration des PF-Vorläufers zu Emulsionströpfchen und Kolloid mit einer größeren Größe führte und zu einem größeren endgültigen MCS-Durchmesser führte. Die Verwendung von Ammoniak in diesem System ist entscheidend für die erfolgreiche Synthese solch hochdispersiver MCS, die das NH4 . liefern können + an der Oberfläche von PF-Kugeln zu haften und die Aggregation zu hemmen. Es ist zu bemerken, dass die MCS nach der Hochtemperatur-Karbonisierung keine offensichtlichen Oberflächendefekte und Strukturkollaps aufwiesen. Dies ist der Hauptvorteil der hohen Vernetzungsreaktion zwischen Phenol und Formaldehyd. Darüber hinaus haben wir auch die Rolle des Triblockcopolymers F108 in diesem System untersucht. Zusätzliche Datei 1:Abbildung S1a zeigt das REM-Bild der Kohlenstoffkugeln, die in Abwesenheit von F108 erhalten wurden. Die Produkte haben eine ungleichmäßige Partikelgröße und stoßen auf Agglomeration. Darüber hinaus nimmt die Partikelgröße mit steigender F108-Dosierung von 20 auf 80 mg systematisch ab, und kleine Partikel und flockige Substanzen erscheinen auf der Oberfläche von Kohlenstoffkugeln und treffen schließlich auf eine starke Verklebung (Zusatzdatei 1:Abbildung S1b~d). Der Grund dafür ist, dass, wenn das Triblockcopolymer F108 im System ausreichend ist, die Oberflächenspannung abnimmt, eine stärkere Vernetzungswechselwirkung auftritt und kleinere Emulsionströpfchen und Kohlenstoffkügelchen gebildet werden. Eine geeignete F108-Konzentration kann jedoch die Oberflächenspannung und die Vernetzungswechselwirkungskräfte ausgleichen und die glatte Oberfläche und gleichgroße Kohlenstoffkügelchen erhalten. Darüber hinaus wurde auch der Einfluss der F108-Konzentration auf die Elektrodeneigenschaften der MCS untersucht, wie in Zusatzdatei 1:Abbildung S2 gezeigt. Das Ergebnis zeigt, dass das Triblockcopolymer F108 als oberflächenaktives Mittel bei der Bildung von MCSs spielte.
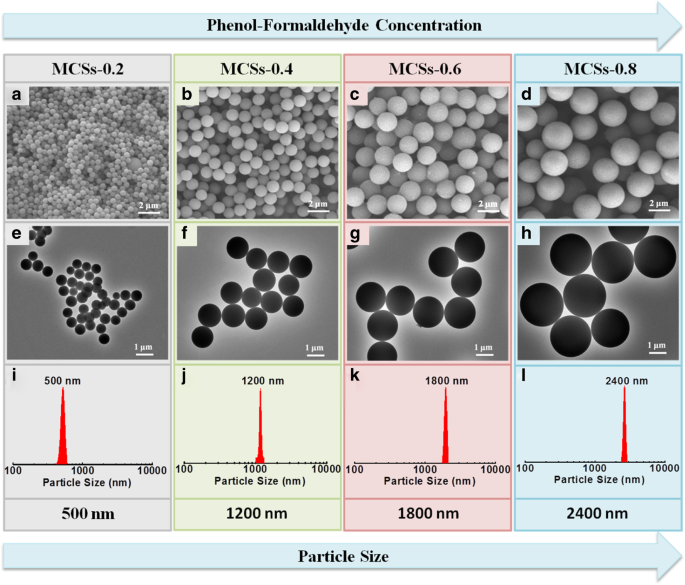
SEM- und TEM-Bilder von MCSs, die mit unterschiedlichen Phenol- und Formaldehyd-Dosierungen von a . hergestellt wurden , e 0,2 ml, b , f 0,4 ml, c , g 0,6 ml und d , h 0,8 ml bzw. ich –l Die Partikelgrößenverteilung von MCSs entsprechend den SEM-Bildern (a –d )
Diese synthetisierten MCSs können einige potenzielle Anwendungen wie Katalyse, Adsorption und Elektrodenmaterialien für Superkondensatoren und Lithium-Ionen-Batterien haben. Um die Struktureigenschaft des so hergestellten Materials zu verstehen, wurde aMCSs-0.4 als weitere Probe für die Charakterisierungsanalyse ausgewählt. Wie in 2a gezeigt, zeigt das XRD-Muster von aMCSs-0.4 zwei offensichtliche breite Beugungspeaks bei 25° und 43°, entsprechend den (002)- bzw. (100)-Gitterebenen des amorphen Kohlenstoffmaterials. Es zeigt auch die vollständige Umwandlung des PF-Harzes in Kohlenstoffmaterial und die fast vollständige Entfernung des Triblockcopolymers F108 nach der Karbonisierung an. Das Raman-Spektrum des aMCSs-0.4 (Abb. 2b) zeigt zwei typische Peaks bei 1337 cm −1 (D-Band) und 1590 cm −1 (G-Band), die den Kristalldefekten bzw. der hexagonalen graphitischen Eigenschaft von Kohlenstoffmaterialien entsprechen. Das Intensitätsverhältnis (I D /Ich G ) von Kohlenstoffmaterialien spiegelt den Graphitisierungsgrad wider [25]. Das Ich D /Ich G der aMCSs-0.4-Wert beträgt etwa 0,88, was auch die amorphen Strukturen bestätigt.
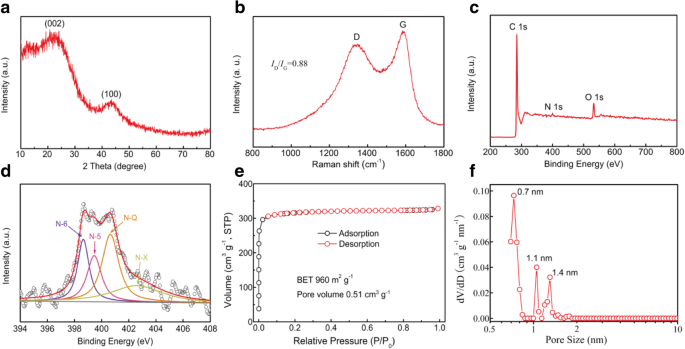
a XRD-Muster. b Raman-Spektren. c XPS-Umfragespektrum. d Hochauflösende N 1s Spektren. e Stickstoffadsorptions-/Desorptionsisothermen. f Porengrößenverteilungskurve des aMCSs-0.4-Materials
Wie in Abb. 2c gezeigt, zeigt die XPS-Untersuchung des aMCSs-0.4 drei Peaks von C 1s (285,2 eV), N 1s (400,1 eV) und O 1s (532,7 eV). Die elementaren Zusammensetzungen von C, N und O in aMCSs-0,4 betragen 92,54 Atom-%, 1,04 Atom-% bzw. 6,42 Atom-%. Die Ergebnisse legen nahe, dass Ammoniak als Stickstoffquelle fungieren kann, um das N-Element in die Kohlenstoffgerüste einzuführen. Abbildung 2d zeigt das hochauflösende N 1s-Spektrum von aMCSs-0.4. Vier Typenpeaks bei 398,6 eV, 399,4 eV, 400,6 eV und 402,4 eV korrelieren mit Pyridin-N (N-6), Pyrrol-N (N-5), Quartär-N (NQ) und Pyridin-N-oxiden (NX) bzw. [10]. Im Allgemeinen kann das Vorhandensein von funktionellen Gruppen auf Stickstoffbasis nicht nur zur zusätzlichen Pseudokapazität beitragen, sondern auch die Oberflächenbenetzbarkeit und elektrische Leitfähigkeit von Kohlenstoffmaterialien verbessern und somit die elektrochemische Leistung verbessern [3, 26].
Die N2 Adsorptions-/Desorptionsmessungen wurden durchgeführt, um die spezifischen Oberflächen und die innere Porenstruktur der hergestellten Materialien zu untersuchen. Wie in Abb. 2e gezeigt, gehört die Isotherme von aMCSs-0.4 zu einer typischen Typ-I-Kurve mit einer steilen Aufnahme bei niedrigen relativen Drücken, und ein fast horizontales Plateau bei höheren relativen Drücken zeigt die mikroporöse Struktur. Die BET-Oberflächen und das Gesamtporenvolumen von aMCSs-0.4 werden mit 960 m 2 . bestimmt g −1 und 0,51 m 3 g −1 , bzw. Die Porengrößenverteilungskurve von aMCSs-0.4 ist in 2f gezeigt, die die Mikroporenstruktur mit Durchmessern von 0.7 nm, 1.1 nm und 1.4 nm zeigt. Auch das hochauflösende TEM-Bild (Zusatzdatei 1:Abbildung S3) stimmt mit diesem Ergebnis gut überein. Die mikroporösen Kohlenstoffstrukturen werden durch die Zersetzung von F108 während der Karbonisierung und die chemische Aktivität von KOH erzeugt [27, 28].
Hier verwenden wir die aMCSs-0.4 als Elektrodenmaterialien für elektrische Doppelschichtkondensatoren (EDLCs), um ihre strukturellen und Leistungsvorteile zu demonstrieren. Die CV-Kurven der aMCSs-0.4-Elektrode zeigen rechteckige Formen bei unterschiedlichen Abtastraten von 10 bis 100 mV s −1 (Abb. 3a) und die GCD-Kurven zeigen typische Dreiecksprofile (Abb. 3b). Diese zeigen, dass die aMCSs-0.4-Materialien eine perfekte EDLC-Leistung aufweisen. Wie in Fig. 3c gezeigt, weist die aMCSs-0.4-Elektrode eine ausgezeichnete spezifische Kapazität von 310 F g –1 . auf bei einer Stromdichte von 0,5 A g −1 , das höher ist als bei anderen ähnlichen MCS-Elektroden [12,13,14]. Die hohe spezifische Kapazität profitiert von den großen Oberflächen und dotierten Heteroatomen. Darüber hinaus behält die spezifische Kapazität immer noch 200 F g –1 . bei selbst bei einer großen Stromdichte von 20 A g −1 ; es weist eine gute Kapazitätserhaltung auf. Das kinetische Verhalten von Ladungstransport und -transfer kann durch EIS untersucht werden. Das Nyquist-Diagramm der aMCSs-0.4-Elektrode (Abb. 3d) weist einen kleinen Innenwiderstand (0.45 Ω) und einen Ladungsübertragungswiderstand (0.12 ) auf, was die hohe Elektronenleitfähigkeit der präparierten aMCSs-0.4-Materialien und die gute Elektroden/Elektrolyt-Kontaktschnittstelle zeigt . Die fast vertikale Linie im Niederfrequenzbereich weist darauf hin, dass die aMCSs-0.4-Elektrode eine ideale Kondensatoreigenschaft und eine effiziente Elektrolytionendiffusion hat. Dieses Ergebnis wurde durch Bode-Plots (Abb. 3e) weiter bestätigt, die den Phasenwinkel (− 80.5°) nahe − 90° darstellen. Darüber hinaus zeigt die aMCSs-0.4-Elektrode eine gute Zyklenstabilität mit 92 % Retention über 10.000 Zyklen bei einer Stromdichte von 20 A g −1 (Abb. 3f). Daher unterstreichen alle Ergebnisse von oben klar die attraktiven potentiellen Anwendungen von MCSs für Elektroden von EDLCs.
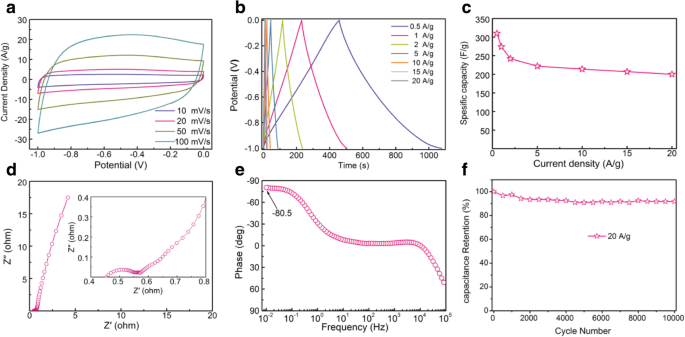
Die elektrochemischen Eigenschaften der aMCSs-0.4-Elektrode. a CV-Kurven bei verschiedenen Abtastraten von 10 bis 100 mV s −1 . b GCD-Kurven bei unterschiedlichen Stromdichten von 0,5 bis 20 A g −1 . c Spezifische Kapazität als Funktion der Stromdichten. d Das Nyquist-Diagramm und der Einschub zeigen die Vergrößerungsdiagramme im Hochfrequenzbereich. e Bode-Plot. f Zyklenleistung bei einer Stromdichte von 20 A g −1 für 10.000 Zyklen
Schlussfolgerungen
Zusammenfassend haben wir eine einfache Tensid-unterstützte hydrothermale Methode demonstriert, um MCSs effektiv zu synthetisieren. Die hergestellten MCSs haben eine perfekte sphärische Morphologie, einheitliche Größe, glatte Oberfläche und einstellbare Partikelgrößen in einem weiten Bereich von 500-2400 nm. Insbesondere ermöglicht diese Methodik dem aMCSs-0.4 einzigartige strukturelle Merkmale mit einer großen Oberfläche (960 m 2 g −1 ) und geeignete Oberflächenfunktionalität von N und O co-dotiert. Eine Hochleistungselektrode von EDLCs wurde unter Verwendung des aMCSs-0.4 als aktives Material hergestellt, das eine ausgezeichnete spezifische Kapazität (310 F g −1 .) lieferte bei 0,5 A g −1 ) und hervorragende Zyklenstabilität (92% Kapazitätserhalt nach 10.000 Zyklen). Diese Forschung bietet eine neue Möglichkeit für die Herstellung von MCSs mit potenziellen Anwendungen.
Abkürzungen
- Lebenslauf:
-
Zyklische Voltammetrie
- EDLCs:
-
Elektrische Doppelschichtkondensatoren
- EIS:
-
Elektrochemische Impedanzspektroskopie
- GCD:
-
Galvanostatische Aufladung/Entladung
- MCS:
-
Monodisperse Kohlenstoffkugeln
- PF:
-
Phenol und Formaldehyd
Nanomaterialien
- Einfache Synthese und optische Eigenschaften kleiner Selen-Nanokristalle und -Nanostäbe
- Nanostrukturiertes Siliciumdioxid/Gold-Cellulose-gebundenes Amino-POSS-Hybrid-Komposit über den Sol-Gel-Prozess und seine Eigenschaften
- Synthese und elektrochemische Eigenschaften von LiNi0.5Mn1.5O4 Kathodenmaterialien mit Cr3+ und F− Verbunddotierung für Lithium-Ionen-Batterien
- Synthese wasserlöslicher Antimonsulfid-Quantenpunkte und ihre photoelektrischen Eigenschaften
- Einfache Synthese von Wurmloch-ähnlichem mesoporösem Zinnoxid durch verdunstungsinduzierte Selbstorganisation und die verbesserten Gassensoreigenschaften
- Auswirkung der Synthesemethode von La1 − xSr x MnO3 Manganit-Nanopartikeln auf ihre Eigenschaften
- Eintopfsynthese von Cu2ZnSnSe4-Nanoplatten und ihre durch sichtbares Licht getriebene photokatalytische Aktivität
- Umweltfreundliche und einfache Synthese von Co3O4-Nanodrähten und ihre vielversprechende Anwendung mit Graphen in Lithium-Ionen-Batterien
- Abhängigkeit der Nanopartikeltoxizität von ihren physikalischen und chemischen Eigenschaften
- Material und optische Eigenschaften von fluoreszierenden Kohlenstoff-Quantenpunkten, die durch hydrothermale Reaktion aus Zitronensaft hergestellt werden



