Schnelle Bildung von Ag-Nanofasern durch Pt-Nanopartikel-unterstützte H2-freie Reduktion von Ag+-haltigen Polymeren
Zusammenfassung
Eindimensionale auf Ag-Nanostrukturen basierende Netzwerke haben als transparente leitfähige Materialien der nächsten Generation große Aufmerksamkeit erregt. Ag-Nanofasern (NFs) mit hohen Aspektverhältnissen verringern die für die Perkolation erforderliche Anzahldichte; daher bilden sie qualitativ überlegene transparente leitfähige Filme. Diese Studie berichtet über eine neuartige Methode zur schnellen Herstellung von Ag-NFs über Pt-Nanopartikel-unterstütztes H2 -freie Reduktion von Festkörper-AgNO3 . Unsere Ergebnisse zeigten zunächst, dass Polymere in Gegenwart von Pt-Nanopartikeln eine Quelle für Wasserstoffgas sein können; Ag-NFs mit Seitenverhältnissen über 10 5 wurden hier durch Erhitzen von AgNO3 -enthaltende polymere NF in kurzer Zeit und im Freien. Unsere Methode reduzierte nicht nur erfolgreich die Menge an Polymerrückständen, die häufig in gesponnenen NFs anzutreffen sind, sondern schuf auch ein effektives selbsttragendes Reduktionssystem, das keine externe Reduktionsgaszufuhr erfordert. Die erhaltenen Ag-NF-Netzwerke waren hochleitfähig und transparent. Darüber hinaus wurde der Mechanismus der Ag-NF-Bildung untersucht. Wir zeigen, dass die vorgeschlagene Methode ein hohes Potenzial besitzt, um auf einfache und schnelle Weise hohe Ausbeuten an Ag-NFs zu produzieren.
Einführung
Transparente leitfähige Filme werden häufig als transparente Elektroden in Flüssigkristallanzeigen, Solarzellen, intelligenten Fenstern, Touchscreens [1,2,3,4,5,6], transparenten Filmheizungen [7,8,9,10,11] verwendet. und Materialien zur Abschirmung elektromagnetischer Wellen [12,13,14]. Das neueste transparente leitfähige Material, Indium-Zinn-Oxid (ITO), weist eine hervorragende Leitfähigkeit und Transparenz im sichtbaren Bereich auf [15]. Mit der steigenden Nachfrage nach flexiblen leitfähigen Materialien in den letzten Jahren haben jedoch der Mangel an Flexibilität von ITO und die Knappheit von In die Forschung nach praktikablen Alternativen veranlasst. Zahlreiche Kandidaten, wie Kohlenstoffnanoröhren [1, 7, 16], Graphit [8, 17, 18], leitfähige Polymere [19, 20] und metallische Nanodrähte (NWs) [3,4,5, 9,10,11 ], wurden ausführlich untersucht. Insbesondere Ag-NW-Netzwerke [3, 4, 9] scheinen vielversprechende Alternativen zu sein. Neben der hervorragenden Leitfähigkeit, Dehnbarkeit und Flexibilität, die sich aus den metallischen Eigenschaften von Ag ergibt, gewährleistet ein Drahtdurchmesser kleiner als die Wellenlängen des sichtbaren Lichts eine hohe Transparenz des Netzwerks. Im Vergleich zu ITO haben Ag-NW-Netzwerke die Vorteile eines breiteren Wellenlängenbereichs mit außerordentlich hoher Transparenz [21]. Diese Eigenschaften können auf Photovoltaikanlagen angewendet werden, um die Umwandlungseffizienz von Solarzellen zu verbessern.
Derzeit ist der Polyol-Ansatz [22, 23] der vielversprechendste Weg zur Synthese von Ag-NWs. Die nach diesem lösungsbasierten Verfahren synthetisierten Ag-NWs können leicht zu einem Netzwerk dispergiert werden. Die Kontaktstellen zwischen den NWs beeinflussen jedoch stark die Eigenschaften der Netzwerke. Der hohe Übergangswiderstand erhöht den Schichtwiderstand stark, während eine schwache Bindung die mechanischen Eigenschaften bei Verformung des Netzwerks verschlechtert. Frühere Studien haben gezeigt, dass längere NWs qualitativ besser transparente leitfähige Filme ergeben könnten, da eine Verdoppelung der Länge der NWs die für die Perkolation erforderliche Anzahldichte um den Faktor vier verringert [24]. Dennoch haben bestehende Synthesemethoden die Länge von Ag-NWs auf mehrere zehn Mikrometer und die Seitenverhältnisse auf 10 2 . begrenzt –10 3 ; daher bleiben die durch die Kontaktpunkte verursachten Probleme eine Herausforderung.
Im Vergleich zu Ag-NWs haben Ag-Nanofasern (NFs) ungefähr den gleichen Durchmesser, sind jedoch viel länger (normalerweise mehrere zehn Millimeter) und haben ein höheres Seitenverhältnis, das 10 5 . erreichen kann –10 6 . Es gibt jedoch nur wenige Berichte über die Synthese von Ag-NFs. Obwohl Ag + -haltige Vorläufer-NFs können durch Elektrospinnen [2] und Blasspinnen [25] in Massenproduktion hergestellt werden. Zu den Herausforderungen dieser Synthese gehört die Reduktion von Ag + um kontinuierliche Ag-NFs zu bilden und die Zersetzung der restlichen isolierenden Polymere, die aus der Vorläuferlösung stammen. Kürzlich haben Lin et al. berichtete über eine Methode zur Reduktion von Silbernitrat (AgNO3 ) NFs durch UV-Bestrahlung [6]. Nach 3 Stunden UV-Bestrahlung wurde ein großflächiges Ag-NF-Netzwerk erhalten, um Ag + . zu reduzieren . Trotzdem war der Reduktionsprozess relativ lang und die Zersetzung von Restpolymeren blieb ein Problem. Die katalytische Wirkung von Metallnanopartikeln [26, 27] hat uns jedoch dazu inspiriert, Polymere in Gegenwart bestimmter Metallnanopartikel effektiv einzusetzen.
Diese Studie berichtet über eine einfache Methode zur Herstellung von Ag-NFs. Unsere Ergebnisse deuten darauf hin, dass Polymere in Gegenwart von Pt-Nanopartikeln eine Quelle für Wasserstoffgas sein können; wir erhielten Ag-NFs mit hohen Aspektverhältnissen durch Erhitzen von AgNO3 -haltige Polymer-NFs. Die resultierenden Ag-NF-Netzwerke waren hochleitfähig und transparent. Dieses vorgeschlagene Verfahren hat ein hohes Potenzial, um auf einfache und schnelle Weise hohe Ausbeuten an Ag-NFs zu erzeugen.
Experimentell
Das experimentelle Verfahren zur Herstellung der Ag-NF-Netzwerke ist in Abb. 1 dargestellt. Pt-Nanopartikel wurden auf einem 18 × 18 mm 2 . abgeschieden Mikrodeckglassubstrat mit einer Dicke von 120–170 µm unter Verwendung eines Magnetron-Sputtersystems (SC-701HMCII, SANYU ELECTRON Co., Ltd.) bei 23 °C (Abb. 1a). Die Reinheit des Pt-Targets betrug 99,99 %. Der Abscheidungsdruck und die Abscheidungsrate betrugen 1,5 Pa bzw. 2,5 Å/s bei 25 mA und wurden bestimmt, um eine homogene Verteilung von Nanopartikeln in einer genauen Menge zu erhalten. Die Abscheidungszeit betrug 4 s, danach betrug die Dicke des abgeschiedenen Pt 1 nm. Bemerkenswerterweise führte diese Dicke nicht zu einem kontinuierlichen Pt-Film, sondern zu diskontinuierlichen Inseln (Nanopartikeln). Dieses Phänomen ist als Anfangsstadium des Wachstums dünner Metallfilme bekannt [28,29,30]. Diese Pt-Nanopartikel sind entscheidend für die Herstellung von Ag-NFs, wie in späteren Abschnitten ausführlich diskutiert wird. Nach der Abscheidung der Pt-Nanopartikel wird ein elektrogesponnenes AgNO3 /Polyvinylalkohol (PVA)/Polyvinylpyrrolidon (PVP)-gemischtes NF-Netzwerk wurde auf dem Substrat abgeschieden, indem eine Spannung von 20 kV an das AgNO3 . angelegt wurde /PVA/PVP wässrige Lösung für 5 Minuten in einem Sammelabstand von 15 cm (Abb. 1b). Eine Spritze mit einer Nadel von 0,41 mm Innendurchmesser wurde mit einer Mikropumpe verbunden. Die Flussrate der Mikropumpe wurde auf 0,05 ml/h eingestellt. Die gepumpte Lösung bestand aus AgNO3 (Pulver, Reinheit 99,8 %), PVA (Polymerisationsgrad:1500), PVP und entionisiertes Wasser in einem Gewichtsverhältnis von 10:8,5:4:100 in Gew.-%. Die Viskosität der Lösung betrug 277 mPa s. Die Molekulargewichte von PVA und PVP betragen 6,6 × 10 4 g/mol und 4 × 10 4 g/mol bzw. PVA ist ein übliches Polymermaterial, das für das Elektrospinnen verwendet wird, während PVP als molekulares Abdeckmittel verwendet wird. Schließlich wurden die Proben an der Luft bei 250 °C für 30 Minuten erhitzt, um AgNO3 . zu reduzieren zu Ag in Gegenwart von Pt-Nanopartikeln (Abb. 1c). Die Produkte wurden mit der Vier-Sonden-Methode gemessen und durch Rasterkraftmikroskopie (AFM:Dimension Icon, Bruker Japan Co., Ltd.), Röntgenbeugung (XRD:Smart Lab, Rigaku Co., Ltd.), Feld . analysiert -Emissions-Rasterelektronenmikroskopie (FE-SEM:SU-70, HITACHI Co., Ltd.), ringförmiges Dunkelfeld-Rastertransmissionselektronenmikroskop mit großem Winkel (HAADF-STEM:Talos F200X, FEI Co., Ltd.), energiedispersiv Röntgen (EDX) und Raman-Spektrometrie (RAMANtouch, Nanophoton Co., Ltd.).
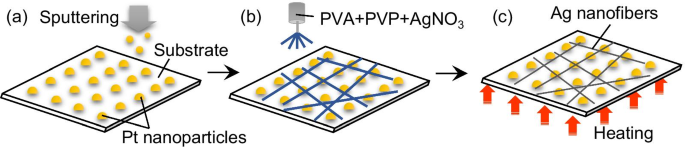
Schema, das den Herstellungsprozess des Ag-NF-Netzwerks zeigt:a Pt-Sputtern, b Elektrospinnen des AgNO3 /PVA/PVP-gemischtes NF-Netzwerk und c Erhitzen in Luft
Ergebnisse und Diskussion
Abbildung 2a zeigt die Zustände der Proben während des Experiments. Jedes Exemplar ist mit einer gestrichelten Linie gekennzeichnet. Die Abbildungen von links nach rechts zeigen das vorbereitete Glassubstrat, das Glas nach dem Pt-Sputtern, das NF-Netzwerk nach dem Elektrospinnen, die Probe nach dem Erhitzen (die gelben Teile sind Au-Elektroden mit einer Größe von 18 × 1,5 mm 2 zur Widerstandsmessung verwendet) und ein 15 nm dicker Ag-Film, der als Referenz auf einem Glassubstrat abgeschieden wurde. Abbildung 2b zeigt ein AFM-Bild von Pt, das mit 2,5 Å/s für 8 s auf einem Glassubstrat abgeschieden wurde. Die Bildung eines diskontinuierlichen Films mit einer rauen Oberfläche und einer großen Anzahl kleiner Löcher mit einem Durchmesser von 10–20 nm und einer Tiefe von 2–3 nm wurde bestätigt. Die Tiefe stimmte in hohem Maße mit der gewünschten Filmdicke überein. Die Pt-Nanopartikel waren in Clustern mit einer durchschnittlichen In-Plane-Größe von 32 nm verteilt. Dies kann daran liegen, dass Metalle mit hohen Siedepunkten hohe Übersättigungswerte und kleine kritische Kerne aufweisen und leicht kondensieren [31]. Wir glauben, dass die Pt-Nanopartikel in einem stärker dispergierten Zustand verteilt sind, wenn die Filmdicke 1 nm beträgt. Nach dem Erhitzen zeigt die Probe eine hohe Transparenz im sichtbaren Bereich (Abb. 2c). Das lange NF-perkolierte Netzwerk ist in der vergrößerten Ansicht der REM-Aufnahme (Abb. 2c) deutlich zu erkennen. Der Flächenanteil des Netzwerks, gemessen durch Anwenden von Schwellenwerten auf die SEM-Mikroaufnahme unter Verwendung einer Bildanalysesoftware (WinROOF2015, MITANI Corporation), beträgt ungefähr 47%. Die HAADF-STEM-Analyse (Abb. 2d) zeigt, dass die NFs einen Durchmesser von mehreren zehn Nanometern hatten und eine polykristalline Mikrostruktur aufwiesen. Die elektrogesponnenen NFs überspannten das Substrat; daher war ihre Länge ungefähr 18 mm oder sogar länger. Daher erreichte das Seitenverhältnis der aktuellen NFs eine Größenordnung von 10 5 oder noch größer. Alle Peaks im XRD-Muster (Abb. 2e) stimmen gut mit denen der kubisch-flächenzentrierten Struktur von Ag überein, was darauf hindeutet, dass Ag-NFs erfolgreich erhalten und fein kristallisiert wurden. Die Ergebnisse der EDX-Analyse (Abb. 2f–i) zeigen, dass das Netzwerk aus Ag-NFs ohne C-bezogene Verteilung in den NFs bestand. Darüber hinaus wurde Pt nicht nachgewiesen, wahrscheinlich weil es nur in geringer Menge vorhanden war. Die detektierten Si-, O-, Na-, Al- und K-Elemente (Abb. 2i) stammen vom Glassubstrat und können daher ignoriert werden. Die gemessenen Strom-Spannungs-Kurven (Abb. 2j) zeigen, dass die gebildeten Ag-NF-Netzwerke metallische Eigenschaften haben und ihre Schichtwiderstände nur einige zehn Ω/sq betragen, was mit kommerziell erhältlichen ITOs vergleichbar ist. Das vorliegende Ag-NF-Netzwerk kann leicht als flexible transparente Elektrode auf ein Foliensubstrat aufgebracht werden (z. B. siehe Zusatzdatei 1:Abb. S1).
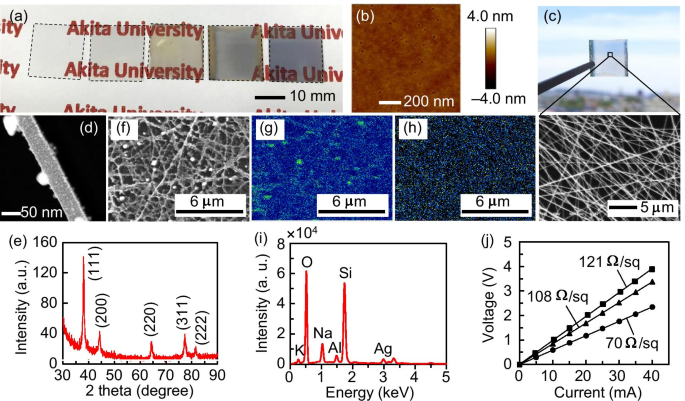
a Zustände der Proben während des Experiments. b AFM-Bild von Pt, das auf ein Glassubstrat gesputtert wurde. c Optische und FE-REM-Aufnahmen der Probe nach dem Erhitzen. d HAADF-STEM-Bild von Ag NF. e XRD-Muster von Ag NF. EDX-Analyseergebnisse des Ag-NF-Netzwerks:f SEM-Bild, g Ag und h C-Verteilungszuordnungen und i qualitative Analyse des in (f . gezeigten Bereichs ). j Strom-Spannungs-Kurven der Proben gemessen mit der Vier-Sonden-Methode
Infolgedessen wurden die Rolle von Pt-Nanopartikeln und die Bedeutung des Erhitzens in Luft statt im Vakuum in Frage gestellt. Daher werden diese Aspekte in den folgenden Abschnitten erörtert.
Der ursprüngliche Zweck der Abscheidung von Pt-Nanopartikeln bestand darin, den Elektrospinnprozess so zu verbessern, dass mehr AgNO3 /PVA/PVP-NFs könnten auf dem Isolierglassubstrat abgeschieden werden. Interessanterweise haben wir beim Erhitzen des AgNO3 /PVA/PVP NFs mit Pt-Nanopartikeln bei 250 °C erhielten wir Ag-NFs. Die Ergebnisse der XRD- und EDX-Analyse (Abb. 2e–i) unterstützen diese neue Erkenntnis nachdrücklich. Es ist höchst unwahrscheinlich, dass Ag durch die thermische Zersetzung von AgNO3 . entstanden ist nach dem Erhitzen auf 250 °C wegen der Zersetzung von AgNO3 tritt bei Temperaturen über 500 °C auf [32]. Daher ist es wahrscheinlicher, dass Ag aus der Wasserstoffreduktion von AgNO3 . hergestellt wurde . Darüber hinaus stammte das Wasserstoffgas höchstwahrscheinlich von PVA und PVP, die in den Experimenten verwendet wurden. Bis heute gab es jedoch keine Berichte darüber, dass Wasserstoffgas direkt aus der thermischen Zersetzung von PVA oder PVP erzeugt werden kann. Die meisten Berichte haben gezeigt, dass das Hauptzersetzungsprodukt von PVA bei etwa 200 °C H2 . ist O [33,34,35,36]. Wir postulieren, dass Pt-Nanopartikel der entscheidende Faktor für den Reduktionsprozess sind. Pt war Gegenstand vieler Forschungen und ist als Katalysator für chemische Reaktionen bekannt.
Die obige Diskussion wird durch Gl. (1) und (2) unten angegeben.
$${\left[{\textrm{CH}}_{2}\textrm{CHOH}\right]}_{n}\begin{array}{c}\stackrel{\textrm{ Pt}}{\to }\\ {\mathrm{ in~Luft}}\end{array}{\mathrm{CO}}_{2}+{\mathrm{H}}_{2}+{\mathrm{H}}_{ 2}\mathrm{O}$$ (1)und
$${\mathrm{H}}_{2}+{\mathrm{Ag}}^{+}\to \mathrm{Ag}+{\mathrm{H}}^{+}.$$ (2)Die Hauptkomponenten von PVA ([CH2 CHOH]n ) und PVP ([C6 H9 NEIN]n ) sind ähnlich, und PVA macht den Großteil der Elektrospinnlösung aus; Daher konzentrieren wir uns in der folgenden Diskussion auf PVA. Die in Gl. (1) und (2) wurden basierend auf unseren Spekulationen vorgeschlagen, da es sehr schwierig ist zu beweisen, dass PVA durch thermische Zersetzung in Gegenwart von Pt-Nanopartikeln Wasserstoffgas produziert. Nach unseren experimentellen Ergebnissen und anderen umfassenden Überlegungen scheinen diese Reaktionen jedoch am wahrscheinlichsten aufgetreten zu sein. Um die katalytische Wirkung der Pt-Nanopartikel zu verifizieren, wurden auch andere Metallnanopartikel abgeschieden (ähnlich dem in Abb. 1a gezeigten Prozess) und die Experimente wurden wiederholt. Wie in Tabelle 1 gezeigt, wurden Ag- und Au-Nanopartikel auf Glassubstraten abgeschieden. Ihre Dicke wurde auf 1 nm beschränkt, was einer ähnlichen Größe wie die der Pt-Nanopartikel entspricht. Zum Vergleich wurden auch Glassubstrate ohne jegliche Nanopartikelabscheidung hergestellt. Um die Reproduzierbarkeit der Versuchsergebnisse zu gewährleisten, wurden für jede Art von Metallnanopartikeln mindestens vier Prüfkörper hergestellt. Diese Teststücke wurden dann einem Elektrospinnen (Abb. 1b) und Erhitzen (Abb. 1c) unter den gleichen Bedingungen unterzogen, die für die Pt-Nanopartikel verwendet wurden. Der Vergleich der Schichtwiderstände vor und nach dem Erhitzen zeigt, dass nur die Schichtwiderstände der Prüfkörper mit Pt-Nanopartikeln von isoliert auf einige zehn bis hundert Ω/sq stark reduziert wurden. Dieses Ergebnis impliziert, dass das AgNO3 Komponente auf Ag geändert. Daraus schließen wir, dass Pt-Nanopartikel eine entscheidende Rolle bei der erfolgreichen Herstellung von Ag-NFs spielen. Aufgrund der Anwesenheit von Pt-Nanopartikeln zersetzten sich die isolierenden Polymermaterialien (PVA und PVP) nicht nur thermisch, sondern produzierten auch effektiv Wasserstoffgas, das AgNO3 . reduzieren konnte .
Die Reduktion von Metallionen mit reduzierenden Gasen wird üblicherweise im Vakuum durchgeführt. Daher wird die Größe der Probe durch die Vakuumkammer begrenzt, und es wird viel Zeit damit verbracht, das Vakuum zu erzeugen. Glücklicherweise erfordert unsere Methode keine Vakuumumgebung, da wir festgestellt haben, dass eine Umgebung im Freien besser für die Herstellung hochleitfähiger Ag-NFs geeignet ist. Abb. 3a zeigt beispielsweise eine Probe (hergestellt nach den gleichen Verfahren wie in Abb. 1a, b) nach dem Erhitzen unter Vakuum (unter Verwendung einer Flussrate von 200 sccm Ar-Gas und einem Druck von 130 Pa bei 250 °C für 30 Minuten ). Im Gegensatz zu den an Luft erhitzten Proben waren die unter Vakuum erhitzten Stücke durchscheinend und von hellbrauner Farbe. Bemerkenswert ist, dass ihre Schichtwiderstände bis zu mehreren Tausend Ω/sq hoch waren, was ein bis zwei Größenordnungen höher ist als bei an Luft erhitzten. Die Ergebnisse der EDX-Analyse (Abb. 3b–e) zeigen, dass in den NFs eine signifikante Menge C vorhanden ist, während das nachgewiesene Si, O, Na und Al (Abb. 3e) vom Glassubstrat stammt und daher ignoriert wurde. Die Raman-spektroskopische Analyse (Abb. 3f) zeigt, dass diese Kohlenstoffatome eine amorphe Struktur haben. Zwei charakteristische Raman-Peaks bei ungefähr 1325 und 1583 cm −1 nachgewiesen wurden, die mit den an anderer Stelle berichteten Peaks übereinstimmen [6]. Darüber hinaus wurde, wie in Abb. 3f gezeigt, ein Anstieg der Basislinie des Raman-Spektrums aufgrund von Fluoreszenz festgestellt, was eine hohe Wahrscheinlichkeit von organischen Reststoffen (Polymeren) impliziert. Daher zeigten die unter Vakuum erhitzten Teststücke sehr große Schichtwiderstände.
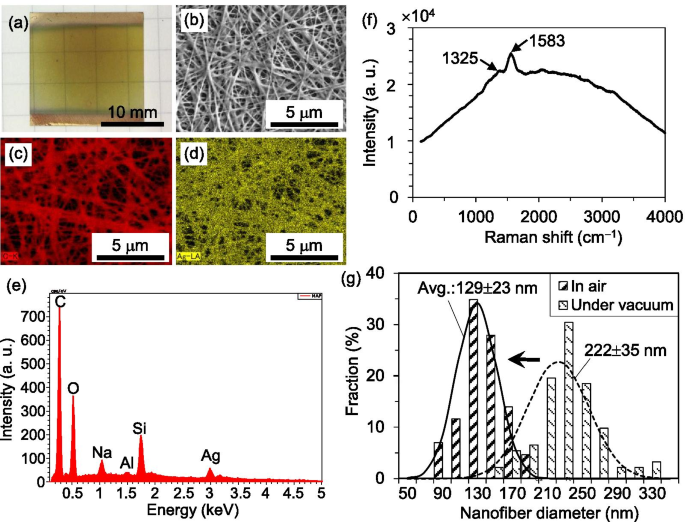
Probe nach dem Erhitzen unter Vakuum mit a Ergebnisse der optischen Bild- und EDX-Analyse:b SEM, c C und d Ag-Verteilungsabbildungen; e qualitative Analyse des in (b gezeigten Bereichs ); und f das Raman-Spektrum. g Histogramme des NF-Durchmessers nach Erhitzen an Luft und unter Vakuum
Abbildung 3g zeigt die Histogramme des NF-Durchmessers nach dem Erhitzen an Luft und unter Vakuum. Die Durchmesser wurden mit der Messfunktion von SEM gemessen. Unter jeder Heizbedingung wurden mehr als 40 NFs zufällig für die SEM-Beobachtungen (bei 5000 × Vergrößerung) und die nachfolgenden Messungen ausgewählt. Im Vergleich zu denen, die unter Vakuum erhitzt werden, ist der durchschnittliche Durchmesser der NFs nach dem Erhitzen an der Luft etwa 100 nm dünner. Dies kann das Ergebnis der Oxidation von amorphen Kohlenstoffen und ihrer Freisetzung durch die Dampfphase sein (CO2 ). Die Entfernung von amorphen Kohlenstoffen aus den NFs verringerte möglicherweise die Schichtwiderstände stark. Die obige Diskussion kann durch die folgende chemische Reaktion erklärt werden:
$${\left[{\textrm{CH}}_{2}\textrm{CHOH}\right]}_{n}\begin{array}{c}\stackrel{\textrm{ Pt}}{\to }\\ {\mathrm{ Vakuum}}\end{array}\mathrm{C}+{\mathrm{H}}_{2}+{\mathrm{H}}_{2}\mathrm{O }.$$ (3)Das bevorzugte Produkt der thermischen PVA-Zersetzung ist H2 O während des Erhitzens unter Vakuum; daher kann C nicht durch Sauerstoff oxidiert werden und es werden restliche amorphe Kohlenstoffe erzeugt. Im Gegensatz dazu, wie in Gl. (1) liefert die Anwesenheit von Luft während des Erhitzens den Sauerstoff, der für die Oxidation von Kohlenstoff benötigt wird. Daher ist eine Umgebung im Freien besser geeignet, um hochleitfähige Ag-NFs herzustellen.
Neben der Bereitstellung eines einfachen Herstellungsverfahrens überlegten wir, ob das vorgeschlagene Verfahren effizienter und energiesparender sein könnte. Abbildung 4 zeigt die In-situ-Messungen des Schichtwiderstands. Die Probe wurde unter Vakuum (mit einer Flussrate von 200 sccm Ar-Gas und einem Druck von 130 Pa bei 250 °C für 30 Minuten) vorgewärmt, sodass ihr anfänglicher Schichtwiderstand ungefähr 6340 Ω/sq betrug. Anschließend wurde die Probe an der Luft von 150 auf 250 °C erhitzt. Der Verlauf der Heiztemperatur wird in Fig. 4 durch die durchgezogene Linie dargestellt, während der Schichtwiderstand durch die gestrichelte Linie dargestellt wird. Der Schichtwiderstand stieg fast linear an, wenn die Probe von 150 auf 200 °C erhitzt wurde, da der spezifische elektrische Widerstand mit steigender Temperatur zunahm. Trotzdem begann der Schichtwiderstand bei 200 °C schnell abzunehmen, obwohl die Heiztemperatur weiter anstieg. Nach ungefähr 55 Minuten fiel der Schichtwiderstand von 6420 Ω/sq auf ungefähr 400 Ω/sq, und dann begann der abnehmende Trend in die Sättigung zu gehen. Dieses Phänomen könnte durch die Oxidation amorpher Kohlenstoffe und deren Freisetzung, wie oben diskutiert, verursacht worden sein. Daher kann die Heiztemperatur für die Herstellung von Ag-NFs auf etwa 200 °C gesenkt werden. Dieser Fortschritt hilft nicht nur beim Energiesparen, sondern erweitert auch die Möglichkeiten für hitzebeständige Untergründe.
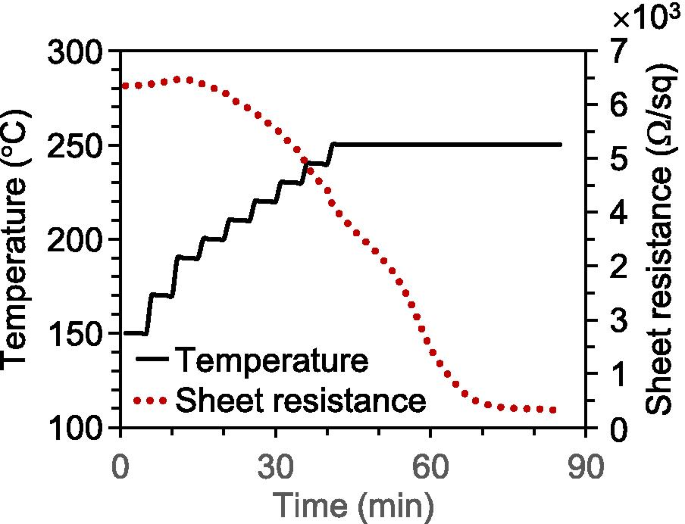
Variation des Schichtwiderstandes mit Heiztemperatur und -zeit
Schlussfolgerungen
Zusammenfassend lässt sich sagen, dass eine einfache Methode zur Herstellung von Ag-NFs durch Pt-Nanopartikel-unterstützte Reduktion von AgNO3 vorgeschlagen und der Mechanismus untersucht. Obwohl das Verfahren weiter verbessert werden muss, hat es ein hohes Potenzial, um auf einfache, schnelle und wirtschaftliche Weise hohe Ausbeuten an Ag-NFs mit hohen Aspektverhältnissen und transparenten leitfähigen Filmen herzustellen. Pt-Nanopartikel können auf einem Substrat durch Vakuumabscheidung oder unter Verwendung einer handelsüblichen Pt-Dispersionsflüssigkeit abgeschieden werden. Theoretisch können die meisten Silbersalze wie Silberchlorid, Silbersulfid und Silberfluorid reduziert werden; daher die Quelle von Ag + ist nicht auf AgNO3 . beschränkt . Darüber hinaus sagen wir voraus, dass die anderen Metalle der Platingruppe, wie Pd und Rh, aufgrund ihrer ähnlichen chemischen Eigenschaften die gleiche katalytische Wirkung wie Pt entfalten können.
Verfügbarkeit von Daten und Materialien
Alle während dieser Studie generierten oder analysierten Daten sind in diesem Artikel und seiner ergänzenden Informationsdatei enthalten.
Abkürzungen
- AFM:
-
Rasterkraftmikroskopie
- AgNO3 :
-
Silbernitrat
- EDX:
-
Energiedispersive Röntgenstrahlung
- FE-REM:
-
Feldemissions-Rasterelektronenmikroskopie
- HAADF-STEM:
-
Ringförmige Dunkelfeld-Rastertransmissionselektronenmikroskopie mit großem Winkel
- ITO:
-
Indium-Zinn-Oxid
- NW:
-
Nanodraht
- NF:
-
Nanofaser
- PVA:
-
Polyvinylalkohol
- PVP:
-
Polyvinylpyrrolidon
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Vollständige Terahertz-Polarisationskontrolle mit erweiterter Bandbreite über dielektrische Metaoberflächen
- Einfluss der Bedingungen der Bildung von Pd/SnO2-Nanomaterialien auf die Eigenschaften von Wasserstoffsensoren
- Morphologische Evolution von Si(001)-Substraten mit Grubenmuster durch Reduktion der Oberflächenenergie
- Kontrollieren des Wachstums von Indiumselenid (In2Se3)-Nanodrähten mit hoher Gleichmäßigkeit durch den schnellen thermischen Glühprozess bei niedrigen Temperaturen
- Herstellung und Charakterisierung eines neuen anodischen Tio2-Kohlenstoff-Nanofaser-Verbundkatalysators für eine Direkt-Methanol-Brennstoffzelle mittels Elektrospinnverfahren
- Verbesserte Antitumorwirksamkeit und Pharmakokinetik von Bufalin durch PEGylierte Liposomen
- Erhöhte Protonenleitfähigkeit und Methanolpermeabilitätsreduktion durch Natriumalginat-Elektrolyt-sulfonierte Graphenoxid-Biomembran
- Sauerstoffreduktionsreaktion auf PtCo-Nanokatalysator:(Bi)Sulfat-Anionenvergiftung
- Abstimmung des Gleit-Roll-Bewegungsmodus von Kohlenstoffnanoröhren über Hydroxylgruppen
- In-situ-Synthese von bimetallischen Wolfram-Kupfer-Nanopartikeln durch thermisches Hochfrequenzplasma (RF)



