Mesoporöse Silica-Nanopartikel-basierte Kombination von NQO1-Inhibitor und 5-Fluorouracil für eine starke Antitumorwirkung gegen Plattenepithelkarzinom im Kopf-Hals-Bereich (HNSCC)
Zusammenfassung
Plattenepithelkarzinome im Kopf-Hals-Bereich (HNSCC) gehören zu den tödlichsten Krebsarten und stammen zu 90 % aus Plattenepithelkarzinomen. NAD(P)H:Chinon-Oxidoreduktase 1 (NQO1), ein bei Plattenepithelkarzinomen überexprimiertes Enzym, spielt eine wichtige Rolle bei der Proliferation und Chemoresistenz. Die Hauptziele waren die Untersuchung der hemmenden Wirkung von ß-Lapachon (ARQ761 in klinischer Form) bei HNSCC und die Untersuchung der kombinatorischen Wirkung von 5-FU und ß-lap bei der Verbesserung der therapeutischen Wirksamkeit bei HNSCC. Mit 5-FU/ß-lap beladene, aus Lipiddoppelschichten aufgebaute mesoporöse Siliciumdioxid-Nanopartikel wurden hergestellt und auf ihre physikalisch-chemischen und biologischen Eigenschaften untersucht. ß-lap zeigte eine konzentrationsabhängige Hemmung der NQO1-Enzymaktivität in Cal33-Zellen. Bemerkenswerterweise wurde eine signifikante Hemmwirkung bei einer Dosis von 20–50 µg/ml ß-lap beobachtet. Die Kombination von 5-FU+ß-lap führte zu einer geringeren Lebensfähigkeit der Zellen; vor allem zeigten 5-FU/ß-lap-beladene mesoporöse Siliziumdioxid-Nanopartikel (FNQ-MSN) eine signifikant geringere Zelllebensfähigkeit im Vergleich zu den einzelnen Wirkstoff- oder physikalischen Kombinationen. ß-lap führte zu einer Abnahme der Proteinbande von NQO1 im Vergleich zur Kontrolle; jedoch wurde die bemerkenswerteste Abnahme des NQO1-Spiegels in der mit FNQ-MSN behandelten Zellgruppe beobachtet. FNQ-MSN führte zu mehr als 60 % der Zellapoptose (frühe und späte Apoptose) und einer vorherrschenden nuklearen Fragmentierung von Krebszellen, was auf die überlegene Antikrebswirkung einer trägerbasierten Kombinationstherapie hinweist. Bei der physikalischen Mischung von 5-FU+ß-lap wurde eine bemerkenswerte Abnahme des Tumorvolumens beobachtet; jedoch verzögerte die kombinierte Behandlung von trägerbasiertem 5-FU und ß-lap (FNQ-MSN) signifikant das Tumorwachstum und verlängerte das Überleben von tumortragenden Xenotransplantat-Mäusen. Diese Ergebnisse deuten auf das Potenzial des NQO1-Inhibitors zur Verbesserung des chemotherapeutischen Potenzials von 5-FU bei der Behandlung von HNSCC hin.
Einführung
Plattenepithelkarzinome im Kopf-Hals-Bereich (HNSCC) gehören zu den tödlichsten Krebsarten und stammen zu 90 % aus Plattenepithelkarzinomen [1]. HNSCC ist von Natur aus stark angiogen und sein Gefäßsystem exprimiert verschiedene Zytokine, darunter Fibroblasten-Wachstumsfaktoren (FGFs) und vaskuläre endotheliale Wachstumsfaktoren (VEGFs), die mit einer höheren Metastasierung und einem schlechten Überleben verbunden sind [2]. Die Inzidenz von HNSCC in China ist bei krebsbedingten Todesfällen an sechster Stelle, wobei 2015 etwa 250.000 neue Fälle registriert wurden und 77.500 Todesfälle. Die 5-Jahres-Gesamtüberlebensrate des HNSCC ist aufgrund der Faktoren wie Aggressivität, frühes Rezidiv, hohe Metastasierung und hohe Sterblichkeitsrate aufgrund einer schlechten Prognose sehr niedrig [3]. Die wichtigste Behandlungsoption bei HNSCC ist ein chirurgischer Eingriff gefolgt von einer Strahlen- oder Chemotherapie. Genauer gesagt würde eine Chemotherapie, wenn sie in frühen Stadien oder in postoperativen Stadien wirksam eingesetzt wird, dem Tumorwachstum entgegenwirken [4, 5]. Eine wirksame Chemotherapie wird die Krebszellen im Tumorgewebe beseitigen und den Tumorrückfall hemmen. Allerdings führt eine Langzeit-Chemotherapie auf Basis eines Einzelwirkstoffs häufig zu Arzneimittelresistenzen und verringerter therapeutischer Wirksamkeit [6]. Daher ist es notwendig, innovative Strategien anzuwenden, um das Überleben und die Lebensqualität von HNSCC-Patienten zu verbessern.
Mehrere Antikrebsmittel, die bei der Behandlung von HNSCC verwendet werden, umfassen Cisplatin, 5-Fluorouracil (5-FU), Paclitaxel oder Docetaxel. Unter anderem wird 5-Fluorouracil (5-FU) als Erstlinientherapie bei HNSCC und anderen Plattenepithelkarzinomen eingesetzt [7]. 5-FU ist ein Pyrimidin-Analogon, das die Thymidylat-Synthase in den Krebszellen irreversibel hemmt und dadurch die zum Zelltod führende DNA-Replikation unterdrückt [8]. Wie alle Krebsmedikamente ist 5-FU nicht ohne Nebenwirkungen im systemischen Kreislauf und verursacht eine Toxizität für das normale Gewebe, während berichtet wird, dass die Kombination von 5-FU mit einem sekundären Wirkstoff die Nebenwirkungen potenziell reduzieren und die Wirkung verbessern könnte therapeutische Gesamtwirksamkeit bei der Krebsbehandlung [9].
NAD(P)H:Chinon-Oxidoreduktase 1 (NQO1) ist ein Flavoprotein, das in Tumorgeweben um das 100-200-fache im Vergleich zu Normalgeweben erhöht ist [10]. Die Zwei-Elektronen-Oxidoreduktase ist ein induzierbares Phase-II-Entgiftungsenzym, das in der Lage ist, Chinone durch Bildung stabiler Hydrochinone zu entgiften [11]. Es wurde gezeigt, dass NQO1 in normalen menschlichen Geweben in einem niedrigen Basalspiegel exprimiert wird, wo es die Zellen vor Redoxzyklen und oxidativem Stress schützt und den p53-Suppressor stabilisiert. NQO1 wird bei mehreren Krebsarten, einschließlich Brust-, Pankreas- und Plattenepithelkarzinomen, konstitutiv überexprimiert [12]. Die Überexpression von NQO1 fördert das Fortschreiten der Krebsbelastung und macht die Krebszellen resistenter gegen Chemotherapeutika wie 5-FU oder Cisplatin (oxidative Stressinduktoren), was NQO1 zu einem potentiellen Oncotarget zur Verbesserung der therapeutischen Wirksamkeit macht [13]. Es wurde berichtet, dass der Knockdown von NQO1 durch siRNA die zytotoxische Wirkung mehrerer Medikamente wie Gemcitabin oder Doxorubicin verstärkt [14]. Außerdem werden mehrere synthetische und natürliche NQO1-Inhibitoren wie Cumarine oder Curcumine oder ES936 berichtet [15,16,17]. In dieser Studie haben wir ß-Lapachon (ß-lap, 3,4-Dihydro-2,2-dimethyl-2H-naphtho [1,2-b]pyran-5,6-dion) als NQO1-Inhibitor eingesetzt [ 18]. ß-lap wirkt durch einen NQO1-abhängigen Mechanismus und erzeugt eine signifikante Menge an reaktiven Sauerstoffspezies (ROS), die zu Schäden an den DNA-Strängen und zum Tod von Krebszellen führen [19].
Der Einsatz von Nanopartikeln für die systemische Abgabe kleiner Moleküle wird ein vielversprechender Ansatz in der Krebsbehandlung [20]. Die arzneimittelbeladenen Nanopartikel erfordern einen geringeren Dosierungsplan und haben gezeigt, dass sie die Antikrebswirkung verbessern und die Nebenwirkungen relativ reduzieren. Unter allen Trägern bergen mesoporöse Siliziumdioxid-Nanopartikel (MSN) ein erhebliches Potenzial, die Nutzlast effektiv an das Tumorgewebe zu liefern [21, 22]. Die mikrometergroßen Poren ermöglichen die stabile Beladung der Medikamente und verhindern ihre Freisetzung in den systemischen Kreislauf und ermöglichen die bevorzugte Anreicherung in den undichten Krebsgeweben durch den verbesserten Permeations- und Retentionseffekt (EPR) [23].
Insgesamt war das Hauptziel der vorliegenden Studie, den therapeutischen Nutzen von 5-FU und NQO1-Inhibitor zu kombinieren, um die Antikrebswirkung bei HNSCC zu verstärken. Die In-vitro-Krebswirkung wurde unter Verwendung verschiedener Techniken wie Zelllebensfähigkeit, Western-Blot-Analyse, Durchflusszytometer/Hoechst-basierter Apoptose-Assay und Lebend-/Tot-Assay analysiert. In-vivo-Studien wurden am Cal33-Tumorzellen-tragenden Xenograft-Modell durchgeführt.
Schlussfolgerung
Zusammenfassend haben wir erfolgreich eine 5-FU+ß-lap-beladene Lipid-Doppelschicht-beschichtete mesoporöse Silica-Nanopartikel formuliert. Wir haben gezeigt, dass (i) konzentrationsabhängige Antitumorwirkung von ß-lap in HNSCC-Tumorzellen, (ii) die Kombination von 5-FU+ß-lap zu einer signifikanten Hemmung des NQO1-Proteins und des Bcl-2-Proteins führt, ( iii) kombinationsbasiertes FNQ-MSN zeigte eine signifikante Verringerung der Tumorlast bei HNSCC-Xenotransplantaten. Diese Daten weisen eindeutig auf die Tatsache hin, dass eine subletale Dosis des NQO1-Inhibitors (ß-lap) möglicherweise die therapeutische Wirksamkeit von 5-FU bei HNSCC-Tumoren verbessern und möglicherweise auf die klinische Behandlung anderer bösartiger Erkrankungen ausgeweitet werden könnte.
Materialien und Methoden
Herstellung von 5-FU/ß-lap-beladenen Lipid-Doppelschicht-mesoporösen Silica-Nanopartikeln
Die arzneimittelbeladene MSN wurde durch Auflösen von Cetyltrimethylammoniumbromid (CTAB) (210 mg) in 180 ml Wasser und Kochen auf 80 °C hergestellt, gefolgt von 5-FU und ß-lap wurden 20 % w/w der gesamten Nanopartikel zugegeben und dann wurde Ammoniumfluorid (NH4F) (30 mg) zugegeben und 60 min gut gerührt. Als nächstes wurden 1,6 ml Tetraethylorthosilikat (TEOS) tropfenweise 30 min lang zugegeben und 3 h lang kontinuierlich gerührt. Es bildeten sich halbtransparente weiße Kolloide, die nach Zentrifugieren (15 min) bei 10000 U/min bei 24 ± 1 °C gesammelt wurden. Die MSN wurden in Reinstwasser resuspendiert und der Zentrifugationszyklus wurde zweimal wiederholt. Getrennt davon wurde eine Dünnfilmmembran unter Verwendung von DSPE-PEG2000 (2% des Gesamt-MSN-Gewichts) hergestellt und mit Wasser, suspendiert mit arzneimittelbeladenem MSN, hydratisiert. Die Mischung wurde sofort 5 min lang bei 50 W bei Raumtemperatur (25 ºC) mit Sondenbeschallung behandelt. Die MSN mit PEGylierter Lipiddoppelschicht wurde schließlich zweimal gewaschen und in Reinstwasser resuspendiert.
Partikelgröße, Zetapotentialanalyse und Morphologieanalyse
Der Partikeldurchmesser, der Polydispersitätsindex (PDI) und das Zetapotential wurden unter Verwendung von Zetasizer Nano ZS (Malvern Instruments, Malvern, UK) bewertet. Die Partikel wurden unter Verwendung des dynamischen Lichtstreuungsmechanismus (DLS) analysiert und die Partikeldispersionen wurden vor dem Experiment gut verdünnt. Alle Experimente wurden dreifach bei Raumtemperatur durchgeführt. Die Morphologie der Nanopartikel wurde durch Transmissionselektronenmikroskopie (TEM) unter Verwendung von CM 200 UT, Philips, MA, USA) bei 100 kV bestimmt. Kurz gesagt, Teilchendispersionen wurden verdünnt, ein Tropfen wurde in ein 300-mesh-TEM-Gitter gegeben und 10&supmin; absetzen gelassen. Die Partikel wurden mit 2% Phosphowolframsäure (PTA) als Negativfärbung gegengefärbt, luftgetrocknet und unter einem TEM-Mikroskop betrachtet.
Drogenladen
Die Analyse der Wirkstoffbeladung wurde auf zwei Arten durchgeführt, indem der unbeladene oder ungebundene Wirkstoff im Überstand und der Wirkstoff in den Nanopartikeln berechnet wurden. Die Wirksamkeit der Wirkstoffbeladung wurde durch das HPLC-Verfahren durchgeführt. Die HPLC war mit einer Shimadzu LC-20 AD PLC-Pumpe und einem SPD-M20A PDA-Detektor und einer Shimadzu LC-Analysesoftware mit einer Umkehrphasen-C18-Säule (Phenomenex C18, 150 4,6 mm, 5 µm) ausgestattet. Die mobile Phase für 5-FU besteht aus einer Mischung aus Acetonitril und Wasser (10:90, v/v) und wird mit einer Geschwindigkeit von 1 µml/min gepumpt. Die Detektionswellenlänge wurde für 5-FU auf 265 nm eingestellt. Die mobile Phase für ß-lap besteht aus Acetonitril/Wasser (31:69, v/v) und einer Detektionswellenlänge von 254 nm bei 35 °C. Die Ladekapazität (LC) und Ladeeffizienz (LE) von 5-FU/ß-lap wurden mit der entsprechenden Formel berechnet.
$$ \mathrm{LE}\ \left(\%\right)={W}_{t\mathrm{gesamt}\ 5-\mathrm{FU}+\mathrm{\ss}-\mathrm{lap}} -{W}_{\mathrm{frei}\ 5-\mathrm{FU}+\mathrm{\ss}-\mathrm{lap}}/{W}_{\mathrm{gesamt}\ 5-\mathrm{ FU}+\mathrm{\ss}-\mathrm{lap}}\times 100 $$$$ \mathrm{LC}\ \left(\%\right)={W}_{\mathrm{total}\ 5 -\mathrm{FU}+\mathrm{\ss}-\mathrm{lap}}-{W}_{\mathrm{frei}\ 5-\mathrm{FU}+\mathrm{\ss}-\mathrm{ Runde}}/{W}_{\mathrm{gesamt}\ \mathrm{NP}\ \mathrm{Masse}}\times 100 $$Studie zur Arzneimittelfreigabe
Die Freisetzung von 5-FU und ß-lap wurde in PBS (pH 7,4) und ABS (pH 5,0) bei 37 °C mit der Dialysemethode untersucht. Kurz gesagt, 1 µg Äquivalent jedes mit Wirkstoff beladenen Nanopartikels wurde in 1 µl des jeweiligen Puffers in eine Dialysemembran geladen und die Enden wurden verschlossen. Die versiegelte Dialysemembran wurde in 25 ml ABS- bzw. PBS-Puffer gegeben und in ein Schüttelwasserbad bei 37 °C gegeben. Proben wurden in vorbestimmten Zeitintervallen gesammelt und durch ein gleiches Volumen frischen Puffers ersetzt. Die im jeweiligen Puffer freigesetzte Arzneimittelmenge wurde durch die HPLC-Methode bewertet, wie im vorherigen Abschnitt beschrieben.
Zellkultur- und NAD(P)H:Chinon-Oxidoreduktase-1-(NQO1)-Aktivitätsassay
Die Cal33 HNSCC-Zelle wurde in Dulbeccos modifiziertem Eagle-Medium (DMEM), ergänzt mit 10 % FBS und 1 % Antibiotikamischung, kultiviert. Die Zellen wurden bei Umgebungsbedingungen in einem Inkubator gehalten. Für den NQO1-Aktivitätsassay wurden Cal33-Zellen in einer 96-Well-Platte mit einer Aussaatdichte von 8 × 10 3 . ausgesät Zellen pro Vertiefung und über Nacht inkubiert. Die Zellen wurden mit unterschiedlichen Konzentrationen von ß-lap behandelt und 24 h inkubiert. 0,8% Digitonin (50 µl 2 µl EDTA) wurde verwendet, um die Zellen zu lysieren, und der Assay wurde unter Verwendung von Menadiol und MTT (3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazoliumbromid) als A durchgeführt Substratkupplungsreaktion und Aktivität wurden bei 620 nm gemessen. Der Assay wurde dreifach durchgeführt.
In-vitro-Zelllebensfähigkeitsassay
Der Zellviabilitätstest von ß-lap in ansteigender Konzentration und der Zellviabilitätstest von Einzel- und Kombinationstherapie wurden mit einem 3-(4,5-Dimethylthiazol-2-yl)-5-(3-Carboxymethoxyphenyl)-2-(4 .) getestet -Sulfophenyl)-2H-tetrazolium (MTS)-Assay. Kurz gesagt wurden Cal33-Zellen in einer 96-Well-Platte mit einer Impfdichte von 1 × 10 4 . ausgesät Zellen pro Vertiefung und über Nacht inkubiert. Am nächsten Tag wurden die Zellen separat mit einer steigenden Konzentration von ß-lap behandelt; Die Zellen wurden mit einer individuellen und kombinierten Behandlung mit 5-FU und ß-lap bei einer Basenkonzentration von 5, 10 und 20 µg/ml behandelt und 24 Stunden inkubiert. Die Zellen wurden zweimal gewaschen und mit MTS-Lösung gemäß den Richtlinien des Herstellers behandelt. Die Lebensfähigkeit der Zellen wurde in Bezug auf unbehandelte Zellen berechnet und ein Mikroplatten-Lesegerät wurde für die Absorption bei 460 nm verwendet.
Western Blot-Analyse
Die ausgesäten Zellen in einer 6-Well-Platte wurden separat mit steigender Konzentration von ß-lap behandelt; Zellen wurden mit individuellem (5-FU oder ß-lap) und Kombinationsschema von 5-FU und ß-lap (FNQ-MSN) behandelt und für 24 Stunden inkubiert. Die Zellen wurden geerntet, lysiert (M-pro Puffer) und zentrifugiert und der Protein enthaltende Überstand wurde gesammelt. Die Proteinkonzentration im Zelllysat wurde unter Verwendung der Bicinchoninsäure (BCA)-Methode bestimmt. 10 % Bis-Tris-Polyacrylamidgel wurden verwendet, um die Proteine zu trennen und sofort auf eine Polyvinylidenfluorid (PVDF)-Membran übertragen. Die Membran wurde unter Verwendung von 5% Magermilch, hergestellt in n Tris-gepufferter Kochsalzlösung (TBS)-Puffer, der Tween 20 (TBST, pH 7,2) enthielt, blockiert. Primäre Antikörper des polyklonalen Kaninchen-NQO1 (1:1000), des monoklonalen Maus-Bcl-2 (1:1000) und des monoklonalen Maus-GAPDH (1:1000) wurden über Nacht bei 4°C auf einer Membran inkubiert. Die Membran wurde mit TBST gewaschen und dann mit sekundären Antikörpern (Anti-Maus- oder Anti-Kaninchen-IgG) in einer Verdünnung von 1:10000 inkubiert. Die Membran wurde erneut mit TBST gewaschen und die Blots wurden einer ECL-Substratlösung ausgesetzt und die Dichten der Proteinbanden wurden unter Verwendung eines Photoentwicklers bewertet.
Apoptose und Hoechst-Assay
Cal33-Zellen wurden in einer 6-Well-Platte mit einer Aussaatdichte von 2 × 10 5 . ausgesät Zellen pro Vertiefung und über Nacht inkubiert. Die Zellen wurden dann mit individuellem (5-FU oder ß-lap) und Kombinationsschema von 5-FU und ß-lap (FNQ-MSN) behandelt und für 24 Stunden inkubiert. Die Zellen wurden geerntet, gewaschen, zentrifugiert und pelletiert. Die Zellen wurden mit 2,5 µl Annexin V und 2,5 µl PI behandelt und 15 min im Dunkeln inkubiert. Die Zellen wurden dann auf 1 &mgr;ml aufgefüllt und mittels fluoreszenzaktivierter Zellsortierung (FACS, BD, FACSverse) ausgewertet. Insgesamt wurden 10.000 Zellen analysiert. Ein ähnliches Verfahren zur Zellaussaat und Arzneimittelbehandlung wurde befolgt und dann mit Hoechst 33342 Farbstoff (10&mgr;g/ml) gefärbt und 10&supmin; inkubiert. Die Zellen wurden gewaschen und mit 4% Paraformaldehyd (PFA) fixiert und erneut gewaschen. Die Zellmorphologie wurde unter einem Fluoreszenzmikroskop (Nikon A1, Japan) beobachtet.
Antitumorwirksamkeit von FNQ-MSN IM HNSCC-Xenotransplantat-Tumormodell
18 bis 22 Gramm schwere männliche BALB/c-Mäuse mit einem Durchschnittsalter von 4–5 Wochen wurden vom In-House Animal Facility Center der Zhengzhou University of Light Industry, Henan, beschafft. Die Tiere wurden in einem klimatisierten Raum mit einem 12 h Dunkel-Licht-Zyklus gehalten und erhielten freien Zugang zu Futter und Wasser. Alle Tierprotokolle wurden von der Ethikkommission der Zhengzhou University of Light Industry, Henan, genehmigt. Um ein Xenotransplantatmodell zu erstellen, 1 × 10 7 Cal33-Zellen in 150 µl Kulturmedium wurden subkutan in die rechte Hüfte der Maus geimpft. Wenn die durchschnittliche Tumorgröße 80–100 mm3 erreichte, wurden die Mäuse zufällig in 5 Kontrollgruppen eingeteilt, 5-FU, ß-lap, 5-FU+ß-lap und FNQ-MSN, jeweils mit 8 Mäusen in jeder Gruppe . 5-FU wurde in einer festen Dosis von 5 µg/kg und ß-lap in einer festen Dosis von 25 µg/kg verabreicht und dreimal im Abstand von 3 Tagen für jede Schwanzveneninjektion verabreicht. Mäusegewicht und Tumorvolumen wurden 18 Tage lang regelmäßig überwacht. Das Tumorvolumen wurde mit der Formel berechnet
$$ V\ \left({\mathrm{mm}}^3\right)={\mathrm{Breite}}^2\ \left({\mathrm{mm}}^2\right)\times \mathrm{ Länge}\ \left(\textrm{mm}\right)/2 $$In der vorliegenden Studie wurde kein Maustod aufgrund der Tumorzellbelastung beobachtet und alle Tiere wurden mit CO2 . euthanasiert und dann gegen Ende der Studie durch zervikale Luxation geopfert.
Statistische Analyse
Mehrere Gruppen wurden unter Verwendung einer Zwei-Wege-Varianzanalyse (ANOVA) verglichen. Signifikanzniveau von p <0,05 wurde als signifikant erachtet und alle Daten werden als Mittelwert ± Standardabweichung dargestellt, es sei denn, dies wird in den jeweiligen Experimenten ausdrücklich erwähnt.
Ergebnis und Diskussion
Herstellung von 5-FU/ß-lap-beladenen Lipid-Doppelschicht-gestützten mesoporösen Silica-Nanopartikeln
In dieser Studie haben wir ein mesoporöses Siliciumdioxid-Nanopartikel angepasst, das durch eine PEGylierte Lipiddoppelschicht stabilisiert wird. Das mit 5-FU/ß-lap beladene MSN wurde durch das Emulsions-Beschallungsverfahren hergestellt, und dann wurde mit Arzneimittel beladenes MSN in den Kolben eingebracht, der einen Lipid-Dünnfilm aus DSPE-PEG2000 enthielt. Die Mischung wurde beschallt und die lipidbeschichtete MSN mit 5-FU/ß-lap wurde erhalten (FNQ-MSN) (Abb. 1a). Die Belastungseffizienzen (LE) von 5-FU und ß-lap betrugen 91,5 ± 1,65% bzw. 92,9 ± 1,24%. Der FNQ-MSN wies 8,1 ± 1,12 Gew.-% 5-FU und 7,6 ± 0,95 Gew.-% ß-lap auf, was auf die hohe Ladekapazität (LC) des MSN-Trägers hinweist. Die Anwesenheit der Lipiddoppelschicht verhindert ihre ungewollte Freisetzung in den systemischen Kreislauf und verhindert dadurch die Toxizität. Die durchschnittliche Partikelgröße von arzneimittelbeladenem MSN betrug 92,1 ± 0,85 nm (PDI ~ 0,089), während der Aufbau der Lipiddoppelschicht auf der MSN-Oberfläche (FNQ-MSN) die durchschnittliche Partikelgröße auf 128,4 ± 1,24 nm (PDI ~ 0,115) erhöhte, was auf a . hinweist feste Anwesenheit von Lipidmaterialien auf der Oberfläche von MSN (Abb. 1b). Das Zetapotential änderte sich von − 18,2 ± 1,22 auf − 26,4 ± mV. Die kleine Partikelgröße von FNQ-MSN wird aufgrund des EPR-Effekts die bevorzugte Akkumulation von arzneimittelbeladenem Träger in den undichten Tumorgeweben ermöglichen. Außerdem verleiht die PEGylierte Oberfläche eine ausgezeichnete Stabilität und verlängerte Blutzirkulationszeit, die die Wahrscheinlichkeit von FNQ-MSN in den Tumorgeweben weiter erhöht. Das TEM-Bild zeigte eine morphologische Ähnlichkeit mit der von Liposomen und zeigte eine perfekte Kugelform, die gleichmäßig auf dem Gitter verteilt war. Das TEM-Bild zeigte deutlich einen gräulichen äußeren späteren und dunkleren Kern, was auf das Vorhandensein von Lipidaufbau auf der MSN-Oberfläche hindeutet (Abb. 1c). Die von TEM beobachtete Größe bestätigt mit der DLS-Partikelgröße von einem Zetasizer. MSN besitzen wohlgeordnete Kanäle für die homogene Verteilung von Wirkstoffmolekülen. Die Oberflächeneigenschaft von Poren ist einer der wichtigen Faktoren für die stabile Beladung der kleinen Moleküle. Die verschiedenen physikalischen Kräfte, die an der Wirt-Gast-Interaktion beteiligt sind, umfassen hauptsächlich die hydrophoben Kräfte und die Van-der-Waals-Wechselwirkungskräfte. Die höhere Wirkstoffbeladungskapazität liefert die höhere intrazelluläre Konzentration und die höhere Abtötungseffizienz an den Tumorstellen. Das FNQ-MSN zeigte eine ausgezeichnete Stabilität im PBS-Medium und die Partikelgröße blieb während des Untersuchungszeitraums bis 30 Tage unverändert. Diese verbesserte Stabilität des Trägersystems und die hohe Belastbarkeit des Trägersystems verbessern die Bioverteilung und Effizienz bei der Tumorbehandlung.
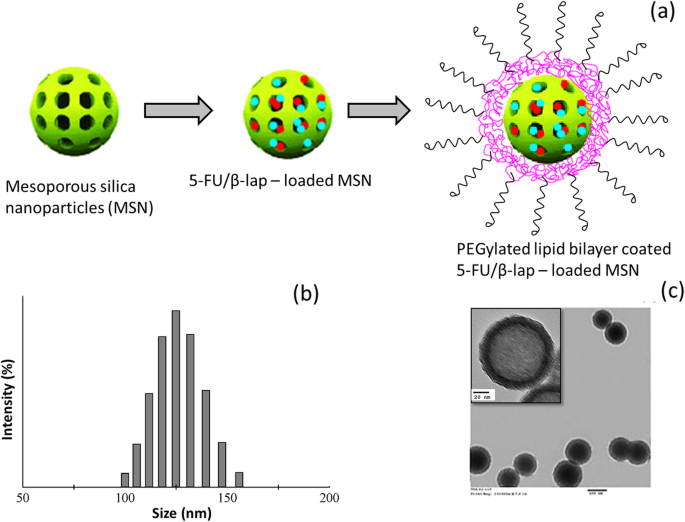
a Schematische Darstellung des Aufbaus von 5-FU- und ß-lap-beladenen Lipid-Doppelschicht-beschichteten mesoporösen Siliciumdioxid-Nanopartikeln. Zwei Medikamente werden in die Poren des MSN geladen, die durch die PEGylierte Lipiddoppelschichtanordnung auf der äußeren Oberfläche des MSN weiter stabilisiert wurden. b Partikelgrößenverteilung von FNQ-MSN. c TEM-Bild von FNQ-MSN mit einer Einfügung höherer Vergrößerungen
In-vitro-Wirkstofffreisetzung
Die in vitro-Wirkstofffreisetzung von 5-FU und ß-lap aus FNQ-MSN wurde in PBS und ABS untersucht (Abb. 2). Wie gezeigt, wurden bei pH 7,4 und pH 5,0 zwei unterschiedliche Freisetzungstrends beobachtet. Zum Beispiel werden 25 % 5-FU in 24 Stunden bei pH 7,4 freigesetzt, verglichen mit ~ 40 % der Wirkstofffreisetzung bei pH 5,0 in 24 Stunden. In ähnlicher Weise wurden 20 % und 30 % ß-lap bei pH 7,4 bzw. pH 5,0 freigesetzt. Die Freisetzungskinetik war während des gesamten Studienzeitraums identisch, wobei nach 72 Stunden Studienzeit 50 % 5-FU in alkalischem Puffer und 80 % der Wirkstofffreisetzung bei pH 5,0 freigesetzt wurden. Eine pH-abhängige Freisetzung des Arzneimittels unter sauren Bedingungen ist für die Krebsbehandlung vorteilhaft. Bei beiden pH-Bedingungen wurde kein Burst-Release-Phänomen beobachtet, was hauptsächlich auf das Vorhandensein der DSPE-PEG-Schicht zurückzuführen ist, die die Freisetzung des Arzneimittels aus dem FNQ-MSN während des gesamten Untersuchungszeitraums kontrollierte. Zwischen pH 7,4 und pH 5,0 wurde ein signifikanter Unterschied in der Wirkstofffreisetzung beobachtet. Bei pH 7,4 Bedingungen PEG-b -DSPE weist eine hohe Tarnschichteigenschaft auf, wodurch die Freisetzung der eingekapselten Verbindung verhindert wird. Das vorliegende Ergebnis zeigte, dass die Wirkstofffreisetzung bei pH 5,0 beschleunigt wurde, was auf die Demontage der schützenden Hülle um die MSN-Oberfläche hinweist. Die pH-abhängige Wirkstofffreisetzungsrate, die eine maximale Wirkstofffreisetzung innerhalb der Krebszellen gewährleistet, kann die Antitumorwirkung verbessern und die unerwünschte Toxizität für normales Gewebe verringern. Es ist möglich, dass FNQ-MSN in Gegenwart eines pH-responsiven Elements zum Ablösen der Lipiddoppelschicht auf dem MSN führt, was zu einer verstärkten Freisetzung bei niedrigeren pH-Bedingungen führt.
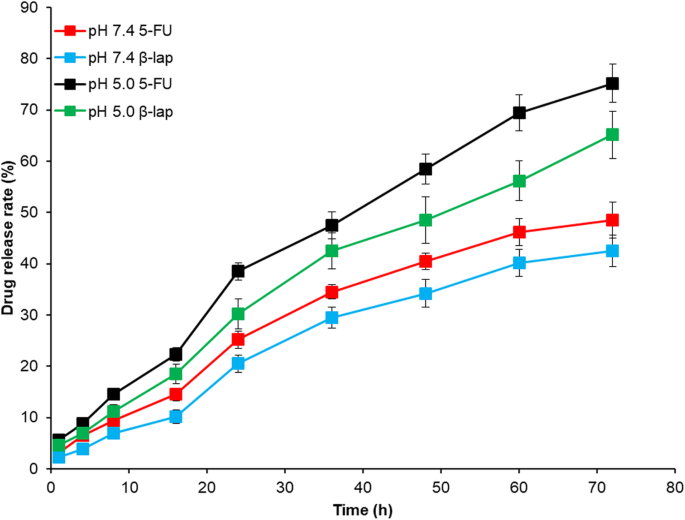
In-vitro-Freisetzung von 5-FU und ß-lap aus FNQ-MSN unter pH 7,4 und pH 5,0 Pufferbedingungen. Die Freisetzungsstudie wurde bis 72 h fortgesetzt und die Wirkstofffreisetzung wurde mit der HPLC-Methode quantifiziert. **p <0,01
Empfindlichkeit von NQO1 gegenüber ß-lap
Da die Hochregulierung von NQO1 in vielen Krebszellen, einschließlich HNSCC, mit einer schlechten Prognose und einem schlechten therapeutischen Ergebnis einhergeht, könnten Medikamente gegen NQO1 eine potenzielle Strategie zur Krebsbehandlung sein [24]. NQO1 wird bei Plattenepithelkarzinomen im Vergleich zu normalem Gewebe 100- bis 200-fach überexprimiert. Daher wurde der ß-lap-Einfluss auf die NQO1-Enzymaktivität in Cal33-Zellen untersucht. Wie gezeigt, zeigte ß-lap eine konzentrationsabhängige Hemmung der NQO1-Enzymaktivität in Cal33-Zellen (Abb. 3a). Bemerkenswerterweise wurde eine signifikante Hemmwirkung bei einer Dosis von 20–50 µg/ml ß-lap beobachtet. Darüber hinaus wurde das Hemmpotential von ß-lap auf das NQO1-Protein durch Western-Blot-Analyse weiter untersucht (Abb. 3b). Die Ergebnisse zeigten deutlich die signifikante Abnahme des NQO1-Proteins in den Krebszellen mit einem Anstieg der Konzentration von ß-lap. Ungefähr 80 % NQO1-Hemmung bei 100 µg/ml ß-lap beobachtet. Bioaktivierbares NQO1-Medikament wie ß-lap wird von NQO1 metabolisiert und bildet eine instabile Hydrochinonverbindung, die sich sofort wieder in die ursprüngliche Komponente umwandelt, wobei 2 Ein-Elektronen-Oxidationen zurückbleiben und 2 O 2− . verbraucht werden . Dies führt zu einem sinnlosen Redoxzyklus, in dem 1 Molekül ß-lap 130 Mol Superoxid auf Kosten des Verbrauchs von 60–70 Mol NAD(P)H6 erzeugt. Die so gebildeten Superoxid (O2.−) Radikale werden in Wasserstoffperoxid (H2O2−) umgewandelt und verursachen Zellapoptose und Zelltod [25].
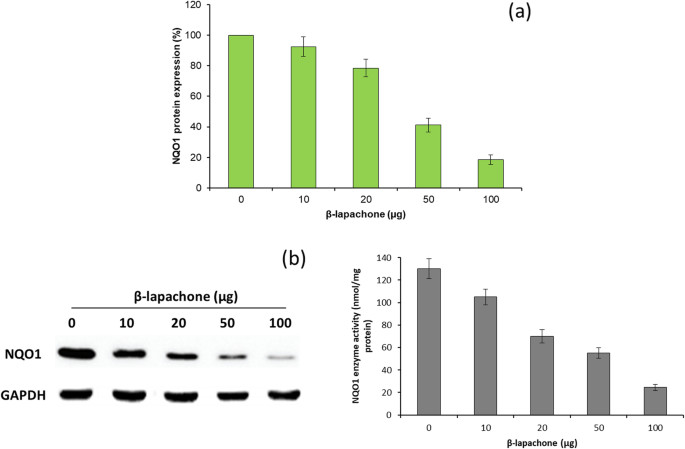
a Wirkung der konzentrationsabhängigen Aktivität von ß-lap auf die NQO1-Aktivität von Cal33-Krebszellen durch die enzymatische Methode. b Wirkung der konzentrationsabhängigen Aktivität von ß-lap auf die NQO1-Proteinspiegel durch Western-Blot-Analyse unter Verwendung von GAPDH als Housekeeping-Protein
In-vitro-Antikrebswirkung von FNQ-MSN in HNSCC-Zellen
Die In-vitro-Krebswirkung von ß-lap in Cal33-Zellen wurde mittels MTT-Assay untersucht. Die Ergebnisse zeigten, dass ß-lap eine typische konzentrationsabhängige Abnahme der Zelllebensfähigkeit aufwies (Abb. 4a). Bemerkenswerterweise wurde eine signifikante Abnahme der Lebensfähigkeit der Zellen bei einer Konzentration von 50 µg/ml beobachtet. Für weitere Experimente wurde 20µg/ml gewählt (unterhalb des IC50-Wertes von ß-lap). Als nächstes wurde die Potenzierungswirkung von ß-lap auf 5-FU bei 3 verschiedenen Konzentrationen (5, 10 und 20 µg/ml) untersucht. Wie gezeigt führte die Kombination von 5-FU+ß-lap zu einer geringeren Lebensfähigkeit der Zellen; am bemerkenswertesten zeigte FNQ-MSN eine signifikant niedrigere Zelllebensfähigkeit im Vergleich zu jeder der einzelnen Wirkstoff- oder physikalischen Kombinationen ( 4b ). Beispielsweise zeigten 5-FU und ß-lap eine Zelllebensfähigkeit von 35,7% bzw. 70,2%, während 5-FU+ß-lap 26,5% bzw. FNQ-MSN 13,1% aufwies. Die Ergebnisse zeigten deutlich, dass die zytotoxische Wirkung von 5-FU in Kombination mit ß-lap signifikant erhöht war. Es ist erwähnenswert, dass FNQ-MSN im Vergleich zu 5-FU+ß-lap effektiver war, was auf die bessere Internalisierung und kontrollierte Freisetzung der beladenen Therapeutika aus dem Trägersystem zurückzuführen ist. Die Ergebnisse zeigen deutlich die hemmende Wirkung von ß-lap auf die enzymatische Aktivität und den Proteinspiegel von NQO1 und verstärken die krebshemmende Wirkung von 5-FU und führen zu einem verbesserten therapeutischen Ergebnis bei der Behandlung von HNSCC.
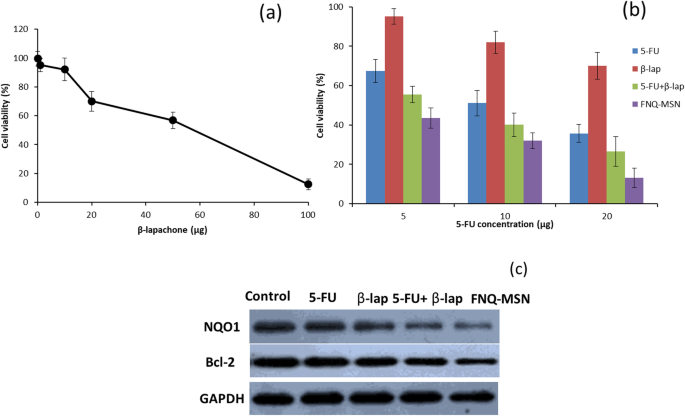
a Wirkung der konzentrationsabhängigen Aktivität von ß-lap auf die Zelllebensfähigkeit von Cal33-Zellen. b Zytotoxische Einzelwirkung und Kombination mit dem zweiten Chemotherapeutikum 5-FU in 3 verschiedenen Konzentrationen von 5–20 µg/ml. Die Lebensfähigkeit der Zellen wurde durch den MTT-Assay nach 24 h Inkubation bewertet. c Western-Blot-Analyse der NQO1- und Bcl-2-Proteinexpression nach Behandlung mit Einzel- und Kombinationstherapie von 5-FU und ß-lap
FNQ-MSN-Rolle in den Signalwegen:Western Blot-Analyse
Der Mechanismus der ß-lap-vermittelten zytotoxischen Wirkung wurde durch Western-Blot-Analyse weiter untersucht. Wie gezeigt führte ß-lap zu einer Abnahme der Proteinbande von NQO1 im Vergleich zur Kontrolle; jedoch wurde die bemerkenswerteste Abnahme des NQO1-Spiegels in der mit FNQ-MSN behandelten Zellgruppe beobachtet (Fig. 4c). Die ß-lap-induzierte Verstärkung der Chemosensitivität von Cal33 durch Verstärkung der Zellapoptose wurde anhand des Bcl-2-Proteinspiegels bewertet. Die Bcl-2-Familie spielt eine wichtige Rolle bei der Regulierung der Zellhomöostase und kontrolliert die Proliferation und den Tod von Krebszellen. Der Prozess der Abnahme von Bcl-2 und der Zunahme von Bax führt zur Freisetzung von Cytochrom C im Cytosol, das die gesamte Caspase-Kaskade einleitet, was zum Zelltod führt [26]. Die Ergebnisse zeigten deutlich, dass die Kombination von 5-FU und ß-lap (FNQ-MSN) das Bcl-2 signifikant herunterregulierte, was auf eine verstärkte Antikrebswirkung in den Cal33-Krebszellen hinweist.
Apoptose-Analyse von HNSCC
Nach der Zelllebensfähigkeitsanalyse wurde die Apoptosewirkung des einzelnen und kombinierten Arzneimittels auf Cal33-Zellen nach Annexin V/PI-Färbung mit einem Durchflusszytometer bewertet (Fig. 5). Die Apoptosewirkung einzelner 5-FU (10µg/ml) oder ß-lap (30µg/ml) führte zu keiner nennenswerten Apoptose von Krebszellen; 5-FU+ß-lap führte jedoch zu einem dramatischen Anstieg des Apoptoseanteils von Krebszellen. Wichtig ist, dass FNQ-MSN zu mehr als 60 % der Zellapoptose (frühe und späte Apoptose) führte, was die überlegene therapeutische Wirkung der trägerbasierten Kombinationstherapie anzeigt. Der Apoptoseeffekt wurde weiter durch Hoechst 33342-Färbung bestätigt. Wie gezeigt, führen mit FNQ-MSN behandelte Zellen zu einer höheren Anzahl von Zellen, die Apoptose, Kernkondensation und Fragmentierungsmerkmalen durchlaufen, verglichen mit der von entweder 5-FU oder ß-lap allein ( 6 ). Während des Apoptoseprozesses schrumpfen Zellen, ohne in der äußeren Zellmembran geschädigt zu werden, und führt zu einer Chromatinkondensation mit erhöhter apoptotischer Körperbildung.
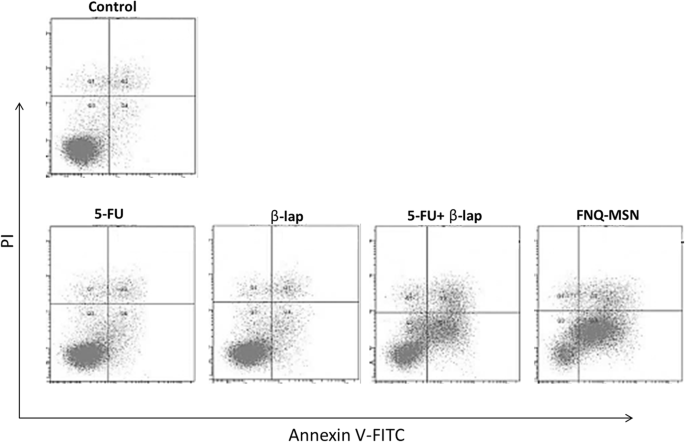
Durchflusszytometer-Analyse von Cal33-Zellen mittels Doppelfärbung von Annexin V und PI nach Behandlung mit Einzel- und Kombinationsbehandlungen von 5-FU und ß-lap. 10.000 Ereignisse wurden im Durchflusszytometer aufgezeichnet
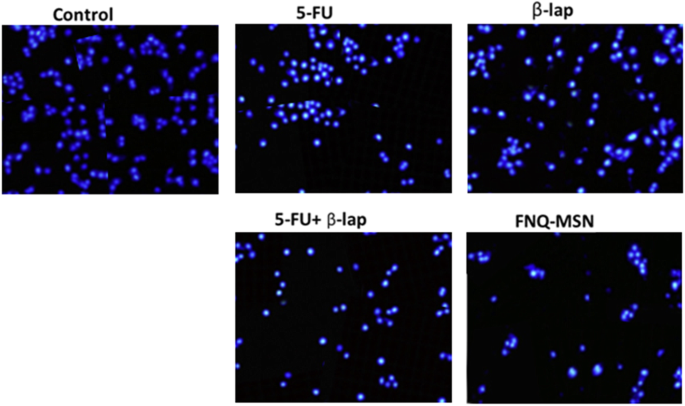
Kernmorphologieanalyse von Cal33-Zellen nach Färbung mit Hoechst 33342; Zellen wurden mit Einzel- und Kombinationen von 5-FU und ß-lap behandelt. 10.000 Ereignisse wurden im Durchflusszytometer aufgezeichnet
Live/Dead-Assay
Die Antikrebswirkung einzelner und kombinierter Medikamente wurde weiter durch den Live/Dead-Assay bewertet. Die behandelten Zellen wurden einer Calcein AM- und Ethidiumbromid-Färbung als jeweiliger Marker für lebende und tote Zellen unterzogen (Fig. 7). Wie gezeigt, werden unbehandelte Zellen mit 100 % grüner Fluoreszenz gefärbt. Die einzelnen Medikamente, 5-FU (10 µg/ml) oder ß-lap (30 µg/ml) zeigten jedoch leicht rot fluoreszenzgefärbte Zellen; jedoch zeigten vorherrschende Zellen eine grüne Fluoreszenz, was auf einen begrenzten Zelltod hinweist. Bemerkenswerter Zelltod wurde in mit FNQ-MSN behandelten Krebszellen beobachtet, wie durch vorherrschende rote Fluoreszenz und weniger grün fluoreszenzgefärbte Zellen gezeigt. Die höhere Antikrebswirkung von FNQ-MSN wurde der synergistischen Aktivität von 5-FU und ß-lap in den Krebszellen und der Fähigkeit von ß-lap, die Chemosensitivität von 5-FU zu erhöhen, zugeschrieben.
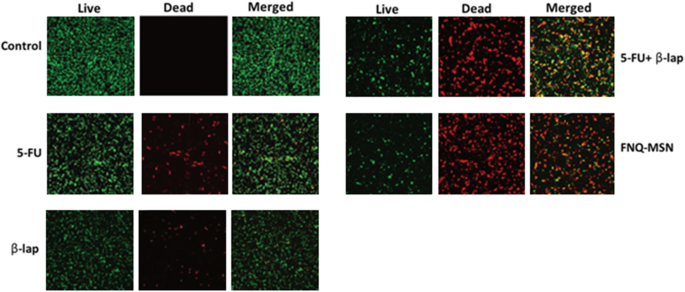
Lebend/Tot-Analyse von Cal33-Zellen durch Doppelfärbung von Calcein AM und Ethidiumbromid nach Behandlung mit Einzel- und Kombinationsbehandlung von 5-FU und ß-lap
In-vivo-Antitumor-Wirksamkeit von FNQ-MSN gegen das HNSCC-Xenograft-Modell
Um die Wirksamkeit der Kombinationstherapie in einem Tiermodell weiter zu bewerten, wurde HNSCC-Xenotransplantat hergestellt und mit 5 mg/kg 5-FU bzw. 10 mg/kg ß-lap verabreicht. Die pharmazeutische Qualität von ß-lap ist ARQ761, das sich derzeit in der klinischen Phase-I-Studie zur Behandlung metastasierender Malignome befindet. ß-lap hat den Grenzwert für die maximal tolerierbare Dosis beim Menschen gemäß den präklinischen Studien festgelegt [27]. Vor diesem Hintergrund haben wir für die In-vivo-Studien eine Dosis von 10 mg/kg ß-lap optimal gewählt. Wie gezeigt, wurde bei individuell verabreichtem 5-FU und ß-lap im Vergleich zu der nicht behandelten Kontrolle keine signifikante Abnahme des Tumorvolumens beobachtet ( 8a ). Eine bemerkenswerte Abnahme des Tumorvolumens wurde mit einer physikalischen Mischung von 5-FU+ß-lap beobachtet; jedoch verzögerte die kombinierte Behandlung von trägerbasiertem 5-FU und ß-lap (FNQ-MSN) signifikant das Tumorwachstum und verlängerte das Überleben von tumortragenden Xenotransplantat-Mäusen. Der Tumorvolumengraph von FNQ-MSN konnte in zwei Teile geteilt werden; bis Tag 9 wurde ein unbedeutendes Wachstum des Tumorvolumens beobachtet, während der Tumor nach Tag 9 bis Tag 18 signifikant zunahm, dennoch war das Gesamttumorvolumen im Vergleich zu dem der Kontroll- oder anderen Gruppen um ein Vielfaches kleiner. Die Bedenken hinsichtlich der Toxizität des individuellen und kombinierten Regimes wurden in Bezug auf das Körpergewicht bewertet ( 8b ). Wie gezeigt, führte die physikalische Mischung von 5-FU+ß-lap zu einer schweren Toxizität, die durch einen Verlust von mehr als 10 % des Körpergewichts dargestellt wurde, während 5-FU zu 5 % des Körpergewichts führte. Wie erwartet führte FNQ-MSN zu keinem Verlust des Körpergewichts, was auf den einzigartigen Vorteil des Lipid-MSN-basierten Trägersystems hinweist. Die verstärkte Antitumorwirkung von FNQ-MSN wurde der hemmenden Wirkung von ß-lap gegenüber dem NQO1-Enzym und -Protein zugeschrieben, was wiederum die Chemosensitivität von 5-FU erhöhte und zu einer synergistischen Antikrebswirkung in humanen Cal33-Tumoren führte, zweitens Lipiddoppelschicht –beschichtetes MSN schützte das Medikament während der systemischen Zirkulation und könnte kontrolliert im Tumorgewebe freigesetzt werden, drittens könnte die PEGylierung von Nanocarriern die Blutzirkulationszeit verlängern, was die bevorzugte Akkumulation im Tumorgewebe aufgrund des EPR-Effekts ermöglicht [28, 29 ]. PEGylierte MSN wurden hauptsächlich im RES der Leber, Milz und Lunge eingeschlossen, was über 80 % der verabreichten Dosis ausmachte. Die PEG-Modifikation von MSN verringerte offensichtlich die Clearance-Rate von MSN in Organen, was zeigt, dass die PEGylierten NPs unabhängig von der Partikelform schwieriger aus den RES-Organen zu entfernen waren [30, 31]. Insgesamt bietet die In-vivo-Studie am HNSCC-Modell einen „Proof of Concept“, dass eine wirksame Kombination von 5-FU+ß-lap in einem stabilen Nanoträger die therapeutische Wirksamkeit bei Tumoren verbessern und gleichzeitig die damit verbundene toxische Wirkung abschwächen könnte.
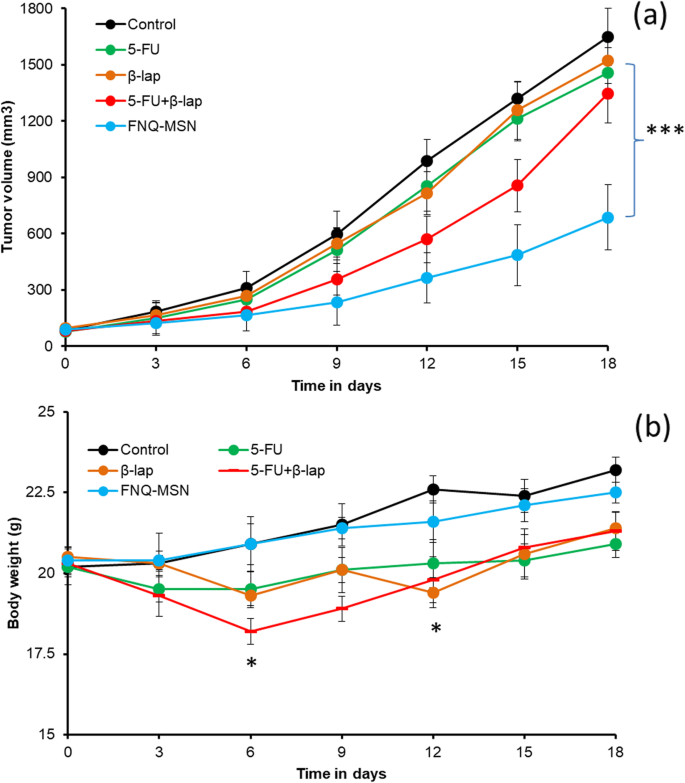
a In-vivo-Antitumorwirksamkeit von FNQ-MSN im HNSCC-Xenotransplantatmodell. Die Mäuse mit HNSCC-Tumoren wurden mit 5-FU, ß-lap, 5-FU+ß-lap und FNQ-MSN in einer festen Dosis von 5 mg/kg 5-FU und 10 mg/kg ß-lap intravenös behandelt für 3 mal. Das Tumorvolumen wurde als Teil der Wirksamkeitsanalyse notiert und mit der unbehandelten Kontrolle verglichen. b Körpergewichtsanalyse entsprechend Tumorvolumendaten. *p <0,05 und ***p <0,001
Verfügbarkeit von Daten und Materialien
Alle während dieser Studie generierten oder analysierten Daten sind in diesem veröffentlichten Artikel und seinen ergänzenden Informationsdateien enthalten.
Abkürzungen
- 5-FU:
-
5-Fluorouracil
- EPR:
-
Verbesserte Permeations- und Retentionswirkung
- FNQ-MSN:
-
5-FU/ß-lap-beladene mesoporöse Silica-Nanopartikel
- HNSCC:
-
Plattenepithelkarzinome im Kopf-Hals-Bereich
- MSN:
-
Mesoporöse Siliziumdioxid-Nanopartikel
- NQO1:
-
NAD(P)H:Chinon-Oxidoreduktase 1
- ß-lap:
-
ß-Lapachon
Nanomaterialien
- Nanopartikel als Effluxpumpe und Biofilm-Inhibitor zur Verjüngung der bakteriziden Wirkung konventioneller Antibiotika
- Silica Aerogel-gestütztes Hydrozincit und Carbonat-interkaliertes Hydrotalcit zur hocheffizienten Entfernung von Pb(II)-Ionen durch Fällungs-Umwandlungsreaktionen
- Vergleich zwischen Folsäure und gH625-Peptid-basierter Funktionalisierung von magnetischen Fe3O4-Nanopartikeln für eine verbesserte Zellinternalisierung
- mit Titandioxid beschichtetes Siliziumdioxid allein und modifiziert durch Natriumalginat als Sorbentien für Schwermetallionen
- Siliziumdioxid-Diatomeenschalen mit Au-Nanopartikeln ermöglichen eine empfindliche Analyse von Molekülen für biologische, Sicherheits- und Umweltanwendungen
- Neuartige anodische Katalysatorunterstützung für Direktmethanol-Brennstoffzelle:Charakterisierungen und Einzelzellleistung
- Autophagie-Inhibitor (LY294002) und 5-Fluorouracil (5-FU) Kombinations-basiertes Nanoliposom für verbesserte Wirksamkeit gegen Plattenepithelkarzinom des Ösophagus
- Platinbasierte Katalysatoren auf verschiedenen Kohlenstoffträgern und leitfähigen Polymeren für Direktmethanol-Brennstoffzellenanwendungen:eine Übersicht
- Antitumorwirkung von 131I-markierten anti-VEGFR2 zielgerichteten mesoporösen Silica-Nanopartikeln bei anaplastischem Schilddrüsenkrebs
- Anwendung von Silizium-Nanostruktur-Arrays für mono- und multikristalline 6-Zoll-Solarzellen



