Biokompatible Nanopartikel als Plattform zur Verbesserung der Antitumorwirksamkeit der Cisplatin-Tetradrin-Kombination
Zusammenfassung
Die Kombinationstherapie ist eine Standardstrategie in der klinischen Tumorbehandlung. Wir haben gezeigt, dass die Kombination von Tetradrin (Tet) und Cisplatin (CDDP) eine deutliche synergistische Antikrebsaktivität zeigt, aber unvermeidliche Nebenwirkungen begrenzen ihre therapeutische Konzentration. Unter Berücksichtigung der unterschiedlichen physikalisch-chemischen und pharmakokinetischen Eigenschaften der beiden Medikamente haben wir sie gemeinsam durch die verbesserte Doppelemulsionsmethode in ein Nanovehikel geladen. Die Nanopartikel (NPs) wurden aus der Mischung von Poly(ethylenglycol)-Polycaprolacton (PEG-PCL) und Polycarprolacton (HO-PCL) hergestellt, sodass CDDP und Tet gleichzeitig in den NPs lokalisiert werden können, was zu geringer Störwirkung und hoher Stabilität führt . Bilder aus dem Fluoreszenzmikroskop zeigten die zelluläre Aufnahme sowohl hydrophiler als auch hydrophober Wirkstoffe, die von den NPs abgegeben werden. In-vitro-Studien an verschiedenen Tumorzelllinien und Tumorgewebe zeigten erhöhte Tumorhemmungs- und Apoptoseraten. In den In-vivo-Studien wurden in der NPs-Gruppe eine überlegene Antitumorwirksamkeit und geringere Nebenwirkungen beobachtet. Außerdem 18 FDG-PET/CT-Bildgebung zeigte, dass NPs die metabolischen Aktivitäten von Tumoren stärker reduzierten. Unsere Ergebnisse legen nahe, dass PEG-PCL-Blockcopolymer-NP ein vielversprechender Träger für eine kombinierte Chemotherapie mit solider Wirksamkeit und geringen Nebenwirkungen sein könnten.
Einführung
Mit der Entwicklung einer tumorübergreifenden Therapie spielen Platinverbindungen eine wichtige Rolle bei der Behandlung verschiedener Krebsarten, unter denen Cisplatin (CDDP) in der Klinik weit verbreitet ist [1, 2]. Auch heute noch ist CDDP in Kombination mit einer Tumorimmuntherapie von Bedeutung und zeigt eine günstige Wirkung bei bösartigen Tumoren wie dem nicht-kleinzelligen Lungenkrebs (NSCLC) [3]. Diese Chemotherapeutika erreichen jedoch immer eine Antitumoraktivität auf Kosten einer unerwünschten Toxizität [4], so dass Therapeutika, die die Toxizität reduzieren und die Wirksamkeit der Chemotherapie erhöhen können, unaufhörlich untersucht wurden [5, 6]. Tetrandrin (Tet) ist ein Mitglied des Bis-Benzylisochinolin-Alkaloids [7] und zeigt eine zufriedenstellende Wirkung bei der Sensibilisierung gegenüber Chemotherapie. Unsere frühere Arbeit hat gezeigt, dass die Kombination von Tet und CDDP eine deutliche synergistische Antikrebsaktivität hat, indem sie die Expression von Chemotherapeutika-assoziierten Genen hemmt, einschließlich der Exzisionsreparatur-Kreuzkomplementation Gruppe 1 (ERCC1), Thymidylat-Synthase (TS), β- Tubulin III usw. [8]. Die klinische Anwendung von Tet leidet jedoch unter seiner schlechten Wasserlöslichkeit und geringen oralen Bioverfügbarkeit [7]. Darüber hinaus verteilt sich hydrophiles CDDP am leichtesten in der extrazellulären Matrix (ECM), während hydrophobes Tet penetrierende Lipidmembranen durch Zellen transportiert werden können, sodass die beiden Medikamente nicht wirklich zusammenarbeiten können. Daher ist es wichtig, einen Weg zu finden, um die beiden Medikamente gleichzeitig effektiv zu verabreichen und die antineoplastische Wirkung mit reduzierten Nebenwirkungen zu verbessern.
Jüngste Fortschritte auf dem Gebiet der Nanotechnologie ermöglichen neuartige Ansätze zur Diagnose und Behandlung von Krebs [9, 10]. Nanopartikel (NPs), die mit amphiphilen Copolymeren, insbesondere Polyethylenglykol (PEG), aufgebaut sind, sind für ihre Fähigkeit bekannt, die Anhaftung von Serumprotein zu reduzieren und die Aufnahme durch das retikuloendotheliale System (RES) zu verhindern [11]. Wenn sie zum Transport hydrophober Medikamente verwendet werden, erhöhen die Nanocarrier taktvoll die Löslichkeit und verlängern sowie erhöhen die Wirkstoffresidenz im Blutkreislauf und im Tumor [12]. Mit dem klinischen Einsatz von copolymeren NPs erfährt die Biokompatibilität der NPs immer mehr Aufmerksamkeit. Neuere Erkenntnisse haben beispielsweise gezeigt, dass einige injizierte Titandioxid-, Siliziumdioxid- und Gold-Nanopartikel die Intravasation und Extravasation von Krebszellen in Tiermodellen beschleunigen [13]. Die aus Nanomaterialien mit guter Biokompatibilität und Sicherheit hergestellten Nanopartikel, insbesondere die von der FDA zugelassenen, sind bessere Kandidaten für Wirkstoffträger.
Vorläufig ist es uns gelungen, CDDP-beladene NPs [14, 15] und Tet-beladene NPs unter Verwendung von Polyethylenglycol-Poly(caprolacton) (PCL-PEG) [16] zu konstruieren, deren in-vivo-Antitumorwirkungen beide nachgewiesen wurden. In dieser Studie verwendeten wir PEG-PCL für die gemeinsame Abgabe von CDDP und Tet. Mit einer nahezu neutralen Ladung bildet PEG die hydrophile Hülle eines Nanopartikels, die antigene Epitope verbirgt und immunologische Reaktionen verhindert [14]. Bilder aus dem Fluoreszenzmikroskop zeigten, dass die Zelle sowohl hydrophile als auch hydrophobe Wirkstoffe aufnehmen kann, die von den NPs abgegeben werden. Die Ergebnisse von In-vitro-Studien, nicht nur an verschiedenen Tumorzelllinien, sondern auch an Tumorgeweben, zeigten, dass CDDP-Tet-NPs das Tumorwachstum wirksamer hemmen als die freien Medikamente. Bei in-vivo-Untersuchungen wurden in der NPs-Gruppe eine erhöhte Antitumorwirksamkeit und verringerte Nebenwirkungen beobachtet. Außerdem 18 Die FDG-PET/CT-Bildgebung zeigte die schlechteste Metabolisierungsrate des Tumors in der NPs-Gruppe und zeigte damit die Fähigkeit von CDDP-Tet-NPs, das Tumorwachstum zu verlangsamen.
Methoden
Materialien
Reagenzien und Zellen
CDDP (Molekülformel PtCl2 (NH3 )2 ) wurde von Shandong Boyuan Pharmaceutical Co. Ltd. (Jinan China) gekauft [15]. Tetrandrin (Molekülformel C38 .) H42 N2 O6 ) wurde als Pulver mit einer Reinheit von > 98% von der Jiangxi Yibo Pharmaceutical Development Company (Jiangxi, China) erhalten [16]. Methoxypolyethylenglykol [MePEG; gewichtsmittleres Molekulargewicht (Mw = 4 kDa; Nanjing Well Chemical Co. Ltd. China) wurde durch azeotrope Destillation mit Toluol dehydratisiert und dann vor der Verwendung bei 50 °C für 12 h vakuumgetrocknet. ε-Caprolacton (ε-CL; Aldrich , USA) wurde durch Trocknen über CaH2 . gereinigt bei Raumtemperatur, gefolgt von Destillation unter vermindertem Druck. Polyvinylalkohol (PVA; Polymerisationsgrad = 500, Alkoholisierungsgrad = 88 %; Shanghai Dongcang International Trading Co. Ltd., China) und Zinnoctoat (Molekülformel SnCl2) (Sigma) wurden wie erhalten verwendet. RPMI 1640 Medium (Gibco, USA), Kalbsblutserum (Lanzhou Minhai Bioengineering, China) und Dimethylthiazoly-2,5-diphenyltetrazoliumbromid (MTT; Amersco, USA) wurden wie erhalten verwendet.
Humane gut differenzierte Magenkrebszelllinie MKN28 , humane kolorektale Adenokarzinom-Zelllinie LoVo, humane Zervixkarzinom-Zelllinie Hela und Maus-Hepatom-Zelllinie H22 wurden vom Shanghai Institute of Cell Biology (Shanghai, China) erhalten. Alle Zelllinien wurden in RPMI 1640-Medium vermehrt, ergänzt mit 10 % Rinderserum, Penicillin (100 U/ml)-Streptomycin (100 g/ml), Pyruvat, Glutamin und Insulin bei 37 °C in einer wassergesättigten Atmosphäre mit 5 % CO2 .
Synthese der Copolymere
Wie bereits beschrieben [16, 17], wurden mPEG-PCL- und HO-PCL-Copolymere durch eine ringöffnende Copolymerisation synthetisiert. Kurz gesagt, wurde eine vorbestimmte Menge an -CL in ein Polymerisationsröhrchen gegeben, das PEG und eine kleine Menge Zinnoctoat (0,1 Gew.-%) enthielt. Das Rohr wurde dann an ein Vakuumsystem angeschlossen, abgedichtet und für 48 h in ein Ölbad bei 130 °C gelegt. Für die Synthese von HO-PCL-Copolymeren wurden eine vorbestimmte Menge an -CL und Zinnoctoat ohne Trocknung in ein Polymerisationsröhrchen gegeben. Nach Beendigung der Polymerisation wurden die rohen Copolymere mit Chloroform gelöst und in einer überschüssigen Menge kaltem Methanol ausgefällt, um das nicht umgesetzte Monomer und Oligomer zu entfernen. Die Niederschläge wurden dann abfiltriert und mehrmals mit Wasser gewaschen, bevor sie bei reduziertem Druck gründlich getrocknet wurden.
Herstellung von CDDP-Tet-beladenen Nanopartikeln
Eine vorbestimmte Menge an CDDP und Tet-beladenen Nanopartikeln wurde durch das Doppelemulsionsverfahren (DE) hergestellt [14, 18]. CDDP und Tet wurden mit 1 ml Dichlormethan (DCM)-Lösung, die 5 mg mPEG-PCL und 15 mg HO-PCL enthielt, durch Beschallung für 15 s (15 W) in einem Eisbad (Lösung W1) emulgiert. Dann wurden 4 ml einer 3% (w/v) PVA-Lösung W2 zugegeben und 30 s lang beschallt, um eine W1/O/W2-Emulsion herzustellen. Die Doppelemulsion wurde in 50 ml einer 0,3%igen (w/v) wässrigen PVA-Lösung verdünnt und DCM wurde unter Vakuum verdampft. Die erhaltenen Nanopartikel wurden gesammelt, gewaschen und gefriergetrocknet (Abb. 1).
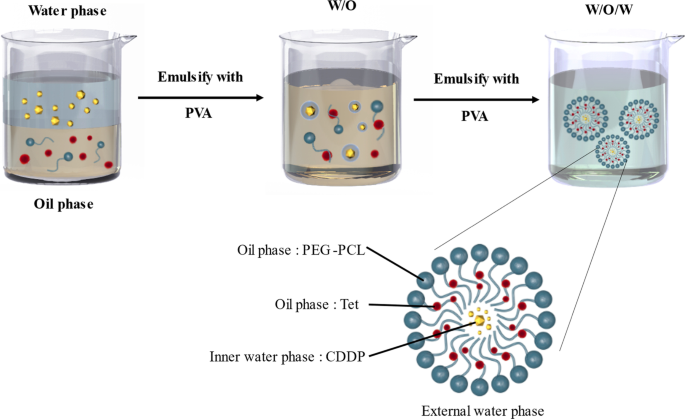
Das Schema der CDDP-Tet-NP-Präparation
Drug-loading Content und Verkapselungseffizienz
Um den Wirkstoffbeladungsgehalt zu bestimmen, wurde das gefriergetrocknete CDDP-Tet-beladene NP-Pulver in Dimethylformamid (DMF) gelöst und 30 l dieser Lösung wurden mit 30 l 2 mmol/l HCL vermischt, gefolgt von der Zugabe von 2,94 ml von 0,2 mmol/l SnCl2 Lösung in 2 mmol/l HCL. Die Absorption bei 403 nm wurde nach 1 h unter Bezugnahme auf eine Kalibrierungskurve mit einem Shimadzu UV-1205-Spektrophotometer (Kyoto, Japan) gemessen. Die Gesamtmenge des Medikaments in den NPs könnte dann berechnet werden. Der Wirkstoffbeladungsgehalt bzw. die Verkapselungseffizienz wurden durch Gl. (1) und (2):
$${\text{Drug Loading content}}\, (\% ) =\frac{{{\text{Gewicht des Medikaments in Nanopartikeln}}}}{{{\text{Gewicht der Nanopartikel}}}} \times 100\,(\% )$$ (1) $${\text{Verkapselungseffizienz }}\,(\% ) =\frac{{{\text{Gewicht des Wirkstoffs in Nanopartikeln}}}}{ {{\text{Gewicht des Nahrungsergänzungsmittels}}}} \mal 100\,(\% )$$ (2)In-vitro-Zytotoxizität der Nanopartikel und die Biokompatibilitätsstudie
Zelluläre Aufnahmestudien
Auf der Grundlage unserer früheren Arbeit [15] wurden LoVo-Zellen mit etwa 5 × 10 5 . auf den Deckel einer 6-Poren-Platte platziert Zellen jede Pore und wurden 24 h lang inkubiert (37 °C, 5 % CO2 .). ). NPs mit Rhodamin B (21 μg/ml) wurden in die Poren gegeben. Nach 2 h Inkubation wurde die Pastete jeweils 3–4 Mal mit 4 °C und 37 °C PBS gewaschen. LoVo-Zellen auf Deckgläsern wurden dann einem Fluoreszenzmikroskop unterzogen.
Zytotoxizitäts-Assay
Die In-vitro-Zytotoxizität der Medikamente wurde durch Standard-MTT-Assays unter Verwendung von MKN28 und H22 . bestimmt Zelllinien. Kurz gesagt, Zellen wurden 24 h vor dem Assay in einer 96-Well-Platte mit einer Dichte von 5000 Zellen pro Well ausgesät. Dann wurden die Zellen einer Reihe von Dosen von freiem CDDP, freiem Tet, freiem CDDP plus Tet und CDDP-Tet-beladenen Nanopartikeln ausgesetzt. Nach der Inkubation wurden 20 μL einer 5 mg/ml MTT-Lösung in jede Vertiefung gegeben und die Platte wurde 4 h lang inkubiert, damit die lebensfähigen Zellen das gelbe MTT in dunkelblaue Formazankristalle umwandeln konnten, die in 200 μL Dimethyl gelöst wurden Sulfoxid (DMSO). Die optische Dichte (OD) jeder Vertiefung wurde mit einem ELISA-Lesegerät (ELX800 Biotek, USA) unter Verwendung von Test- und Referenzwellenlängen von 490 bzw. 630 nm gemessen. Die Lebensfähigkeit der Zellen wurde durch die folgende Formel bestimmt:
$${\text{Zelllebensfähigkeit}}\,(\% ) =\frac{{{\text{OD (Testbrunnen)}}}}{{{\text{OD (Referenzbrunnen)}}}} \ mal 100\,(\% )$$ (3)Die In-vitro-Kompatibilität der leeren Nanopartikel wurde auch durch MTT-Assays mit MKN28 . bestimmt und H22 Zelllinien. Alle von MTT-Assays erhaltenen Ergebnisse wurden bestätigt, indem das Experiment bei mindestens drei unabhängigen Gelegenheiten wiederholt und jedes Mal in dreifacher Ausführung getestet wurde.
Apoptose-Assay
Das Annexin V-FITC-Kit (Bender MedSystem, USA) wurde verwendet, um die Veränderung der Zell-Apoptose-Raten zu untersuchen. MKN28 Zellen wurden für 24 h einer 6 cm-Kulturschale ausgesetzt. Die Kulturmedien wurden durch 1 μg/ml freies CDDP, 1 μg/ml CDDP-beladene NPs bzw. 200 μg/ml leere NPs ersetzt. Die Kontrollgruppe wurde durch Kulturmedien ohne Medikamente ersetzt. Das Enzym wurde nach 48 h Kultur zugegeben. Die Zellen wurden dann gesammelt, zweimal mit PBS gewaschen und in 100 μl Puffer resuspendiert. Annexin V 5 μL und PI 1 μL wurden nacheinander zugegeben, gemischt und 15 min bei Raumtemperatur ohne Lichteinwirkung stehen gelassen. 400 ml Puffer wurden hinzugefügt und einem FCM-Verfahren (BD FACS CantoTM, USA) zur Analyse der Zellapoptoseraten unterzogen.
Histoculture Drug Response Assay (HDRA)
Die HDRA wurde nach unseren bisherigen Studien durchgeführt [14, 19]. Kurz gesagt wurde männlichen ICR-Mäusen subkutan in beide Achselhöhlen 4–6 × 10 6 . injiziert H22 Zellen in Kochsalzlösung. Wenn die Tumoren 400–600 mm 3 . erreichten dem Volumen nach wurden die Mäuse durch zervikale Dislokation getötet, und es wurden frische Proben entnommen, zweimal in Kochsalzlösung gewaschen, in Hanks Lösung eingetaucht und in Stücke mit einem Gewicht von etwa 15 mg geteilt. Die Gewebeproben wurden in eine 24-Well-Platte gelegt, in die quadratische Gelatineschwämme mit Abmessungen von 1 cm in RPMI-1640-Medium, ergänzt mit 20 % fötalem Kälberserum und Amikacinsulfat (100 I.E./ml), das freies CDDP oder CDDP enthielt, eingetaucht wurden. beladene NPs in zwei verschiedenen Konzentrationen. Vier Tumorproben wurden ohne Arzneimittel als Kontrolle inkubiert. Die Gewebe wurden dann 7 Tage lang bei 37 °C, 5 % CO2 . kultiviert . Eine gemischte Lösung von Typ-I-Kollagenase (100 l, 0,6 mg/ml) und MTT (100 l, 5 mg/ml) in 100 mg/ml Natriumsuccinat wurde zugegeben. Nach weiteren 24 h Inkubation wurde MTT-Formazan mit 1 ml DMSO extrahiert und 100 l Lösung aus jedem Well wurden in die Wells einer 96-Well-Mikrotiterplatte überführt. Die OD jeder Vertiefung in der Mikrotiterplatte wurde mit dem ELISA-Lesegerät mit Test- und Referenzwellenlängen von 490 bzw. 630 nm gemessen. Die Lebensfähigkeit der Gewebe wurde nach der folgenden Formel (4) berechnet:
$${\text{Gewebelebensfähigkeit}}\,(\% ) =\frac{{{\text{OD (Test)}}/{\text{Gewicht (Test)/mg}}}}{{{\ text{OD (Kontrolle)}}/{\text{Gewicht (Kontrolle)/mg}}}} \times 100\,(\%)$$ (4)In-vivo-Antitumor-Wirksamkeit
Tumorvolumenmessung
Männlichen ICR-Mäusen mit einem Gewicht zwischen 18 und 20 g wurde die Maus-Hepatom-Zelllinie H22 . implantiert und verwendet, um die relative Wirksamkeit von CDDP-Tet-beladenen NPs zu qualifizieren. Die Mäuse, die unter bestimmten pathogenfreien (SPF) Bedingungen aufgezogen wurden, wurden in Übereinstimmung mit den vom Animal Care Committee des Drum Tower Hospitals genehmigten Richtlinien behandelt. 0,2 ml Zellsuspension mit 4–6 × 10 6 H22 Zellen wurden subkutan in den linken Achselraum der Mäuse injiziert. Die Mäuse wurden in 6 Gruppen eingeteilt:Kontrollgruppe (Kochsalzlösung), leere NPs-Gruppe, freies CDDP (3 mg/kg) Gruppe, freies CDDP plus Tet (CDDP 3 mg/kg + Tet 7,2 mg/kg) Gruppe und CDDP- Tet-beladene NPs (CDDP 3 mg/kg + Tet 7,2 mg/kg) Gruppe. Jede Gruppe bestand aus 6 Mäusen. Die Behandlungen wurden 7–8 Tage nach der Implantation begonnen und der Tag wurde als "Tag 0" bezeichnet. Jedes Tier wurde zum Zeitpunkt der Behandlung gewogen, so dass die Dosierungen angepasst werden konnten, um die angegebenen mg/kg-Dosen zu erreichen. Die Tiere wurden während des gesamten Experiments auch jeden zweiten Tag gewogen.
Immunfluoreszenz-Assay
Die Tumorgewebe der Mäuse in der Kontrollgruppe, die freies CDDP plus Tet und CDDP-Tet-NPs erhielten, wurden am 21. Tag nach der Behandlung zur histologischen Beobachtung ausgewählt. Die Tumoren wurden seziert und in 10 % neutral gepuffertem Formalin fixiert, routinemäßig zu Paraffin verarbeitet und in einer Dicke von 5 mm geschnitten. Die Gewebeschnitte wurden unter einem konfokalen Mikroskop Zeiss LSM510 Meta beobachtet, nachdem die Proben mit (40,6-Diamidino-2-phenylindol) (DAPI, blau) und terminaler Desoxynukleotidyltransferase dUTP Nick-End-Markierung (TUNEL, grün) gefärbt wurden [20] .
18 FDG-PET/CT-Bildgebung
Mäuse der Gruppe mit freiem CDDP plus Tet und der Gruppe mit CDDP-Tet-beladenen NPs erhielten dann am Tag 6 nach der Behandlung eine PET/CT-Bildgebung. Vor der Tracer-Injektion wurden 4 Stunden gefastet. 14,8 MBq (400 lCi) von 18 F-FDG wurde als Radiotracer über die Schwanzvene injiziert. Die Bilder wurden mit einem kombinierten PET/CT-Scanner (Jemini JXL, Philips, USA) erstellt. Hochauflösende PET-Bilder und das gleiche CT-Sichtfeld wurden mit den Mäusen 45 Minuten nach der Verabreichung von 18 . aufgenommen F-FDG. PET-Bilder wurden auf Basis der CT-Daten hinsichtlich Schwächung und Streuung korrigiert. Die Bildfusion wurde durch ein automatisches Bildfusionssystem unter Verwendung einer vom Hersteller bereitgestellten Software durchgeführt. Die maximalen FDG-Aufnahmewerte im Tumor wurden für die Berechnungen des Standard-Aufnahmewerts (SUV) erhalten, wobei Korrekturen für das Körpergewicht und die injizierte Aktivität angewendet wurden.
Statistische Methoden
Statistische Datenanalysen wurden mit Student's t . durchgeführt Prüfung. Die Daten sind als Mittelwert ± SD und Werte von P . aufgeführt < 0,05 wurden als statistisch signifikanter Unterschied akzeptiert.
Ergebnisse
Copolymersynthese und Charakterisierung
Gemäß unserer vorherigen Studie synthetisierten wir die NPs mit PEG-PCL und HO-PCL (das optimale Verhältnis war 1:3) [14]. Der Durchmesser, die Polydispersität, das Zahlenmittel des Molekulargewichts (Mn) und das Gewichtsmittel des Molekulargewichts (Mw) der optimalen PEG-PCL-Copolymer-NP sind in Zusatzdatei 1:Tabelle S1 aufgeführt. Bei Beladung mit CDDP und Tet wurden auch der Wirkstoffgehalt und die Verkapselungseffizienz gemessen (Zusatzdatei 1:Tabelle S2), die denen von CDDP-beladenen PEG-PCL-copolymeren NPs ähneln. Allerdings sind der Wirkstoffbeladungsgehalt und die Beladungseffizienz von Tet geringer als die von Tet-beladenen PEG-PCL-copolymeren NP, was etwas mit HO-PCL-Komponenten zu tun haben könnte.
Durch dynamische Lichtstreuung (DLS) betrug der Durchmesser von CDDP-Tet-beladenen PEG-PCL-Copolymer-NP 359,1 ± 5,3 nm mit einer Polydispersität von etwa 0,231. Bei Beobachtung mit TEM und AFM (Zusatzdatei 1:Abb. S1a und S1b) zeigten die NPs eine regelmäßige Kugelform und ähnliche Größen, die mit den Daten von DLS übereinstimmen. Außerdem werden kleine Tröpfchen in den Nanopartikeln dispergiert, was bestätigt, dass Nanopartikel tatsächlich die Struktur einer Doppelemulsion haben.
Zelluläre Aufnahme von CDDP-Tet-beladenen NPs
Partikel, die mit Fluoreszenzfarbstoffen beladen sind, wurden als gängige Methode zur Untersuchung der zellulären Aufnahme verwendet, die eine visuelle und Echtzeiterkennung ermöglicht. Wir haben gezeigt, dass die farbstoffbeladenen NPs durch Endozytose in die Zellen gelangen können. In dieser Studie ist Rhodamin-B hydrophil und kann in PI-Fluoreszenzkanälen nachgewiesen werden, die zur Simulation von CDDP verwendet werden. Als Simulation von Tet ist Cumarin-6 hydrophob, dessen Signal im FITC-Fluoreszenzkanal empfangen werden kann. Nach 2 h Coinkubation mit NPs, die mit Cumarin-6 und Rhodamin-B beladen waren, wurden LoVo-Zellen durch Fluoreszenzmikroskopie und optische Linse (200 ×) nachgewiesen. Wie in Abb. 2 zu sehen ist, können Fluoreszenzsignale im PI-Fluoreszenzkanal, im FITC-Fluoreszenzkanal sowie im PI/FITC-Dual-Fluoreszenzkanal nachgewiesen werden. Die Ergebnisse bestätigten, dass die NPs gleichzeitig Cumarin-6 und Rhodamin-B zu Tumorzellen transportieren können, woraus wir schließen können, dass CDDP und Tet gleichzeitig in die NPs geladen und von Tumorzellen absorbiert werden können.
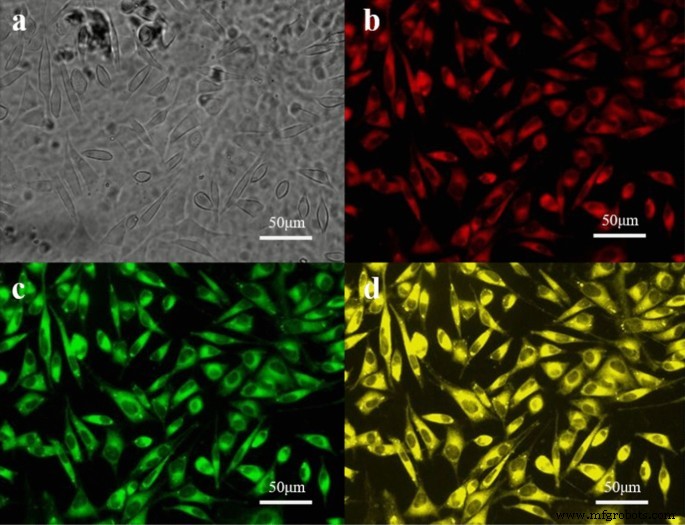
Fotografien von LoVo-Zellen nach 2 h Färbung mit NPs, die mit Rhodamin B und Cumarin-6 beladen waren (200 × ; Balken:50 um). a Zellmorphologie unter dem Lichtmikroskop, b Zellmorphologie unter dem Fluoreszenzmikroskop (PI-Fluoreszenzkanal), c Zellmorphologie unter dem Fluoreszenzmikroskop (FITC-Fluoreszenzkanal) und d Zellmorphologie unter dem Fluoreszenzmikroskop (PI/FITC Dual-Fluoreszenzkanal)
In-vitro-Zytotoxizität der Nanopartikel
Die Zytotoxizität von freiem CDDP, freiem Tet, freiem CDDP plus Tet und CDDP-Tet-beladenen NPs wurden in der Magenzelllinie MKN28 verglichen. Die Konzentration von Tet war 2,4 mal so hoch wie die Konzentration von CDDP. Wie in Abb. 3 gezeigt, war die Zytotoxizität von CDDP-Tet-beladenen NPs unter den vier Gruppen am stärksten. Der Unterschied der Zytotoxizität zwischen freiem Tet und der NPs-Gruppe und drei anderen freien Arzneimitteln wurde mit steigender Konzentration deutlich. Ähnliche Ergebnisse wurden bei menschlichen Gebärmutterhalskrebszellen Hela und hepatozellulären Karzinomzellen H22 . beobachtet (Zusätzliche Datei 1:Abb. S2a, S2b).
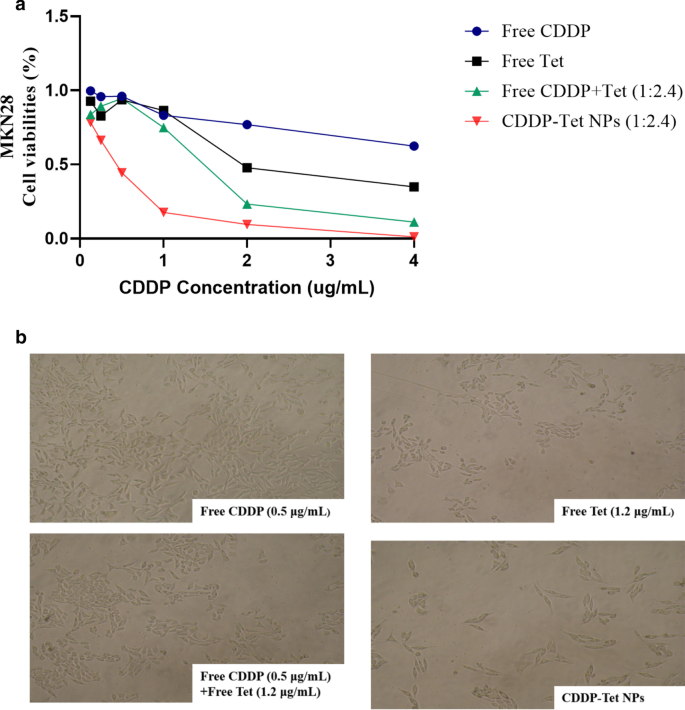
In-vitro-Zytotoxizität der Nanopartikel. a Zelllebensfähigkeit von MKN28 nach 48 Stunden gemeinsamer Kultivierung mit Medikamenten. Die Konzentration von Tet war 2,4 mal so hoch wie die Konzentration von CDDP. b Fotos von MKN28-Zellen unter dem Lichtmikroskop (200 ×) nach 48 Stunden gemeinsamer Kultivierung mit Medikamenten
In unserer früheren Arbeit wurde eine Toxizitätsstudie von leeren NPs durchgeführt. In der vorherigen Studie wies der leere NP eine geringe Toxizität auf Tumorzelllinien auf, was darauf hinwies, dass leere NPs eine zufriedenstellende Biokompatibilität aufweisen [14, 16].
In-vitro-Apoptose-Analyse von CDDP-Tet-beladenen NPs
Wir haben die Auswirkungen von 1 μg/ml freiem CDDP, 2,4 μg/ml freiem Tet, freiem CDDP plus Tet (1 μg/ml + 2,4 μg/ml) und CDDP-Tet-beladenen NPs (1 μg/ml + 2,4 μg .) gemessen /mL) auf die Apoptoserate von MKN28-Zellen nach 48 h Cokultivierung. Die Zellapoptoserate wurde als Q2 + Q4 berechnet (in Fig. 4 gezeigt). Die Veränderung der Apoptoseraten der Zellen war bei den Gruppen von freiem CDDP plus Tet, freiem CDDP und freiem Tet ähnlich (Abb. 4a–c). Die Apoptoserate von MKN28-Zellen, die durch CDDP-Tet-beladene NPs induziert wurde, war jedoch signifikant höher als bei drei anderen Gruppen (Abb. 4d).
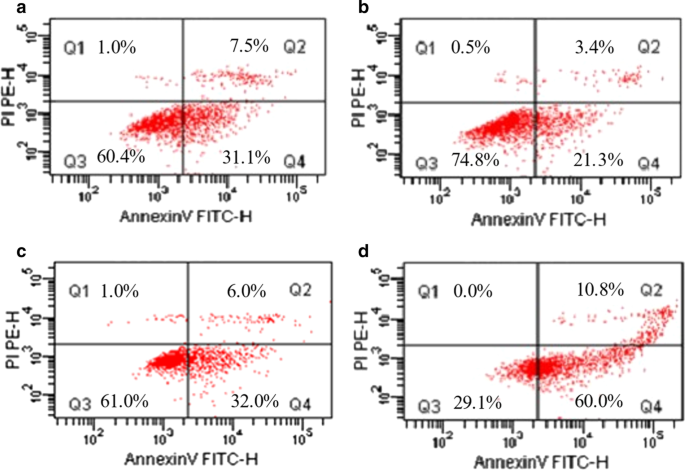
In-vitro-Apoptose-Analyse durch Durchflusszytometrie a kostenloses CDDP, b kostenlos Tet, c kostenloses CDDP + Tet und d CDDP-Tet-NPs
Histoculture Drug Response Assay (HDRA)
Um die Antitumorwirksamkeit der NPs umfassender zu bewerten, haben wir die Antitumorwirkungen von freiem CDDP, freiem CDDP plus Tet und CDDP-Tet-beladenen NPs auf H22 . untersucht Zelllinien mit HDRA. Als klinische Methode zur Vorhersage der Chemosensitivität simuliert HDRA die Praxisbedingungen von Tumorgewebe authentischer als zytologische Experimente [19], deren Ergebnisse durch die Mikroumgebung und Mikrostruktur des Tumorgewebes wie Penetration des Wirkstoffs, extrazelluläre pH-Werte, interstitielle . beeinflusst werden können Flüssigkeitsdruck usw.
Die Konzentration von Tet ist 2,4-mal so hoch wie die Konzentration von CDDP. Wie in Abb. 5 gezeigt, war die Antitumorwirkung von freiem CDDP und der Tet-Gruppe bei der niedrigsten Konzentration besser als die von CDDP, jedoch waren die Wirkungen mit der Zunahme der Arzneimittelkonzentration ähnlich. In Übereinstimmung mit der Apoptoseanalyse hatten CDDP-Tet-beladene NPs bei allen getesteten Konzentrationen unter drei Gruppen eine deutlich bessere Antitumorwirkung.
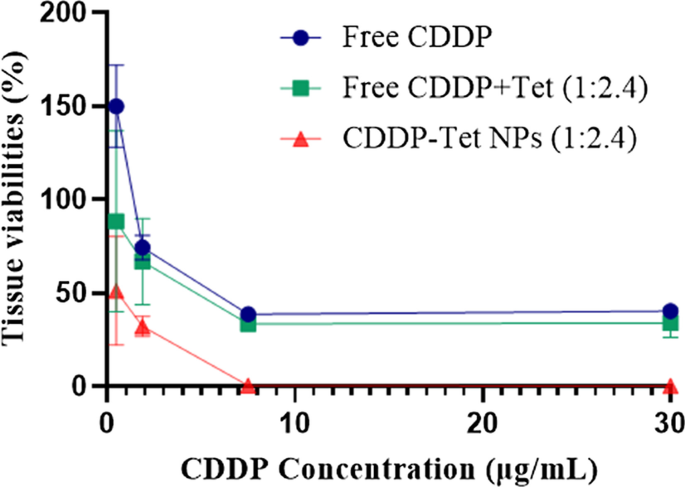
Histokultur-Arzneimittel-Antwort-Assay
In-vivo-Antitumor-Wirksamkeitsanalyse
Evaluation der Wirksamkeit und Nebenwirkungen
Von H22 . gebildete Mausmodelle Zelllinien-Engraftment wurden mit 3 mg/kg freiem CDDP, freiem CDDP zusammen mit Tet (CDDP 3 mg/kg + Tet 7,2 mg/kg), CDDP-Tet-beladenen NPs (CDDP 3 mg/kg + Tet 7,2 mg/ kg) bzw. Der Tumor wurde 12 Tage nach der medikamentösen Behandlung erhalten. Die Tumorgröße wurde alle 2 Tage erfasst, um den optimalsten Inhalt der Wirkstoffabgabe zu bestimmen. Wie in der Tumorwachstumskurve (Abb. 6) gezeigt, war der Tumorwachstumstrend der Kontrollgruppe sowie der leeren Nanopartikelgruppe ähnlich, aber in anderen drei Gruppen mit Wirkstoffabgabe bestand eine deutliche Hemmung des Tumors. Im Vergleich zur Gruppe mit freiem CDDP zeigte die Gruppe mit freiem CDDP plus Tet während der ersten 6 Tage eine bessere Antitumorwirksamkeit. Nach 6 Tagen begann sich der Unterschied der Tumorhemmungsrate zwischen den beiden Gruppen jedoch zu verringern und nach 10 Tagen hatte freies CDDP plus Tet eine noch schlimmere Antitumorwirkung.
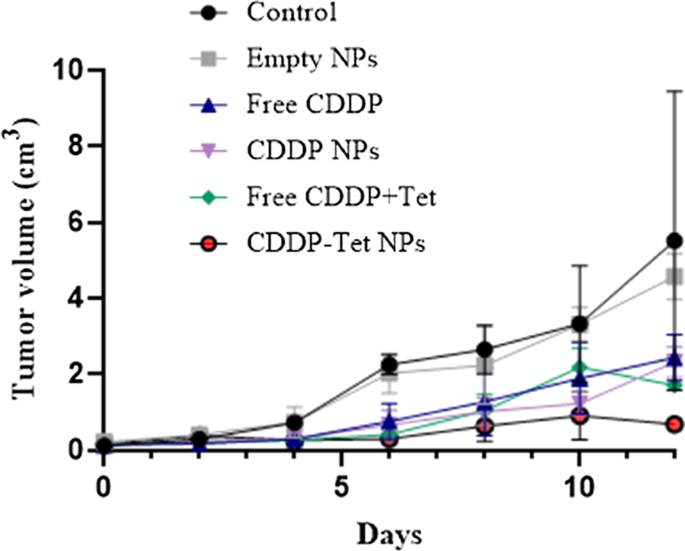
Tumorvolumen von etabliertem H22 Xenotransplantate bei ICR-Mäusen während der Therapie unter verschiedenen Behandlungen. Mäuse wurden an Tag 0 mit unterschiedlichen Strategien behandelt, wie in der Abbildung gezeigt:3 mg/kg freies CDDP, freies CDDP zusammen mit Tet (CDDP 3 mg/kg + Tet 7,2 mg/kg) und CDDP-Tet-beladene NPs ( CDDP 3 mg/kg + Tet 7,2 mg/kg). Mittlere ± SD (n = 6) jeder Gruppe wurde gemessen
Während der ersten 6 Tage waren die Antitumorwirkungen der Gruppen mit freiem CDDP plus Tet und CDDP Tet-beladenen NPs ähnlich. Daher zeigten Mäuse, die CDDP-Tet-beladene NPs erhielten, seit dem 6. Tag nach der Behandlung eine bessere Antitumorwirksamkeit. Zusätzliche Datei 1:Abbildung S3a zeigt unterschiedliche Tumorgrößen jeder Gruppe. Das Tumorvolumen der CDDP-Tet-beladenen NPs-Gruppe war am kleinsten, was als direktes Spiegelbild der prominenten Antitumorwirkung angesehen werden kann. Zusätzlich zur Tumorhemmungskapazität befanden sich im Vergleich zur Gruppe mit freiem CDDP oder freiem CDDP plus Tet weniger Blutgefäße auf der Oberfläche des Tumors). In ähnlicher Weise war, wie in Zusatzdatei 1:Abbildung S3b gezeigt, die Gefäßdichte in der NPs-Gruppe im Vergleich zur Kontrollgruppe und der Gruppe mit freiem CDDP plus Tet am niedrigsten.
Um das Verhältnis apoptotischer Zellen in Tumorgewebe in vivo weiter zu untersuchen, wurde ein TUNEL-Assay zum Nachweis apoptotischer Zellen durchgeführt. Wie in Abb. 7 gezeigt, können die apoptotischen Zellen in Tumoren mit grüner Fluoreszenz gefärbt werden, um Apoptose anzuzeigen. Die zusammengeführten Bilder zeigen weniger grün fluoreszierende Regionen in der Kontrollgruppe und der Gruppe mit freiem CDDP plus Tet, was auf das Vorhandensein von weniger apoptotischen Zellen hinweist. Darüber hinaus wurde in der mit CDDP-Tet-NPs behandelten Gruppe eine große Anzahl grün fluoreszierender Regionen beobachtet, was auf eine große Menge apoptotischer Zellen hinweist. Die Ergebnisse bestätigten, dass CDDP-Tet-NPs die Tumorapoptose in vivo fördern können.
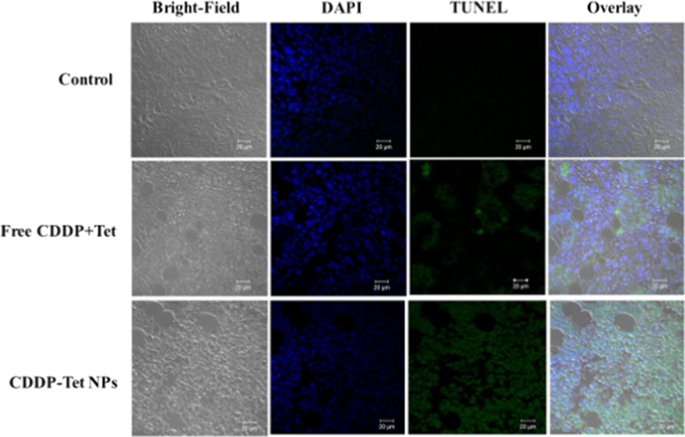
Apoptotische Zellen wurden durch einen TUNEL-Test (grün) nachgewiesen und durch Kernfärbung DAPI (blau) mitgefärbt
Neben einer besseren Antitumorwirksamkeit als die Gruppe mit freiem CDDP und mit freiem CDDP plus Tet zeigten die CDDP-Tet-beladenen NPs auch weniger Nebenwirkungen. Wie in 8a gezeigt, verursachten freies CDDP und freies CDDP plus Tet einen signifikanten Gewichtsverlust im Vergleich zur Kontrollgruppe, was auf die Toxizität bei direkter Arzneimittelabgabe hindeutet. Die Gewichtsänderungskurve der leeren NPs-Gruppe war der der Kontrollgruppe ähnlich, was darauf hindeutet, dass die Toxizität der leeren NPs vernachlässigt werden konnte. Der Gewichtsverlust durch CDDP-Tet-beladene NPs und Kontrollgruppen war während der ersten 6 Tage vergleichbar. Von Tag 6 bis Tag 12 waren die Mäusegewichtsniveaus in der NPs-Gruppe etwas niedriger als in der Kontrollgruppe, aber höher als in der Gruppe mit freiem CDDP oder freiem CDDP plus Tet. Es ist bemerkenswert, dass die Gruppe mit freiem CDDP plus Tet zu einem offensichtlichen Gewichtsverlust beitrug und den Appetit von Mäusen während der ersten 4 Tage verringerte, was darauf hindeutet, dass die Aufnahme von Arzneimitteln für den gesamten Körper schädlich war. Im Gegensatz dazu können CDDP-Tet-beladene NPs langsam im Gewebe freigesetzt werden und die Konzentration stabil halten; Daher waren die Nebenwirkungen im Vergleich zur direkten Arzneimittelabgabe offensichtlich geringer. Anschließend wurden die Nebenwirkungen der Behandlung auch durch Leberbiopsie bewertet (Abb. 8b). Im Vergleich zur Kontrollgruppe ist die Grenze zwischen den Leberzellen der Doppel-Drug-Nacked-Drug-Gruppe verschwommen, einige Leberzellen haben ballonierte Veränderungen, Zellkörper schrumpfen, nukleäre Pyknose und erhöhte Eosinophilie (gelber Pfeil), während die Doppel-Drug Nanopartikel-Gruppe. Die Struktur der Stammzellen ist normal, der Interzellularraum ist klar und es gibt keine offensichtlichen pathologischen Veränderungen. Diese Ergebnisse deuten darauf hin, dass die NP-Abgabe nur wenig beeinträchtigt ist.
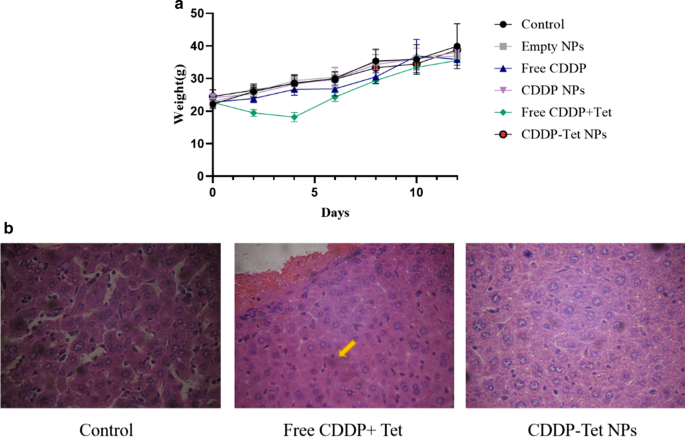
Bewertung der Nebenwirkungen a Körpergewichte von nachgewiesenem H22 Xenotransplantate bei ICR-Mäusen während der Therapie unter verschiedenen Behandlungen. b Leberproben mit HE-Färbung wurden lichtmikroskopisch untersucht (400 ×)
PET–CT
Um die therapeutische Wirkung in vivo jeder Gruppe besser vergleichen zu können, wurden die Mäuse am Tag 6 nach der Behandlung einem CT, PET/CT-Scan unterzogen. Die Fusionsbilder von CT und PET-Scan sind in Abb. 9 dargestellt. PET/CT ist eine effiziente Methode, um metabolische Veränderungen durch 18 . widerzuspiegeln Nachweis der FDG-Aufnahme [21]. As shown in CT scan (Fig. 9), the tumor volume of free CDDP plus Tet group and CDDP-Tet-loaded NPs group were comparable (Fig. 9a) but the tumor metabolic rate in free CDDP plus Tet group was significantly higher than NPs group (Fig. 9b). The decreased intensity at the tumor site of the murine received CDDP-Tet-loaded NPs symbolized poor metabolism rate of the tumor, and thereby indicating the capability of NPs to retard tumor growth.
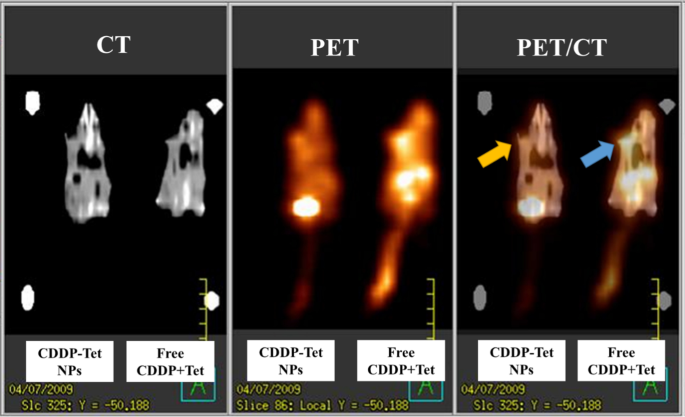
Male ICR mice bearing a subcutaneous H22 tumor at the left axillary (arrows). CT, PET and fused PET/CT images are arranged in the figure from left to right. Tumor metabolic rate in free CDDP plus Tet group (blue arrow) was significantly higher than NPs group (yellow arrow)
Diskussion
Considering the heterogeneity and complexity of tumor, combination therapy has become a standard strategy in the clinical treatment of tumor [22]. Nevertheless, simple combination of two individual therapeutics can't necessarily reach anticipated effect because of the different physicochemical and pharmacokinetic properties of the two drugs [23]. To deliver different drugs to tumor cells in a synergistic ratio, a combination therapy vehicle has been designed in this study. CDDP is hydrophilic while Tet is hydrophobic, which cause problems for the loading method. In this study, we used the amphiphilic copolymer with PCL as the hydrophobic core and PEG as the hydrophilic corona [14]. By the improved double emulsion method, Tet located in the oil layer and CDDP located in the water layer, the unique structure imparts the NPs with the capacity to simultaneous encapsulation of Tet and CDDP to form NPs. CDDP and Tet are located in different layers of NPs, resulting in low interfering effect and high stability [24].
The combination therapy vehicle loaded with CDDP and Tet can enhance the efficacy of CDDP-Tet combination. Not only in the cellular experiments, CDDP-Tet NPs also significantly inhibit tumor tissue viabilities in the HDRA assays, validating the anti-tumor effect of the NPs in the model which take into account of tumor microenvironment [19]. As to in vivo study, antitumor efficacy was observed in tumor volume change, which demonstrated that CDDP-Tet NPs effectively suppressed tumor growth with lower proliferation level. 18 FDG-PET/CT imaging revealed that the glucose metabolism of the tumors in the CDDP-Tet group was inhibited more prominently and early by inducing higher apoptosis level of tumors, which was confirmed in the immunofluorescence assays [21]. Compared with free CDDP plus Tet, CDDP-Tet NPs are faster and safer to take effect, which can be explained by the three mechanisms as follows.
Firstly, as a lipid-soluble drug, Tet can hardly distribute in the ECM and therefore rarely diffuse around tumor cells [9]. Located in the oil phase of NPs, Tet is endowed with better solubility and bioavailability, reaching the tumor sites in the same synergistic ratio as CDDP. Furthermore, CDDP, which used to have systemic side effect, once carried by the nanoparticle, can easily reach the interstitium of tumor tissues from leaky tumor blood vessels and be held within the tumor on account of pressure made by destitute lymphatic drainage [25]. The more CDDP tumor tissues hold, the less damage will be done to normal organs. As a result of passive targeting strategies, CDDP-Tet NPs are much safer than free CDDP plus Tet, which can be observed in the murine body weight changes and liver biopsies.
Drug resistance is regarded as one of the greatest challenges in cancer treatment, not only because of genetic changes at the level of a single cell, but also due to tumor tissues and microenvironment [26]. On one hand, Tet is alkaline, so it will be protonated in the acidic tumor microenvironment and thus can’t cross the electronegative tumor cytomembranes, which is called pH-induced physiological drug resistance [27]. On the other hand, large distances between blood vessels in solid tumors and high interstitial fluid pressure contribute to limited distribution of CDDP and Tet [28]. Carried by the nanovehicle, Tet can enter tumor cells via endocytosis without influence of tumor microenvironment, overcoming the pH-induced physiological drug resistance. The small size of nanocarriers allows them to enter tumor vasculature and preferentially accumulating at the tumor site in vivo [29, 30].
In summary, this study represents an example of delivering a chemotherapeutic drug along with a chemosensitizer simultaneously. Carried by the NPs, both drugs are targeted to tumor site passively, reducing systemic toxicity. Besides, NPs offer a solution to physiological drug resistance by helping the chemosensitizer enter tumor cells more and faster, which play an important role in improving the efficacy of tumor chemotherapy. Therefore, we believed that this PEG–PCL block copolymeric NPs could be a promising carrier for combined chemotherapy.
Conclusions
Based on our previous studies [8, 14, 16], this paper investigated the application of PEG–PCL/HO-PCL NPs for delivery of the combination of two drugs with different physicochemical properties. For in vitro studies, NPs exhibited superior antitumor effect with great biocompatibility. Enhanced antitumor efficacy was observed in tumor volume change and 18 FDG-PET/CT Imaging as to in vivo study in murine model. The mice in NPs group also exhibited reduced side effects. Additionally, the apoptosis rate of tumor cells was promoted by NPs in both in vitro and in vivo studies. In summary, this block copolymeric NPs could be a promising carrier for the delivery of Cisplatin–Tetradrine combinations and other combinations, with enhanced antitumor effect and reduced toxicity, for the treatment of cancer.
Verfügbarkeit von Daten und Materialien
The datasets used and/or analysed during the current study are available from the corresponding author on reasonable request.
Abkürzungen
- Tet:
-
Tetradrine
- CDDP:
-
Cisplatin
- NP:
-
Nanopartikel
- PEG–PCL:
-
Poly(ethyleneglycol)–polycaprolactone
- HO-PCL:
-
Polycarprolactone
- ECM:
-
Extracellular matrix
- PEG:
-
Polyethylenglykol
- RES:
-
Reticuloendothelial system
- DMF:
-
Dimethylformamid
- SPF:
-
Specific pathogen-free
- Mn:
-
Zahlenmittel des Molekulargewichts
- Mw:
-
Gewichtsmittel des Molekulargewichts
- DLS:
-
Dynamische Lichtstreuung
Nanomaterialien
- IBM-Wissenschaftler demonstrieren als erstes rockige Brownsche Motoren für Nanopartikel
- Goldnanopartikel für Chemosensoren
- Nanopartikel für die Krebstherapie:Aktuelle Fortschritte und Herausforderungen
- Biokompatible FePO4-Nanopartikel:Wirkstofftransport, RNA-Stabilisierung und funktionelle Aktivität
- Gehirn-gezielte Polysorbat 80-emulgierte Donepezil-Wirkstoff-beladene Nanopartikel für die Neuroprotektion
- Resveratrol-beladene Albumin-Nanopartikel mit verlängerter Durchblutung und verbesserter Biokompatibilität für eine hochwirksame gezielte Pankreastumortherapie
- Neuartige biokompatible Au-Nanostars@PEG-Nanopartikel für die In-vivo-CT-Bildgebung und renale Clearance-Eigenschaften
- Nachbehandlungsmethode zur Synthese monodisperser binärer FePt-Fe3O4-Nanopartikel
- Modifiziertes hyperverzweigtes Polyglycerin als Dispergiermittel zur Größenkontrolle und Stabilisierung von Goldnanopartikeln in Kohlenwasserstoffen
- Mehrfachverwendung für einen Plattformwagen



