Synthese wasserlöslicher Antimonsulfid-Quantenpunkte und ihre photoelektrischen Eigenschaften
Zusammenfassung
Antimonsulfid (Sb2 .) S3 ) wird seit langem in photoelektrischen Geräten eingesetzt. Es fehlten jedoch Informationen zu Sb2 S3 Quantenpunkte (QDs) wegen der Syntheseschwierigkeiten. Um diese Stelle zu besetzen, wasserlösliches Sb2 S3 QDs wurden durch Heißinjektion hergestellt, wobei eine Mischung aus Hexadecyltrimethylammoniumbromid (CTAB) und Natriumdodecylsulfat (SDS) als anionisch-kationisches Tensid, Alkanolamid (DEA) als Stabilisator und Ethylendiamintetraessigsäure (EDTA) als Dispergiermittel verwendet wurden. Photoelektrische Eigenschaften einschließlich Absorption und Emission wurden durch UV-Vis-IR-Spektrophotometer und Photolumineszenz-(PL)-Spektroskopie-Technik charakterisiert. Es wurde eine intensive PL-Emission bei 880 nm gefunden, was auf Sb2 . hinweist S3 QDs haben gute Aussichten bei Nahinfrarot-LED- und Nahinfrarot-Laseranwendungen. Sb2 S3 QD-Dünnfilme wurden durch Selbstorganisationswachstum hergestellt und dann in Argon- oder Selendampf getempert. Ihre Bandlücken (E g s) wurden nach Transmissionsspektren berechnet. Das E g von Sb2 S3 Es wurde festgestellt, dass die QD-Dünnschicht durch Tempern oder Selenylierung von 1,82 bis 1,09 eV abstimmbar ist, was die guten Aussichten für Photovoltaikanwendungen demonstriert.
Hintergrund
Quantum Dots (QDs) haben in den letzten zehn Jahren aufgrund ihrer manipulierten photoelektrischen Eigenschaften und ihrer überlegenen Verarbeitbarkeit in Lösung für die Geräteentwicklung große Aufmerksamkeit erhalten [1,2,3]. Typischerweise haben sich Bleiverbindungs-QDs wie PbS und Bleihalogenidperowskite aufgrund ihrer einfachen Synthese und zufriedenstellenden Leistung in letzter Zeit als vielversprechende Materialkandidaten für photoelektrische Anwendungen wie Photovoltaik, OLEDs, Laser und Photodetektoren herausgestellt [4,5,6]. Außerdem eine Reihe von Halbleiter-QDs wie CdS, CdSe, ZnS, ZnSe, HgTe, CuInSe2 , CuInS2 , und CdHgTe und Basisgerät wurden überall gemeldet.
Sb2 S3 ist als häufigstes Antimonsulfid bekannt, das ein vielversprechendes Halbleitermaterial für die photoelektrische Halbleiterherstellung ist [7, 8]. Es hat in kristalliner Form (Stibnit) eine moderate Bandlücke von etwa 1,7–1,8 eV. Seltsamerweise ist die Bandlücke im Bereich von 1,1–1,8 eV einstellbar, wenn Schwefel teilweise durch Selen ersetzt wird [9]. Natürlich Sb2 S3 ist ein Multifunktionsmaterial, das als Absorber oder Sensibilisator für photovoltaische Geräte, photochemische Katalyse und Photodetektoren verwendet werden könnte. Außerdem sind Sb und S vergleichsweise häufig vorkommende, kostengünstige und wenig toxische Elemente, was es zu einem Potenzial für eine großtechnische Anwendung macht. Antimonsulfid hat eine einzigartige Verarbeitbarkeit. Sie können bei niedriger Temperatur (~ 400 °C) vakuumverdampft oder mit verschiedenen Materialien lösungsverarbeitet werden. Sb2 S3 wurde meist in sensibilisierten Solarzellen eingesetzt. Verwendung eines mit Thioacetamid behandelten Sb2 S3 mittels chemischer Lösungsabscheidung (CBD) abgeschiedenem Sensibilisator wurde eine sensibilisierte Hybridsolarzelle mit einer Leistungsumwandlungseffizienz (PCE) von 7,5% realisiert [10]. Kürzlich erreichten lösungsverarbeitete planare Heterojunction-Solarzellen mit einfacher Struktur einen sehr zufriedenstellenden PCE von 4,3 %, bei dem ein Sb2 S3 Film wurde durch konventionelle Schleudergusstechnik mit einem Sb2 . enthaltenden Vorläufer hergestellt O3 , CS2 , und n-Butylamin [7]. Nanostruktur Sb2 S3 durch Lösungsmethode synthetisiert wurde wild für Hochleistungs-Photodetektoren eingesetzt [11,12,13]. Sb2 S3 NW-basierte Photodetektoren zeigten eine gute Photoantwort in einem breiten Spektralbereich von 300 bis 800 nm. Insbesondere bei 638 nm zeigten sie optimale Werte mit einem hohen ON/OFF-Verhältnis von etwa 210, einer spektralen Empfindlichkeit von 1152 A/W und einer Detektivität von 2 × 10 13 Jones, und die Anstiegs- und Abfallzeiten von etwa 37 ms [11]. Lösungsverarbeiteter Sb2 S3 Nanostäbchen wurden üblicherweise als effizienter Photokatalysator für den Farbstoffabbau [14] und Hochleistungs-Natriumionenbatterien [15] verwendet. Leider wurden nur wenige Informationen zu Sb2 . gemeldet S3 QDs.
Wir glauben, Sb2 S3 Nulldimensionale Materialien müssen aufgrund des Quanteneinschlusseffekts im Vergleich zu mehrdimensionalen Materialien ungewöhnliche optische und elektrische Eigenschaften aufweisen. Um diese Lücke zu füllen, berichtete die vorliegende Arbeit zunächst über die Synthese wasserlöslicher Antimonsulfid-QDs unter Verwendung von CTAB und SDS-Mischungen als anionisch-kationisches Tensid, DEA als Stabilisator und EDTA als Dispergiermittel unter 120 °C Ölbadbedingungen. Um die Interferenz von Hydroxyl zu überwinden, wurde die Reaktion in wasserfreiem 2-Methoxyethanol anstelle von Wasser durchgeführt. Diese Vorstufen sind im Vergleich zu herkömmlichen Additiven ungiftig, geruchlos und kostengünstig [16, 17]. Vor der wesentlichen Anwendung wurden hier die strukturellen, optischen und elektrischen Eigenschaften untersucht.
Experimentell
Sb2 S3 QDs wurden durch das schnelle Heißinjektionsverfahren synthetisiert. In einem typischen Verfahren zur Herstellung wurden SDS (0,05 mmol, 99,5 %), CTAB (0,05 mmol, 99,5 %), EDTA (0,2 mmol, 99,5 %) und DEA (4 ml, 99,9 %) in die 100- ml wasserfreies 2-Methoxyethanol und nach 20 min magnetischem Rühren in 120 °C Ölbad gelöst. Als nächstes wurden 0,5 mmol Thioacetamid (TAA) in der heißen Lösung gelöst. Dann wurden 2 ml Antimonacetat – Essigsäurelösung (0,25 M) – unter magnetischem Rühren in die Vorläuferlösung injiziert. Sofort verfärbte sich die Lösung von transparent zu leuchtend gelb, was die Bildung von Sulfid anzeigte. Der Behälter wurde dann in ein Eisbad gedreht, um die Reaktion zu beenden. Das Endprodukt wurde 10 Minuten bei 15.000 U/min zentrifugiert und dann mindestens dreimal mit Isopropanol gewaschen und schließlich 5 Minuten bei 6000 U/min zentrifugiert, um die groben Partikel zu entfernen.
Sb2 S3 QDs wurden bei Raumtemperatur vakuumgetrocknet und dann mit einem simultanen Thermoanalysator (STA 449 F3, NETZSCH) getestet. Die Kristallstruktur wurde durch Röntgenbeugung (XRD, Bruker D8) charakterisiert. Die Zusammensetzungsmessung wurde mit einem energiedispersiven Spektrometer (EDS, EDAX Inc.) durchgeführt. Sb2 S3 Pulver (99,99%, Aladdin) wurde als Standard für die Kalibrierung von EDS-Messungen verwendet. Nanoskalige Informationen von QDs wurden durch hochauflösende Transmissionselektronenmikroskopie (HRTEM; Zeiss Libra200) mit Selected-Area-Elektronenbeugung (SAED) charakterisiert. Die Emissionsspektren wurden mit photolumineszenzspektroskopischer Technik (PL, Horiba iHR550) mit einem He-Ne-Laser (325 nm) als Anregungsquelle aufgenommen. Optische Transmissionsspektren wurden an QD-Dispersion und Filmen unter Verwendung eines UV-Vis-IR-Spektrophotometers (Agilent Cary 5000) durchgeführt.
Ergebnisse und Diskussion
Die Synthese von Sb2 S3 QDs ist ein kostengünstiger, einfacher Vorgang und wiederholbarer Prozess. Die chemische Reaktion kann in den folgenden zwei einfachen Reaktionsgleichungen beschrieben werden.
$$ {\mathrm{CH}}_3{\mathrm{CSNH}}_2+2{\mathrm{CH}}_3{\mathrm{OCH}}_2{\mathrm{CH}}_2\mathrm{O}\ mathrm{H}\to {\mathrm{CH}}_3\mathrm{C}{\left({\mathrm{CH}}_3{\mathrm{OCH}}_2{\mathrm{CH}}_2\mathrm{ O}\right)}_2{\mathrm{NH}}_2+{\mathrm{H}}_2\mathrm{S} $$ (1) $$ 2\mathrm{S}\mathrm{b}{\left( {\mathrm{CH}}_3\mathrm{COO}\right)}_3+3{\mathrm{H}}_2\mathrm{S}\to {\mathrm{S}\mathrm{b}}_2{\ mathrm{S}}_3+6{\mathrm{CH}}_3\mathrm{COO}\mathrm{H} $$ (2)Nach dem LaMer-Modell [18] ist die Trennung von Nukleations- und Kristallwachstumsstadien die Hauptvoraussetzung für die Bildung kleiner Partikel mit engen Größenverteilungen. Im frühen Stadium dieser Reaktion neigte die Lösung mit äquimolarem SDS/CTAB dazu, relativ größere katanionische Vesikel statt gemischter Micellen zu bilden [16]. Die Reaktion zwischen S 2− und Sb 2+ erfolgte schnell, was zu der explosiven Nukleation führte. Als nächstes verringert die Bildung der Metallionen-ETDA-Komplexe aufgrund des Chelatisierungseffekts die Konzentration der freien Metallionen [19]. Somit wurde das Kornwachstum wirksam gehemmt, wobei Sb2 . zurückblieb S3 QDs in der Lösung.
Der Einfluss von Temperatur und Reaktionszeit auf die Morphologien von QDs wurde zuerst untersucht. Wir fanden heraus, dass Form und Größe nahezu unveränderlich waren, wenn die Temperatur von 90 bis 120 °C variierte und die Reaktionszeit von 30 s bis 15 min kontrolliert wurde. Abbildung 1a, b zeigen ein TEM-Bild und ein hochauflösendes Bild der Probensynthese bei 120 °C. Die Bilder zeigen eine gute Monodispersität von QDs mit einer einheitlichen Kugelform, und die Durchmesser liegen hauptsächlich im Bereich von 3 bis 5 nm. Das hochauflösende Bild zeigt einen klaren Gittersaum, der zeigt, dass jedes Teilchen ein monokristallines Quant ist. SAED weist einige konzentrische Kreise mit undeutlichen Grenzen auf, was darauf hindeutet, dass das synthetisierte Nanomaterial eine geringe Kristallinität aufweist. Die chemischen Zusammensetzungen wurden durch EDS analysiert, wie in Abb. 1c gezeigt. Eine quantitative elementare EDS-Analyse von QDs zeigt, dass das durchschnittliche Atomverhältnis (S%:Sb%) 1,68 beträgt, was darauf hindeutet, dass das stöchiometrische Verhältnis des Schwefelelements etwas höher ist. Wir folgerten, dass etwas Schwefel an der Oberfläche von QDs chemisorbiert oder physikalisch adsorbiert wurde. Abbildung 1d zeigt das XRD-Spektrum von vakuumgetrockneten QDs. Grob gesagt entspricht das XRD-Muster dem orthorhombischen Sb2 S3 (JCPDS Nr. 73-0393), die die Ergebnisse der EDS-Analyse bestätigt. Die undeutlichen XRD-Peaks weisen auf die niedrige Kristallinität hin, die mit dem SAED-Muster recht gut übereinstimmt.
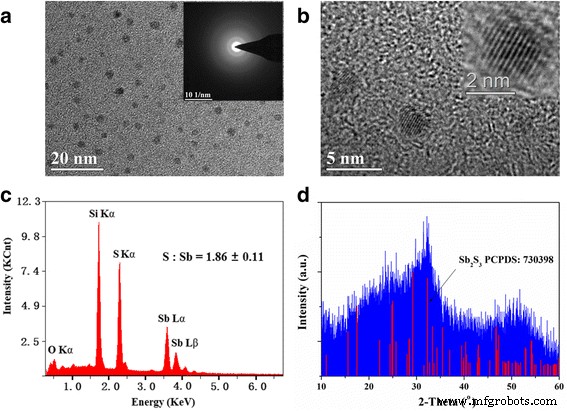
Morphologie und strukturelle Eigenschaften von Sb2 S3 QDs. a TEM-Bild und SAED-Muster. b Hochauflösendes TEM-Bild. c EDS-Analyse und d XRD-Muster
Die optische Absorption der QDs-Isopropanol-Dispersion wurde mit einem Agilent Cary 5000 Spektrophotometer gemessen. Wie wir in Abb. 2a sehen, ist Sb2 S3 QDs-Dispersion ist hellgelb und hat eine breite Absorption im fast gesamten sichtbaren Bereich. Es zeigt eine nahezu vollständige Absorption bei kurzen Wellenlängen von 300 bis 500 nm und eine hohe Transmission im nahen Infrarotbereich. Abbildung 2b zeigt die Photolumineszenzspektren (PL) der Dispersion mit einer Konzentration von 2 mg/ml, wobei Sb2 S3 wurde mit unterschiedlichen Reaktionszeiten hergestellt. PL-Spektren für alle Sb2 S3 Proben zeigen zwei unterschiedliche Emissionspeaks bei etwa 510 nm (2,43 eV) und 880 nm (1,41 eV), was sich deutlich von nanostrukturiertem Sb2 . unterscheidet S3 hergestellt durch chemische Lösungsabscheidung (CBD) [20]. Laut dem vorherigen Bericht ist CBD-synthetisiertes Sb2 S3 Nanokristalle zeigen eine schwache Bandkantenemission mit einem Spitzenwert bei etwa 610 nm (2,03 eV), die vermutlich auf Exzitonen zurückzuführen ist, und eine durch Schwefelleerstellen bedingte starke Emission mit einem Spitzenwert bei 717 nm (1,72 eV). Für wasserlösliches Sb2 S3 QDs hier, die grüne Emission um 510 nm resultiert vermutlich aus Exzitonen [21, 22], die für Halbleiter-Nanokristalle bekannt und weit verbreitet sind [23], was darauf hindeutet, dass der Quantengrößeneffekt (QSE) eine breitere Bandlücke für Sb2 S3 QDs. Die Emission im nahen Infrarot um 880 nm kann auf das Vorhandensein von stöchiometriebezogenen Punktdefekten zurückgeführt werden. Gemäß der oben diskutierten EDS-Analyse beträgt das durchschnittliche Atomverhältnis (S%:Sb%) 1,68; Wir folgerten, dass Schwefel übermäßig ist und die Art von Punktdefekten hier wahrscheinlich Antimon-Leerstellen sind (V * Sb ). Eine sorgfältige Beobachtung der Kurven zeigt, dass die Emission von Sb2 . bei 880 nm ihren Höhepunkt erreichte S3 QDs, die mit langer Reaktionszeit hergestellt wurden, zeigen im Vergleich zu schnell synthetisierten QDs eine leichte Blauverschiebung. Diese Verschiebung ist wahrscheinlich auf die leichte Verbesserung des stöchiometrischen Verhältnisses zurückzuführen. Die intensive PL-Emission und die hohe Transmission im nahen Infrarotbereich weisen darauf hin, dass Sb2 S3 QDs haben gute Aussichten bei der Herstellung von Nahinfrarot-LEDs [17, 24] und Nahinfrarot-Lasern, die in der Sensorik und Sondierung eingesetzt werden.
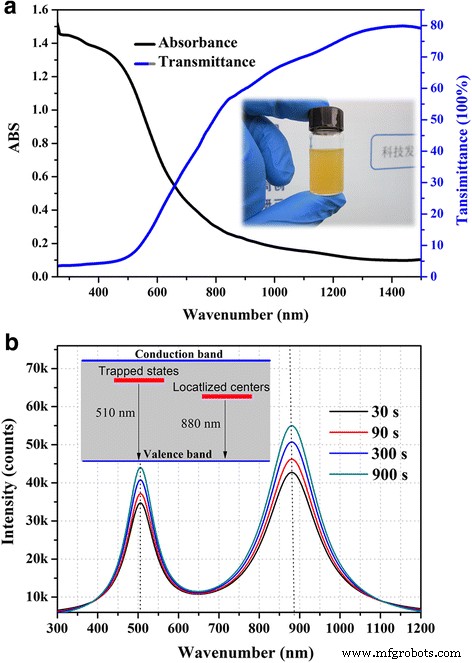
Optische Eigenschaften von Sb2 S3 QD-Dispersion. a Absorption und b PL-Spektrum von Sb2 S3 Streuung
Um die Anwendungen von Sb2 . weiter zu studieren S3 QDs in der Halbleiterverarbeitung, Sb2 S3 Filme wurden durch Selbstorganisationswachstum auf Glas aus einer 5 mg/ml QDs-Isopropanol-Dispersion hergestellt. Vor der Glühbehandlung wurde eine thermogravimetrische Analyse für den Stabilitätstest verwendet. Gemäß TG- und DSC-Profilen für die vakuumgetrockneten QDs in Abb. 3a, Sb2 S3 QDs weisen ab Raumtemperatur eine Gewichtszunahme von ungefähr 12% auf, was darauf hindeutet, dass diese eine hohe Aktivität aufweisen und wahrscheinlich teilweise oxidiert oder an der Oberfläche haften. Sb2 S3 QDs zeigen eine relative Stabilität in Argon bei Raumtemperatur und zeigen dann den ersten offensichtlichen Gewichtsverlust, gefolgt von der Entfernung von überschüssigem S, die bei 236 °C begann. Der Schmelzpunkt von Sb2 S3 QDs wurde mit 508 °C gemessen, was deutlich niedriger ist als die von kristallinem Sb2 S3 Pulver (550 °C, Sigma Aldrich). Wir stellten fest, dass es im gesamten Testtemperaturbereich einen allmählichen langsamen Gewichtsverlust gab, der von einem S-Bestandteilverlust begleitet wurde. Sb2 S3 Anschließend wurde die Glühbehandlung von QD-Filmen in Ar- und Se-Dampf untersucht. Optische Transmissionsspektren für unbehandelte, getemperte und selenisierte Filme sind in Fig. 3b gezeigt, und die Fotografie der drei Proben ist in Fig. 3c gezeigt. Bei den getemperten und selenisierten Proben wurden beide 5 Minuten lang bei 250 °C behandelt. Die absorbierenden Kanten der getemperten und selenisierten Proben wurden von 500 nm auf 650 nm bzw. 850 nm verschoben. Da sowohl Sb2 S3 und Sb2 Se3 Halbleiter mit direkter Bandlücke sind [24, 25], könnte die durchschnittliche Bandlücke nach folgender Formel berechnet werden:
$$ \upalpha =\left(A/\mathrm{h}\upnu \right)\times {\left(\mathrm{h}\upnu -\mathrm{Eg}\right)}^{1/2} $ $ (3)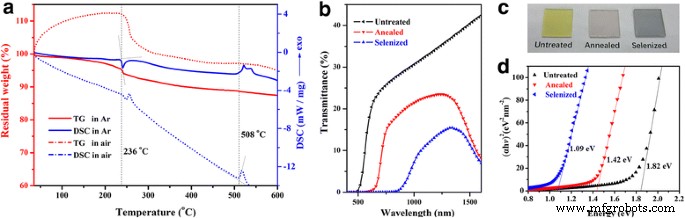
Photoelektrische Eigenschaften von Sb2 S3 QD-Dünnschichten. a TG- und DSC-Profile von getrocknetem Sb2 S3 QDs getestet in Ar und Luft. b Transmissionsspektrum, c ein Foto und d Bandlückenanalyse von vor- und nachgetempertem Sb2 S3 QD-Dünnschichten
wo A ist eine Konstante, h ist die Plancksche Konstante und ν ist die Frequenz des einfallenden Photons. Wir haben die lineare Zone angepasst, indem wir (αhv ) 2 gegen (hv ) und berechnete den Durchschnitt E g wie in Abb. 3 gezeigt. Wie wir sehen, ist das E g der unbehandelten Probe betrug 1,82 eV und sank auf 1,42 eV nach 5-minütigem Tempern bei 250 °C. Die Variation von E g gibt die Kristallinität von Sb2 . an S3 wurde durch eine Ordnungs-Unordnungs-Transformation verbessert, begleitet von der Entfernung von überschüssigem S-Element [26]. Für die selenisierte Probe ist das E g auf ein Minimum von 1,09 eV gesenkt, was sehr nahe an kristallinem Silizium liegt. Die quantitative elementare EDS-Analyse ergab, dass Sb2 S3 wurde in Sb2 . umgewandelt (S1−x Se x )3 und schließlich zu Sb2 Se3 nachdem der größte Teil des Schwefels durch Selen ersetzt wurde [7, 9]. Da die Selenylierung unter 250 °C liegt, war dies unserer Meinung nach für die Herstellung und Leistungssteigerung flexibler Geräte von Vorteil. Wie wir wissen, betrug die optimale Bandlücke für Solarzellenabsorber 1,45 eV. Somit wird das geglühte und selenisierte Sb2 S3 QD-Filme sind gute Kandidaten für photovoltaische Absorbermaterialien.
Schlussfolgerungen
Ein neuer Weg zur Synthese von wasserlöslichem Sb2 S3 QDs wurde durch Heißinjektion unter Verwendung von CTAB- und SDS-Mischungen als anionisch-kationisches Tensid, DEA als Stabilisator und EDTA als Dispergiermittel entwickelt. Der Syntheseprozess ist einfach zu bedienen und wiederholbar. Alle Reagenzien und Zusatzstoffe sind ungiftig, geruchlos und kostengünstig. Sb2 S3 QDs haben eine intensive PL-Emission bei 880 nm und eine hohe Transmission im Nahinfrarotbereich, was darauf hindeutet, dass sie gute Aussichten bei der Herstellung von Nahinfrarot-LEDs und Nahinfrarot-Lasern haben. Sb2 S3 QDs zeigen eine gute Monodispersität und Verarbeitbarkeit, die zu Sb2 . abgeschieden werden können S3 Filme. Das E g von Sb2 S3 QD-Filme konnten nach einer Glühbehandlung in Ar- oder Se-Dampf bei weniger als 250 °C auf 1,42 und 1,09 eV gebracht werden, was ihre guten Aussichten für Photovoltaikanwendungen demonstriert.
Abkürzungen
- CBD:
-
Abscheidung chemischer Lösungen
- CTAB:
-
Hexadecyltrimethylammoniumbromid
- DEA:
-
Alkanolamid
- DSC:
-
Differenzkalorimeter
- EDS:
-
Energiedispersives Spektrometer
- EDTA:
-
Ethylendiamintetraessigsäure
- HRTEM:
-
Hochauflösende Transmissionselektronenmikroskopie
- LED:
-
Leuchtdiode
- OLED:
-
Organische Leuchtdiode
- PL:
-
Photolumineszenz
- QD:
-
Quantenpunkt
- QSE:
-
Quantengrößeneffekt
- SAED:
-
Elektronenbeugung in ausgewählten Bereichen
- SDS:
-
Natriumdodecylsulfat
- STA:
-
Simultaner Thermoanalysator
- TAA:
-
Thioacetamid
- TGA:
-
Thermogravimetrische Analyse
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Einfache Synthese und optische Eigenschaften kleiner Selen-Nanokristalle und -Nanostäbe
- Synthese von reabsorptionsunterdrückten Typ-II/Typ-I-ZnSe/CdS/ZnS-Kern/Schale-Quantenpunkten und ihre Anwendung für Immunsorbent-Assays
- Synthese von Pyridin-reichen N,S-codotierten Kohlenstoff-Quantenpunkten als wirksame Enzymnachahmer
- Auswirkung der Synthesemethode von La1 − xSr x MnO3 Manganit-Nanopartikeln auf ihre Eigenschaften
- Eintopfsynthese von Cu2ZnSnSe4-Nanoplatten und ihre durch sichtbares Licht getriebene photokatalytische Aktivität
- Einfache sonochemische Synthese in einem Schritt und photokatalytische Eigenschaften von Graphen/Ag3PO4-Quantenpunkt-Kompositen
- Abhängigkeit der Nanopartikeltoxizität von ihren physikalischen und chemischen Eigenschaften
- Material und optische Eigenschaften von fluoreszierenden Kohlenstoff-Quantenpunkten, die durch hydrothermale Reaktion aus Zitronensaft hergestellt werden
- 20 verschiedene Metallarten und ihre Eigenschaften
- Arten von Metallen und ihre Eigenschaften



