Schwefelsäureunterstützte Herstellung von rot emittierenden karbonisierten Polymerpunkten und Anwendung von Bio-Imaging
Zusammenfassung
Rot emittierende karbonisierte Polymerpunkte (CPDs) wurden aus p . hergestellt -Phenylendiamin (p -PD) wässrige Lösung mit Hilfe von Schwefelsäure (H2 .) SO4 ) und die optischen Eigenschaften und die Anwendung der Bio-Bildgebung wurden in diesem Artikel untersucht. Im Vergleich zu anderen stark säureunterstützten Systemen sind SA-CPDs (hergestellt aus H2 SO4 -unterstütztes System, durchschnittlicher Durchmesser beträgt ~ 5 nm) ist am hellsten. Die Photolumineszenz-Quantenausbeute (QYs) beträgt 21,4% (in Wasser) und die Produktausbeute 16,5%. Die wässrige Lösung von SA-CPDs emittiert bei 600 nm, wenn sie durch Licht von 300 bis 580 nm angeregt wird. Die Emissionswellenlänge ist unabhängig von der Anregungswellenlänge. Die Bildungsenergien von CPDs wurden auf zwei Arten berechnet, um zu zeigen, dass das Längswachstum (Bildung von Polymeren) schwierig ist und das Querwachstum (Bildung von CPDs) einfach ist. Darüber hinaus wurden die Zweiphotonen-Photolumineszenzeigenschaften (emittiert bei 602 nm bei Anregung mit einem 850 nm Femtosekunden-Pulslaser) von SA-CPDs in den Experimenten zur Färbung von HeLa-Zellen genutzt und haben gezeigt, dass sie potenzielle Anwendungen in der Biobildgebung haben.
Hintergrund
Carbon Dots (CDs) haben aufgrund ihrer Vorteile wie ausgezeichnete Wasserlöslichkeit, optische Stabilität, einzigartige Fluoreszenzeigenschaften, geringe Toxizität, niedrige Kosten usw. viel Aufmerksamkeit auf sich gezogen [1]. Die meisten CDs wurden als potenzielle Kandidaten für verschiedene Anwendungen untersucht, wie zum Beispiel elektrochemische Immunsensoren [2], Bio-Imaging-[3,4,5,6]-Sensoren [7,8,9,10,11,12], Photo- Katalyse [13,14,15], lichtemittierende Bauelemente [16] und Optoelektronik [17,18,19]. Bei den Untersuchungen zu den optischen Eigenschaften und Anwendungen spielt die Synthese von CDs eine wichtige Rolle. Die beschriebenen Ansätze zur Herstellung von CDs lassen sich hauptsächlich als „top-down“ aus verschiedenen Kohlenstoffmaterialien und „bottom-up“ aus organischen Molekülen, Polymeren oder Naturstoffen zusammenfassen [20]. Die „bottom-up“-Methoden sind effiziente Wege zur Synthese fluoreszierender CDs im großen Maßstab [21]. Gruppen in den aufgetragenen Molekülen einschließlich –OH, –COOH, –C=O und –NH2 kann bei erhöhter Temperatur durch Hydrothermal, Mikrowelle, Verbrennung, Pyrolyse usw. entwässert und karbonisiert werden.
Rot emittierende Punkte haben aufgrund der größeren Eindringtiefe im Bio-Imaging-Bereich erhebliches Interesse geweckt. Insbesondere die reinen Farbpunkte sind für eine bestimmte Gelegenheit kritisch, da die von der Anregungswellenlänge unabhängigen Lumineszenzmaterialien ein einzelnes und stabiles Photolumineszenz-(PL)-Licht liefern können. Die meisten Emissionen von CDs sind von der Anregungswellenlänge abhängig, und CDs emittieren normalerweise blaues, grünes oder gelbes Licht, wenige CDs emittieren helles rotes Licht [22].
Vor kurzem wurden Isomere von Phenylendiamin (PD) wie o -, m -, und p -PD, wurde als Kohlenstoffquelle zur Herstellung von CDs untersucht [8, 9, 23, 24]. Blau, grün und rot emittierende CDs können von m . hergestellt werden -, o -, und p -PD-Ethanollösung bzw. [23]. Vollfarbige lichtemittierende CDs können aus p . hergestellt werden -PD und wässrige Harnstofflösung [24]. In unserer früheren Arbeit [25] haben wir vorgeschlagen, dass neue rote Kohlenstoffpunkte (Quantenausbeuten = 15,8%, in Wasser) leicht aus „p . synthetisiert werden können -PD + HNO3 ” wässriges System und wird beim Nachweis von Metallionen in Wasser eingesetzt. Vor kurzem wurde das ähnliche „o -PD + H3 PO4 “ [26] und „o -PD + HNO3 ” [27] wurden Systeme beschrieben, und Liu et al. [27] benannten ihre CDs (QYs = 10.8%, in Wasser) in „carbonized polymer dots (CPDs)“ um. Im Gegensatz zu den herkömmlichen Kohlenstoffpunkten hängen die Emissionswellenlängen der CPDs nicht von der Anregungswellenlänge ab, und daher sollten die PD-basierten „CDs“ genauer als CPDs bezeichnet werden.
Hier berichten wir über eine einfache und hocheffiziente Methode der stark säureunterstützten hydrothermalen Route zur Herstellung von rot emittierenden CPDs und die Anwendung von Bio-Imaging mit Zwei-Photonen-Photolumineszenz-Eigenschaften. Ein Mechanismus zur Bildung von CPDs wird unter Verwendung des Programmpakets Gaussian 09 vorgeschlagen.
Methoden
Synthese von roten CPDs aus säureunterstütztem p -PD-Systeme
Basierend auf unseren früheren Arbeiten [25] haben wir Schwefelsäure (H2 SO4 ), Salzsäure (HCl) und Perchlorsäure (HClO4 ) als Assistenten für die Herstellung von roten CPDs wurden die entsprechenden CPDs als SA-CPDs, HC-CPDs bzw. PA-CPDs gekennzeichnet. Um die experimentellen Bedingungen von H2 . zu optimieren SO4 -unterstütztes System, wir haben mehrere Parameter ausgewählt, wie zum Beispiel c (Säure) bis c (p -PD) Verhältnis, c (p -PD), Temperatur (T ) und Reaktionszeit (t ). CPDs-Produkte wurden mit Hexan gewaschen, um das nicht umgesetzte p . zu entfernen -PD und durch Ethylalkohol zur Entfernung von Säuren, zentrifugiert bei 14000 U/min für 30 Minuten, um Polymerausfällungen zu entfernen, und durch eine 0,22 μm-Filtermembran filtriert. Wenn Pulver erwünscht ist, kann die gereinigte CPDs-Lösung mit einem Rotationsverdampfer bei 80 °C und einem niedrigen Vakuum fast trocken eingedampft werden (der Rest ist in Pulverform).
Charakterisierung und Messung
Hochauflösende TEM-Bilder (HR-TEM) wurden mit dem Transmissionsmikroskop JEM-2100 aufgenommen, das bei 200 kV betrieben wurde. Infrarotspektren von CPDs-Lösungen wurden unter Verwendung von Prestige-21 FT-IR-Spektrometer unter Verwendung von KRS-5-Fensterscheiben (Mischung aus TlBr und TlI) gesammelt, typischerweise wurden flüssige Phasen auf eine Scheibe getropft und getrocknet. Die Scheibe wurde von der anderen Scheibe abgedeckt und auf dem Prüfstand fixiert. Dann wurden die Infrarotspektren aufgenommen.
Die Fluoreszenzspektren von CPDs wurden auf einem F-2500-Fluoreszenzspektrophotometer gemessen. UV-Vis-Absorptionsspektren wurden auf einem Lambda 950 UV/VIS/NIR-Spektrometer aufgezeichnet. Die Zweiphotonen-Emissionsspektren von CPDs wurden mit einem Faserspektrographen (QE65000, Ocean Optics) im Mikroskopsystem aufgenommen. Die wässrige Lösung von SA-CPDs und die wiederaufgelöste Lösung des Pulvers wurden auf Objektträger zentrifugiert und die Zweiphotonen-Photolumineszenzeigenschaften wurden dann gemessen.
Photolumineszenz-Quantenausbeuten (QYs) der CPDs wurden mit Rhodamin B (QYs = 56% in Ethanol) als Referenzfarbstoff im Emissionsbereich von 580–610 nm bei Anregung mit 365 nm UV-Licht gemessen [25, 28], das Verfahren von QYs-Messungen wurden in der zusätzlichen Datei 1 angezeigt.
Berechnungsmethoden
Für die Berechnungen der Dichtefunktionstheorie (DFT) wurde das Paket Gaussian 09 verwendet [29]. Die Gleichgewichtsstrukturen wurden durch die B3LYP-Methode in Verbindung mit dem 6–311++G (d)-Basissatzniveau optimiert [30]. Um die Rolle von Lösungsmitteleffekten zu untersuchen, wurde Wasser in einem polarisierten Kontinuumsmodell (PCM) verwendet. Frequenzanalysen wurden mit demselben Pegel durchgeführt, um zu bestätigen, dass jede optimierte Struktur einem stationären Punkt entsprach.
Zellkultur und Behandlung
1,35 ml HeLa-Zellen in Dulbecco's Modified Eagle Medium (DMEM; Gibco) mit einer Anfangsdichte von 4 × 10 4 Zellen pro Milliliter wurden in jede Schale ausgesät und bei 37 °C für 24 Stunden unter einer befeuchteten Atmosphäre mit 5 % CO2 . kultiviert . SA-CPDs-Pulver wurden in Wasser wieder aufgelöst, um die Reservelösung herzustellen (400 μg ml − 1 ). 1350 μl-Zellen wurden mit 150 μl SA-CPDs-Reservelösung kultiviert (die Endkonzentration beträgt 40 μg ml − 1 ) für 12 h und dann dreimal mit PBS gewaschen, um die freien SA-CPDs zu entfernen. Schließlich wurden die Ergebnisse der zellulären Bildgebung mit einem konfokalen Mikroskop unter 850-nm-Femtosekunden-Laseranregung (30 mW) gesammelt.
Ergebnisse und Diskussion
Optimierung der Vorbereitung auf rote CPDs
In Basisexperimenten wurden verschiedene säureunterstützte Systeme mit unterschiedlichen Konzentrationsverhältnissen, Reaktionstemperaturen und -zeiten untersucht (siehe Zusatzdatei 1:Abbildung S1). Wir fanden heraus, dass rote CPDs über 180 °C (Reaktion für 2 h) für verschiedene Säuresysteme gebildet werden können und die Reaktionen nicht durch Anionen in den Lösungen beeinflusst werden. Langzeit (4–12 h, 240 °C für H3 .) PO4 und HF-Systeme, siehe Zusatzdatei 1:Abbildung S1f) die Reaktion wird die Partikelgröße erhöhen und die rote Fluoreszenz wird schließlich verblasst, während die Fluoreszenzänderung beim HCl-System nicht offensichtlich ist (2–6 h, 200 °C, siehe Zusatz Datei 1:Abbildung S2). Unter Berücksichtigung der Energieeinsparung und der oberen Temperaturgrenze des Teflon-Liners werden die optimale Temperatur und Reaktionszeit mit 200 °C bzw. 2 h gewählt. Basierend auf der Optimierungsstrategie von p -PD + HCl-System (siehe Zusätzliche Datei 1:Abbildung S2), wir haben das p . optimiert -PD + H2 SO4 und p -PD + HClO4 Systeme und erhalten die in Tabelle 1 gezeigten Optimierungsergebnisse.
SA-CPDs, HC-CPDs und PA-CPDs wurden aus p . hergestellt -PD-Lösung mit Hilfe von H2 SO4 , HCl und HClO4 , bzw. Das optimierte c (Säure) bis c (p -PD) Verhältnisse von H2 SO4 -, HCl- und HClO4 -unterstützte Systeme sind 1, 3 bzw. 3 (siehe Zusätzliche Datei 1:Abbildung S3a). Das passende c (p -PD) Bereich für die Herstellung von roten CPDs ist breit (von 0,02 bis 0,20 mol L − 1 ). Die optimierte Temperatur (T ) und die Reaktionszeit (t ) sind 200 °C und 2 h. SA-CPDs sind die hellsten roten CPDs mit einem hohen QY von 21,4 % (zusätzliche Datei 1:Abbildung S3b). Es gibt zwei Gründe, warum H2 SO4 -assisted carbon dots haben eine bessere Qualität als HCl-, HClO4 -, und HNO3 -assistierte (veröffentlicht in unserer früheren Arbeit [25]). Zuerst H2 SO4 ist eine nichtflüchtige starke Säure, die ihre Acidität in einer Hochtemperatur- und Hochdruckreaktionslösung beibehält. Zweitens H2 SO4 -unterstütztes System ist das einzige, das eine Ammoniumsalzausfällung im Vorläufer bilden kann, und die Ausfällungen setzen die freien Reaktanten langsam frei, wodurch die Bildung von Polymerausfällungen mit großen Partikeln vermieden und die Bildung hochwertiger Kohlenstoffpunkte weiter gefördert wird. HA-CPDs und PA-CPDs sind dunkelrot-braune dicke Lösungen und emittieren dunkelroten PL unter 365-nm-UV-Licht-Bestrahlung, während die vorbereiteten SA-CPDs eine hellrote transparente dünne Lösung sind und hellrotes Licht emittieren (Zusätzliche Datei 1:Abbildung S3c). Nach Reinigung durch Waschen, Konzentrieren, Filtrieren und Eindampfen wurden dunkelrot-braune Pulver von SA-CPDs (Zusatzdatei 1:Abbildung S3d) mit einer Produktausbeute von 16,5 % erhalten. Die Pulver können in Wasser wieder aufgelöst werden und die Lösung emittiert eine helle und rote Fluoreszenz (Zusatzdatei 1:Abbildung S3e).
TEM-Charakterisierung und FT-IR-Analyse
TEM-Bilder einer OpPD-Probe (ohne H2 .) SO4 ) und SA-CPDs (mit H2 SO4 ) wurden in Abb. 1 gezeigt. OpPD-Probe besteht aus Fragmenten (Oligomere, Abb. 1a) und Polymeren (Abb. 1a-Einsatz). SA-CPDs sind monodisperse CPDs mit einer durchschnittlichen Größe von ~ 5 nm (Abb. 1c). Es zeigt gut aufgelöste Gitterfinger mit einem Abstand von ~ 0,21 nm (Abb. 1b Insert), was dem (100) Gitterabstand von Graphen in der Ebene entspricht [31, 32].
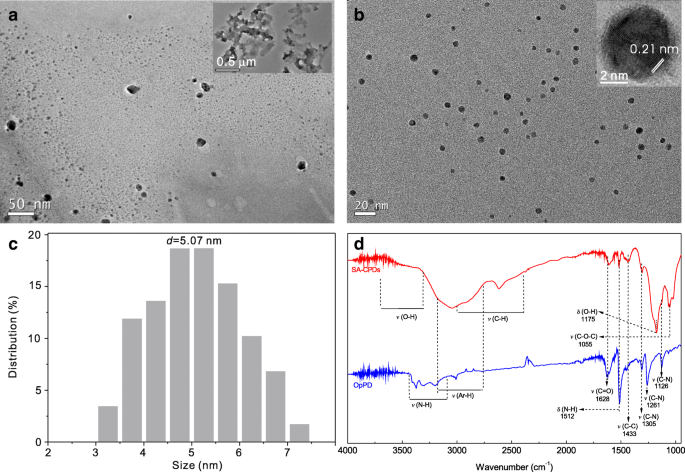
TEM-Bilder einer OpPD-Probe (ohne H2 .) SO4 ) (a ) und SA-CPDs (b ). c Die Größenverteilung von SA-CPDs. d Die FT-IR-Spektren von Proben-OpPD und roten CPDs. Proben von OpPD und SA-CPDs wurden von p . hergestellt -PD wässrige Lösung ohne und mit H2 SO4 -unterstützt
Oberflächenzustände von CPDs können die optischen Eigenschaften beeinflussen. Die oberflächenchemischen Gruppen der OpPD- und SA-CPD-Proben wurden durch FT-IR-Spektren charakterisiert (Abb. 1d). Zwei Proben haben mehrere ähnliche Gruppen, z. B. Ar-H (2700–3200 cm − 1 [33], gehört zur aromatischen C-H-Streckschwingung), C-C (~ 1433 cm − 1 , gehört zur aromatischen C-Knochen-Streckschwingung, zeigt das Vorhandensein aromatischer Streckschwingungen, die für Benzenoid-Einheiten charakteristisch sind) [34] und C=O (1628 cm − 1 , gehört zu den –COOH-Gruppen). Im Vergleich zu Beispiel-OpPD sind die neuen Gruppen wie O-H (3300–3700 cm − 1 und 1175 cm − 1 gehören zu den –COOH-Gruppen), C-O-C (1055 cm − 1 , in Estern vorkommen) und C-H (2400–3000 cm − 1 gehört zu den bei Ringöffnungsreaktionen gebildeten Alkylradikalen), findet man in den CPDs, während das –NH2 oder –NH– verwandte Gruppen wie N-H (3100–3300 cm − 1 und 1512 cm − 1 und C-N (1126, 1261 und 1305 cm – 1 gehören zum freien –NH2 oder –NH– Gruppen aus p -PD-Vorläufer, sind geschwächt oder verschwunden. Die Existenz von –OH- oder –COOH-Gruppen weist darauf hin, dass der Oxidationsgrad der Oberfläche von SA-CPDs (mit H2 SO4 Zugabe) ist höher als die der Probe OpPD (ohne Säurezugabe).
Vorgeschlagener Mechanismus zur Bildung von CDs
Die Bildungsenergien wurden mit dem Programmpaket Gaussian 09 berechnet. Nach der Protonierung durch Säureunterstützung können Bipolymere auf zwei Arten polymerisiert werden, die als Längs- und Querwachstum bezeichnet werden. Die berechnete Bildungsenergie des transversalen Wachstums (− 1406.07 kJ mol − 1 ) ist deutlich höher als beim Längswachstum (− 616,25 kJ mol − 1 ). Es zeigt, dass die vollständig protonierten Bipolymere (pH 3, nach überschüssigem H + hinzugefügt wurde) neigen dazu, in Querrichtung zu einer planaren Struktur zu polymerisieren (Abb. 2). Diese planaren Strukturen wurden dann selbstorganisiert, um sphärische CPDs zu bilden.
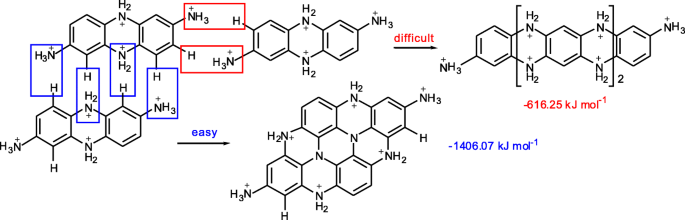
Bildungsenergien von Längs- und Querwachstum
Optische Eigenschaften
Obwohl sie mit Hilfe verschiedener Säuren hergestellt werden, haben alle CPDs ähnliche optische Eigenschaften [25]. Für die UV-Vis-Spektren der wässrigen Lösung von SA-CPDs (Abb. 3a) ist der Absorptionspeak bei ~ 290 nm mit den Übergängen im Benzolring verbunden, und die Peaks bei 430 nm und 510 nm könnten π . zugeordnet werden -π*-Übergang von substituiertem Phenazin, konjugiert an die einsamen Elektronenpaare der benachbarten Amingruppe bzw. der Elektronenübergang vom benzenoiden Ring zu den chinoiden Ringen [32]. Die Anregungskurve beschreibt einen breiten und allmählichen Aufwärtstrend im sichtbaren Bereich, und der maximale Anregungspeak (~ 580 nm) liegt nahe dem Emissionspeak (~ 600 nm). Die CPDs emittieren im Rotlichtbereich (600–700 nm), wenn sie von 220 nm bis 310 nm angeregt werden, während sie bei orangefarbenem Licht (~ 600 nm) emittieren, wenn sie von 310 nm bis 580 nm angeregt werden (Abb. 3b). Es ist erwähnenswert, dass die Fluoreszenz dieser Art von rot emittierenden CPDs von der Anregungswellenlänge unabhängig ist [22, 35].
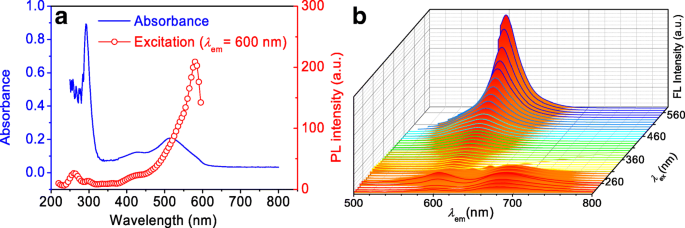
a UV-Vis-Absorption, Anregung (Peak bei 600 nm) und b Emissionsspektren (angeregte 220–580 nm) von SA-CPDs
Mobile Bildgebung
Die Zweiphotonen-Photolumineszenzeigenschaften von SA-CPDs vor und nach dem Pulverisierungsprozess sind in Abb. 4a gezeigt. Es gibt eine Blauverschiebung von 602 nm (vor dem Pulverisierungsprozess) auf 529 nm (nach dem Pulverisierungsprozess) bei derselben Anregungswellenlänge von 850 nm durch einen Femtosekunden-Pulslaser (30 mW). Die PL-Intensität wurde nach dem Pulverisieren erhöht.
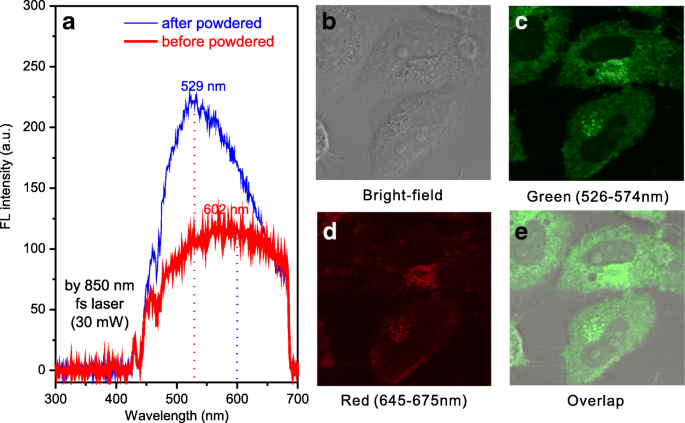
Zweiphotonen-Photolumineszenzspektren von SA-CPDs (a ) und konfokale Fluoreszenzmikroskopiebilder von HeLa-Zellen, die mit SA-CPDs behandelt wurden, die mit einem 850 nm, 30 mW-Femtosekunden-Pulslaser angeregt wurden (b –e )
SA-CPDs-Pulver wurden in PBS (1X) wieder aufgelöst und bei der Bildgebung von HeLa-Zellen mit konfokaler Fluoreszenzmikroskopie und einem 850-nm-Femtosekunden-Pulslaser (30 mW) angewendet (siehe Abb. 4b–e). Nach 12 stündiger Kultivierung mit HeLa-Zellen wurden SA-CPDs von HeLa-Zellen geschluckt und CPDs traten in das Zytoplasma ein. Die FL-Intensität des Rotkanals (645–675 nm) ist schwach, während die des Grünkanals (526–574 nm) hell ist. Sie stimmt mit der Blauverschiebung beim Puderprozess überein.
Schlussfolgerungen
Es wurde über eine einfache Methode der säureunterstützten hydrothermalen Route zur Herstellung von Kohlenstoffpunkten und die Anwendung von Bio-Imaging berichtet. Innerhalb von H2 SO4 -, HCl- und HClO4 -unterstützte Systeme, SA-CPDs erstellt aus H2 SO4 -unterstützte Systeme sind die hellsten CPDs mit einer durchschnittlichen Größe von ~ 5 nm, einer QYs von 21,4 % und einer Produktausbeute von 16,5 %. Die wässrige Lösung von SA-CPDs emittiert bei 600 nm, wenn sie durch Licht von 300 bis 580 nm angeregt wird. Die Emissionswellenlänge ist unabhängig von der Anregungswellenlänge. Darüber hinaus haben SA-CPDs Zweiphotonen-Photolumineszenzeigenschaften, die bei 602 nm emittieren, wenn sie mit einem 850 nm Femtosekundenpulslaser (30 mW) angeregt werden. Das Verfahren wurde auch bei der Bildgebung für HeLa-Zellen verwendet und hat das Potenzial beispielsweise für Bio-Imaging-Anwendungen.
Abkürzungen
- CDs:
-
Karbonpunkte
- CPDs:
-
Karbonisierte Polymerpunkte
- HC-CPDs:
-
Carbon Dots wurden aus p . hergestellt -PD mit HCl-unterstütztem System
- PA-CPDs:
-
Carbon Dots wurden aus p . hergestellt -PD mit HClO4 -unterstütztes System
- p -PD:
-
P -Phenylendiamin
- QYs:
-
Quantenerträge
- SA-CPDs:
-
Carbon Dots wurden aus p . hergestellt -PD mit H2 SO4 -unterstütztes System
Nanomaterialien
- Anwendung saurer Farbstoffe in der Welt der Stoffe
- Die Entwicklung und Anwendung von Glasfasergewebe
- Herstellung von ICA-beladenen mPEG-ICA-Nanopartikeln und ihre Anwendung bei der Behandlung von LPS-induzierter H9c2-Zellschädigung
- Synthese von reabsorptionsunterdrückten Typ-II/Typ-I-ZnSe/CdS/ZnS-Kern/Schale-Quantenpunkten und ihre Anwendung für Immunsorbent-Assays
- Ultraschmalbandiger perfekter Absorber und seine Anwendung als plasmonischer Sensor im sichtbaren Bereich
- Die Auswirkungen des Li/Nb-Verhältnisses auf die Herstellung und photokatalytische Leistung von Li-Nb-O-Verbindungen
- Die Herstellung einer Au@TiO2-Dotter-Schale-Nanostruktur und ihre Anwendungen für den Abbau und den Nachweis von Methylenblau
- Synthese von ZnO-Nanokristallen und Anwendung in invertierten Polymersolarzellen
- Untersuchung der Adhäsionskraft und des Glasübergangs dünner Polystyrolfolien durch Rasterkraftmikroskopie
- Kondensatorfolie:Eigenschaften, Aufbau und Anwendung



