F-Aktin reguliert osteoblastische Differenzierung mesenchymaler Stammzellen auf TiO2-Nanoröhren durch MKL1 und YAP/TAZ
Zusammenfassung
Titan und Titanlegierungen werden häufig in orthopädischen Implantaten verwendet. Die Modifizierung der Nanotopographie bietet eine neue Strategie zur Verbesserung der Osseointegration von Titansubstraten. Die filamentöse Aktin-(F-Aktin)-Polymerisation als mechanische Belastungsstruktur wird allgemein als an der Zellmigration, Endozytose, Zellteilung und der Aufrechterhaltung der Zellform beteiligt angesehen. Ob F-Aktin beteiligt ist und wie es bei der durch Nanoröhren induzierten osteogenen Differenzierung mesenchymaler Stammzellen (MSCs) funktioniert, muss noch geklärt werden. In dieser Studie haben wir TiO2 . hergestellt Nanoröhren auf der Oberfläche eines Titansubstrats durch anodische Oxidation und charakterisierten ihre Eigenschaften durch Rasterelektronenmikroskopie (REM), Röntgenenergiedispersionsanalyse (EDS) und Rasterkraftmikroskopie (AFM). Alkalische Phosphatase (ALP)-Färbung, Western-Blotting, qRT-PCR und Immunfluoreszenz-Färbung wurden durchgeführt, um das osteogene Potenzial, den F-Aktin-Spiegel und die Expression von MKL1 und YAP/TAZ zu untersuchen. Unsere Ergebnisse zeigten, dass der Innendurchmesser und die Rauheit von TiO2 Nanoröhren nahmen mit der anodischen Oxidationsspannung von 30 auf 70 V zu, während ihre Höhe konstant 2 μm betrug. Je größer der Rohrdurchmesser ist, desto stärker ist die Fähigkeit von TiO2 Nanotubes zur Förderung der osteogenen Differenzierung von MSCs. Die Hemmung der F-Aktin-Polymerisation durch Cyto D hemmte die osteogene Differenzierung von MSCs sowie die Expression von Proteinen, die in fokalen Adhäsionskomplexen wie Vinculin (VCL) und fokaler Adhäsionskinase (FAK) enthalten sind. Im Gegensatz dazu verstärkte die Polymerisation von F-Actin nach Jasp-Behandlung die Expression von RhoA und den Transkriptionsfaktoren YAP/TAZ. Basierend auf diesen Daten kamen wir zu dem Schluss, dass TiO2 Nanoröhren erleichterten die osteogene Differenzierung von MSCs, und diese Fähigkeit wurde mit zunehmendem Durchmesser der Nanoröhren innerhalb eines bestimmten Bereichs (30–70 V) verstärkt. F-Aktin vermittelte diesen Prozess über MKL1 und YAP/TAZ.
Einführung
Titan und Titanlegierungen werden aufgrund ihrer hervorragenden Biokompatibilität, Korrosionsbeständigkeit und mechanischen Eigenschaften häufig in klinischen Anwendungen wie dem vollständigen Gelenkersatz und Zahnimplantaten eingesetzt [1,2,3]. Es sind jedoch noch viele Herausforderungen zu lösen, darunter aseptische Lockerungen und Infektionen [4, 5]. In den letzten Jahren wurden eine Reihe von Studien zur Verbesserung der Osseointegration und der antibakteriellen Eigenschaften durchgeführt. Zum Beispiel das MoS2 /PDA-RGD-Beschichtung auf Titanimplantaten kann nicht nur die Integration eines Titanimplantats in den Wirtsknochen fördern, sondern auch das Bakterienwachstum mit hoher Effizienz hemmen [6]. Darüber hinaus hat die Oberflächentopographie immer mehr Aufmerksamkeit auf sich gezogen, und die topographische Modifikation unterscheidet sich von chemischen Modifikationen nur durch die Änderung der mikro- und nanoskaligen Struktur. Die Stimulation chemischer Signale auf Zellen ist instabil und zytotoxisch. Im Vergleich dazu können sichere und kontrollierbare physikalische Signale einige Nebenwirkungen durch chemische Moleküle vermeiden. Daher können die topografische Modifikation der Oberfläche von Implantaten und die Regulierung der Osseointegration durch die topografische Struktur einen neuen Weg zur Lösung des klinischen Problems der schlechten Osseointegration nach Implantation von Prothesen bieten.
Auf dem Gebiet des Knochengewebe-Engineerings und der Knochenregeneration gilt die Zellmorphologie-Interaktion als vielversprechende Managementstrategie zur präzisen Kontrolle der Samenzellfunktion und -differenzierung. Gleichzeitig weist der Knochen selbst eine elegante Hierarchie im Nanometer- und Mikrometerbereich auf [7]. Daher kann die Oberflächenmorphologie eine ähnliche Nische bieten, die die natürliche Knochenstruktur nachahmen und die osteogene Differenzierung mesenchymaler Stammzellen auf der Oberfläche des Wirtsknochens und des Implantats fördern kann. Oberflächenmorphologien können aus vielen verschiedenen Strukturen bestehen, einschließlich Nanoröhren, Nanodrähten, Nanoporen usw. Insbesondere Nanoröhren-Arrays haben in den letzten Jahren aufgrund ihrer einzigartigen Oberflächeneigenschaften, wie z. Eine neue Studie zeigt beispielsweise, dass Bornitrid-Nanotubes (BNNT) ein gassensitives Material darstellen, das als Gassensor zur Überwachung des Betriebs von Transformatoren verwendet werden kann, indem die Zusammensetzung und der Gehalt an gelösten Gasen im Öl erfasst werden [8]. In der Biomedizin kann die Oberflächentopographie auch das zelluläre Verhalten steuern, einschließlich Zellmigration, Adhäsion, Proliferation und Differenzierung. Die neuesten Studien zeigen, dass die Nanotopographie mesenchymale Stammzellen (MSCs) dazu bringen kann, sich in Osteoblasten zu differenzieren, um die frühe Osseointegration zu verstärken [9,10,11,12]. Es wird sogar berichtet, dass eine kombinierte Oberflächenmodifikation im Mikro- und Nanobereich dazu führen kann, dass sich MSCs in kontraktile glatte Muskelzellen differenzieren [13]. Die molekularen Mechanismen, wie die Oberflächentopographie das Zellschicksal steuert, müssen jedoch noch aufgeklärt werden, was für die Bewertung der Materialsicherheit und das Materialdesign wichtig ist.
Filamentöses (F)-Aktin, auch Mikrofilament genannt, ist einer der drei Hauptbestandteile des Zytoskeletts in eukaryontischen Zellen. Es besteht aus Polymeren des globulären (G)-Aktins, modifiziert durch zahlreiche andere Proteine. F-Aktin hat eine strukturelle Polarität aufgrund der Tatsache, dass alle Untereinheiten des Mikrofilaments auf das gleiche Ende zeigen. Das mit Widerhaken versehene Ende ist auf ein anderes benachbartes Monomer gerichtet, während das spitze Ende eine Aktin-Untereinheit mit exponierter ATP-Bindungsstelle besitzt. Das heißt, ATP ist am Transformationsprozess zwischen G-Aktin und F-Aktin beteiligt. Dieser Prozess befindet sich in einem dynamischen Gleichgewicht, bei dem gleichzeitig Polymerisation und Depolymerisation stattfinden, auch als Tretmilling bekannt, das häufig bei Lamellipodien und Filopodien beobachtet wird [14]. Daher ist es offensichtlich, dass die Aktindynamik eine wichtige Rolle bei solchen zellulären Funktionen wie Zellmigration, Zellteilung und Aufrechterhaltung der Zellform spielt. F-Aktin fungiert jedoch nicht nur als physikalische Struktur, die die mechanische Belastung unterstützt, sondern ist auch an anderen biologischen Verhaltensweisen wie der Signalübertragung und der Genexpression beteiligt. Immer mehr Beweise zeigen, dass F-Actin physikalische Signale in chemische Signale umwandeln kann, indem es mit anderen Proteinen interagiert [15,16,17,18]. Beispielsweise fördern biomechanische und geometrische Rekonstruktionen die Apoptose von Tumorzellen, indem sie die Überlagerung der Aktinmonomerpolymerisation mit F-Aktin verhindern [15]. Ultraschallpulse verbessern die Osteogenese menschlicher mesenchymaler Stammzellen, indem sie die Depolymerisation von F-Aktin hemmen [16]. Unsere vorherige Studie zeigte auch, dass mechanische Belastung die Stabilität von F-Aktin erhöht [17]. Da die Hohlstruktur von Nanoröhren weniger Adhäsionsstellen für Zellen bietet, ist eine Neuordnung des Zytoskeletts unvermeidlich, um das biomechanische Gleichgewicht zu erhalten. Folglich haben wir definitiv Grund zu der Annahme, dass F-Aktin wahrscheinlich die durch Nanotopographie induzierte Zelldifferenzierung vermittelt.
In dieser Studie haben wir TiO2 . hergestellt Nanoröhren, modifizierten ihre Topographie durch anodische Oxidation und untersuchten ihre Fähigkeit, die osteogene Differenzierung von MSCs zu fördern. Als nächstes untersuchten wir, ob F-Aktin eine entscheidende Rolle bei der Mechanotransduktion spielt. Cytochalasin D (Cyto D), das kompetitiv an das mit Widerhaken versehene Ende von F-Aktin bindet, um zu verhindern, dass G-Aktin in das Filament eingebaut wird, wurde verwendet, um die F-Aktin-Polymerisation zu hemmen, und Jasplakinolid (Jasp) wurde verwendet, um die Stabilisierung des Aktin-Montage. Darüber hinaus wollten wir auch aufklären, wie F-Aktin bei der Umwandlung physikalischer Hinweise in biochemische Signale funktioniert. Basierend auf den Ergebnissen unserer vorherigen Studie stellten wir die Hypothese auf, dass der MAPK-Weg an diesem Prozess beteiligt sein könnte [17]. Transkriptionsfaktoren wie Yes-assoziiertes Protein (YAP)/transkriptionaler Coaktivator mit PDZ-bindendem Motiv (TAZ) und MKL1, die als Mechanosensoren und Mechanotransducer gelten, waren ebenfalls Gegenstand unserer Studie, um zu untersuchen, wie F-Aktin Stammzellen beeinflusst Schicksal, weil einige Studien in anderen Bereichen implizierten, dass sie mit F-Aktin in Verbindung standen [19,20,21]. Im Allgemeinen hoffen wir, die Rolle von F-Aktin im Prozess der durch Nanoröhrchen induzierten Stammzelldifferenzierung zu klären, um das Materialdesign und die Bewertung der biologischen Sicherheit von durch Nanoröhrchen modifizierten Implantaten zu leiten.
Materialien und Methoden
Herstellung von TiO2 Nanoröhren
Als Substrat verwendete Reintitanscheiben (99,9 % Reinheit, 2 mm Dicke; Shengshida, Hebei, China) wurden mit Siliziumkarbid-Schleifpapier der Körnung Nr. 400 und 1500 poliert. Die Proben wurden dann nacheinander mit Aceton, wasserfreiem Alkohol und entionisiertem Wasser in einer Ultraschallreinigungsmaschine gewaschen und schließlich 3 h bei Raumtemperatur getrocknet. Zur Herstellung der Nanotopographie wurden die vorbehandelten Proben als Anode fixiert, während ein Platinstück als Gegenkathode in einer wässrigen Elektrolytlösung von 0,15 M NH4 . verwendet wurde F und 90 % Glykol für 1 h. Die Anodisierungsspannung war eine konstante Spannung von 30, 40, 50, 60 oder 70 V. Nach der anodischen Oxidation wurde jede Probe 30 min mit entionisiertem Wasser gespült und 15 min mit wasserfreiem Alkohol in einer Ultraschallreinigungsmaschine gewaschen. Schließlich wurden alle Proben in einem Autoklaven bei 120 °C für 1 h sterilisiert und dann vor der Verwendung mit Kulturmedium befeuchtet.
Der Reaktionsmechanismus der Nanoröhrenherstellung ist nicht klar, und die aktuelle Mainstream-Theorie ist die feldverstärkte Auflösungstheorie. Die Bildung von Nanoröhren-Arrays ist das Ergebnis eines dynamischen Gleichgewichts unter Einwirkung von Feldoxidation, Feldauflösung und chemischer Auflösung (Abb. 1b). Der Anodisierungsprozess kann wie folgt beschrieben werden:Im ersten Schritt wird eine Oxidsperrschicht auf der Elektrolyt-Metall-Grenzfläche gebildet:
$$ {\mathrm{Ti}}^{4+}+2{\mathrm{H}}_2\mathrm{O}\to {\mathrm{Ti}\mathrm{O}}_2+4{\mathrm{ H}}^{+} $$ (1)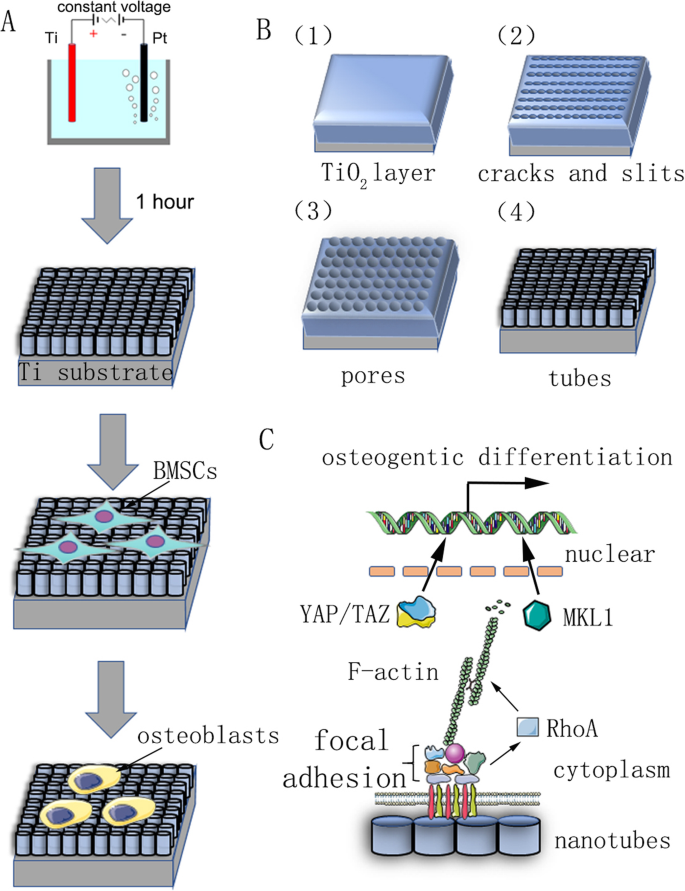
Ein zusammenfassendes Diagramm unserer Studie. a Flussdiagramm, das die anodische Oxidation und die Induktion der Zelldifferenzierung zeigt. b Das vorbehandelte Titansubstrat wurde als Anode in einer wässrigen Elektrolytlösung mit 0,15 M NH4 . fixiert F und 90 % Glykol bei konstanter Spannung für 1 h. Es wurde vorhergesagt, dass selbstorganisierte Nanoröhren gleichmäßig gebildet werden. Sein Reaktionsmechanismus ist in Materialien und Methoden beschrieben. c Schematische Darstellung des Mechanismus der durch Nanoröhren induzierten osteogenen Differenzierung von Stammzellen
Dann treten Risse und schmale Schlitze an der Oberfläche aufgrund der feldunterstützten Auflösung der Oxidschicht auf. Diffusion von F − Ionen in diese Risse und Schlitze erhöht die Auflösungsgeschwindigkeit. Risse vergrößern sich und verbinden sich mit benachbarten Rissen. Schließlich erreichen die Bildungsrate und Auflösungsrate der Titanoxidschicht ein dynamisches Gleichgewicht und die Nanoröhren wachsen nicht mehr:
$$ {\mathrm{TiO}}_2+6{\mathrm{F}}^{-}+4{\mathrm{H}}^{+}\to {\left[{\mathrm{TiF}}_6 \right]}^{2-}+2{\textrm{H}}_2\textrm{O} $$ (2)Oberflächencharakterisierung
Mit unterschiedlichen Spannungen (30, 40, 50, 60 oder 70 V) hergestellte Proben wurden 15 min mit Ethanol und entionisiertem Wasser gespült und dann bei Raumtemperatur getrocknet. Rasterelektronenmikroskopie (SEM450, FEI Nova Nano SEM; Thermo Fisher Scientific, Waltham, MA, USA) wurde verwendet, um die Oberflächenstruktur zu charakterisieren und den Innendurchmesser und die Höhe der Nanoröhren nach der Beschichtung der Proben mit einer dünnen Goldschicht zu messen. In der Zwischenzeit wurde eine energiedispersive Röntgenanalyse (EDS) durchgeführt, um die elementare Zusammensetzung von Nanoröhren zu analysieren. Zur Untersuchung der Oberflächenmorphologie und Oberflächenrauheit der Proben wurde Rasterkraftmikroskopie (AFM, NanoManVS, Bruker Nano Surfaces, Bruker MicroCT, Kontich, Belgien) verwendet. Aus jeder Probe wurden drei verschiedene Bereiche ausgewählt und die Messungen wurden dreimal wiederholt.
Zellkultur
Vier Wochen alte männliche Sprague-Dawley (SD)-Ratten wurden vom Versuchstierzentrum des Shanghai Ninth People’s Hospital (Shanghai, China) gekauft. Mesenchymale Stammzellen (BMSCs) des Knochenmarks von Ratten wurden aseptisch aus Oberschenkelknochen und Schienbeinen isoliert. BMSCs wurden gereinigt und in α-minimalem essentiellem Medium (α-MEM; Hyclone, Logan, UT, USA) mit 10 % (v/v) fötalem Rinderserum (FBS) (Gibco/Life Technologies, Carlsbad, CA, USA) weiter expandiert ), 100 mg/ml Streptomycin (Gibco) und 100 U/ml Penicillin (Gibco) und inkubiert bei 37 °C in einer befeuchteten Atmosphäre bestehend aus 95 % Luft und 5 % CO2 . Das Kulturmedium wurde alle 2 Tage erneuert und die Zellen wurden trypsiniert und bei 80% Konfluenz subkultiviert. Alle in dieser Studie verwendeten Zellen befanden sich zwischen den Passagen 3 und 5. Das osteogene Induktionsmedium bestand aus Wachstumsmedium, ergänzt mit 100 nM Dexamethason, 10 mM β-Glycerophosphat und 50 mM Ascorbinsäure (Sigma-Aldrich, St. Louis, MO, USA) .
Zellproliferationsassay
Das TiO2 Nanoröhren-modifizierte Titanscheiben wurden in kreisförmige Formen geschnitten und in die Vertiefungen einer 24-Well-Zellkulturplatte gegeben. BMSCs zwischen den Passagen 3–5 wurden auf TiO2 . kultiviert Nanoröhren mit einer Dichte von 3 × 10 4 Zellen/Scheibe entweder in Wachstumsmedium oder osteogenem Medium. Nach 2 Tagen Zellkultur wurden Cytochalasin D (Cyto D, Sigma-Aldrich) und Jasplakinolid (Jasp, Sigma-Aldrich), die verwendet wurden, um die F-Aktin-Polymerisation zu stören, 3 Tage lang täglich zum Medium gegeben. Die Endkonzentration und Verarbeitungszeit von Cyto D und Jasp betrugen 5 µM, 1 h bzw. 2 µM, 3 h. Das Kulturmedium wurde nach der Inkubation mit den Reagenzien erneuert. Die Lebensfähigkeit und Proliferation der Zellen wurden unter Verwendung des Cell Counting Kit-8 (CCK8)-Assays (Dojindo, Kumamoto, Japan) 12 h nach der Cyto D- oder Jasp-Behandlung bewertet. Die Zellen wurden mit 10 % (v/v) CCK8-Lösung für 2 h in einem Zellinkubator bei 37 °C unter 5 % CO2 . inkubiert . Dann überführten wir 100 μL der Reaktionsmischung in die Wells einer 96-Well-Platte und die Extinktion (OD) des Formazan-Farbstoffprodukts in der Kultur wurde bei 450 nm mit einem Multiscan-UV-Vis-Spektrophotometer (Safire2; TECAN, Mannedorf, Schweiz) gemessen ). Darüber hinaus haben wir mit einem automatischen Zellzähler (AMQAX1000, Life Technologies) auch ungefähre Zellzahlen gezählt. Vor der Zellzählung wurden BMSCs enzymatisch von TiO2 . abgelöst Nanoröhrchen und gefärbt mit Trypanblau (Sigma-Aldrich).
Färbung mit alkalischer Phosphatase und ALP-Aktivitätsanalyse
BMSCs wurden auf fünf verschiedene TiO2 . ausgesät Nanoröhren-modifizierte Titanscheiben (30, 40, 50, 60 oder 70 V) mit einer Dichte von 3 × 10 4 pro Vertiefung und in osteogenem Medium kultiviert. Reagenzien wurden wie oben beschrieben zugegeben. Nach 7-tägiger Inkubation wurden auf TiO2 . kultivierte BMSCs Nanoröhrchen wurden dreimal mit PBS gewaschen, mit 4% Paraformaldehyd fixiert und in alkalischer Phosphatase (ALP)-Arbeitslösung eines ALP-Kits gemäß den Anweisungen des Herstellers (Hongqiao, Shanghai, China) inkubiert. Die Ergebnisse wurden nach dem Waschen mit PBS unter einem Stereomikroskop beobachtet.
Für die ALP-Aktivitätsanalyse wurden die Zellen zuerst mit RIPA-Puffer ohne Protease- und Phosphatase-Inhibitoren lysiert, und dann wurden die zentrifugierten Lysate unter Verwendung eines ALP-Assay-Kits (Beyotime Institute of Biotechnology, Jiangsu, China) nach dem bereitgestellten Protokoll getestet. Die Aktivität wurde schließlich auf die Proteinkonzentration des entsprechenden Lysats normalisiert.
Immunozytochemie
Nach 3 Tagen Cyto D- und Jasp-Behandlung wurden BMSCs mit 4% Paraformaldehyd für 20 min bei Raumtemperatur fixiert und dann dreimal mit PBS gewaschen. Die Zellen wurden mit 0,3% Triton-X 100 für 30 min permeabilisiert, dreimal mit PBS gewaschen und mit Rhodamin-konjugiertem Phalloidin 1 h bei Raumtemperatur im Dunkeln gefärbt. Dann wurden die Zellen mit PBS gespült und mit DAPI (Beyotime Institute of Biotechnology) 10 min bei Raumtemperatur gegengefärbt. Nach drei zusätzlichen Waschvorgängen mit PBS wurden die Proben auf einem Glasobjektträger fixiert und durch konfokale Mikroskopie beobachtet.
Western Blotting
Zur Evaluierung der Proteinexpression wurden auf TiO2 . kultivierte BMSCs Nanoröhren wurden mit Trypsin (Gibco) geerntet. Die Zellen wurden dreimal mit PBS gewaschen und mit RIPA-Puffer, ergänzt mit einem Protease- und Phosphatase-Inhibitor-Cocktail, für 30 Minuten auf Eis lysiert. Das Lysat wurde durch Zentrifugation bei 12.000 × g . gesammelt 15 Minuten bei 4 °C. Die Konzentration der Gesamtproteine im Überstand wurde mit einem Bicinchoninsäure (BCA) Protein Assay Kit (Beyotime) gemäß den Anweisungen des Herstellers gemessen. Beladungspuffer wurde wie oben zu Proteinproben zugegeben, die dann 15 min bei 95 °C gekocht wurden. Für die Western-Blotting-Analyse wurden 10 µl des Proteinpräparats auf ein 12,5 % SDS-PAGE-Gel (EpiZyme Inc., Cambridge, MA, USA) geladen und 1 h bei 120 V einer Elektrophorese unterzogen, dann auf ein Polyvinylidendifluorid elektrotransferiert (PVDF) Membran bei 250 mA für 2 h. Anschließend wurden die Membranen mit 5–10 % fettfreier Trockenmilch in TBST für 1 h auf einem Schüttler bei Raumtemperatur blockiert und mit in Verdünnungspuffer (Beyotime) verdünntem Primärantikörper über Nacht bei 4 °C inkubiert. Als nächstes wurde den Membranen nach dreimaligem Waschen mit TBST für 5 min fluoreszenzkonjugierter sekundärer Antikörper, verdünnt in Verdünnungspuffer, zugesetzt, und die Membranen wurden dann bei Raumtemperatur für 1 h im Dunkeln inkubiert. Die Proteinbanden wurden durch ein Zweifarben-Infrarot-Fluoreszenz-Bildgebungssystem (Odyssey, LiCor Biosciences, Lincoln, NE, USA) nachgewiesen. Insbesondere wenn die Banden des internen Referenzproteins vereinigt wurden, wurde die Membran gestrippt und mit einem anderen primären Antikörper erneut sondiert, gefolgt von demselben Verfahren. Wir verwendeten den GAPDH-Antikörper als unser internes Referenzprotein, um die Proteinexpression zu normalisieren, und die anderen primären Antikörper, die in dieser Studie verwendet wurden, waren Anti-Vinculin (1:1000 Verdünnung, Abcam, Cambridge, MA, USA), Anti-FAK (1:1000 Verdünnung) , Cell Signaling Technology, Danvers, MA, USA), Anti-Runx2 (1:1000 Verdünnung, Cell Signaling Technology), Anti-RhoA (1:1000 Verdünnung, Cell Signaling Technology), Anti-F-Aktin (1:500 Verdünnung .) , Abcam), Anti-Osx (1:500 Verdünnung, Abcam) und Anti-pYAP (1:1000 Verdünnung, Cell Signaling Technology). Sekundäre Antikörper waren Ziegen-Anti-Maus-IgG H&L (IRDye® 680RD, 1:5000 Verdünnung, Abcam) und Ziegen-Anti-Kaninchen IgG H&L (IRDye® 680RD, 1:5000 Verdünnung, Abcam).
Quantitative Real-Time-PCR
An Tag 7 wurde eine quantitative Real-Time-PCR durchgeführt, um die Genexpression von Runt-related Transcription Factor 2 (Runx2), Osterix (Osx), Alp, Osteocalcin (OCN), RhoA, YAP, TAZ, Vinculin (VCL), fokale Adhäsionskinase (FAK) und megakaryoblastische Leukämie 1 (MKL1) in Zellen, die in osteogenem Medium auf TiO2 . gezüchtet wurden Nanoröhren. Gesamt-RNA wurde aus den Zellen unter Verwendung eines Gesamt-RNA-Kits (R6812-01HP, Omega Bio-Tek Inc., Norcross, GA, USA) extrahiert. Die Konzentration und Reinheit der RNA-Proben wurden durch die optische Dichte bei einer Wellenlänge von 260 bestimmt und es wurden nur Proben analysiert, die sowohl A260/280-Verhältnisse als auch A260/230-Verhältnisse von mehr als 1,8 aufwiesen. RNA-Proben wurden mit einem qScript cDNA-Synthese-Kit (Takara, Shiga, Japan) gemäß den Anweisungen des Herstellers in cDNA revers transkribiert. Eine quantitative Echtzeit-PCR wurde mit SYBR® Premix Ex Taq™ (Takara) unter Verwendung eines QuantStudio 6 Flex-Echtzeit-PCR-Systems (Life Technologies) durchgeführt. Als interne Referenz diente GAPDH, ein Haushaltsgen. Die Daten wurden mit dem Vergleich Ct (2 -ΔΔCt )-Methode und ausgedrückt als Faltungsänderungen im Vergleich zur Kontrolle. Die Sequenzen der verwendeten Primer sind in Tabelle 1 aufgeführt.
Statistische Analyse
Alle Daten sind repräsentativ für mindestens drei unabhängige Experimente mit dreifachen Proben, sofern nicht anders angegeben. Die Daten werden als Mittelwert ± Standardabweichung (SD) ausgedrückt. Die Unterschiede zwischen den Gruppen wurden durch eine einseitige Varianzanalyse, gefolgt von dem Student-Newman-Keuls-Post-hoc-Test oder dem Student-t . bewertet Prüfung. P Werte < 0,05 wurden als statistisch signifikant angesehen.
Ergebnisse
Oberflächencharakterisierung
Um die Nanotopographie herzustellen, TiO2 Nanoröhren wurden auf einem reinen Titansubstrat unter Verwendung einer anodischen Oxidationsausrüstung bei verschiedenen konstanten Spannungen (30, 40, 50, 60 und 70 V) für 1 h gebildet (Abb. 1). Eine gleichmäßig verteilte Anordnung von selbstorganisierten Nanoröhren wurde durch Rasterelektronenmikroskopie (REM) beobachtet. Seitenansichten und Draufsichten der Nanoröhren sind in Abb. 2a, b gezeigt. Die Höhe der Nanoröhren in allen Proben in dieser Studie betrug ca. 2 µm, während die Innendurchmesser der Nanoröhren ca. 74 nm (30 V), 92 nm (40 V), 112 nm (50 V), 128 nm (60 .) betrugen V) und 148 nm (70 V) (Abb. 2c). Dies zeigte, dass die Höhe der Nanoröhren mit der Zeit der anodischen Oxidation und der Innendurchmesser mit der Spannung der anodischen Oxidation in Zusammenhang stand. Anschließend wurde eine Röntgenenergiedispersive Analyse (EDS) durchgeführt, um die elementare Zusammensetzung der Nanoröhren zu analysieren. Dabei zeigte sich, dass die Nanoröhren nur aus zwei Elementen, O und Ti, bestehen (Abb. 2d, e). Rasterkraftmikroskopie (AFM) wurde verwendet, um die Nanoröhrenstrukturen zu erkennen und die arithmetische mittlere Abweichung des Profils von Nanoröhren als Oberflächenrauheit (Ra) zu messen (Abb. 2f). Die Daten zeigten, dass die Oberflächenrauheit von Nanoröhren mit zunehmendem Durchmesser (d. h. der Spannung der anodischen Oxidation) zunahm (Abb. 2g).
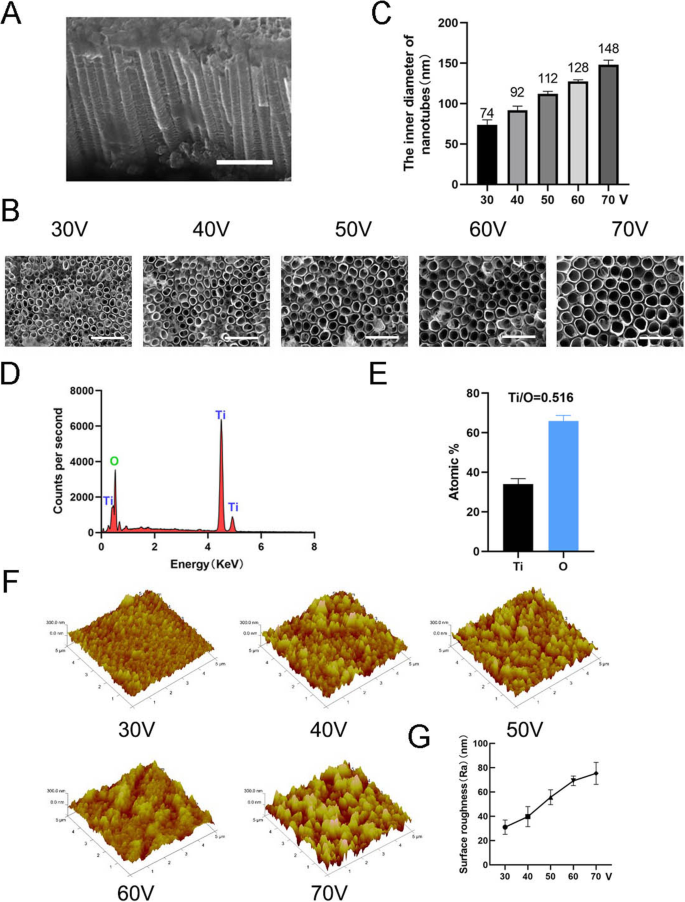
Oberflächencharakterisierung von Nanoröhren. a Seitenansicht von Nanoröhren. Maßstabsbalken:1 µm. b Draufsicht auf Nanoröhren. Maßstabsbalken:500 nm. c Der Innendurchmesser der Nanoröhren bei fünf verschiedenen konstanten Spannungen (30, 40, 50, 60, 70 V). d Die chemische EDS-Elementzusammensetzung von Nanoröhrenstrukturen. e Das Elementverhältnis von Ti und O. f Rasterkraftmikroskopie (AFM) Bilder von Nanoröhrenstrukturen. g Die durchschnittliche Oberflächenrauheit (Ra) der Nanoröhren
TiO2 Nanotubes induzierte osteogene Differenzierung von MSCs
Nach 7 Tagen Osteoinduktion wurde zunächst eine ALP-Färbung durchgeführt, um die osteogene Differenzierung von MSCs zu bewerten. Die Färbeergebnisse zeigten, dass auf TiO2 . kultivierte MSCs Nanoröhren hatten eine höhere ALP-Aktivität als Zellen, die auf einem glatten Titansubstrat kultiviert wurden (Kontrollgruppe) (Abb. 3a). Die statistische Analyse des Färbebereichs zeigte, dass die Fähigkeit der Nanoröhren, eine osteogene Differenzierung zu induzieren, im Vergleich zur Kontrollgruppe signifikant verbessert war. In der Zwischenzeit beobachteten wir einen Trend, dass innerhalb des Durchmesserbereichs dieses Experiments der Durchmesser des TiO2 . größer wird Nanoröhren, desto stärker ist die Fähigkeit, eine osteogene Differenzierung zu induzieren (Abb. 3b). Daher wurde die 70-V-Gruppe in nachfolgenden Experimenten verwendet, um die Ergebnisse besser darzustellen. Als nächstes analysierten wir die osteogene Genexpression an den Tagen 3 und 7. MSCs kultiviert auf TiO2 Nanotubes für 3 Tage und 7 Tage zeigten beide eine signifikante Förderung der Expression von osteogenen Genen (RUNX2, ALP, OCN und OSX) im Vergleich zur Kontrollgruppe (Abb. 3d–g). Western-Blot-Ergebnisse bestätigten, dass die Proteinexpression von RUNX2 und OSX auch nach 7 Tagen Osteoinduktion zunahm (Abb. 3c). Interessanterweise fanden wir heraus, dass F-Aktin im TiO2 . hochreguliert war Gruppe der Nanoröhren. Daher war es offensichtlich, dass TiO2 Nanoröhren lenkten MSCs in Richtung Osteoblastendifferenzierung, die mit dem Durchmesser der Nanoröhren zusammenhängt. Unsere Ergebnisse legten auch die Beteiligung von F-Aktin an diesem Prozess nahe.
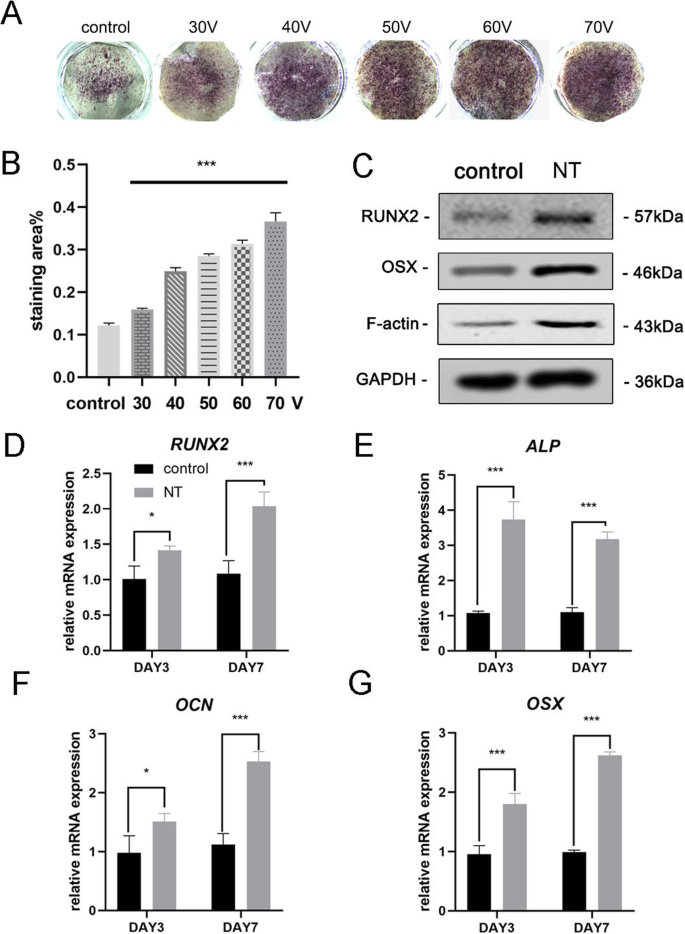
TiO2 Nanotubes verstärkten die osteogene Genexpression von BMSCs. a ALP-Färbung des glatten Titansubstrats und fünf verschiedener Nanotube-Substrate. Die Zellen wurden mit osteogenem Medium für 7 Tage induziert. b Die statistische Analyse des Färbebereichs wurde mit ImageJ durchgeführt. c Osteogenese-assoziierte Proteine (RUNX2 und OSX) und F-Aktin in MSCs wurden am Tag 7 durch Western-Blotting analysiert. Die mRNA-Expression von RUNX2 (d ), ALP (e ), OCN (f ) und OSX (g ) an den Tagen 3 und 7, analysiert durch qRT-PCR. NT die Nanoröhren-Gruppe. Die Daten repräsentieren den Mittelwert ± SD von drei Proben. *P <0,05, **P <0,01 und ***P <0,001
F-Aktin-vermittelte Osteoblastendifferenzierung von MSCs auf TiO2 Nanoröhren
Um weiter zu untersuchen, ob F-Aktin an der durch Nanotopographie induzierten Zelldifferenzierung beteiligt ist, verwendeten wir zwei Reagenzien, Jasplakinolid (Jasp) und Cytochalasin D (Cyto D), um die F-Aktin-Polymerisation positiv bzw. negativ zu regulieren. Die konfokalen Mikrophotographien der Rhodamin-Phalloidin-Färbung zeigten, dass F-Aktin in der Cyto-D-Behandlungsgruppe fast depolymerisiert war und faserige Strukturen selten zu sehen waren, während Jasp F-Aktin stabilisierte und polymerisierte, was durch deutlichere und hellere bündelähnliche Strukturen bestätigt wurde als beobachtet in der Kontrollgruppe (Abb. 5a). Darüber hinaus bestätigte die Western-Blot-Analyse auch, dass die Proteinexpression von F-Aktin beeinflusst wurde, was bewies, dass Cyto D und Jasp beide wie erwartet wirkten (Fig. 5b). Der Zellproliferationsassay zeigte, dass Cyto D die Zellproliferation signifikant hemmte, während Jasp das Zellwachstum förderte ( 4a ). Die Zellzahlergebnisse stimmten mit diesem Befund überein (Abb. 4b).
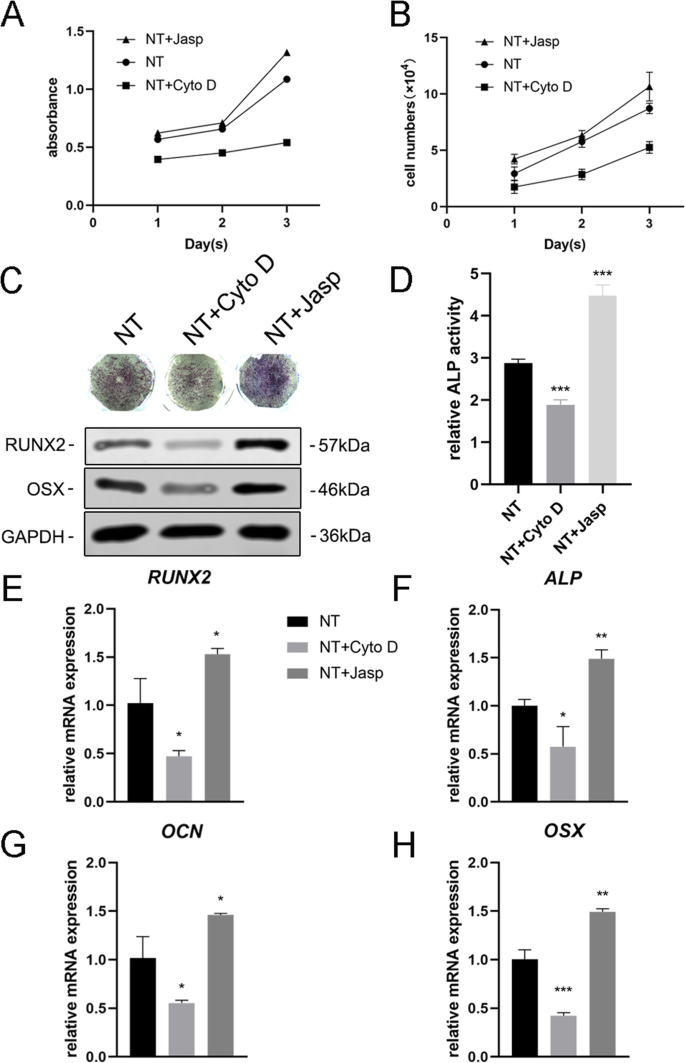
Die F-Aktin-Assemblierung regulierte die Expression osteogener Gene in BMSCs. a , b Die Zellproliferation nach Cyto D- und Jasp-Behandlung wurde mit dem CCK-8-Assay oder einem automatisierten Zellzähler an den Tagen 1, 2 und 3 bestimmt. c , d ALP-Färbung und ALP-Aktivitätsanalyse wurden durchgeführt, um die Expression von ALP in MSCs nach 3-tägiger Arzneimittelbehandlung zu bewerten. Der Färbebereich wurde unter Verwendung von ImageJ analysiert. c , e –h Western-Blotting und qRT-PCR wurden verwendet, um die Veränderungen der Osteogenese-bezogenen Marker in der NT+ Cyto D-Gruppe und der NT+ Jasp-Gruppe mit denen in der Kontrollgruppe (ohne medikamentöse Behandlung) zu vergleichen. NT die Gruppe der Nanoröhren. Die Daten repräsentieren den Mittelwert ± SD von drei Proben. *P <0,05, **P <0,01 und ***P <0,001
Als nächstes untersuchten wir die Fähigkeit von MSCs, sich in Osteoblasten zu differenzieren, um zu untersuchen, ob F-Aktin diesen Prozess vermittelt. Wir entdeckten zuerst ALP als einen frühen Marker der Osteogenese. Im Vergleich zur Kontrollgruppe reduzierte die Cyto-D-Behandlung die Expression von ALP und seine Aktivität, während diejenige in der Jasp-Behandlungsgruppe hochreguliert war ( 4c , d). In Übereinstimmung mit diesem Ergebnis führte die Behandlung mit Jasp zu einem Anstieg der Proteinspiegel von RUNX2 und OSX, während Cyto D den gegenteiligen Effekt hatte ( 4c ). In Übereinstimmung damit zeigten die mRNA-Expressionsniveaus osteospezifischer Gene, einschließlich RUNX2, ALP, OCN und OSX, den gleichen Trend nach medikamentöser Behandlung (Abb. 4e–h). Diese Daten zeigten vor allem, dass F-Aktin eine wichtige Rolle bei dem durch TiO2 . induzierten Prozess der osteogenen Differenzierung von MSCs spielte Nanoröhren. Die Förderung der F-Aktin-Depolymerisation hemmte die durch die Nanotopographie induzierte Osteoblastendifferenzierung, während die Stabilisierung und Polymerisation von F-Aktin die Osteoblastendifferenzierung verstärkte.
F-Aktin-regulierte Osteoblastendifferenzierung von MSCs auf TiO2 Nanoröhren durch MKL1 und YAP/TAZ
Um den zugrunde liegenden Mechanismus zu analysieren, der F-Aktin bei der Regulation des Schicksals von MSCs einbezieht, untersuchten wir Proteine/Moleküle, die direkt mit F-Aktin interagieren oder die F-Aktin-Polymerisation beeinflussen. Zuerst versuchten wir herauszufinden, wie die Nanotopographie das Gleichgewicht zwischen F-Aktin und G-Aktin beeinflusst. TiO2 Nanoröhren als physikalisches Signal unterscheiden sich von membrandurchlässigen chemischen Signalen und müssen daher einige Bestandteile der Zellmembran nutzen, um Reize in die Zellen zu übertragen. Es gibt immer mehr Hinweise darauf, dass der fokale Adhäsionskomplex, einschließlich Integrin, Talin, fokale Adhäsionskinase (FAK), Vinculin (VCL), Tensin und andere Proteine, als Signalträger fungiert, der Zellen über den Zustand der extrazellulären Matrix (ECM .) informiert ) und beeinflusst damit deren biologisches Verhalten [22, 23]. Noch wichtiger ist, dass F-Aktin über solche fokalen Adhäsionskomplexe an Integrine bindet und dadurch mechanische Verbindungen zwischen intrazellulären Aktinbündeln und der ECM bildet [24]. Folglich analysierten wir als nächstes die Expression von Komponenten des fokalen Adhäsionskomplexes. Die Ergebnisse zeigten, dass die Protein- und mRNA-Expression von VCL und FAK mit der Veränderung von F-Aktin übereinstimmte, was darauf hindeutet, dass der fokale Adhäsionskomplex an dem durch TiO2 . induzierten Prozess der osteogenen Differenzierung von MSCs beteiligt ist Nanoröhren (Abb. 5b und 6a, b). Darüber hinaus fanden wir auch, dass RhoA, ein kleines GTPase-Protein in der Rho-Familie der GTPasen, in der Jasp-Behandlungsgruppe hochreguliert und durch Cyto D gehemmt wurde (Fig. 5b und 6a, b). RhoA ist ein wichtiges Upstream-Signaltransduktionsmolekül im MAPK-Weg und könnte durch FAK reguliert werden [25, 26]. Die primäre Funktion von RhoA besteht darin, die Polymerisation und Stabilität von Stressfasern (F-Aktin) und den Aufbau des fokalen Adhäsionskomplexes zu fördern [27]. Zusammengenommen legen diese Daten nahe, dass TiO2 Nanoröhren könnten die F-Aktin-Polymerisation durch den fokalen Adhäsionskomplex und RhoA beeinflussen.
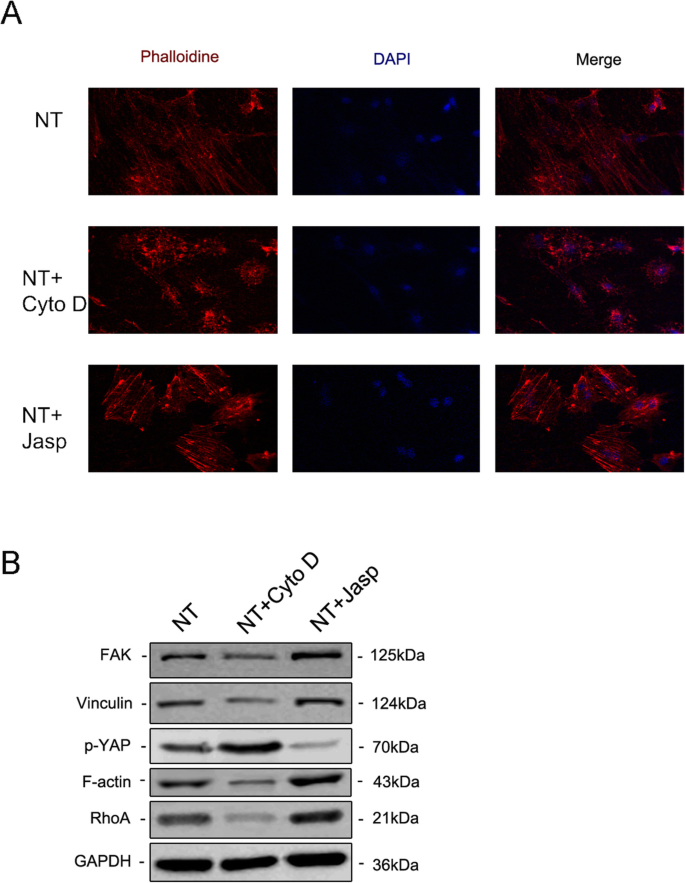
Immunfluoreszenz-Färbung zeigte den F-Aktin-Spiegel durch Färbung mit Rhodamin-konjugiertem Phalloidin (a ). The protein expression of FAK and VCL contained in the focal adhesion complex, RhoA and phosphorylated YAP were investigated by Western blotting (b ). NT the nanotubes group
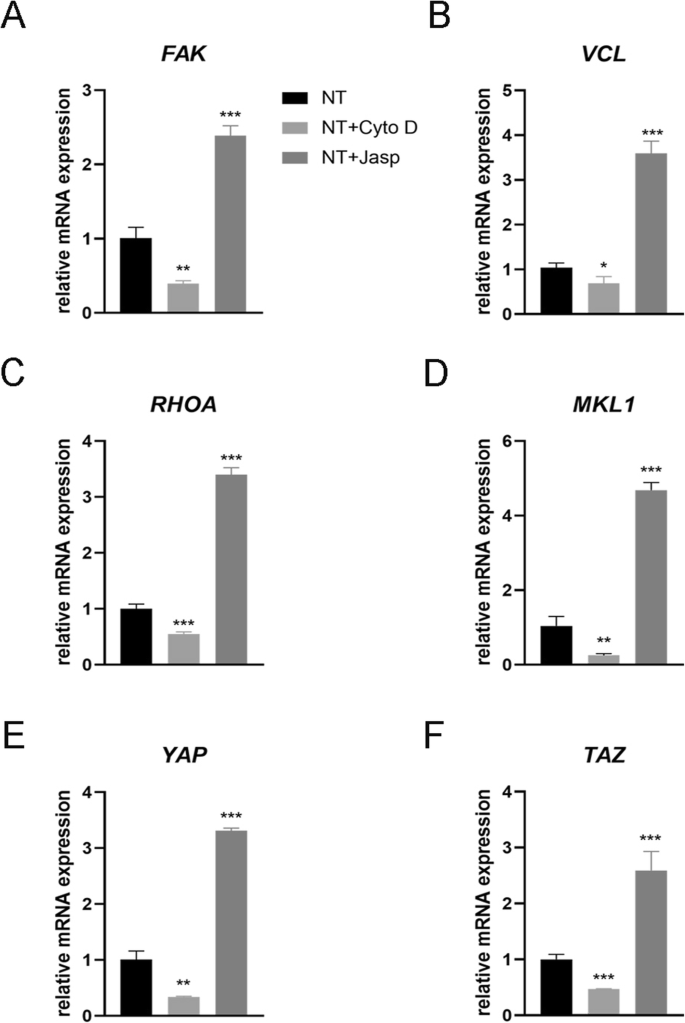
Effect of F-actin assembly on FAK (a ), vinculin (VCL) (b ), RhoA (c ), MKL1 (d ), YAP (e ), and TAZ (f ) gene expression in MSCs. NT the nanotubes group. Data represent the mean ± SD of three samples. *P <0.05, **P <0.01, and ***P <0.001
But how does F-actin regulate cell fate? Most studies have demonstrated that F-actin is involved in cell migration, cell division, endocytosis, and especially tumor cell invasion [28,29,30]. Few studies have suggested that F-actin could also regulate cell differentiation, let alone its specific molecular mechanism [31, 32]. Consequently, we searched for articles that mentioned the F-actin changes and found that YAP/TAZ, two closely related transcriptional co-activators in the Hippo signaling pathway, which shuttle between the cytoplasm and the nucleus, may serve as mechanotransducers in regulating MSC differentiation [33,34,35]. In addition, we also found that MKL1, a key regulator of smooth muscle cell differentiation, which interacts with the transcription factor serum response factor, could bind to G-actin and also circulate between the cytoplasm and the nucleus [21, 36]. Our results ultimately identified the involvement of YAP/TAZ and MKL1 in nanotube-induced osteoblast differentiation mediated by F-actin (Figs. 5b and 6d–f). Interestingly, the protein expression of phosphorylated YAP showed the opposite trend, indicating that not only was the expression of YAP changed, but the phosphorylation of YAP was also changed by Cyto D and Jasp (Fig. 5b). This result was consistent with the report that the phosphorylation of YAP/TAZ could be sequestrated in the cytoplasm [35].
In summary, our results preliminarily demonstrated that F-actin regulated osteoblast differentiation of MSCs on TiO2 nanotubes through MKL1 and YAP/TAZ (Fig. 7).
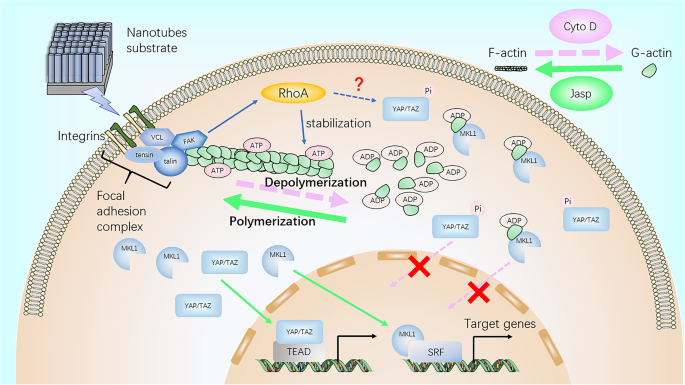
Schematic representation of F-actin assembly induced by nanotubes, and the putative role of MKL1 and YAP/TAZ in acting as the downstream mediators of F-actin signaling to regulate gene expression
Diskussion
Titanium and titanium alloys are the most widely used metal materials in orthopedic clinical implants due to the good properties of titanium [3]. However, aseptic loosening is still an urgent problem to be solved and improved, and the key is likely to lie in improving the integration of the implant and the host bone. Previous studies have shown that surface coating and modification or immobilization of biofunctional molecules will be beneficial to osseointegration [37]. Recently, the surface topography of implants has attracted the attention of many researchers thanks to studies into the cell response to physical cues [9,10,11, 13, 38]. In this study, we demonstrated the ability of nanotubes to promote osteogenic differentiation of MSCs, and this ability was enhanced with increasing inner diameter of the nanotubes (30–70 V). This will help guide the diameter of the nanotubes on the surface of the implants.
As a topographical structure, nanotubes first change the physical properties of the material, such as adsorption capacity and electrical and thermal conductivity. These physical properties determine their application in the industrial field. For example, most high-voltage power transformers need to be filled with insulating material, which is usually transformer oil or insulating gas. When the insulation of a transformer fails due to overheating and partial discharge, a serious discharge accident will occur. Therefore, finding an effective method that accurately detects the concentration and types of dissolved gases or insulating gas decomposition components in a transformer is necessary to monitor the operating state of the transformer [8, 39,40,41]. The traditional approach is to look for materials with good gas adsorption in transition elements, which are rich in d electrons, such as Pd(1 1 1) [39]. Nowadays, nanotubes are widely studied for their good gas adsorption properties. He et al. found that CuO-BNNT was suitable for the adsorption of C2 H2 , because of its stronger adsorption on C2 H2 [8]. Meanwhile, TiO2 itself can be a gas-sensing material. Gui et al. found that Co-doped TiO2 further enhanced gas adsorption capacity and exhibited a superior adsorption ability and conductivity change toward C2 H4 molecules [40]. Consistent with this study, Mn-doped graphene also exhibited enhanced conductivity and superior capability of C2 H2 and CO detection than pristine graphene [41]. The above research indicates that the TiO2 nanotubes prepared in our experiment have a potential application in the field of monitoring the operative state of a transformer. However, the adsorption capacity and electrical conductivity of the nanotubes to gases need to be further studied, especially whether these properties are enhanced after doping with transition elements (e.g., Mn).
In addition to changing the physical properties of a surface, nanoscale morphology also affects the biological behavior of the cells attached to it. Cells first adhere to the surface of the material and then migrate, proliferate, and differentiate. Compared to a flat surface, the hollow structure of the nanotubes provides fewer adhesion sites for cells. Therefore, in order for the cells to adhere to the nanotube surface steadily and maintain the biomechanical balance within the cell, the focal adhesion complex begins to assemble and mature, and F-actin becomes strong and stable.
F-actin, a linear polymer microfilament consisting of G-actin monomers, is one of the three major components of the cytoskeleton. As a mechanical-loading structure, F-actin is generally believed to be involved in cell division, cell migration, endocytosis, and tumor cell invasion [28,29,30], but some recent studies showed that it can also affect cell differentiation [31,32,33, 36]. For example, actin cytoskeletal depolymerization by simvastatin induces chondrocyte differentiation [31], and actin depolymerization enhances adipogenic differentiation in human stromal stem cells [32]. Our results also revealed that, compared with the control group, MSCs cultured on nanotubes had higher F-actin levels and a more obvious fibrous structure. Meanwhile, promotion of F-actin polymerization by Jasp enhanced osteogenic differentiation, while the depolymerization of F-actin inhibited osteogenic differentiation, suggesting that F-actin mediates TiO2 nanotube-induced osteoblastic differentiation of MSCs.
F-actin can be regulated by Rho GTPases, members of the Ras superfamily [23, 42], and Rho can induce actin reorganization through at least two effectors, ROCK and Dia. ROCK is activated by binding to Rho-GTP and then myosin light chain (MLC), the substrate of ROCK, plays an important role in F-actin assembly. ROCK inhibits the activity of MLC phosphatase, leading to an increase in MLC phosphorylation, which stimulates the ATPase activity of myosin II and promotes the assembly of F-actin. In addition, ROCK also targets LIM kinase (LIMK). Phosphorylated LIMK inactivates cofilin by phosphorylation, which can disassemble F-actin in its active state. Another effector is Dia, a member of the formin-homology (FH) family of proteins which contains two FH domains. These domains contain multiple proline-rich motifs which bind to the G-actin-binding protein, profilin. This interaction contributes to actin polymerization and F-actin organization [42]. We detected one of the Rho GTPases, RhoA, and found that the expression of RhoA was consistent with the level of F-actin. However, we were unable to clearly describe how the nanotubes regulate the expression of RhoA, because there are many other regulators, including integrin signaling, other adhesion receptors, G protein-coupled receptors (GPCRs), soluble factors such as LPA, receptor tyrosine kinase signaling, and so on [43].
Knowing that F-actin can be regulated by RhoA, we next asked what role focal adhesion played in this process, because focal adhesion complexes, containing integrins, talin, vinculin, paxillin, and focal adhesion kinase (FAK), are formed and mature when cells attach to the surface of nanotubes. Integrins are transmembrane heterodimers that couple the ECM to the other focal adhesion proteins so as to facilitate cell attachment. They not only act simply as hooks but also transmit to the cell critical signals about the nature of its surroundings, which along with other signals such as EGFR, prompt the cell to make decisions about its biological behaviors. These signals are further transmitted to F-actin, which is directly connected to the focal adhesion complexes. On the one hand, the nanoscale morphology causes focal adhesion complex assembly and maturation. On the other hand, kinases such as FAK and Src kinase family members will recruit molecules such as CRK to self-regulate the assembly and maturation of focal adhesion complexes [44,45,46]. Our results demonstrated that the formation and maturation of focal adhesion complexes were impaired by F-actin depolymerization, suggesting that there was a feedback from focal adhesion complexes to actin assembly in line with published reports.
However, it should not be ignored that these proteins contained in focal adhesion complexes have the function of signal transduction [47]. That is to say, nanotubes may directly regulate gene expression through signal cascades, and F-actin may just participate in or be affected by this process. For instance, the dual kinase complex of FAK and Src can regulate Rho GTPases such as RhoA. This shows that nanotubes can regulate RhoA through integrins and the FAK/Src complex. In addition Src, a non-receptor tyrosine kinase protein, can activate Ras (small GTPase) by phosphorylating FAK at tyrosine residue 925 [47, 48]. Then, Ras activates numerous biochemical pathways, including the well-studied MAPK pathway and the PI3K/AKT/mTOR pathway. In the MAPK pathway, Ras activates c-Raf, followed by mitogen-activated protein kinase kinase (MAP2K) and then MAPK1/2, also known as extracellular signal-regulated kinase (ERK). ERK in turn activates transcription factors such as serum response factor (SRF) and c-Myc that are involved in regulating growth and differentiation [49]. What is more, Runx2, a key transcription factor in osteogenic differentiation, can also be regulated by ERK [50], and our previous study confirmed that mechanical strain promoted osteogenic differentiation of BMSCs through the FAK-Erk1/2-Runx2 pathway [17]. Therefore, we cannot rule out that ERK plays a role in nanotube-induced osteogenic differentiation and further study is still needed.
So what exactly is the role of F-actin in inducing differentiation of nanotubes, because its change can affect cell differentiation? One possibility is that the change of F-actin assembly can inversely regulate the level of FAK so as to induce osteogenic differentiation through the FAK-Erk1/2-Runx2 pathway as described above, because in our results, focal adhesion complexes and actin polymerization showed the same trends of change, indicating that they act as a whole in response to the extracellular environment. However, some other possibilities also exist, and a number of articles have shown that MKL1 and YAP/TAZ act downstream of the actin dynamic balance [20, 51,52,53,54]. Both of them shuttle between the cytoplasm and the nucleus, and may help to transduce signals from the cytoskeleton to the nucleus.
MKL1, also termed myocardin-related transcription factor A, is sensitive to changes in G-actin levels. When cytoplasmic G-actin levels increase, monomeric G-actin binds to MKL1 and prevents it from binding to SRF and activating transcription. SRF target genes include actins such as smooth muscle actin (SMA) as well as other actin-binding proteins, including immediate early genes like c-fos and egr1. Recent studies have demonstrated that changing SRF activity could regulate adipogenesis by activating the adipogenesis transcription factor peroxisome proliferator-activated receptor γ (PPARγ), and also regulate bone formation via IGF-1 and Runx2 signaling [55, 56].
YAP and TAZ are two transcriptional coactivators in the Hippo signaling pathway, identified as an important regulatory pathway that restricts cell proliferation, thereby controlling organ size and morphogenesis [20]. Large tumor suppressor genes 1 and 2 (LATS1/2) phosphorylate them, thereby creating a binding site for 14-3-3 proteins, the binding of which prevents their nuclear import [53, 54]. As a consequence, phosphorylated forms of YAP/TAZ are sequestered in the cytoplasm, preventing the expression of genes like Ctgf and Areg. In addition, some studies have shown that YAP/TAZ can interact with T-box 5 (TBX5), RUNX2, and p73 to regulate gene expression [57,58,59]. Further, cell adhesion to cell matrix proteins has been shown to trigger YAP nuclear localization through an integrin/FAK/Src axis. In our study, the results suggested that this pathway was possibly involved in nanotube-induced differentiation. Further study into the downstream mediators of the integrin/FAK/Src axis should be carried out to clarify the specific mechanism.
On the other hand, more and more studies illustrate that F-actin interacts with Hippo signaling, and somehow inhibits the phosphorylation of YAP [54, 60], which is consistent with our experimental results that promoting F-actin polymerization reduces the expression of phosphorylated YAP. We hypothesize that ATP involved in the process of the transformation between G-actin and F-actin may also play an important role in the phosphorylation of YAP, which is yet to be studied.
After understanding the above possible molecular mechanisms, we can try to explain some of the experimental phenomena found in this study. Our results revealed that the larger the diameter of the nanotubes, the stronger the ability of the nanotubes to promote osteogenic differentiation. This is consistent with previous research [61, 62]. The reason for this phenomenon is that the larger the diameter of the nanotubes, the less adhesion sites they can provide to the cells, and the greater the assembly and maturity of focal adhesion complexes. Along with these, stress fibers made of F-actin will have greater strength and stability. These structures enhance the signaling that promotes osteogenic differentiation. Predictably, however, this effect is significantly reduced when the nanotubes become too large in diameter, making it difficult for the cells to adhere to the surface [12]. Similarly, when the height of the nanotubes is inconsistent, the differences in height can result in a change of adhesion site and rearrangement of the cytoskeleton, which will further affect cell differentiation. Intriguingly, even flat surface materials without nanotube modification can induce changes in cell differentiation. A number of studies have demonstrated that focal adhesion formation and stress fiber organization are regulated by substrate stiffness [63,64,65], and YAP/TAZ also plays an important role in this process. Therefore, it is obvious that the integrins–FAs (focal adhesions)–F-actin axis plays a role in the transduction of physical signals into intracellular chemical signals.
In summary, our results demonstrated that F-actin regulates osteoblastic differentiation of mesenchymal stem cells on TiO2 nanotubes through MKL1 and YAP/TAZ, whose target genes partly explained the proliferation and differentiation of MSCs. We know that there is no single change in the signal network and any change is regulated by numerous molecules and proteins. One type of biological behavior must be the result of the regulation of a series of signaling pathways. Nanotubes induce cell differentiation by triggering a complex network of signals, including integrins, proteins contained in focal adhesion complexes, FAK, Src, Rho GTPase, the MAPK pathway, the Hippo pathway, and other reported signaling pathways. At least as important, there are many signal cycles in the signal network and a downstream signal can regulate the upstream signal via feedback. In this study, we found that vinculin and FAK can be regulated backwards by F-actin assembly, increasing the uncertainty of molecular function. Therefore, more details of the molecular mechanism await further study.
Schlussfolgerungen
Our results showed that TiO2 nanotubes promoted the osteogenic differentiation of MSCs, and this ability was enhanced with the increasing diameter of nanotubes within a certain range (30–70 V). F-actin mediated nanotube-induced cell differentiation through MKL1 and YAP/TAZ, providing a novel insight into the study of cell differentiation.
Verfügbarkeit von Daten und Materialien
Die in der aktuellen Studie verwendeten und analysierten Datensätze sind auf begründete Anfrage beim entsprechenden Autor erhältlich.
Abkürzungen
- MSCs:
-
Mesenchymal stem cells
- SEM:
-
Rasterelektronenmikroskopie
- EDS:
-
X-ray energy dispersive analysis
- AFM:
-
Rasterkraftmikroskopie
- ALP:
-
Alkaline phosphatase
- Cyto D:
-
Cytochalasin D
- Jasp:
-
Jasplakinolide
- VCL:
-
Vinculin
- FAK:
-
Focal adhesion kinase
- BCA:
-
Bicinchoninic acid
- PVDF:
-
Polyvinylidenedifluoride
- Runx2:
-
Runt-related transcription factor 2
- Osx:
-
Osterix
- OCN:
-
Osteocalcin
- YAP:
-
Yes-associated protein
- MKL1:
-
Megakaryoblastic leukemia 1
- FBS:
-
Fötales Rinderserum
- ECM:
-
Extracellular matrix
- MLC:
-
Myosin light chain
- LIMK:
-
LIM kinase
- FH:
-
Formin-homology
- GPCR:
-
G protein-coupled receptors
- MAP2K:
-
Mitogen-activated protein kinase kinase
- ERK:
-
Extracellular signal-regulated kinase
- SRF:
-
Serum response factor
- SMA:
-
Smooth muscle actin
- PPARγ:
-
Peroxisome proliferator-activated receptor γ
- LATS1/2:
-
Large tumor suppressor gene 1 and 2
- TBX5:
-
T-box 5
Nanomaterialien
- TITANDIOXID - TiO2 - Preis, Markt und Analyse
- Auf dem Weg zu TiO2-Nanofluiden – Teil 1:Vorbereitung und Eigenschaften
- Nanotechniken inaktivieren Krebsstammzellen
- Auf dem Weg zu TiO2-Nanofluiden – Teil 2:Anwendungen und Herausforderungen
- Auswirkung der Verteilung von Goldnanopartikeln in TiO2 auf die optischen und elektrischen Eigenschaften von farbstoffsensibilisierten Solarzellen
- Synthese von ZnO-Nanokristallen und Anwendung in invertierten Polymersolarzellen
- Die optimale Titan-Vorstufe zur Herstellung einer kompakten TiO2-Schicht für Perowskit-Solarzellen
- Einfluss der elastischen Steifigkeit und Oberflächenhaftung auf das Prellen von Nanopartikeln
- Einfluss von in einer TiO2-Kompaktschicht eingebetteten Ag-Nanopartikeln unterschiedlicher Größe und Konzentration auf die Konversionseffizienz von Perowskit-Solarzellen
- Ein neues Up-Conversion-Material von Ho3+-Yb3+-Mg2+ Tri-dotiertem TiO2 und seine Anwendungen auf Perowskit-Solarzellen



