Herunterregulierung von microRNA-342-5p oder Hochregulierung von Wnt3a hemmt die Angiogenese und erhält die Stabilität der atherosklerotischen Plaque bei Arteriosklerose-Mäusen
Zusammenfassung
Es gibt Hinweise darauf, dass microRNA-342-5p (miR-342-5p) an Atherosklerose (AS) beteiligt ist, aber über ihre intrinsischen Regulationsmechanismen ist wenig bekannt. Hier zielten wir darauf ab, die Wirkung von miR-342-5p, das auf Wnt3a abzielt, auf die Bildung von anfälligen Plaques und die Angiogenese von AS zu untersuchen. ApoE −/− Mäuse wurden 16 w lang mit fettreichem Futter gefüttert, um das AS-gefährdete Plaque-Modell zu replizieren. miR-342-5p- und Wnt3a-Expression in Aortengeweben von AS wurden nachgewiesen. Die Zielbeziehung zwischen miR-342-5p und Wnt3a wurde verifiziert. Darüber hinaus ist ApoE −/− Mäusen wurde miR-342-5p-Antagomir und der Überexpressions-Wnt3a-Vektor injiziert, um ihre Funktionen in Bezug auf Serumlipidspiegel, Zytokine im Zusammenhang mit entzündlichem und oxidativem Stress, Aortenplaquestabilität und Angiogenese in Plaque von AS-Mäusen zu testen. Die miR-342-5p-Expression wurde verstärkt und die Wnt3a-Expression wurde in Aortengeweben von AS-Mäusen abgebaut und miR-342-5p zielte direkt auf Wnt3a ab. Die Hochregulierung von Wnt3a oder die Herunterregulierung von miR-342-5p reduzierte den Blutfettgehalt, entzündlichen und oxidativen Stress, die Anfälligkeit von Aortengewebeplaque und hemmte die Angiogenese in Aortenplaque von AS-Mäusen. Funktionelle Studien zeigen, dass die Depletion von miR-342-5p Aortengewebe-Plaque stabilisieren und die Angiogenese in Plaque bei AS-Mäusen durch Wiederherstellung von Wnt3a reduzieren kann.
Einführung
Atherosklerose (AS) ist eine altersbedingte Arterienerkrankung, die durch Verdickung, Stenose, Verhärtung und Bildung atherosklerotischer Plaques der Arterien gekennzeichnet ist [1]. Es ist die vorherrschende Todes- und Morbiditätsursache in den Industrieländern [2]. Histopathologische Studien an humanen atherosklerotischen Läsionen haben gezeigt, dass Plaqueentwicklung und -ruptur durch eine Lipid-/nekrotische Kernexpansion, eine Verringerung der Anzahl glatter Muskelzellen, eine Makrophageninfiltration und einen verringerten Kollagengehalt gekennzeichnet sind [3]. Die zellulären Schlüsselelemente der AS umfassen Hyperlipidämie, Schaumzellbildung, Differenzierung in Makrophagen, Monozytenrekrutierung und induzierte Entzündung [4]. Obwohl viele Medikamente zur Behandlung von AS in der Klinik weit verbreitet sind, haben einige Untergruppen von Patienten immer noch ein hohes Risiko für Myokardinfarkt, Myokardischämie, Herzinsuffizienz und Schlaganfall [5]. Daher kann die weitere Erforschung potenzieller molekularer Mechanismen mehr Beweise für die Behandlung von AS liefern.
Eine einzelne microRNA (miRNA) kann gleichzeitig mehrere Gen-Targets regulieren [6]. Es wird untersucht, dass miR-342-5p im geprägten 14q32 miRNA-Cluster enthalten ist, als innovatives Notch-Downstream-Molekül wirkt [7] und mehrere angiogene Signalwege moduliert, wie z. Verwandte immunmodulatorische microRNAs, wie miR-342-5p, spielen mehrere wichtige Rollen bei der Regulierung des Fortschreitens der Atherosklerose [9]. Darüber hinaus wurde vorgeschlagen, dass einige miRNAs an der Auflösung von AS beteiligt sind, wie z. B. miR-155 und miR-217 [10, 11]. Eine Studie hat berichtet, dass miR-342-5p als neuer Modulator für die Makrophagenaktivierung bei AS wirkt [12]. Eine andere Studie hat gezeigt, dass von Makrophagen abgeleitetes miR-342-5p AS erleichtert und die Entzündungsstimulation von Makrophagen erhöht [13]. Qu et al. haben herausgefunden, dass die Wnt3a-Expression bei anorektalen Fehlbildungen durch miR-342-5p negativ moduliert wird [14], was darauf hindeutet, dass es eine Zielbeziehung zwischen miR-342-5p und Wnt3a gibt. Der Wnt-Signalweg spielt während der Embryogenese eine wesentliche Rolle für die Modulation der Zellpolarität, Zellproliferation, Achsenbildung und Apoptose [15]. Wnt3a, eine Schlüsselkomponente des Mesoderm-Gens, spielt eine entscheidende Rolle in der Embryonalentwicklung [16]. Es wurde präsentiert, dass die epigenomgesteuerte Analyse des Transkriptoms der Plaque-Makrophagen während der AS-Regression eine Aktivierung des Wnt-Signalwegs aufdeckt [17]. Darüber hinaus hat eine Studie berichtet, dass Wnt3a die Adhäsion und Migration von vaskulären glatten Muskelzellen moduliert, die zur Pathogenese von AS und Restenose beitragen [18]. Daher untersuchte diese Studie zum ersten Mal die Wirkung von miR-342-5p gezieltem Wnt3a auf die Bildung von empfindlichen Plaques und die Angiogenese von AS.
Materialien und Methoden
Ethikerklärung
Die Tiere wurden nach anerkannten Verfahren in Übereinstimmung mit den Empfehlungen im Leitfaden für die Pflege und Verwendung von Labortieren der National Institutes of Health human behandelt. Das Protokoll wurde vom Institutional Animal Care and Use Committee des Qinghai Provincial People’s Hospital (Ethiknummer:201870726) genehmigt.
Versuchstiere
Männlicher ApoE −/− Mäuse und C57BL/6J-Mäuse (spezifischer pathogenfreier Grad) im Alter von 8 Wochen waren von Beijing Vital Laboratory Animal Technology (Beijing, China) erhältlich. Mäuse (5–6 Mäuse in einem Käfig) wurden mit einem Tag/Nacht-Zyklus von 12 h/12 h mit freiem Zugang zu Futter und Wasser gehalten.
Etablierung von Mäusemodellen von AS
ApoE −/− Mäuse wurden 16 w lang mit fettreichem Futter gefüttert, um das AS-gefährdete Plaque-Modell zu etablieren. C57BL/6 J-Mäuse wurden als normale Gruppe mit natürlichem Getränk und Nahrung verwendet. ApoE −/− Mäuse hatten nach 12 W glänzendes helles Haar und Haarausfall im Rücken. Der Aortenbogen und die brachiocephale Arterie von 3 Modellmäusen wurden seziert, um eine Hämatoxylin-Eosin (HE)-Färbung durchzuführen, und es gab keine signifikanten Plaqueablagerungen auf der Intima. Weitere 3 modellierte Mäuse wurden nach 4 Wochen wieder identifiziert, und die HE-Färbung zeigte, dass es offensichtliche Plaqueablagerungen auf der Intima des Aortenbogens gab, was auf den Erfolg der Modellherstellung hinweist.
Gruppierung und Behandlung von Mäusen
ApoE −/− Mäuse mit AS-gefährdeten Plaques wurden in 6 Gruppen mit 12 Mäusen in jeder Gruppe eingeteilt:AS-Gruppe, negative Kontrollgruppe (NC) (injiziert mit normaler Kochsalzlösung in ApoE −/− Mäuse), miR-342-5p-Agomir-Gruppe (injiziert mit miR-342-5p-Agomir, um die miR-342-5p-Expression in ApoE zu überexprimieren −/− Mäuse), miR-342-5p-Antagomir-Gruppe (injiziert mit miR-342-5p-Antagomir, um die miR-342-5p-Expression in ApoE zu reduzieren −/− Mäuse), Überexpression (oe)-Wnt3a-Gruppe (injiziert mit oe-Wnt3a-Vektor zur Hochregulierung der Wnt3a-Expression in ApoE −/− Mäuse) und miR-342-5p-Agomir + oe-Wnt3a-Gruppe (injiziert mit miR-342-5p-Agomir und oe-Wnt3a-Vektor zur Hochregulierung der Expression von miR-342-5p und Wnt3a in ApoE −/− Mäuse). C57BL/6 J-Mäuse als normale Gruppe wurden mit normaler Nahrung gefüttert. Das fettreiche Futter enthielt 20 % Fett und 0,25 % Cholesterin. miR-342-5p-Agomir, miR-342-5p-Antagomir und oe-Wnt3a-Vektor wurden von Sangon (Shanghai, China) gekauft. Die oe-Wnt3a-Vektoren miR-342-5p-Agomir, miR-342-5p-Antagomir wurden alle in 0,2 ml normaler Kochsalzlösung gelöst und Mäusen in einer Dosis von 40 mg/kg alle zwei Wochen über die Schwanzvene injiziert. Nach 8 Wochen wurden Blutproben aus Augäpfeln entnommen und anschließend wurden die Mäuse eingeschläfert, um arterielles Gewebe zu entnehmen [19].
Im Vorversuch ApoE −/− Mäusen mit AS wurden 10 mg/kg, 20 mg/kg, 40 mg/kg miR-342-5p-Agomir, miR-342-5p-Antagomir oder oe-Wnt3a-Vektor injiziert (einmal alle zwei Wochen; insgesamt 4-mal). Dann wurden die Expressionsspiegel von β-Catenin durch die quantitative Polymerase-Kettenreaktion der reversen Transkription (RT-qPCR) nachgewiesen.
Probenentnahme und -behandlung
Vor der Probenahme wurden die Mäuse 12 Stunden lang gefastet und durch Etherinhalation anästhesiert, und es wurden Blutproben aus Augäpfeln entnommen. Der Brustkorb von Mäusen wurde geöffnet, die Brustschlagader wurde bis zum Ende der Bauchschlagader dissoziiert und das gesamte Gefäß wurde entfernt. Nach der Reinigung mit RNA-freier phosphatgepufferter Kochsalzlösung (PBS) wurden die Gewebe für HE-Färbung, Ölrot-O-, Sirius-Rot-Färbung und immunhistochemische Färbung eingebettet. Einige der Gefäßgewebe wurden bei – 80 °C für RT-qPCR und Western-Blot konserviert.
Blutlipidspiegelerkennung
Der automatische biochemische Analysator (Roche, Basel, Schweiz) wurde zum Nachweis von Gesamtcholesterin (TC), Triglycerid (TG), Low-Density-Lipoprotein-Cholesterin (LDL-C) und High-Density-Lipoprotein-Cholesterin (HDL-C) im Serum eingesetzt. Die Detektion wurde gemäß der Spezifikation der Kits implementiert (NanJing JianCheng Bioengineering Institute, Nanjing, China).
Enzyme-Linked Immunosorbent Assay (ELISA)
Bestimmung des Serumzytokingehalts:Es wurden kommerzielle Interleukin (IL)-5, IL-12p70, Tumornekrosefaktor alpha (TNF-α) und Interferon (IFN)-γ ELISA-Kits verwendet. Schließlich wurde der Wert der optischen Dichte (OD) jeder Vertiefung mit einem Mikroplatten-Lesegerät bei 450 nm getestet.
Bestimmung der Schädigung durch oxidativen Stress:Malondialdeyde (MDA)-Gehalt und Superoxid-Dismutase (SOD)-Aktivität im Serum wurden mit dem MDA-Kit (OD-Wert wurde mit einem Spektrophotometer bei 532 nm getestet) und dem SOD-Kit (OD-Wert wurde mit einem Mikroplatten-Lesegerät bei 450 . bestimmt) getestet nm). IL-5-, IL-12p70-, TNF-α-, IFN-γ-, MDA- und SOD-ELISA-Kits wurden von MultiSciences (Lianke) Biotechnology Corporate Limited (Hangzhou, Zhejiang, China) bezogen.
HE-Färbung, Oil Red O-Färbung und Sirius-Rot-Färbung
Nach der Fixierung und Einbettung wurden die Proben in aufeinanderfolgende Abschnitte von 4 Mikrometer Dicke geschnitten. Die Schnitte wurden entwachst und hydratisiert, mit Hämatoxylin und Eosin gefärbt, differenziert, dehydratisiert, mit Xylol geklärt, getrocknet und mit neutralem Gummi versiegelt. Der Kern war blau und andere Gewebe wie Zytoplasma und Bindegewebe waren in verschiedenen Schattierungen rot. Die Plaquebildung wurde mit einem Fluoreszenzmikroskop beobachtet. Die Arterienwände von HE-gefärbten Schnitten wurden unter dem Mikroskop ausgewählt und die experimentellen Ergebnisse wurden mit einer Digitalkamera gesammelt. Das Bildanalyse-Softwaremodul Image Pro Plus6.0 (IPP6.0) wurde verwendet, um die Plaque-Querschnittsfläche jeder Schicht und die Wandfläche sowie deren Verhältnis zu berechnen.
Für die Ölrot-O-Färbung wurden Schnitte mit 4–5 μm gewählt. Die Schnitte wurden 20 Minuten bei Übertemperatur getrocknet und 5 Minuten mit 100 % Isopropanol inkubiert. Anschließend wurden die Schnitte mit 0,5 % ölroter O-Färbelösung in einem 60 °C-Ofen 8 min inkubiert, 3 min in 85 % Isopropanol gewaschen, 1 min mit Hämatoxylin gefärbt, gereinigt und versiegelt. Die Ergebnisse der Ölrot-O-Färbung legten nahe, dass das Lipid rot oder orange und der Zellkern hellblau war. Die Software IPP6.0 wurde verwendet, um den Fettbereich und den Plaquebereich in der Plaque des Gewebeschnitts zu berechnen. Der Lipidgehalt = Ölrot O-positiver Färbungsbereich/Plaquebereich × 100%.
Sirius-Rot-Färbung:Schnitte wurden entwachst und hydratisiert, 10 Minuten mit Celestine-Blau-Färbelösung, mit Sirius-Rot-Färbelösung 20 Minuten gefärbt und 10 Minuten mit Hämatoxylin gegengefärbt. Schließlich wurden die Scheiben durch Gradienten-Ethanol entwässert, mit Xylol geklärt und mit neutralem Gummi versiegelt. Die Kollagenfläche in der Plaque des Gewebeschnitts wurde mit der Software IPP6.0 berechnet. Der Kollagenbereich =Siriusrot positiver Färbebereich/Plaquebereich × 100%. Der Prozentsatz an Lipid und Kollagen im Plaquebereich wurde berechnet.
Hämatoxylin, Eosin und Sirius-Farbstoff waren von China Pharmaceutical Group Shanghai Chemical Reagent Co. Ltd. (Shanghai, China) erhältlich. Das ölrote O-Pulver wurde von Sigma-Aldrich Chemical Company (St. Louis, MO, USA) gekauft.
Quantitative Reverse Transkription der Polymerase-Kettenreaktion (RT-qPCR)
Die Aortengewebe wurden dem Gesamt-RNA-Extraktionsreagenz Trizol (Invitrogen, Carlsbad, Kalifornien, USA) zugesetzt und dann homogenisiert, um die Gesamt-RNA zu extrahieren und komplementäre DNA zusammenzusetzen. Die Primer wurden alle auf die von Genbank bereitgestellte Sequenz bezogen, entworfen von Primer 5.0 und synthetisiert von Shanghai Sangon Biotechnology Co. Ltd. MiR-342-5p:Vorwärts:5'-CGGAGGGGTGCTATCTGATTGAG-3' Firma, Hilden, Deutschland); Wnt3a:vorwärts:5′-AGGTAAGCTACTCCCTCAACTA-3′, rückwärts:5′-CTGAAGCACCCTCTCATGTATC-3′; β-Aktin:vorwärts:5′-GCACCACACCTTCTACAATGAGC -3′, rückwärts:5′-TCGTTGCCAATAGTGATGACC-3′; β-Catenin:vorwärts:5′-TCAAGAGAGCAAGCTCATCATTCT-3′, rückwärts:5′-CACCTTCAGCACTCTGCTTGTG-3′. Nach der Reaktion wurde der Schwellenzyklus (Ct) per Computer analysiert. Das relative Verhältnis von miR-342-5p zu U6 wurde als seine Expression verwendet, das relative Verhältnis von Wnt3a zu β-Aktin wurde als seine Expression verwendet und das relative Verhältnis wurde mit 2 −ΔΔCt . berechnet Methode.
Western Blot-Analyse
Das Gesamtprotein wurde aus dem Aortengewebe abstrahiert. Die Proteinkonzentration wurde durch das Bicinchoninsäure-Verfahren gemessen. Es wurde eine Polyacrylamid-Gelelektrophorese durchgeführt. Dann wurde Protein auf die Polyvinylidenfluoridmembran übertragen und die Zielbande wurde erhalten. Die Membran wurde 1 h in 5% Magermilch versiegelt, mit Primärantikörpern Wnt3a (1:500), β-Catenin (1:1000, Santa Cruz Biotechnology, Inc., Santa Cruz, CA, USA), CD34 (1 .) :2500, Abcam, MA, USA) und β-Actin (1:2000, Beyotime Biotechnology Co., Shanghai, China) bei 4 °C über Nacht. Die Membran wurde mit Tris-gepufferter Kochsalzlösung mit Tween 20 (pH = 7,5, 10 mmol/l Tris-HCl, 100 mmol/l NaCl und 0,2% Tween-20) 10 min lang × 3-mal gewaschen und dann mit sekundärem Antikörper . angehängt (1:1000, ZSGB-Bio, Peking, China) für 2 h. Die ImageJ-Software wurde verwendet, um den Grauwert der Banden zu bewerten und die Proteinexpression zu quantifizieren.
Immunhistochemische Färbung
Auf die mit 100 mg/l Polylysin beschichteten Objektträger wurden Scheiben von 4–5 μm gelegt und mit Aceton fixiert. Die endogene Peroxidase wurde durch Rinderserumalbumin blockiert. Die Gewebe wurden mit MOMA-2-Antikörper (1:200), α-SMA (1:200) und CD34 (1:200, Abcam Inc., Cambridge, MA, USA) sowie mit Sekundärantikörper-Arbeitslösung ( 1:1000). Die Gewebe wurden mit Diaminobenzidin entwickelt, mit Hämatoxylin gegengefärbt (1 min), dehydriert, gereinigt, versiegelt und unter dem Mikroskop beobachtet. Für jeden immunhistochemischen Schnitt wurden drei verschiedene Gesichtsfelder ausgewählt. Zur quantitativen Analyse wurde die Software IPP6.0 durchgeführt. Eine positive immunhistochemische Färbung von MOMA-2 bzw. α-SMA zeigt an, dass Makrophagen und glatte Muskelzellen hauptsächlich im Zytoplasma lokalisiert sind, das gelb bis braun ist. Die Prozentsätze von Makrophagen und glatten Muskelzellen wurden separat berechnet, die mit dem Prozentanteil von Lipid und Kollagen in der Plaque kombiniert wurden, um den Plaque-Vulnerabilitätsindex zu berechnen. Der Vulnerabilitätsindex von Plaque = (positiver Prozentsatz von Makrophagen + positiver Prozentsatz von Lipiden)/(positiver Prozentsatz von Kollagen + positiver Prozentsatz von glatten Muskelzellen) [20]. Die Mikrogefäßdichte (MVD) wurde durch Messung der CD34-Expression bestimmt und als Anzahl der Mikrogefäße/mm 2 . quantifiziert .
Dualer Luciferase-Reporter-Gen-Assay
Das Zielgen von miR-342-5p wurde von der Website für biologische Vorhersage (http://www.microRNA.org) analysiert. Der duale Luciferase-Reportergen-Assay wurde verwendet, um zu überprüfen, ob Wnt3a das Zielgen von miR-342-5p war. Die Wildtyp- oder Mutantensequenz der 3'-untranslatierten Region von Wnt3a (3'-UTR) wurde in den GP-miRGLO-Vektor (GenePharma, Shanghai, China) kloniert. Der Reporter (0,5 μg) und 1, 10 oder 100 pM miR-342-5p-Agomir wurden 48 h lang in Maus-Aorten-Endothelzellen (Nr. 506, MingzhouBio, Ningbo, China) transfiziert, um die Luciferase-Aktivität mit einem dualen Luciferase-Assay-System zu testen (Promega, WI, USA).
Statistische Analyse
Alle Daten wurden mit der Software SPSS 21.0 (IBM Corp. Armonk, NY, USA) interpretiert. Die Messdaten wurden als Mittelwert ± Standardabweichung angegeben. Unterschiede zwischen zwei Gruppen wurden von t . formuliert -Test, während diejenigen unter mehreren Gruppen durch Einweg-Varianzanalyse (ANOVA) gefolgt von Tukeys Mehrfachvergleichstest. Statistische Signifikanz wurde festgestellt von P Wert < 0.05.
Ergebnisse
miR-342-5p erhöht und Wnt3a sinkt im Aortengewebe von ApoE −/− Mäuse und miR-342-5p zielen direkt auf Wnt3a ab
MicroRNA (miRNA)-Zielgene sind mit Atherosklerose-bezogenen Funktionen verbunden. miR-342-5p, Wnt3a und β-Catenin wurden in Aortengeweben von AS-Modellmäusen mittels RT-qPCR und Western-Blot-Assay getestet. Es zeigte sich, dass im Vergleich zur Normalgruppe miR-342-5p erhöht war, während Wnt3a und β-Catenin in der AS-Gruppe verringert waren (beide P < 0,05). Im Vergleich zur NC-Gruppe war miR-342-5p erhöht sowie Wnt3a und β-Catenin in der miR-342-5p-Agomir-Gruppe verringert (beide P < 0,05), während miR-342-5p verringert war, waren Wnt3a und β-Catenin in der miR-342-5p-Antagomir-Gruppe erhöht (beide P < 0,05). Wnt3a- und β-Catenin-Expression waren in der oe-Wnt3a-Gruppe im Vergleich zur NC-Gruppe erhöht (beide P < 0,05). Im Vergleich zur miR-342-5p-Agomir-Gruppe war die Wnt3a- und β-Catenin-Expression in der miR-342-5p-Agomir + oe-Wnt3a-Gruppe erhöht (P < 0,05) (Abb. 1A–D). Außerdem wurde im Vorversuch die β-Catenin-Expression unter Behandlung unterschiedlicher Konzentrationen von miR-342-5p-Agomir, miR-342-5p-Antagomir und oe-Wnt3a getestet und die Ergebnisse gezeigt (Zusatzdatei 1:Abb. S1 ) je höher die Konzentration von miR-342-5p-Agomir, desto niedriger die β-Catenin-Expression; je höher die miR-342-5p-Antagomir-Konzentration, desto höher die β-Catenin-Expression; und je höher die oe-Wnt3a-Konzentration, desto höher die β-Catenin-Expression.
miR-342-5p steigt und Wnt3a sinkt im Aortengewebe von ApoE −/− Mäuse und miR-342-5p zielen direkt auf Wnt3a ab. A Expression von miR-342-5p im Aortengewebe von Mäusen, nachgewiesen durch RT-qPCR. B Expression von Wnt3a-mRNA im Aortengewebe von Mäusen, nachgewiesen durch RT-qPCR (n = 12). C , D Wnt3a- und β-Catenin-Proteinexpression in Aortengeweben von Mäusen, getestet durch Western-Blot-Analyse (n = 12). E Bindungsstelle von miR-342-5p innerhalb von Wnt3a 3′-UTR. F miR-342-5p-Agomir verringerte dosisabhängig die relative Aktivität in mit Wnt3a 3′-UTR transfizierten Zellen (N = 3). G Relative Aktivität von Luciferase in Zellen mit Wildtyp- und mutiertem Wnt3a 3′-UTR nach Transfektion mit miR-342-5p-Agomir oder Scramble (N = 3). *P < 0,05 im Vergleich zur normalen Gruppe, # P < 0,05 gegenüber der NC-Gruppe. &P < 0,05 gegenüber der miR-342-5p-Agomir-Gruppe. Die Messdaten wurden als Mittelwert ± Standardabweichung angegeben. Vergleiche zwischen zwei Gruppen wurden von t . formuliert -Test, während Vergleiche zwischen mehreren Gruppen durch Einweg-ANOVA bewertet wurden, gefolgt von Tukeys Mehrfachvergleichstest. AS, Arteriosklerose; NC, Negativkontrolle
miRNAs könnten die Translation bestimmter Gene hemmen, indem sie an ihre Boten-RNA 3′UTR binden. Die Bioinformatik-Website sagte voraus, dass es eine Zielbeziehung zwischen miR-342-5p und Wnt3a gibt (Abb. 1E). Dualer Luciferase-Reportergen-Assay berichtete, dass in Wnt3a-3′UTR-Vektor-transfizierten Maus-Aorten-Endothelzellen der Renilla/Firefly-Wert der Luciferase durch die Transfektion mit miR-342-5p-Agomir dosisabhängig verringert wurde, mit einer signifikanten Abnahme von 10 auf 100 pM miR-342-5p-Agomir und ein Rückgang um 64 % trat bei 100 pM miR-342-5p-Agomir-Gruppe im Vergleich zur NC-Gruppe auf. Dies zeigte die Anwesenheit einer miR-342-5p-Zielstelle im Wnt3a-3′UTR an. Der Renilla-/Glühwürmchen-Wert der Luciferase-Aktivität wurde jedoch in der Wnt3a-Mutationsgruppe nicht beeinflusst (Abb. 1F, G). Somit konnte bestätigt werden, dass Wnt3a ein direktes Zielgen von miR-342-5p war und miR-342-5p/Wnt3a die AS-Progression regulieren könnte.
Auswirkungen von hochreguliertem Wnt3a oder runterreguliertem miR-342-5p auf die Lipidwerte bei ApoE −/− Mäuse
Um zu untersuchen, ob miR-342-5p, das den Wnt3a-Signalweg ansteuert und reguliert, die Lipidspiegel von AS-Mäusen beeinflusst, wurde ein automatischer biochemischer Analysator verwendet, um die Veränderung der Lipidspiegel zu beobachten. Die Ergebnisse zeigten, dass (Abb. 2A–D) im Gegensatz zur normalen Gruppe der TC-, TG- und LDL-C-Gehalt erhöht und der HDL-C-Gehalt in der AS-Gruppe (alle P < 0,05). Im Vergleich zur NC-Gruppe waren die TC-, TG- und LDL-C-Gehalte erhöht und der HDL-C-Gehalt in der miR-342-5p-Agomir-Gruppe (alle P < 0,05), während der TC-, TG- und LDL-C-Gehalt verringert und der HDL-C-Gehalt in der miR-342-5p-Antagomir-Gruppe und der oe-Wnt3a-Gruppe (alle P < 0,05). In Bezug auf die miR-342-5p-Agomir-Gruppe waren die TC-, TG- und LDL-C-Gehalte reduziert und der HDL-C-Gehalt in der miR-342-5p-Agomir + oe-Wnt3a-Gruppe (alle P < 0,05). Diese Ergebnisse legten nahe, dass miR-342-5p und Wnt3a den Blutfettspiegel von AS-Mäusen regulierten und veranschaulichten weiter die gezielte Regulationsbeziehung zwischen miR-342-5p und Wnt3a. Eine Überexpression von Wnt3a würde die überexprimierten miR-342-5p-induzierten Wirkungen auf AS-Mäuse umkehren.
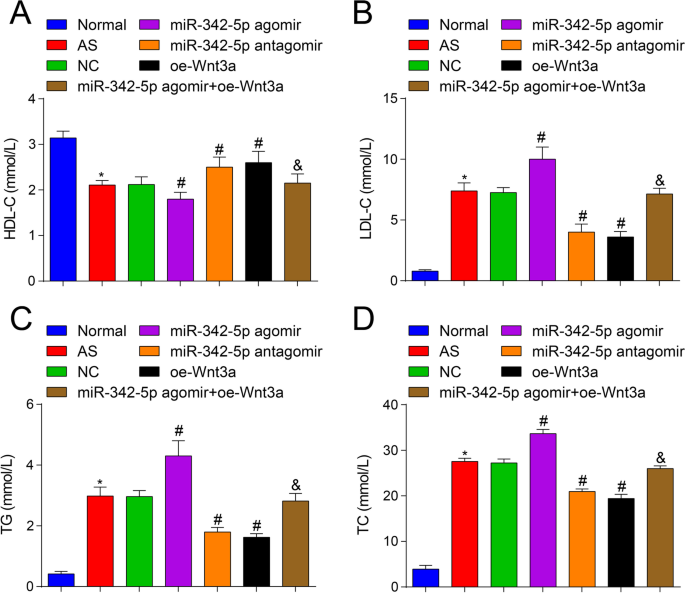
Auswirkungen von hochreguliertem Wnt3a oder herunterreguliertem miR-342-5p auf die Lipidspiegel bei ApoE −/− Mäuse. A Vergleich der HDL-C-Gehalte im Serum der Mäusegruppe. B Vergleich der LDL-C-Gehalte im Serum der Mäusegruppe. C Vergleich der TG-Gehalte im Serum der Mäusegruppe. D Vergleich der TC-Gehalte im Serum der Mäusegruppe. n = 12.*P < 0,05 im Vergleich zur normalen Gruppe, # P < 0,05 gegenüber der NC-Gruppe. &P < 0,05 gegenüber der miR-342-5p-Agomir-Gruppe. Die Messdaten wurden als Mittelwert ± Standardabweichung angegeben. Vergleiche zwischen mehreren Gruppen wurden durch Einweg-ANOVA bewertet, gefolgt von Tukeys Mehrfachvergleichstest. AS, Arteriosklerose; NC, Negativkontrolle
Auswirkungen einer Überexpression von Wnt3a oder einer geringen Expression von miR-342-5p auf entzündliche und oxidative Stress-bedingte Zytokine im Serum von ApoE −/− Mäuse
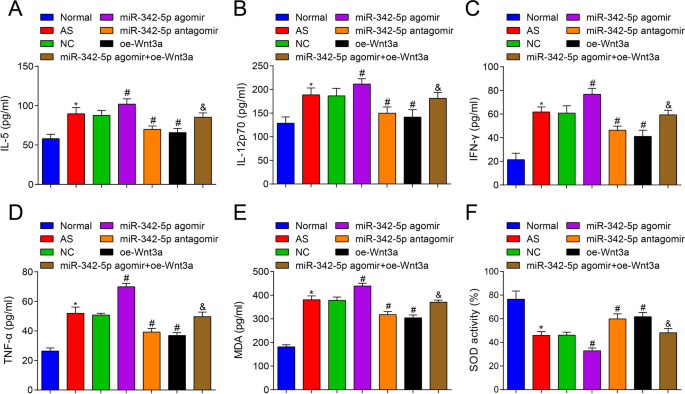
Dann wurde der Gehalt an Zytokinen im Serum von AS-Mäusen durch ELISA getestet, und die Ergebnisse zeigten, dass (Abb. 3A–D) gegenüber der normalen Gruppe IL-5, IL-12p70, IFN-γ und TNF-α erhöht waren in der AS-Gruppe (alle P < 0,05). Im Vergleich zur NC-Gruppe wurden die IL-5-, IL-12p70-, IFN-γ- und TNF-α-Gehalte in der miR-342-5p-Agomir-Gruppe (alle P < 0,05), während die IL-5-, IL-12p70-, IFN-γ- und TNF-α-Gehalte in der miR-342-5p-Antagomir-Gruppe und der oe-Wnt3a-Gruppe (alle P < 0,05). Im Gegensatz zur miR-342-5p-Agomir-Gruppe waren die IL-5-, IL-12p70-, IFN-γ- und TNF-α-Gehalte in der miR-342-5p-Agomir + oe-Wnt3a-Gruppe (alle P < 0,05). Es wurde angedeutet, dass die gezielte Regulierung des Wnt3a-Signalwegs durch miR-342-5p den Spiegel verwandter Zytokine im Serum von AS-Mäusen weiter reguliert.

Auswirkungen einer Überexpression von Wnt3a oder einer geringen Expression von miR-342-5p auf Zytokine im Zusammenhang mit entzündlichem und oxidativem Stress im Serum von ApoE −/− Mäuse. A Vergleich der IL-5-Gehalte im Serum der Mäusegruppe. B Vergleich der IL-12p70-Gehalte im Serum der Mäusegruppe. C Vergleich der IFN-γ-Gehalte im Serum der Mäusegruppe. D Vergleich der TNF-α-Gehalte im Serum der Mäusegruppe. E, Vergleich des MDA-Gehalts im Serum der Mäusegruppe. F Vergleich der SOD-Aktivität im Serum der Mäusegruppe. n = 12.*P < 0,05 im Vergleich zur normalen Gruppe, # P < 0,05 gegenüber der NC-Gruppe. &P < 0,05 gegenüber der miR-342-5p-Agomir-Gruppe. Die Messdaten wurden als Mittelwert ± Standardabweichung angegeben. Vergleiche zwischen mehreren Gruppen wurden durch Einweg-ANOVA bewertet, gefolgt von Tukeys Mehrfachvergleichstest. AS, Arteriosklerose; NC, Negativkontrolle
Darüber hinaus wurden der MDA-Gehalt und die SOD-Aktivität im Serum von Mäusen getestet, und es wurde gezeigt, dass (Fig. 3E, F) im Vergleich zur normalen Gruppe der MDA-Gehalt erhöht und die SOD-Aktivität in der AS-Gruppe (beide P < 0,05). Im Vergleich zur NC-Gruppe war der MDA-Gehalt erhöht und die SOD-Aktivität in der miR-342-5p-Agomir-Gruppe (beide P < 0,05), während der MDA-Gehalt verringert und die SOD-Aktivität in der miR-342-5p-Antagomir-Gruppe und der oe-Wnt3a-Gruppe (alle P < 0,05). Im Vergleich zur miR-342-5p-Agomir-Gruppe war der MDA-Gehalt verringert und die SOD-Aktivität in der miR-342-5p-Agomir + oe-Wnt3a-Gruppe (beide P < 0,05). Daher wurde eine Zusammenfassung erhalten, dass der Abbau von miR-342-5p und die Wiederherstellung von Wnt3a den oxidativen Stress bei AS-Mäusen hemmten.
Auswirkungen des Abbaus von miR-342-5p oder der Wiederherstellung von Wnt3a auf den Lipid- und Kollagengehalt in der Aortenplaque von ApoE −/− Mäuse
Um die Wirkung von miR-342-5p gezieltem Wnt3a auf die Plaquefläche im Aortengewebe von Mäusen zu untersuchen, wurde eine HE-Färbung durchgeführt und die Ergebnisse zeigten, dass (Abb. 4A, B) mit Ausnahme der normalen Gruppe in allen AS-Plaques gebildet wurden Teile der anderen Gruppen. In der AS-Gruppe war die Plaquefläche groß, die Faserkappe war dünner, der Lipidkern war vergrößert, es traten mehr Schaumzellen und Cholesterinkristallpräzipitation in der Plaque auf, die Innenwand der Arterie und die Muskelschicht waren verdickt und die Plaque war instabil. Die Situation in der NC-Gruppe war ähnlich wie in der AS-Gruppe. In der miR-342-5p-Antagomir- und der oe-Wnt3a-Gruppe war die Plaquefläche klein, die Intima der Arterie war glatt und die fibrösen Kappen hatten eine geringe Anzahl und wurden dünner. Es gab keine Ruptur, sondern Schaumzellen in verschiedenen Größen in der Plaque. Die Cholesterinkristalle waren asymmetrisch verteilt und teilweise verkalkt, die Zahl der glatten Muskelzellen und Kollagenfasern war erhöht und die Plaque neigte dazu, stabil zu sein. Im Vergleich zur NC-Gruppe war in der miR-342-5p-Agomir-Gruppe die Plaquefläche vergrößert und die AS-Läsionen verschlimmert (P < 0,05), während die Plaquefläche in der miR-342-5p-Antagomir-Gruppe und der oe-Wnt3a-Gruppe mit reduzierten AS-Läsionen (beide P < 0,05). Im Vergleich zur miR-342-5p-Agomir-Gruppe war die Plaquefläche in der miR-342-5p-Agomir + oe-Wnt3a-Gruppe verringert (P < 0.05).
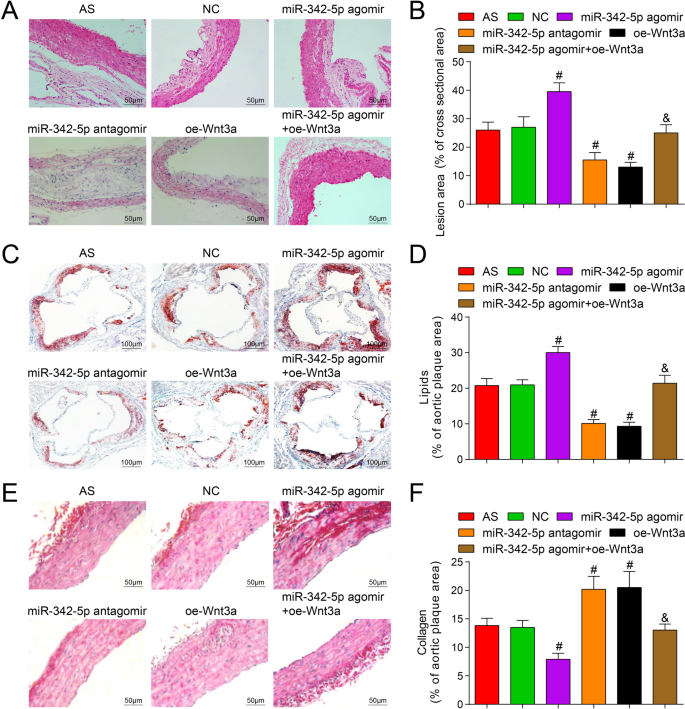
Auswirkungen einer Erschöpfung von miR-342-5p oder einer Wiederherstellung von Wnt3a auf den Lipid- und Kollagengehalt in Aortenplaque von ApoE −/− Mäuse. A Ergebnisse der Aorten-HE-Färbung bei Mäusen (Skalenbalken:50 μm). B Vergleich der Aortenplaquefläche in jeder Mäusegruppe. C Ergebnisse der Aortenöl-Rot-O-Färbung bei allen Mäusegruppen (Skalenbalken:100 μm). D Vergleich des Lipidgehalts im Aortengewebe von Mäusen. E Ergebnisse der Sirius-Rotfärbung der Aorta in jeder Mäusegruppe (Skalenbalken:50 μm). F Vergleich des Kollagengehalts in Aortengeweben von Mäusen. n = 12. # P < 0,05 gegenüber der NC-Gruppe. &P < 0,05 gegenüber der miR-342-5p-Agomir-Gruppe. Die Messdaten wurden als Mittelwert ± Standardabweichung angegeben. Vergleiche zwischen mehreren Gruppen wurden durch Einweg-ANOVA bewertet, gefolgt von Tukeys Mehrfachvergleichstest. AS, Arteriosklerose; NC, Negativkontrolle
Ölrot-O-Färbung und Sirius-Rot-Färbung wurden verwendet, um die Wirkung von miR-342-5p-gerichtetem Wnt3a auf den Lipidgehalt und den Kollagengehalt in Plaque des Aortengewebes von Mäusen nachzuweisen, und die Ergebnisse zeigten, dass (Abb. 4C–F) Ölrot O-Färbung zeigte rotes Fett und blauen Kern, während Sirius-Rot-Färbung rote Kollagenfasern und blauen Kern zeigte. Im Vergleich zur NC-Gruppe war der Lipidgehalt erhöht und der Kollagengehalt in der miR-342-5p-Agomir-Gruppe reduziert sowie der Lipidgehalt wurde reduziert und der Kollagengehalt wurde in der miR-342-5p-Antagomir-Gruppe und dem oe-Wnt3a . akkumuliert Gruppe (alle P < 0,05). In Bezug auf die miR-342-5p-Agomir-Gruppe war der Lipidgehalt verringert und der Kollagengehalt in der miR-342-5p-Agomir + oe-Wnt3a-Gruppe erhöht (beide P < 0,05). Die experimentellen Ergebnisse zeigten vollständig, dass die gezielte miR-342-5p-Regulierung des Wnt3a-Signalwegs eine regulatorische Wirkung auf den Lipid- und Kollagengehalt in Aortenplaques von AS-Mäusen hatte.
Auswirkungen von herunterreguliertem miR-342-5p oder hochreguliertem Wnt3a auf Makrophagen und glatte Muskelzellen in Aortenplaque von ApoE −/− Mäuse
Der Grad der AS ist direkt proportional zum Gehalt an mononuklearen Makrophagen [21]. VSMCs sind die Hauptzellen in der mittleren Schicht der Arterien und sind für die Aufrechterhaltung der Integrität der Arterienwand unerlässlich. VSMCs sind an der Rekonstruktion der Arterienwand beteiligt und spielen bei AS in verschiedenen Stadien eine wichtige Rolle [22]. α-SMA ist ein spezifischer Marker glatter Muskelzellen [23]. In dieser Studie wurde ein Makrophagen-Marker-Antikörper (MOMA-2) verwendet, um Makrophagen zu markieren, und es wurde Immunhistochemie angewendet, um die MOMA-2- bzw. α-SMA-Expression nachzuweisen.
Unter dem Mikroskop zeigt eine positive immunhistochemische Färbung von MOMA-2 bzw. α-SMA, dass Makrophagen und glatte Muskelzellen hauptsächlich im Zytoplasma lokalisiert sind, das gelb bis braun ist. MOMA-2 immunpositiv zeigte an, dass Makrophagen hauptsächlich im Zytoplasma mit Gelb bis Braun lokalisiert waren. Immunhistochemisch bestimmt, zeigte sich, dass im Vergleich zur NC-Gruppe der Prozentsatz der positiven Färbung von Plaque-Makrophagen (MAMO-2) erhöht und der Prozentsatz positiver glatter Muskelzellen im miR-342-5p-Agomir (beide P < 0,05). Der Prozentsatz der positiven Färbung von Plaque-Makrophagen (MAMO-2) wurde in der miR-342-5p-Antagomir-Gruppe und der oe-Wnt3a-Gruppe (alle P < 0,05). Im Vergleich zur miR-342-5p-Agomir-Gruppe war der Prozentsatz der positiven Färbung von Plaque-Makrophagen (MAMO-2) erniedrigt und der Prozentsatz positiver glatter Muskelzellen in der miR-342-5p-Agomir + oe-Wnt3a-Gruppe erhöht (beide P < 0,05) (Abb. 5A–D). Es wurde impliziert, dass die gezielte miR-342-5p-Regulierung des Wnt3a-Signalwegs die Aggregation von Makrophagen und glatten Muskelzellen in arteriellen Gewebeplaques von AS-Mäusen regulieren könnte.
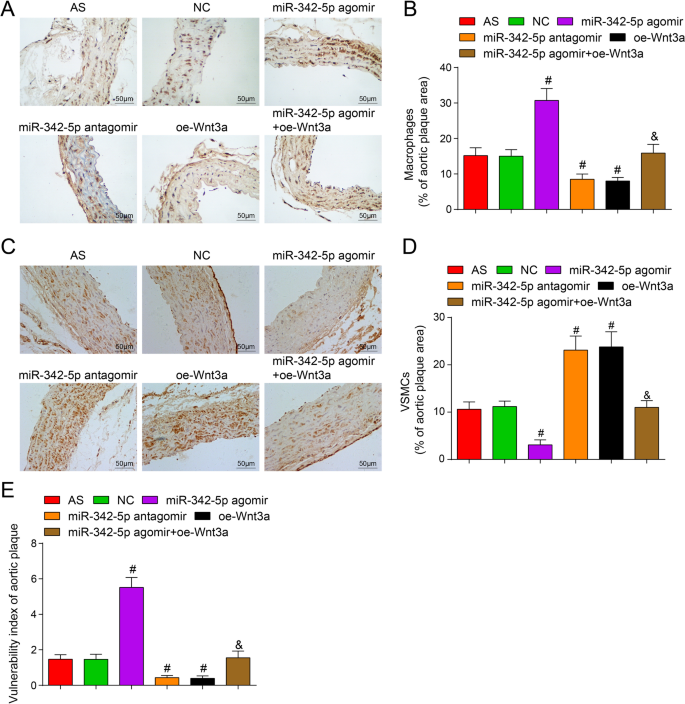
Auswirkungen einer hohen Expression von Wnt3a oder einer geringen Expression von miR-342-5p auf die Aortenplaque-Vulnerabilität von ApoE −/− Mäuse. A Immunhistochemische Färbung von MOMA-2 in jeder Mäusegruppe (Maßstab:50 μm). B Quantitative Analyse von Abbildung A. C Immunhistochemische Färbung von α-SMA in jeder Mäusegruppe (Maßstab:50 μm). D Quantitative Analyse der Figur C . E Vergleich des Plaque-Vulnerabilitätsindex in Aortengeweben von AS-Mäusen. n = 12. # P < 0,05 gegenüber der NC-Gruppe. &P < 0,05 gegenüber der miR-342-5p-Agomir-Gruppe. Die Messdaten wurden als Mittelwert ± Standardabweichung angegeben. Vergleiche zwischen mehreren Gruppen wurden durch Einweg-ANOVA bewertet, gefolgt von Tukeys Mehrfachvergleichstest. AS, Arteriosklerose; NC, Negativkontrolle
Auswirkungen einer hohen Expression von Wnt3a oder einer schlechten Expression von miR-342-5p auf die Aortenplaque-Vulnerabilität von ApoE −/− Mäuse
Der Plaque-Vulnerabilitätsindex wurde berechnet:(positiver Prozentsatz an Makrophagen + positiver Prozentsatz an Lipiden)/(positiver Prozentsatz an glatten Muskelzellen + positiver Prozentsatz an Kollagen). In Bezug auf die NC-Gruppe war der Plaque-Vulnerabilitätsindex in der miR-342-5p-Agomir-Gruppe erhöht (P < 0,05) und sank in der miR-342-5p-Antagomir-Gruppe und der oe-Wnt3a-Gruppe (beide P < 0,05). Im Vergleich zur miR-342-5p-Agomir-Gruppe war der Plaque-Vulnerabilitätsindex in der miR-342-5p-Agomir + oe-Wnt3a-Gruppe verringert (P < 0,05) (Abb. 5E). Kurz gesagt, miR-342-5p zielte auf die Regulierung der Wnt3a-Signalweg-vermittelten Anfälligkeit von Plaques in arteriellen Geweben von AS-Mäusen ab.
Auswirkungen einer geringen Expression von miR-342-5p oder einer Überexpression von Wnt3a auf die Angiogenese in Aortenplaque von ApoE −/− Mäuse
Antikörper gegen den Endothelzellmarker CD34 können die Blutgefäßdichte nachweisen [24]. Durch Immunhistochemie und Western Blot. Im Vergleich zur NC-Gruppe war die MVD in der miR-342-5p-Agomir-Gruppe erhöht und in der miR-342-5p-Antagomir-Gruppe und der oe-Wnt3a-Gruppe abgeschwächt (alle P < 0,05). Im Vergleich zur miR-342-5p-Agomir-Gruppe war die MVD in der miR-342-5p-Agomir + oe-Wnt3a-Gruppe verringert (P < 0,05) (Abb. 6A–C). Insgesamt beteiligte sich miR-342-5p, das den Wnt3a-Signalweg angreift und reguliert, direkt an der Regulierung der Neovaskularisationsdichte in Plaques von AS-Mäusen.
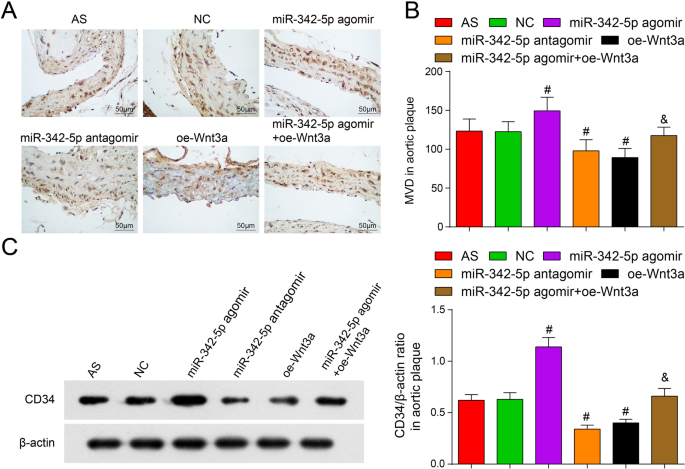
Auswirkungen einer geringen Expression von miR-342-5p oder einer Überexpression von Wnt3a auf MVD in Aortenplaque von ApoE −/− Mäuse. A Immunhistochemische Färbung von CD34 in jeder Gruppe von ApoE −/− Mäuse (Maßstab:50 μm). B Vergleich der MVD in Aortenplaque bei ApoE −/− Mäuse. C Vergleich der CD34-Proteinexpression in ApoE −/− Mäuse. n = 12. # P < 0,05 gegenüber der NC-Gruppe. &P < 0,05 gegenüber der miR-342-5p-Agomir-Gruppe. Die Messdaten wurden als Mittelwert ± Standardabweichung angegeben. Vergleiche zwischen mehreren Gruppen wurden durch Einweg-ANOVA bewertet, gefolgt von Tukeys Mehrfachvergleichstest. AS, Arteriosklerose; NC, Negativkontrolle
Diskussion
AS ist eine unvorhersehbare Krankheit, die Formen chronischer Entzündungen und Gefäßumbauten umfasst, und ist weltweit die Hauptursache für Mortalität und Morbidität [25]. In einer früheren Studie wurde diskutiert, dass miR-342-5p an der Regulierung des Fortschreitens von AS beteiligt ist [26]. Es wurde auch gespiegelt, dass der Wnt-Signalweg an der Erleichterung des Auftretens und der Entwicklung von diabetischer AS beteiligt ist [27]. Da die verwandten Mechanismen von miR-342-5p und Wnt3a bei AS noch erforscht werden müssen, sollte unsere Studie die Wirkung von miR-342-5p gezieltem Wnt3a auf die Bildung von anfälliger Plaque und die Angiogenese von AS untersuchen.
Unsere Studie ergab, dass in Aortengeweben von AS-Mäusen stark exprimiertes miR-342-5p und schwach exprimiertes Wnt3a gefunden wurden. Eine Studie hat gezeigt, dass miR-342-5p aus Makrophagen bei frühen atherosklerotischen Läsionen bei ApoE −/− . dramatisch erhöht ist Mäuse [13]. Eine andere Studie hat gezeigt, dass miR-342-5p bei Patienten mit Vorhofflimmern deutlich erhöht ist [28]. Es wurde berichtet, dass ein Wnt3a-Mangel die Selbsterneuerung von hämatopoetischen Stammzellen irreversibel schädigt und zu Defekten in der Vorläuferzelldifferenzierung führt [29]. Eine Studie hat gezeigt, dass eine Erschöpfung von Wnt3a zu einer gestörten Herzfunktion führt [30]. Es wurde gezeigt, dass die Wnt3a-Expression im Hippocampus von Alzheimer-Mäusen bemerkenswert vermindert ist [31]. Ein weiteres Ergebnis unserer Studie ist, dass Wnt3a direkt von miR-342-5p in AS-Mäusen angegriffen wurde. Es wurde berichtet, dass miR-342-5p auf die 3'-UTR von Wnt3a abzielen und seine Expression negativ regulieren kann [14].
Darüber hinaus hat unsere Studie ergeben, dass die TC-, TG-, LDL-C-, IL-5-, IL-12p70-, IFN-γ-, TNF-α- und MDA-Gehalte im Serum erhöht und der HDL-C-Gehalt und die SOD-Aktivität verringert waren. Darüber hinaus wurden Plaquefläche, Lipidgehalt, Kollagengehalt und MVD erhöht sowie die MOMA-2-Expression erhöht und die α-SMA-Expression bei AS-Mäusen verringert. IFN-γ ist ein lösliches Zytokin mit vielen Funktionen, einschließlich Antifibrose, Antiproliferation, Immunmodulation, Apoptose und antivirale Aktivitäten [32]. Es wurde gezeigt, dass die Behandlung mit Glutamin die SOD-Aktivität deutlich erhöht und den MDA-Gehalt reduziert sowie den Wnt3a-Proteinspiegel bei der Alzheimer-Krankheit erhöht [31]. Eine Studie hat ergeben, dass bei AS die Plasmaspiegel von TC, TG und LDL-C deutlich erhöht und HDL-C deutlich erniedrigt ist [33]. Eine Studie hat berichtet, dass eine Supplementation mit TEMPOL, die einen Wert bei der Unterdrückung von Stoffwechselstörungen und der Erhöhung der atherosklerotischen Plaquestabilität hat, den Kollagengehalt der Plaque erhöht und den Lipidgehalt reduziert [34]. Zhouet al. stellten fest, dass OPCRR-Behandlungen die Serumlipidprofile einschließlich TC, TG und LDL-C sowie HDL-C drastisch reduzieren und den MDA-Gehalt als Produkt der Lipidperoxidation senken und darüber hinaus die Serumspiegel von TNF-α in . senken AS [35]. Es wurde gezeigt, dass atherosklerotische Proben offensichtlich eine reduzierte Expression von α-SMA aufweisen [36]. Eine Studie hat gezeigt, dass eine erhöhte MVD in erkrankten Aorten und insbesondere in rupturierten atherosklerotischen Plaques gefunden wird [37]. Darüber hinaus zeigte unsere Studie, dass eine schlechte Expression von miR-342-5p und eine Überexpression von Wnt3a die Lipidspiegel, den Zytokingehalt, die oxidative Stressreaktion, die Plaquefläche und den Lipidgehalt sowie einen erhöhten Kollagengehalt, eine verminderte MOMA-2-Expression und eine Wiederherstellung von α -SMA-Expression in Aortengeweben bei AS-Mäusen. Es wurde bereits vorgeschlagen, dass miR-342-5p positiv mit LDL-C- und TNF-α-Serumspiegeln verbunden ist und eine inverse Korrelation mit HDL-C bei Patienten mit koronarer Herzkrankheit (KHK) aufweist [12]. Eine andere Studie hat bestätigt, dass die Erschöpfung von miR-342-5p AS hemmt [13]. Darüber hinaus hat ein Experiment gezeigt, dass ein niedriger Wnt1-Serumspiegel mit erhöhten TG- und LDL-C-Werten bei Patienten mit vorzeitiger KHK zusammenhängt [38]. Darüber hinaus hat eine Studie gezeigt, dass in den Curcumin-Gruppen bei Parkinson-Ratten hochreguliertes Wnt3a, ein erhöhter SOD-Gehalt und ein verringerter MDA-Gehalt gefunden werden [39].
Schlussfolgerung
Kurz gesagt, unsere Studie entdeckte zum ersten Mal den Mechanismus der miR-342-5p/Wnt3-Achse bei AS und zeigte, dass die Erschöpfung von miR-342-5p die Bildung von anfälliger Plaque und die Angiogenese bei AS-Mäusen durch die Wiederherstellung von Wnt3a reduzieren könnte ein potenzieller Kandidat für die Behandlung von AS (Zusatzakte 2:Abb. S2). miR-342-5p kann eine synergistische Wirkung mit anderen miRNAs bei atherosklerotischen Gefäßerkrankungen haben, aber aus Zeit- und Finanzgründen haben wir keine weiteren relevanten Diskussionen geführt, was auch eine Einschränkung dieser Studie darstellt.
Verfügbarkeit von Daten und Materialien
Die in der Studie präsentierten Originalbeiträge sind in den Artikel/Ergänzungsmaterial aufgenommen, und Rückfragen können an den entsprechenden Autor gerichtet werden.
Abkürzungen
- miR-342-5p:
-
MicroRNA-342-5p
- A:
-
Arteriosklerose
- α-SMA:
-
α-Glattmuskel-Aktin
- MVD:
-
Mikrogefäßdichte
- miRNA:
-
MicroRNA
- oe:
-
Überexpression
- NC:
-
Negativkontrolle
- PBS:
-
Phosphatgepufferte Kochsalzlösung
- TC:
-
Gesamtcholesterin
- TG:
-
Triglycerid
- LDL-C:
-
Lipoprotein-Cholesterin niedriger Dichte
- HDL-C:
-
Lipoprotein-Cholesterin hoher Dichte
- ELISA:
-
Enzyme-linked Immunosorbent Assay
- IL:
-
Interleukin
- TNF-α:
-
Tumornekrosefaktor alpha
- IFN:
-
Interferon
- MDA:
-
Malondialdeyde
- SOD:
-
Superoxiddismutase
- RT-qPCR:
-
Reverse Transkription quantitative Polymerase-Kettenreaktion
Nanomaterialien
- Charakterisierung von Frequenzabweichungen von Quarzkristallen:Frequenztoleranz, Frequenzstabilität und Alterung
- Die Zustandsüberwachung erhöht und erhält die Effizienz in der Papierproduktion
- Herstellung und Bildgebung von Cyclocarbon
- Graphen in Lautsprechern und Ohrhörern
- Herunterregulierung von microRNA-342-5p oder Hochregulierung von Wnt3a hemmt die Angiogenese und erhält die Stabilität der atherosklerotischen Plaque bei Arteriosklerose-Mäusen
- Experimentelle Forschung zur Stabilität und natürlichen Konvektion von TiO2-Wasser-Nanofluid in Gehäusen mit unterschiedlichen Rotationswinkeln
- Miniaturisierte dehnbare und hochfrequente lineare Superkondensatoren
- First-Principles-Studie zur Stabilität und dem STM-Image von Borophen
- Die potenzielle Leber-, Gehirn- und Embryotoxizität von Titandioxid-Nanopartikeln bei Mäusen
- Hydrothermale Synthese von In2O3-Nanopartikel-Hybrid-Zwillingen hexagonalen Scheiben-ZnO-Heterostrukturen für verbesserte photokatalytische Aktivitäten und Stabilität



