(La0.97RE0.01Yb0.02)2O2S-Nanophosphor, umgewandelt aus geschichtetem Hydroxylsulfat und Untersuchung der Aufkonversions-Photolumineszenz (RE=Ho, Er)
Zusammenfassung
Phasenrein (La0.97 .) RE0.01 Yb0,02 )2 O2 S upconversion (UC) Nanophosphore (durchschnittliche Kristallitgröße ~ 45 nm; RE=Ho, Er) wurden aus ihren hydrothermal kristallisierten geschichteten Hydroxylsulfat-Vorstufen in fließendem Wasserstoff bei 1200 °C für 1 h mit Wasserdampf als einzigem Abgas getempert. Unter 978-nm-Laseranregung (bis zu 2,0 W) ist der Ho 3+ -dotierter Phosphor wies grüne (mittel), rote (schwache) und nahe Infrarot (stark) Emissionen bei ~ 546 ( 5 .) auf F4 → 5 I8 ), 658 ( 5 F7 → 5 I8 ) und 763 nm ( 5 F4 → 5 I7 ). Die Er 3+ -dotierter UC-Phosphor zeigte hingegen schwaches Grün (~ 527/549 nm, 2 H11/2 , 4 S3/2 → 4 I15/2 ), schwaches Rot (~668/672 nm, 4 F9/2 → 4 I15/2 ) und starkes nahes Infrarot (~ 807/58 nm, 4 I9/2 → 4 I15/2 ) Lumineszenz, deren Emissionsfarbe im sichtbaren Bereich mit zunehmender Anregungsleistung von gelblich-grün [(0.36, 0.61)] nach grün [(0.32, 0.64)] driftete. Die Analyse der leistungsabhängigen UC-Lumineszenz ergab Drei- und Zwei-Photonen-Prozesse für RE=Ho bzw. Er, und die möglichen UC-Mechanismen wurden vorgeschlagen.
Hintergrund
Upconversion (UC)-Phosphor zieht aufgrund seiner einzigartigen Fähigkeit, längerwellige Strahlung in kürzerwellige Fluoreszenz umzuwandeln [1, 2] große Aufmerksamkeit auf sich und findet breite Anwendung in den Bereichen Festkörperlaser [3], Mehrfarbendisplays [ 4], Wirkstoffabgabe [5], fluoreszierende biologische Markierungen [6], Wellenlängenumwandler für Solarzellen [7] und so weiter. Ein UC-Leuchtstoff wird üblicherweise durch Dotieren eines Wirtsgitters mit einem Sensibilisator/Aktivator-Paar gebildet, wobei der Sensibilisator normalerweise Yb 3+ . ist und der Aktivator ist häufig Ho 3+ , Er 3+ , oder Tm 3+ . Dies liegt daran, dass Yb 3+ kann eine Nahinfrarot-Laseranregung mit 980 nm effizient absorbieren, und die drei Arten von Aktivatoren haben die leiterähnlichen Energieniveaus, die für die sequentielle Photonenabsorption und Energieübertragung vorteilhaft sind [8]. Die Grundlagen der UC-Lumineszenz und des Energietransfers bei der Lanthanoid-Hochkonversion finden sich in den Übersichtsartikeln von Auzel [9] und Dong et al. [10] bzw. Gai et al. [8] haben kürzlich die jüngsten Fortschritte bei Seltenerd-Mikro-/Nanokristallen für Abwärtskonversions- (DC) und UC-Zwecke zusammengestellt, einschließlich weichchemischer Synthese, Lumineszenzeigenschaften und biomedizinischer Anwendungen. Wanget al. [11] fassten andererseits in ihrem Übersichtsartikel ausführlich die Anwendung von Seltenerdionen-dotierten UC- und DC-Phosphoren in der optischen Thermometrie zusammen. Die Eigenschaft eines UC-Leuchtstoffs wird maßgeblich durch die Art des Wirtsgitters, die Sensibilisator/Aktivator-Kombination, die Dotierstoffkonzentration, die Partikel/Kristallit-Morphologie, die Kristallinität, die Anregungsleistung und den tatsächlichen Gitterplatz beeinflusst, an dem sich das Dotierstoff-Ion befindet [8,9,10 ,11,12,13]. Beispielsweise wurden zwei nicht-äquivalente Gd-aktivierte kristallographische Stellen in einem Er 3+ . identifiziert -dotiertes hexagonales Na1.5 Gd1,5 F6 Phosphor und durch zeitaufgelöste Spektroskopie wurde nachgewiesen, dass die beiden grünen Emissionen der 4 S3/2 Niveau von Er 3+ stammen separat von den kristallographischen Stellen von Gd1 (540 nm) und Na2/Gd2 (550–555 nm), während die rote 657-nm-Emission der 4 F9/2 stammt nur von der Na2/Gd2-Stelle [12]. Eine aktuelle Studie zum Roman Er 3+ -dotiertes transparentes Sr0.69 La0.31 F2.31 Glaskeramiken hingegen zeigten, dass die Spektrumsaufteilung, das thermische Quenching-Verhältnis, die Besetzungsstabilität und die Temperaturempfindlichkeit von den drei thermisch gekoppelten Energieniveaus (TCL) von 2 H11/2 / 4 S3/2 , 4 F9/2(1) / 4 F9/2(2) , und 4 I9/2(1) / 4 I9/2(2) sind von der Pumpleistung des 980-nm-Lasers abhängig, und es wurde eine neue Anpassungsmethode entwickelt, um den Zusammenhang zwischen Fluoreszenzintensitätsverhältnissen und Temperatur herzustellen [13]. Seltenerd(RE)-Halogenide (wie NaYF4 :Yb/Er) sind aufgrund ihrer geringen Phononenenergien (ℏω <400 cm −1 ). Eine andere Art von häufig untersuchten UC-Leuchtstoffen ist RE2 O3 (wie Y2 O3 :Yb/Er), deren relativ hohe Phononenenergie (ℏω ~ 600 cm −1 ; ~ 591 cm −1 für Y2 O3 und 612 cm −1 für Lu2 O3 ) [15] verringert jedoch die Effizienz der UC-Lumineszenz aufgrund der Photon-Phonon-Kopplung. Aus Sicht der Biokompatibilität haben Li et al. [16] synthetisiertes Yb 3+ - und Ho 3+ -kodotierte Fluorapatitkristalle (Nanostäbchen von 16 x 286 nm) über hydrothermale Reaktion und UC-Lumineszenz von Ho 3+ bei 543 und 654 nm wurde durch einen Zwei-Photonen-Prozess unter 980-nm-Laseranregung erreicht. Die Kristalle zeigten auch eine klare fluoreszierende Zellabbildung, nachdem die Oberflächen mit hydrophilem Dextran gepfropft wurden [16].
RE2 O2 S-Oxysulfid ist eine wichtige Familie von Verbindungen auf dem Gebiet der Leuchtstoffe und kann gegenüber Oxiden für Lumineszenzanwendungen vorteilhaft sein. Zum Beispiel das Auftreten von S 2− → Eu 3+ Ladungstransferübergang in Eu 3+ -aktivierte RE2 O2 S erweitert die effektive Anregungswellenlänge deutlich auf ~ 400 nm [17,18,19], was den Leuchtstoff als Rotkomponente in im nahen UV (365–410 nm) angeregten weißen LEDs nützlich macht, wie von Ye et al. [20]. Die ausgereifteste Technik zur Synthese von RE2 O2 S ist eine Festkörperreaktion, die die Vorteile einer hohen Ausbeute und Bequemlichkeit hat, aber hohe Reaktionstemperaturen, unkontrollierbare Produktmorphologie und insbesondere der Einsatz umweltschädlicher Schwefelquellen sind offensichtliche Mängel [21,22,23]. Schwefelung von RE2 O3 von H2 S oder CS2 Gas bei erhöhter Temperatur [24,25,26] ist eine weitere häufig verwendete Strategie zur Herstellung von RE2 O2 S. Da die Methodik zur kontrollierten Synthese von RE2 O3 ist reich und gut entwickelt, RE2 O2 S mit verschiedenen Partikelmorphologien wurde daher durch die Schwefelungsroute hergestellt, obwohl die komplizierten Verfahren für die industrielle Produktion weniger praktikabel sind. Andere Techniken für RE2 O2 Die S-Synthese kann Fällung [27], hydrothermale Reaktion [28], zweistufige Lösungs-Gel-Polymer-Thermolyse [29], Gelatine-gestützte Synthese [30], Gel-Thermolyse [31], solvothermale Druckentlastungssynthese [32] und . umfassen Verbrennung [33]. Die Beteiligung schädlicher Schwefelquellen oder -nebenprodukte (wie C2 .) S, H2 S und Thioharnstoff) ist jedoch immer noch schwer zu vermeiden. Das Auftreten von geschichtetem Seltenerdhydroxid vom Sulfattyp (RE2 (OH)4 SO4 ∙2H2 O, SO4 2− -LREH) im Jahr 2010 [34] bot eine einzigartige Chance, die oben genannten Probleme zu lösen, da diese Gruppe von Verbindungen genau das gleiche RE/S-Molverhältnis von RE2 . aufweist O2 S. Homogene Hydrolyse von RE2 (SO4 )3 ·8H2 O in Gegenwart von Na2 SO4 und Hexamethylentetramin (C6 H12 N4 ) ist die klassische Technik zur Herstellung von SO4 2− -LREH, ist jedoch in der Lanthanoidenfamilie auf RE=Pr-Tb beschränkt [34]. Wir haben die Gruppe der Verbindungen auf RE=La–Dy erweitert, indem wir wässrige Lösungen von RE(NO3 )3 ·n H2 O und (NH4 )2 SO4 unter hydrothermalen Bedingungen [17,18,19] und zeigte anschließend, dass RE2 O2 S kann leicht durch Thermolyse von SO4 . hergestellt werden 2− -LREH in reduzierender Atmosphäre [17,18,19]. RE2 O2 Vor kurzem wurde festgestellt, dass S eine relativ niedrige Phononenenergie hat (ℏω ~ 500 cm −1 ) [1], gute chemische Stabilität und besonders hohe UC-Effizienz vergleichbar mit Halogeniden [35, 36], aber die Untersuchung dieser Art vielversprechender UC-Leuchtstoffe ist noch lange nicht ausreichend [8, 10, 11, 37, 38]. La 3+ hat keine freien 4f suborbital und ist optisch inert, und daher sind seine Verbindungen geeignete Wirtsgitter für die Lumineszenz. So synthetisierten wir in dieser Arbeit La2 O2 S:Yb/RE UC-Leuchtstoffe (RE=Ho, Er) durch Tempern des hydrothermal kristallisierten SO4 2− -LREH in fließendem H2 , und die lumineszierenden Eigenschaften und UC-Prozesse wurden detailliert ausgearbeitet.
Methoden
Die Ausgangsstoffe von RE(NO3 )3 ·6H2 O (RE=La, Ho, Er und Yb;> 99,99 % rein), (NH4 )2 SO4 (> 99,5% rein) und NH3 ·H2 O-Lösung (28%, ultrahohe Reinheit) wurden von Kanto Chemical Co., Inc. (Tokyo, Japan) bezogen und wie erhalten verwendet. Yb 3+ /Ho 3+ - und Yb 3+ /Er 3+ -dotiertes La2 (OH)4 SO4 ·2H2 O wurde separat über eine hydrothermale Reaktion synthetisiert. Der Dotierstoffgehalt beträgt 2 Atom-% für Yb 3+ und 1 Atom-% für beide Ho 3+ und Er 3+ laut Literatur [39]. In einer typischen Synthese [17] werden 6 mmol (NH4 )2 SO4 wurde in 60 ml einer wässrigen Lösung der Seltenen Erden gelöst (0,1 mol/L für Gesamt-RE 3+ ), gefolgt von tropfenweiser Zugabe von NH3 ·H2 0 bis pH =9. Nach kontinuierlichem Rühren für 15 min wurde die resultierende Suspension in einen mit Teflon ausgekleideten Autoklaven mit 100 ml Fassungsvermögen für 24 h hydrothermale Kristallisation in einem auf 100 °C vorgeheizten Elektroofen überführt. Das resultierende Produkt wurde durch Zentrifugation gesammelt, dreimal mit filtriertem Wasser und einmal mit Ethanol gewaschen und schließlich 24 h bei 70 °C an der Luft getrocknet. Die La2 O2 S:Yb/RE UC-Leuchtstoffe wurden dann von ihrem SO4 . getempert 2− -LREH-Vorläufer in fließendem H2 (200 ml/min) bei 1200 °C für 1 h, mit einer Heizrate von 5 °C/min in der Rampenphase.
Die Phasenidentifikation wurde mittels Röntgendiffraktometrie (XRD; Modell RINT2200, Rigaku, Tokio, Japan) unter 40 kV/40 mA unter Verwendung von nickelgefiltertem Cu-K . durchgeführt α-Strahlung (λ =0,15406 nm) und einer Scangeschwindigkeit von 1°/min. Strukturparameter der Produkte wurden mit der Software TOPAS aus den XRD-Daten abgeleitet [40]. Die Teilchenmorphologie wurde durch Feldemissions-Rasterelektronenmikroskopie (FE-SEM; Modell S-5000, Hitachi, Tokio) bei einer Beschleunigungsspannung von 10 kV beobachtet. UC-Lumineszenzspektren wurden bei Raumtemperatur unter Verwendung eines FP-6500-Fluorospektrophotometers (JASCO, Tokio) unter 978-nm-Nah-Infrarot-Laseranregung der Leuchtstoffe mit einer Laserdiode mit kontinuierlicher Wellenlänge (CW) (Modell KS3-12322-105, BWT Beijing .) erhalten Ltd., Peking, China). Das Signal/Rausch-Verhältnis (S/N) des Spektrometers beträgt 200, und die Empfindlichkeit wurde aufgrund der starken UC-Lumineszenz der Leuchtstoffe niedrig eingestellt. Den Versuchsaufbau finden Sie in Zusatzdatei 1:Abbildung S1.
Ergebnisse und Diskussion
Abbildung 1 zeigt XRD-Muster der hydrothermalen Produkte, wobei zu sehen ist, dass in jedem Fall alle Beugungspeaks mit der Schichtverbindung von La2 . gut indiziert werden können (OH)4 SO4 ·2H2 O [17, 18]. In einer wässrigen Lösung mit SO4 2− , würden die Kationen der Seltenen Erden (RE) hydratisiert und teilweise hydrolysiert, um die komplexen Ionen von [RE(OH) x . zu bilden (H2 O) y (SO4 ) z ] 3-x -2z [17,18,19]. Entweder eine höhere Temperatur oder der pH-Wert der Lösung fördert RE 3+ Hydrolyse, was zu mehr OH − . führt während weniger SO4 2− (kleinerer SO4 2− /OH − Molverhältnis) im Komplexion. Unter den optimierten hydrothermalen Bedingungen von 100 °C und pH =9 [17,18,19] kann das Komplexion ein geeignetes SO4 . aufweisen 2− /OH − Molverhältnis und damit das angestrebte SO4 2− -LREH-Verbindung kann durch Kondensationsreaktionen kristallisiert werden. Die Strukturparameter der hydrothermalen Produkte sind in Tabelle 1 zusammengefasst. Es ist klar, dass (La0.97 Ho0.01 Yb0,02 )2 (OH)4 SO4 ·2H2 O hat größere Gitterkonstanten (a , b , c ) und Zellvolumen (V ) als (La0.97 Er0,01 Yb0,02 )2 (OH)4 SO4 ·2H2 O. Dies ist verständlich, da Ho 3+ (1.072 Å für CN =9) ist größer als Er 3+ (1,062 Å für CN =9). Beide Produkte haben kleinere Zellkonstanten und Zellvolumen als das undotierte La2 (OH)4 SO4 ·2H2 O (SO4 2− -LLaH), entsprechend der Tatsache, dass La 3+ ist der größte (1.216 Å für CN =9) unter den vier Arten von RE-Ionen. Die unterschiedlichen Zellparameter lieferten direkte Hinweise auf die Bildung fester Lösungen.
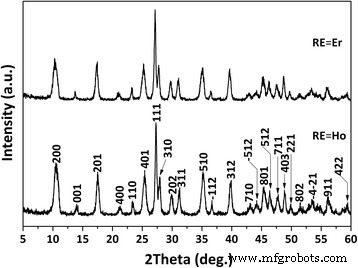
XRD-Muster des (La0.97 RE0.01 Yb0,02 )2 (OH)4 SO4 ·2H2 O-Schichtverbindungen, erhalten durch hydrothermale Reaktion bei 100 °C und pH =9 für 24 h
Abbildung 2 zeigt XRD-Muster der Produkte, die aus ihrem SO4 . getempert wurden 2− -LREH-Vorstufen bei 1200 °C für 1 h in fließendem H2 . Die Beugungspeaks können mit dem hexagonal strukturierten La2 . vollständig indiziert werden O2 S jeweils (Leerzeichengruppe:P- 3m 1; JCPDS-Karte Nr. 00-075-1930). SO4 2− -LLaH würde sich in La2 . zersetzen O2 SO4 bis 1200 °C in Luft durch die Reaktionen von La2 (OH)4 SO4 ·2H2 O → La2 (OH)4 SO4 + 2H2 O (Dehydratation) und La2 (OH)4 SO4 → La2 O2 SO4 + 2H2 O (Dehydroxylierung) [17]. In einem H2 Atmosphäre, die S 6+ in SO4 2− würde auf S 2− . reduziert nach der Reaktion von La2 O2 SO4 + 4H2 → La2 O2 S + 4H2 O und somit La2 O2 S kann mit Wasserdampf als einzigem Nebenprodukt entstehen [17]. Die Gitterparameter und das Zellvolumen von (La0.97 RE0.01 Yb0,02 )2 O2 S sind in Tabelle 2 zusammen mit denen von La2 . gezeigt O2 S [17]. Die abnehmende Zelldimension zu einem kleineren RE 3+ zeigt die erfolgreiche Bildung einer festen Lösung an.
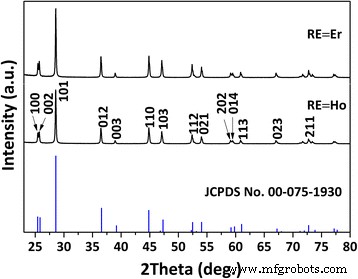
XRD-Muster des (La0.97 RE0.01 Yb0,02 )2 O2 S upconversion-Leuchtstoffe, die aus ihren geschichteten Vorstufen in fließendem H2 . kalziniert wurden (200 ml/min) bei 1200 °C für 1 h. Die Standardbeugungen von La2 O2 S sind als Vergleichsbalken enthalten
Abbildung 3 zeigt die Partikelmorphologie der geschichteten Vorstufen und der resultierenden UC-Leuchtstoffe. Es ist ersichtlich, dass die SO4 2− -LREH kristallisierte als Nanoplättchen von ~ 150–550 nm lateraler Größe und ~ 20–30 nm Dicke. Die Nanoplättchen zerfielen beim Kalzinieren bei 1200 °C erheblich, um abgerundete Partikel zu ergeben. Die durchschnittliche Kristallitgröße wurde mit der Scherrer-Gleichung zu ~ 45 nm für die UC-Leuchtstoffe bestimmt.

FE-REM-Partikelmorphologien des (La0.97 Ho0.01 Yb0,02 )2 (OH)4 SO4 ·2H2 O (a ) und (La0.97 Er0,01 Yb0,02 )2 (OH)4 SO4 ·2H2 O (b ) geschichtete Vorstufen und die (La0.97 Ho0.01 Yb0,02 )2 O2 S (c ) und (La0.97 Er0,01 Yb0,02 )2 O2 S (d ) Upconversion-Phosphore
Abbildung 4a zeigt UC-Lumineszenzspektren von (La0.97 Ho0.01 Yb0,02 )2 O2 S-Phosphor unter 978-nm-Laseranregung. Die Emissionen bei ~ 546, 658 und 763 nm werden dem 5 . zugeschrieben F4 → 5 I8 , 5 F7 → 5 I8 , und 5 F4 → 5 I7 Übergänge von Ho 3+ , bzw. [36], wobei die 763-nm-NIR-Emission vorherrscht. Die sensibilisierende Wirkung von Yb 3+ ist signifikant, und durch Codotierung von 2 Atom-% Yb 3+ . wurden ~ 15 bzw. 20-mal stärkere grüne (546 nm) bzw. NIR-Emissionen (763 nm, nicht empfindlich für das menschliche Auge) erzeugt (Zusatzdatei 1:Abbildung S2a). Unter 50-mW-Laserpumpen wurde eine lebhafte und starke grüne Emission für die (La0.97 Ho0.01 Yb0,02 )2 O2 S-Phosphor mit bloßem Auge, wie im Einschub in Abb. 4a gezeigt. Trotz der Anregungsleistung sind die aus den Emissionsspektren berechneten CIE-Farbkoordinaten im sichtbaren Lichtbereich (400–700 nm) stabil bei etwa (0,30, 0,66), typisch für eine lebendige grüne Farbe (Zusatzdatei 1:Tabelle S1 und Abbildung S3).
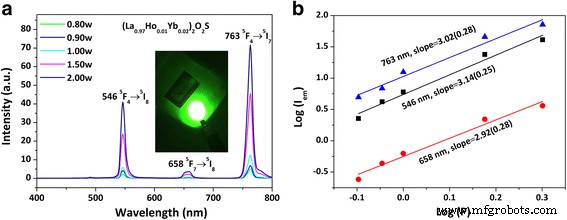
Upconversion-Lumineszenzspektren (a ) und die Beziehung zwischen log(I em ) und log(P ) (b ) für (La0.97 .) Ho0.01 Yb0,02 )2 O2 S Phosphor, wobei I em und P sind die Emissionsintensität bzw. die Anregungsleistung (in Watt). Der Einsatz in a ist ein Foto, das das Auftreten einer starken UC-Emission unter 50 mW einer 978-nm-Laseranregung zeigt
Im Allgemeinen kann die Anzahl der Photonen, die erforderlich sind, um den oberen emittierenden Zustand unter ungesättigten Bedingungen zu besetzen, aus der Beziehung I em ∝P n [41], wobei ich ist die Lumineszenzintensität, P die Pumpleistung und n die Anzahl der Laserphotonen. Abbildung 4b zeigt das Protokoll(I em )-log(P ) Auftragung der obigen Beziehung, aus der die n der Wert wurde aus der Steigung der linearen Anpassung zu ~3,02, 3,14 und 2,92 (ungefähr 3) für die UC-Emissionen mit einem Spitzenwert von ~546, 658 bzw. 763 nm bestimmt. Die Ergebnisse legen daher nahe, dass ein Drei-Photonen-Prozess beteiligt war, um die beobachtete UC-Lumineszenz zu erzeugen.
Im Prinzip können drei grundlegende Populationsmechanismen, nämlich Absorption im angeregten Zustand (ESA), Energietransfer (ET) und Photonenlawine, an einem UC-Prozess beteiligt sein [8,9,10]. Da im Bereich dieser Studie keine Leistungsschwelle beobachtet wurde, kann der Photonenlawinenmechanismus vernachlässigt werden. Das Energiediagramm von Yb 3+ /Ho 3+ in La2 O2 S wurde selten gemeldet und steht uns zum Vergleich nicht zur Verfügung. Nichtsdestotrotz wurde in früheren Arbeiten zu Yb 3+ . eine UC-Lumineszenz mit drei Phononen beobachtet /Ho 3+ -kodotierte andere Materialsysteme [42, 43]. Daher sind das Energiediagramm und der UC-Prozess von (La0.97 Ho0.01 Yb0,02 )2 O2 S wurden in Fig. 5 unter Bezugnahme auf diese früheren Studien konstruiert und sind im Folgenden detailliert beschrieben:(1) Anregung von Yb 3+ durch Laserphotonen [ESA; 2 F7/2 (Yb 3+ ) + hν (978 nm) → 2 F5/2 (Yb 3+ )]; (2) Bevölkerung der 5 Ich6 Energieniveau von Ho 3+ nach Yb 3+ Absorption des ersten Laserphotons und Übertragung von Energie auf Ho 3+ [ET1; 2 F5/2 (Yb 3+ ) + 5 I8 (Ho 3+ ) → 2 F7/2 (Yb 3+ ) + 5 Ich6 (Ho 3+ )]; (3) strahlungsfreie (NR) Relaxation auf die 5 I7 Niveau von Ho 3+ [NR; 5 Ich6 (Ho 3+ ) ~ 5 I7 (Ho 3+ )]; (4) Anregung von Ho 3+ von den 5 I7 bis 5 F5 Niveau nach Yb 3+ Absorbieren des zweiten Laserphotons und Übertragen von Energie auf Ho 3+ [ET2; 2 F5/2 (Yb 3+ ) + 5 I7 (Ho 3+ ) → 2 F7/2 (Yb 3+ ) + 5 F5 (Ho 3+ )]; (5) NR-Entspannung auf die 5 Ich5 Niveau von Ho 3+ [ 5 F5 (Ho 3+ ) ~ 5 Ich5 (Ho 3+ )]; (6) Anregung von Ho 3+ von den 5 Ich5 bis 5 F4 / 5 S2 Niveau nach Yb 3+ Absorbieren des dritten Laserphotons und Übertragen von Energie auf Ho 3+ [ET3; 2 F5/2 (Yb 3+ ) + 5 Ich5 (Ho 3+ ) → 2 F7/2 (Yb 3+ ) + 5 F4 / 5 S2 (Ho 3+ )]; und (7) Rücksprung der angeregten Elektronen von den besetzten 5 F4 / 5 S2 Level auf die 5 I8 Grundzustand zur Erzeugung der grünen Emission (~546 nm; 5 F4 , 5 S2 → 5 I8 ). Die Elektronen können sich auch auf die 5 . entspannen F5 und 5 Ich4 über NR-Prozesse, von denen das Rot (~658 nm; 5 F5 → 5 I8 ) und nahes Infrarot (~763 nm; 5 Ich4 → 5 I8 ) Emissionen resultierten. Die starke Nahinfrarot-UC-Emission bei ~763 nm kann darauf hindeuten, dass die NR-Relaxation auf 5 I8 Energieniveau ist signifikant.
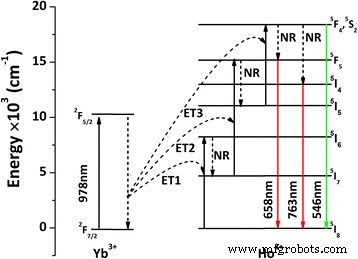
Eine schematische Darstellung der Energieniveaus und UC-Prozesse für die (La0.97 Ho0.01 Yb0,02 )2 O2 S-Phosphor
Die 2 F5/2 → 2 F7/2 Emissionsübergang von Yb 3+ und die 4 I15/2 → 4 I11/2 Anregungsübergang von Er 3+ haben gut passende Energien, was Yb 3+ . macht /Er 3+ das am häufigsten untersuchte Aktivator/Sensibilisator-Paar für UC-Lumineszenz in verschiedenen Arten von Wirtsgittern [8,9,10,11,12,13]. Ähnlich wie Ho 3+ , die UC-Emission von Er 3+ wurde auch durch Yb 3+ . dramatisch verbessert Kodoping (Zusatzdatei 1:Abbildung S2b). Nehmen wir zum Beispiel die grüne Emission von 527 nm, 2 Atom-% von Yb 3+ verbessert die Er 3+ Lumineszenz um einen Faktor von ~ 14. Unter 978-nm-Laseranregung beträgt die (La0.97 Er0,01 Yb0,02 )2 O2 S UC Phosphor weist Emissionsbanden im grünen (~ 527 und 549 nm), roten (~ 668 und 672 nm) und nahen Infrarot (~ 807 und 858 nm) Bereich auf (Abb. 6a), die von den 2 H11/2 / 4 S3/2 → 4 I15/2 , 4 F9/2 → 4 I15/2 , und 4 I9/2 → 4 I15/2 Übergänge von Er 3+ , bzw. [32]. Die für die UC-Lumineszenz bestimmten Farbkoordinaten im sichtbaren Lichtbereich (400–700 nm) drifteten im CIE-Farbdiagramm mit zunehmendem vom gelbgrünen [(0.36, 0.61)] zum grünen [(0.32, 0.64)]-Bereich Erregerleistung von 0,7 bis 2,0 W (Zusatzdatei 1:Abbildung S3b und Tabelle S2). Der Farbwechsel stimmt auch gut mit dem allmählich größeren Intensitätsverhältnis der grünen zu roten Emissionen überein (I 549 /Ich 668 und ich 527 /Ich 668 , Zusatzdatei 1:Tabelle S3) unter einer höheren Erregerleistung. Anregungsleistungsabhängige Emissions-Farbabstimmung des Yb 3+ /Er 3+ Paar wurde zuvor in Y2 . beobachtet O2 S [44]. Die Anzahl der Pumpphotonen, die erforderlich sind, um die emittierenden Zustände zu bevölkern, wurde aus der Steigung des log(I em )-log(P )-Diagramm (Abb. 6b) und die drei Emissionsgruppen hatten ähnliche n Werte von ~ 2. Dies deutet darauf hin, dass ein Zwei-Phonon-Prozess größtenteils für die beobachtete UC-Lumineszenz verantwortlich ist.
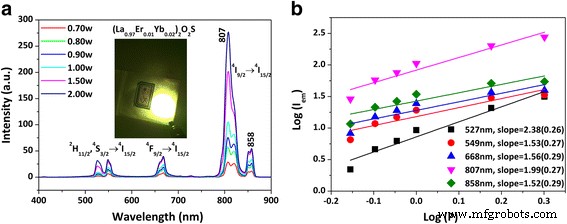
Upconversion-Lumineszenzspektren (a ) und die Beziehung zwischen log(I em ) und log(P ) (b ) für (La0.97 .) Er0,01 Yb0,02 )2 O2 S Phosphor, wobei I em und P sind die Emissionsintensität bzw. die Anregungsleistung (in Watt). Der Einsatz in a ist ein Foto, das die starke UC-Emission von (La0.97 Er0,01 Yb0,02 )2 O2 S unter 50 mW einer 978-nm-Laseranregung
Das Energiediagramm und der Photonenprozess, der zur UC-Lumineszenz von (La0.97 .) führt Er0,01 Yb0,02 )2 O2 S sind in Abb. 7 schematisch dargestellt. Absorption im angeregten Zustand und Yb 3+ → Er 3+ Energietransferanregungen sind hauptsächlich am UC-Mechanismus beteiligt, wobei letzterer dominant ist [8,9,10,11,12,13,14, 39, 43]. Bei Anregung mit einem 978-nm-Laser wird die 2 F7/2 Grundzustandselektronen von Yb 3+ werden auf die 2 gepumpt F5/2 angeregter Zustand (ESA). Seit den 2 F5/2 Niveau von Yb 3+ und die 4 I11/2 Niveau von Er 3+ passen gut zueinander, Energietransfer von Yb 3+ bis Er 3+ ohne weiteres erfolgt. Die Er 3+ Elektronen können somit von den 4 I15/2 Grundzustand zu 4 I11/2 entspricht der von Yb 3+ . übertragenen Energie (ein Photon, ET1). Der Absorptionsquerschnitt von Er 3+ ist kleiner als Yb 3+ bei ~ 980 nm [42, 45], daher dominiert der Energietransfer (ET) die reale Anregung von Er 3+ . Die Anregungsenergie am 4 I11/2 Pegel kann sich strahlungslos (NR) auf 4 entspannen I13/2 Ebene, von der aus die Elektronen zum 4 . angeregt werden können F7/2 Zustand durch ET eines zweiten Laserphotons (ET2). Nach NR-Prozessen können dann die drei Emissionsgruppen (Abb. 6a) über die in Abb. 7 gezeigten elektronischen Übergänge erzeugt werden. Die Photonenreaktionen des gesamten UC-Prozesses lassen sich wie folgt darstellen:(1) 2 F7/2 (Yb 3+ ) + hν (978 nm) → 2 F5/2 (Yb 3+ ) und 4 I15/2 (Er 3+ ) + h ν (978 nm) → 4 I11/2 (Er 3+ ); (2) 2 F5/2 (Yb 3+ ) + 4 I15/2 (Er 3+ ) → 2 F7/2 (Yb 3+ ) + 4 I11/2 (Er 3+ ); (3) 4 I11/2 (Er 3+ ) ~ 4 I13/2 (Er 3+ ); (4) 2 F5/2 (Yb 3+ ) + 4 I13/2 (Er 3+ ) → 2 F7/2 (Yb 3+ ) + 4 F7/2 (Er 3+ ); (5) 4 F7/2 (Er 3+ ) ~ 2 H11/2 / 4 S3/2 (Er 3+ ), 4 F9/2 (Er 3+ ) und 4 I9/2 (Er 3+ ); und (6) 2 H11/2 / 4 S3/2 (Er 3+ ) → 4 I15/2 (Er 3+ ) + hν (~527 und 549 nm), 4 F9/2 (Er 3+ ) → 4 I15/2 (Er 3+ ) + hν (~668 und 672 nm) und 4 I9/2 (Er 3+ ) → 4 I15/2 (Er 3+ ) + hν (~807 und 858 nm). Die oben erwähnte Änderung der Emissionsfarbe könnte auf eine effizientere Population der 4 . hindeuten F7/2 (Er 3+ ) Energieniveau bei einer höheren Anregungsleistung und die 4 F7/2 (Er 3+ ) ~ 2 H11/2 / 4 S3/2 (Er 3+ ) NR-Prozess wird sukzessive stärker als 4 F7/2 (Er 3+ ) ~ 4 F9/2 (Er 3+ ).
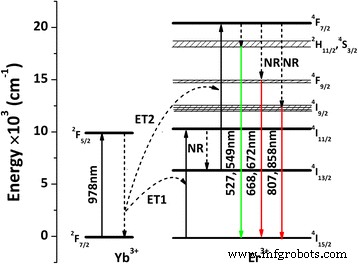
Eine schematische Darstellung der Energieniveaus und UC-Prozesse für (La0.97 Er0,01 Yb0,02 )2 O2 S-Phosphor
Schlussfolgerungen
(La0.97 RE0.01 Yb0,02 )2 O2 S Upconversion (UC) Nanophosphore (RE=Ho, Er) wurden erfolgreich durch thermische Zersetzung ihrer geschichteten Hydroxysulfat-Vorstufen in fließendem H2 . hergestellt bei 1200 °C, mit Wasserdampf als einzigem Abgas. Die Vorstufen kristallisierten als Nanoplättchen mit lateralen Größen von ~150–550 nm und Dicken von ~20–30 nm, die bei thermischer Zersetzung in abgerundete Nanopartikel (durchschnittliche Kristallitgröße:~45 nm) zerfielen. Die Oxysulfid-Leuchtstoffe zeigen eine starke UC-Lumineszenz unter 978-nm-Laseranregung durch einen Drei-Photonen-Prozess für Ho 3+ und ein Zwei-Photonen-Prozess für Er 3+ . Für die UC-Lumineszenz im sichtbaren Bereich (400–700 nm) sind die Farbkoordinaten von (La0.97 Ho0.01 Yb0,02 )2 O2 S sind stabil bei etwa (0,30, 0,66), während diejenigen von (La0,97 Er0,01 Yb0,02 )2 O2 S änderte sich von ungefähr (0,36, 0,61) auf (0,32, 0,64) zusammen mit einer Erhöhung der Anregungsleistung von 0,7 auf 2 W.
Nanomaterialien
- Abstimmung der tribologischen Leistung von geschichteten Zirkoniumphosphat-Nanoplättchen in Öl durch Oberflächen- und Zwischenschichtmodifikationen
- Herstellung von Palladium(II)-ionengeprägten polymeren Nanokügelchen und deren Entfernung von Palladium(II) aus wässriger Lösung
- Synthese und Charakterisierung von modifiziertem BiOCl und ihre Anwendung bei der Adsorption von Farbstoffen niedriger Konzentration aus wässriger Lösung
- Temperaturabhängigkeit von Raman-aktiven E2g-Phononen in der Ebene in geschichteten Graphen- und h-BN-Flocken
- Platycodon-Saponine aus Platycodi Radix (Platycodon grandiflorum) für die grüne Synthese von Gold- und Silber-Nanopartikeln
- Evolution von Photolumineszenz, Raman und Struktur von CH3NH3PbI3-Perowskit-Mikrodrähten unter Feuchtigkeitsbelastung
- Multiband- und Breitband-Absorptionsverbesserung von Monolayer-Graphen bei optischen Frequenzen durch multiple magnetische Dipolresonanzen in Metamaterialien
- Hochaktive und stabile Fe-N-C-Sauerstoffreduktions-Elektrokatalysatoren aus Elektrospinnen und In-situ-Pyrolyse
- Synthese und Untersuchung von CuGeO3-Nanodrähten als Anodenmaterialien für fortschrittliche Natrium-Ionen-Batterien
- Selbst gesätes MOCVD-Wachstum und dramatisch verstärkte Photolumineszenz von InGaAs/InP-Kern-Schale-Nanodrähten



