Eine vergleichende In-vivo-Untersuchung biosynthetisierter Kupfer- und Zinkoxid-Nanopartikel durch intraperitoneale und intravenöse Verabreichungswege bei Ratten
Zusammenfassung
Gegenwärtig werden antimikrobielle Eigenschaften von Kupfer- (Cu) und Zinkoxid (ZnO)-Nanopartikeln (NPs) in großem Umfang verwendet, um das Wachstum pathogener Mikroben zu bekämpfen. CuNPs und ZnONPs werden immer wieder in Kosmetika, Medizin und Lebensmittelzusatzstoffen verwendet, und ihr Potenzial für toxische Auswirkungen auf Mensch und Ökosystem ist von großer Bedeutung. In dieser Studie wurden der Verbleib und die Toxizität von biosynthetisiertem Kupfer (Bio-CuNPs) und Zinkoxid (Bio-ZnONPs) im Bereich von 16 bis 96 nm bei männlichen Wistar-Ratten untersucht. In-vivo-Expositionen der beiden Nanopartikel werden durch zwei verschiedene Verabreichungswege erreicht, nämlich intraperitoneale (i/p) und intravenöse (i/v) Injektionen. Die drei verschiedenen Konzentrationen, Konzentration ohne beobachtbare Nebenwirkungen (NOAEC), Hemmkonzentration (IC50 ) und die letale Gesamtkonzentration (TLC) wurden im Dosisbereich von 6,1 bis 19,82 µg/kg und 11,14 bis 30,3 µg/kg für Bio-CuNPs bzw 14. und 28. Beobachtungstag. Diese Dosisbereiche wurden auf der Grundlage einer früheren Studie zur antibakteriellen Dosis bei multiresistenten pathogenen Bakterien berücksichtigt. In dieser Studie untersuchten wir die toxische Wirkung von Bio-CuNPs und Bio-ZnONPs auf Tierverhalten, Tiermasse, hämatologische Indizes, Organindizes und die Histopathologie von Leber, Milz, Niere und Gehirnorganen. Wir fanden, dass die i/v- und i/p-Verabreichung von Bio-ZnONPs in drei verschiedenen Dosierungen keine Mortalität verursachte und das Körpergewicht bis zur zweiten Verabreichungswoche im Vergleich zur Vehikel-Kontrollgruppe leicht reduziert war. In den Dosisbereichen von 11–16 μg/kg (i/v) und 24–30 μg/kg (i/p) wurden keine signifikanten Veränderungen des Serumkreatininspiegels sowie der Serum-ALT-, Serum-AST-Spiegel und ALP . beobachtet Werte, die 40,7 mg/dl, 37,9 I.E./l und 82,4 I.E./l im Normalbereich im Vergleich zur Vehikelkontrolle am 14. und 28. Beobachtungstag betrugen. Diese Befunde werden durch Leber-, Nieren- und Milzindizes und histopathologische Studien bestätigt. Darüber hinaus traten Leber- und Nierenschäden auf, wenn die Konzentrationen von Bio-CuNPs 9,5 μg/kg betrugen (IC50 ) und 11,7 μg/kg (DC) für den i/v-Verabreichungsweg. In ähnlicher Weise wurde auch ein Anstieg von Serum-ALT (67,7 mg/dl), AST-Spiegel (70 IE/l) und ALP (128 IE/l) beobachtet. Und das Körpergewicht war nach dem 14. Tag signifikant niedriger als in der Kontrollgruppe, und es wurden statistisch signifikante Unterschiede auf diesem Weg beobachtet; interessanterweise ist die Toxizität von Bio-CuNPs im Serum verlängert (bis zum 28. Tag). Die Wirkung von Bio-CuNPs über die i/p-Route war im Vergleich zur Kontrolle beträchtlich gering. Die Ergebnisse der vorliegenden Studie zeigten, dass Bio-ZnONPs im Vergleich zu Bio-CuNPs keinen Einfluss auf die Biomarker der Nieren- und Leberfunktion (sowohl i/v als auch i/p) haben.
Wie in der grafischen Zusammenfassung (Abb. 1) gezeigt, ist es unser Ziel, die Toxizität von Bio-CuNPs und Bio-ZnONPs durch ein In-vivo-Protokoll zu bewerten. Laut Kahru und Dubourguier Reviews wurden AgNPs, CuNPs und ZnONPs in der Vergangenheit als Biozide verwendet, um das Wachstum von Mikroorganismen und Algen zu verhindern (Kahru und Dubourguier 2010). Daher sollten Nanomaterialien wie Pestizide auf ihre toxische Reaktion auf Nichtzielarten, einschließlich Menschen und Tiere, überwacht werden. Um besser zu verstehen, ob die unbeabsichtigte Freisetzung metallhaltiger NP eine Gefahr für Nichtzielarten darstellen kann, ist die Bewertung der toxischen Wirkung unabdingbar in die Umwelt abgeben.
Hintergrund
Bestimmte Metalle werden für die normalen physiologischen Funktionen in lebenden Organismen benötigt. Seit dem letzten Jahrzehnt hat die Verwendung metallbasierter NPs in biomedizinischen Anwendungen zugenommen, die exponentielle Verwendung von NPs warnt vor Sicherheitsbedenken, um NP-induzierte nachteilige Auswirkungen auf das lebende System zu reduzieren und/oder zu verhindern [1]. Unter den Nanopartikeln werden Cu und ZnO im Allgemeinen in Nahrungsergänzungsmitteln und im menschlichen Körper gefunden [2, 3]. Einzigartige physikalisch-chemische Eigenschaften von Cu und ZnONPs erreichen funktionelle Anwendungen in physiologischen Stoffwechselprozessen und steigern so ihren kommerziellen Wert in der Industrie [4,5,6]. Bei einer übermäßigen Aufnahme von Cu und ZnONPs wurden jedoch Nebenwirkungen wie Hämolyse, Magen-Darm-Beschwerden sowie Leber- und Nierenschäden beobachtet [7].
Insbesondere erfolgt die Aufnahme von CuNPs leicht nach oraler Aufnahme, Inhalation und dermaler Exposition [8, 9], signifikant über den Magen-Darm-Trakt [8, 10]. CuNPs zielen auf Schleimhautzellen und bleiben im Inneren durch Bindung mit Metallothionein oder Glutathion [11]. Es wird hauptsächlich in Leber, Gehirn, Herz, Niere und Muskulatur gespeichert. Es wurde berichtet, dass 98% von Cu an Ceruloplasmin binden, ein Serumprotein, das zu zellulärer Toxizität führt. [12, 13].Cu ist ein katalytischer Induktor von Superoxidradikalen, Hydroxylradikalen und Wasserstoffperoxid über die Haber-Weiss-Reaktion [14], höhere Konzentrationen von Cu können oxidativen Stress verursachen.
Basierend auf dem Ausmaß der Löslichkeit wurden ZnONPs als separate Gruppe von NPs innerhalb der Metalloxid-NPs betrachtet [15]. Das Element Zink kommt im menschlichen Körper vor und ZnONPs sind bekanntermaßen weniger toxisch [3]. Es wird jedoch berichtet, dass zu viel Zink toxische Wirkungen hervorruft [16]. Freisetzung von Metallkationen Zn 2 aus ZnONPs haben sich auch bei Mikroorganismen und Nagetieren als toxisch erwiesen [17]. ZnO-NPs können über verschiedene Wege in den Blutfluss gelangen und nachteilige Auswirkungen auf die Organe haben [18]. Vorläufige Ergebnisse zeigten, dass von ZnONPs betroffene Organsysteme Entzündungen, veränderte Herzfrequenz und -funktionen sowie oxidativen Stress aufweisen können [19, 20]. Nach [21] führte die zweimal tägliche Inhalation von 20 nm ZnONP (2,5 mg/kg KG) bei Ratten zu einem erhöhten Zn-Gehalt in der Leber nach 12 h und in den Nieren nach 36 h.
Erhöhtes Bewusstsein für Nanotoxizität, Studien zur In-vivo-Toxizität von CuNPs und ZnONPs bei intranasaler Instillation [22, 23], intratrachealer Instillation [24, 25] und oraler Verabreichung [26, 27, 28], dermaler Exposition [29, 30]. Um die Toxizität zu bewerten, muss eine intravenöse (i/v) und intraperitoneale (i/p) Verabreichung erfolgen. Unseres Wissens liegen nur wenige Berichte über die Toxizität von CuNPs und ZnONPs bei intravenöser und intraperitonealer Verabreichung vor. Darüber hinaus wurden der toxikologische Mechanismus und die Gewebeverteilung der beiden NPs nach i/v- und i/p-Injektionen noch nicht systematisch untersucht.
Hiermit haben wir die Toxizität von biosynthetisierten CuNPs und ZnONPs im Bereich von 16-96 nm bei männlichen Wistar-Ratten durch intraperitoneale (i/p) und intravenöse (i/v) Injektionen am 14. und 28. Beobachtungstag nach Wunsch demonstriert.
Methode
Biosynthese von Bio-CuNPs und Bio-ZnONPs
Biologische Synthese von CuNPs und ZnONPs aus nicht-pathogenem Enterococcus faecalis wurde durch extrazelluläre enzymatische Methode adaptiert [31, 32]. Außerdem wurden die Form und Größe der synthetisierten Nanopartikel unter Verwendung von Feldemissions-Rasterelektronenmikroskopie (FeSEM) und Transmissionselektronenmikroskopie (TEM) bestätigt.
In-vivo-Studien
Versuchstiere und Tierhaltung
Spezifische krankheitsfreie, 12 bis 13 Wochen alte männliche Wistar-Ratten wurden von Mahaveera Enterprises, Hyderabad, Indien, bezogen. Tiere wurden in einem Gewichtsbereich von 160–200 g für jede Gruppe ausgewählt und vor Beginn der Behandlung eine Woche lang akklimatisiert, und der Gesundheitszustand der Ratten wurde täglich überwacht. Die Tiere wurden unter Standardbedingungen von Temperatur (24 ± 1 °C) bzw. relativer Luftfeuchtigkeit (55 ± 10 %) in 12-stündigen Hell-Dunkel-Zyklen gehalten. Während der Behandlung wurden die Tiere in Käfigen mit Edelstahlgitterdeckeln untergebracht. Die Tiere wurden mit kommerziell erhältlicher Standard-Pelletsdiät (VRK Nutrition Solutions, Sangli, Maharashtra, India Ltd.) gefüttert. Trinkwasser wurde den Tieren ad libitum zur Verfügung gestellt.
Toxizitätsstudien wurden am Luqman College of Pharmacy, Kalaburagi, Indien, durchgeführt. Die Handhabung der Tiere erfolgte gemäß der Guten Laborpraxis. Das Studienprotokoll wurde von der Ethikkommission für Tiere des Instituts genehmigt (Zulassungsnummer:346/CPCSEA).
Vorbereitung und Verabreichung von Bio-Cu und ZnONPs
Die Vorratssuspensionen von Bio-CuNPs und Bio-ZnONPs (50 mg/ml) wurden durch separates Auflösen in zweifach destilliertem Wasser über Nacht hergestellt und mit 0,22 μ-Spritzenfiltern filtriert. Filtrate werden verwendet, um den Arbeitsstandard im Bereich von 1,25-175 μg/ml Konzentration herzustellen.
Die Tiere wurden in drei Gruppen mit drei unterschiedlichen Konzentrationen für jeden Nanopartikeltyp eingeteilt. Unter Berücksichtigung von sechs Ratten/Gruppe für die intravenöse Verabreichung (kodiert als Set von Experiment A) und sechs Ratten/Gruppe für die intraperitoneale Verabreichung (kodiert als Set von Experiment B) gemäß Tabellen 1 und 2. In beiden Experimentreihen Gruppe A diente als Kontrolle (Fahrzeugdestilliertes Wasser).
Beobachtungs- und Prüfungsaufgaben
Klinische Anzeichen
Während des Tests wurde einmal täglich eine Beobachtung nach der Behandlung durchgeführt, um die Anzeichen einer klinischen Toxizität und/oder des Todes zu überwachen.
Futter- und Wasserverbrauch
Der Futter- und Wasserverbrauch wurde täglich nach Behandlungsbeginn erfasst, berechnet aus den Differenzen zwischen den zugeführten Mengen und den Restmengen.
Tierverhalten und Körpergewicht
Alle zwei Tage nach der Injektion wurden die Ratten gewogen und auf Verhaltensänderungen untersucht.
Hämatologische Indizes
Unter Verwendung einer Standard-Saphena-Venen-Blutentnahmetechnik wurde Blut für die hämatologische Analyse (unter Verwendung von Kalium-Methylendiamintetraessigsäure-Sammelröhrchen) entnommen. Gemäß der hämatologischen Standardanalyse wurden der Ratte 300 μl Blut entnommen und an 14 und 28 Tagen wurden hämatologische Standardparameter, dh Thrombozytenzahl, Hämatokrit, Hämoglobin, Anzahl roter Blutkörperchen und Anzahl weißer Blutkörperchen, analysiert [33].
Biochemische Panelanalyse von Serum
Zur Bestimmung der biochemischen Serumspiegel, einschließlich Alaninaminotransferase (ALT/GPT), Kreatinin (CRE), Aspartataminotransferase (AST) und alkalischer Phosphatase (ALP), wurden Kontrollratten und behandelte Ratten getötet und Vollblutproben zur Zentrifugation (3000 U/min .) entnommen ) für 15 Minuten. Die Bewertung wurde mit einem automatischen biochemischen Analysegerät für die Proben vom 14. und 28. Tag durchgeführt [34].
Erkennung des Organellengewichts
Nach 14 und 28 Tagen wurden die Ratten durch Ether mit phosphatgepufferter Kochsalzlösung anästhesiert und seziert. Die Organe der Kontroll- und der behandelten Gruppe wurden sofort entnommen. Herz, Lunge, Thymus, Gehirn, Niere, Leber und Milz wurden sorgfältig getrennt und mit Kochsalzlösung gewaschen und mit eiskaltem entionisiertem Wasser gespült und mit Filterpapier getrocknet. Morphologie und Farbe der sezierten Organe wurden untersucht und das Gewicht jedes Organs wurde gemessen. Um den Grad der explizit durch Bio-Cu und ZnONPs verursachten Veränderungen zu untersuchen, muss der Organindex (O X ) wurde separat mit der Formel [35] berechnet:
$$ \mathrm{Organ}\ \mathrm{index}\ \left({\mathrm{O}}_{\mathrm{X}}\right)=\frac{\mathrm{Gewicht}\ \mathrm{of} \ \mathrm{experimentell}\ \mathrm{Organ}/\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{experimentell}\ \mathrm{Tier}}{\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{Kontrolle}\ \mathrm{Organ}/\mathrm{Gewicht}\ \mathrm{of}\ \mathrm{Kontrolle}\ \mathrm{Tier}} $$Wo Organindex (OX ) kann sich ändern als:
Herzindex (HX ), Leberindex (LiX ), Milzindex (SX ), Lungenindex (LuX ), Nierenindex (KX ), Thymusindex (TX ), Gehirnindex (BX ).
Histologie
Eine Ratte aus jeder Gruppe, einschließlich der Kontrollgruppe, wurde mit 10 % gepuffertem Formalin nach Ausblutungen mit Phosphat-gepufferter Kochsalzlösung fixiert. Ein kleines Stück Leber, Niere, Milz und Gehirn wurde mit 10 % Formalin fixiert und in Paraffin eingebettet. Paraffinblöcke wurden geschnitten und für die Hämatoxylin- und Eosin-Färbung verarbeitet. Gefärbte Schnitte wurden mit Hellfeldmikroskopie beobachtet [36].
Statistische Analyse
Alle Daten sind als Mittelwert ± SD des Mittelwerts der drei unabhängigen Experimente ausgedrückt; jeweils in dreifacher Ausfertigung durchgeführt, N = 6 Ratten pro Gruppe.
Ergebnisse und Diskussion
Die Synthese von Bio-CuNPs und Bio-ZnONPs wurde durch eine extrazelluläre enzymatische Methode während der Exposition der Reaktanten gegenüber Enterococcus faecalis . durchgeführt Überstand. Die FeSEM-Analyse von Bio-CuNPs und Bio-ZnONPs ist mit einer Verteilung von 1 bis 100 nm zu sehen (zusätzliche Datei 1). Die TEM-Analyse zeigt das Vorhandensein biosynthetisierter CuNPs und ZnONPs mit einer Kern-Schale-Morphologie der Größe 12–90 nm und einer Kugelform für CuNPs [31] und ZnONPs im Bereich von 16 bis 96 nm [32] (zusätzliche Datei 2).
Die Bewertung von Bio-Cu und ZnONPs an männlichen Wistar-Ratten wurde ohne Anzeichen von Mortalität nach NP-Behandlung untersucht. Darüber hinaus wurde nach der Behandlung und bis zum Ende der Versuchsdauer eine häufige Untersuchung von weißem Kot nach i/v-Verabreichung von Bio-CuNPs in einer Dosierung von 9,5 bis 11,5 μg/kg überwacht. Zwischen der dritten und vierten Woche zeigten die mit Bio-CuNPs behandelten Ratten einen signifikanten Anstieg des Futter- und Wasserverbrauchs für i/v betrug 9,5 μg/kg (IC50 .). ) und 11,5 μg/kg (DC), während für i/p-Weg (Dosisbereich:24,8 bis 30,3 μg/kg) und Ratten der Kontrollgruppe von der 3. bis 4. Woche. Variation des Körpergewichts der Ratten nach i/v und i/ Die p-Gabe von Bio-CuNPs und Bio-ZnONPs wurde in den Tabellen 3 und 4 gezeigt. Reduktion und Zunahme des Körpergewichts sind wertvolle Indikatoren zur Beurteilung der Toxizität einer Testprobe [37]. Frühere Berichte, die in Toxizitätsstudien mit 13,5 nm Gold [33] und 100 nm Silber [38] die Wirkung von NPs auf das Körpergewicht bei i/v-Injektionen belegen, waren geringer als bei i/p und oraler Verabreichung. Gemäß Rhiouani et al., die geringe Gewichtsabnahme nach 4 Tagen der Behandlung bei allen behandelten Gruppen kann auf negative Auswirkungen toxischer Substanzen auf die Tiere hinweisen [39].
Es ist ersichtlich, dass die i/v- und i/p-Gabe von Bio-ZnONPs in den drei verschiedenen Dosierungen (NOAEC, IC50 und TLC) war das Körpergewicht bis zur zweiten Verabreichungswoche im Vergleich zur Kontrollgruppe leicht reduziert. Nach dem 14. Tag wurde das Körpergewicht jedoch wiedererlangt. Im Falle einer i/p-Verabreichung wurde eine Verringerung des Körpergewichts durch Bio-ZnONPs (30,3 μg/kg) bei einer letalen Gesamtkonzentration induziert und war niedriger als in der Kontrollgruppe, was auf eine triviale Toxizität über die i/p-Route gegenüber der i/v-Route hindeutet (Tabelle 4, Abb. 1a). In ähnlicher Weise wurde bei Ratten, die mit Bio-CuNPs behandelt wurden, bei einer Konzentration von 9,5 μg/kg und 11,7 μg/kg über die i/v-Route eine leichte Verringerung des Körpergewichts festgestellt. Bis zur 14-tägigen Behandlung mit Bio-CuNPs wurden keine Anzeichen von Nebenwirkungen auf Wachstum und Körpergewichtszunahme beobachtet. Die Variation des Körpergewichts innerhalb von 28 Tagen bei einer Dosis von 11,7 μg/kg (i/v-Weg) ist in Tabelle 3 dargestellt. Nach dem 14. Behandlungstag wurde eine beträchtliche Abnahme des Körpergewichts über die i/v-Methode im Vergleich zur Kontrolle festgestellt Gruppe. Zeigt somit die Toxizität von Bio-CuNPs über diesen Weg an (Abb. 1b). Mit Bio-CuNPs behandelte Ratten über die i/p-Verabreichung induzierten eine geringfügige Abnahme des Körpergewichts, und es wurden weder bei der i/p- noch bei der i/v-Verabreichung Anzeichen von Mortalität beobachtet. Daher induzierten i/p-Injektionen eine geringere Toxizität (dargestellt in Tabelle 4 und Abb. 1a).
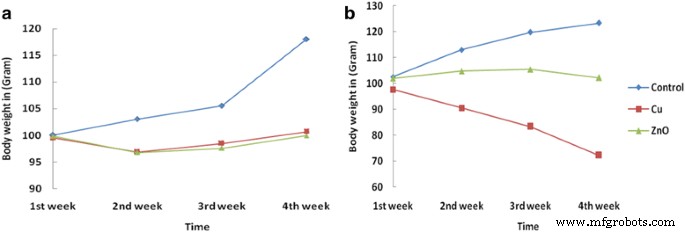
Veränderung des Körpergewichts von unbehandelten (Kontrolle) und behandelten Ratten mit Bio-CuNPs und Bio-ZnONPs. Bio-CuNPs und Bio-ZnONPs, die über (A) intraperitoneale (i/p) und (B) intravenöse (i/v) Verabreichungswege bis zum 28. Tag der Beobachtung behandelt wurden. Alle Behandlungen von Bio-CuNPs (Cu) und Bio-ZnONPs (ZnO) in ihrer letalen Gesamtkonzentration wurden verabreicht und 28 Tage lang beobachtet; N = 6 Ratten pro Gruppe
Hämatologie-Indizes
Die Schätzung hämatologischer Parameter wie Erythrozytenzahl, Leukozytenzahl, Thrombozytenzahl, Hämoglobinspiegel und Blutgerinnungszeit sind die wichtigen Größen, um die Toxizität von behandelten NPs zu messen. Für Tag 14 und 28 sind konzentrationsabhängige hämatologische Ergebnisse in den Tabellen 5 und 6 für den i/p- und i/v-Verabreichungsweg dargestellt. Dosierung von Bio-CuNPs bei 9,5 μg/kg (IC50 .) ) und 11,7 μg/kg (TLC) über die i/v-Route hat im Gegensatz zu Bio-ZnONPs eine reduzierte Erythrozytenzahl gezeigt. Ein konzentrationsabhängiger Trend wurde jedoch nicht festgestellt. Bei Ratten, die mit Bio-ZnONPs über den i/v-Verabreichungsweg behandelt wurden, haben sich der Hämoglobinspiegel, die Thrombozytenzahl und die weißen Blutkörperchen verändert, aber es wird kein signifikanter Unterschied zwischen allen drei Konzentrationen beobachtet (NOAEC, IC50 und DC). Im Fall der i/p-Verabreichung wurden jedoch am 14. Beobachtungstag (Tabelle 5) im Vergleich zur Kontrolle und Bio- CuNPs behandelt. Überraschenderweise sind die hämatologischen Wirkungen am 28. Tag normal (Tabelle 6).
Die hämatologischen Wirkungen der unterschiedlichen Injektionsmethoden (i/v, i/p) für die beiden unterschiedlichen Bio-NPs am 14. und 28. Beobachtungstag sind vielfältig. Es kann beobachtet werden, dass Hämoglobin, rote Blutkörperchen, weiße Blutkörperchen und Blutplättchen über den i/v-Weg bei der Behandlung mit Bio-CuNPs und über den i/p-Weg bei mit Bio-ZnONPs behandelten Ratten abnehmen. Es wurde jedoch eine signifikante Abnahme der Erythrozytenzahlen beobachtet. Dies weist darauf hin, dass die verschiedenen Injektionswege keine signifikanten Unterschiede in der Thrombozytenzahl, Hämoglobin oder weißen Blutkörperchen induzierten, außer bei Ratten, denen Bio-CuNPs injiziert wurden (i/v-Weg). Die roten Blutkörperchen zeigen einen signifikanten Unterschied nach i/p- und i/v-Injektion (wie in den Tabellen 5 und 6) gezeigt.
Biochemischer Serumtest
Serumkreatinin ist ein Abfallprodukt; Eine höhere Kreatininproduktion weist auf eine Nierenschädigung hin. Bio-ZnONPs (i/v-Pfad:Dosierung von 11–16 μg/kg, i/p-Pfad:Dosierung von 24–30 μg/kg) beeinflussten den Serumkreatininspiegel im Vergleich zur Kontrolle am 14. und 28. Tag nicht signifikant. (Tabellen 7 und 8, Abb. 2a, b). Ratten, die mit Bio-CuNPs behandelt wurden (i/v-Weg:Dosierung von 06–12 μg/kg) zeigten im Vergleich zur Kontrolle einen Anstieg des Serumkreatininspiegels auf 2,3 mg/dl. Der i/p-Injektionsweg zeigte jedoch keine signifikanten Veränderungen (Tabellen 7 und 8). Das Blutserum weist eine große Anzahl von Enzymen auf, aber zur Beurteilung der normalen und pathologischen Symptome der Leber sind Alanintransaminasen (Glutamatpyruvattransaminase) und Aspartattransaminasen (Glutamatoxalatacetattransaminase) nützlich. Aspartattransaminase ist mitochondrialen Ursprungs und kommt in großen Mengen in Leber, Herz, Niere und Skelettmuskulatur vor. Die alkalische Phosphatase im Serum ist ein Globulinenzym mit niedrigem Molekulargewicht, das in höheren Konzentrationen in Knochen, Leber- und Gallenwegen und Nieren vorkommt. Die Aktivität dieses Enzyms kann durch die Bestimmung des aus dem Glycerinphosphat freigesetzten organischen Phosphats bestimmt werden. Der Serumspiegel der Enzyme war sowohl bei hepatozellulärem als auch bei obstruktivem Ikterus erhöht. Beim i/v-Verabreichungsweg haben Bio-ZnONPs (40,7 mg/dl, 37,9 IE/l, 82,4 IE/l) keine signifikanten Auswirkungen auf die Serum-ALT-, Serum-AST- und ALP-Spiegel im Vergleich zur Kontrolle. Obwohl die i/p-Verabreichung einen signifikanten Anstieg der ALT-, AST- und ALP-Spiegel im Vergleich zur Kontrolle am 14. und 28. Tag zeigte (Abb. 2a und b). Die Ergebnisse der Toxizitätsstudie mit Serum zeigten, dass Bio-ZnONPs bis 28 Tage keine Veränderungen der Kreatinin-, ALT-, AST- und ALP-Spiegel für die i/v-Route haben.
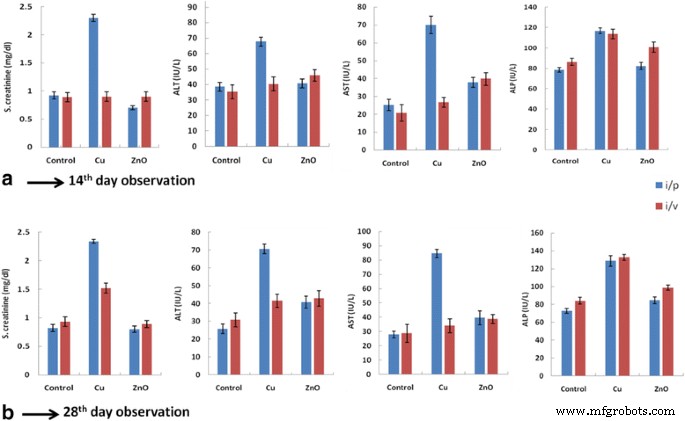
Biochemische Ergebnisse von Ratten, die mit Bio-CuNPs und Bio-ZnONPs behandelt wurden. S.-Kreatinin-, ALT-, AST- und ALP-Spiegel wurden bei Ratten gemessen, die mit Bio-CuNPs und Bio-ZnONPs über intraperitoneale (i/p) und intravenöse (i/v) Verabreichungswege am (A) 14. Tag und (B) behandelt wurden. 28. Tag. Alle Daten sind als Mittelwert ± SD des Mittelwerts der drei unabhängigen Experimente ausgedrückt; jeweils in dreifacher Ausfertigung durchgeführt, N = 6 Ratten pro Gruppe. Hinweis:Cu:Bio-CuNPs, ZnO:Bio-ZnONPs, i/p:intraperitoneal, i/v:intravenös
Im Gegensatz dazu zeigten Ratten, die mit Bio-CuNPs auf dem i/v-Weg behandelt wurden, einen signifikanten Anstieg des Serum-ALT (67,7 mg/dl), des AST-Spiegels (70 I.E./L) und des ALP (128 I.E./L). Die Wirkung von Bio-CuNPs über die i/p-Route war im Vergleich zur Kontrolle beträchtlich gering. Der Unterschied der Ergebnisse könnte auf Unterschiede in den Dosierungswegen, Toxizität der Nanopartikel sowie der Verabreichungsdauer zurückgeführt werden. Wir haben festgestellt, dass Bio-ZnONPs im Vergleich zu Bio-CuNPs keinen Einfluss auf die Biomarker der Nieren- und Leberfunktion (sowohl i/v als auch i/p) haben.
Nachweis des Organellengewichts und histologische Untersuchung
Veränderungen des Organgewichts von Ratten bei verschiedenen Dosen von Bio-NPs veranschaulichen die nachteiligen Wirkungen von NPs auf Organe. Es ist ersichtlich, dass das Gewicht von Herz, Leber, Milz, Lunge, Nieren und Gehirn bei Ratten bei Behandlung mit Bio-ZnONPs verringert ist, wie in den Tabellen 9 und 10 dargestellt. Außerdem Berücksichtigung der Organreaktion und des Grades der Veränderungen wurden durch Berechnung des Organindex (OX ) jedes Organs separat. Der Organindex für Herz, Leber, Milz, Lunge, Nieren, Gehirn und Thymusdrüse sind in den Tabellen 9 und 10 aufgeführt.
Bei mit Bio-CuNPs und Bio-ZnONPs behandelten Ratten wurden nach i/v- und i/p-Verabreichung Unterschiede im Gewicht von Milz und Thymus beobachtet. Am 14. Tag zeigte Bio-ZnONPs einen verringerten Milzindex durch i/p-Injektion und einen Anstieg durch i/v-Verabreichung (Tabelle 9). Im Fall von Bio-CuNPs zeigten die durch i/v-Verabreichung behandelten Ratten eine signifikante Reduktion des Milzindex am 14. (0,265) und 28. Tag (0,49). Dies zeigt an, dass das Immunsystem durch die i/v-Verabreichung von Bio-CuNPs und die i/p-Verabreichung von Bio-ZnONPs beeinflusst wurde. Im Falle einer i/p Bio-ZnONPs-Verabreichung kehrt das Immunsystem der Ratte nach dem 14. Tag in den Normalzustand zurück und beweist, dass die Wirkung nicht verlängert wird. Zusammen mit der vorherigen Variation des Körpergewichts scheint es, dass die i/v-Verabreichungsroute von Bio-CuNPs das Herz, die Leber, die Lunge, die Nieren und das Gehirn beeinflussen kann; außerdem kann es das Immunsystem schädigen. Aus Abb. 3a impliziert dies, dass Milz und Thymus das Hauptziel von Organen durch Bio-CuNPs sind.
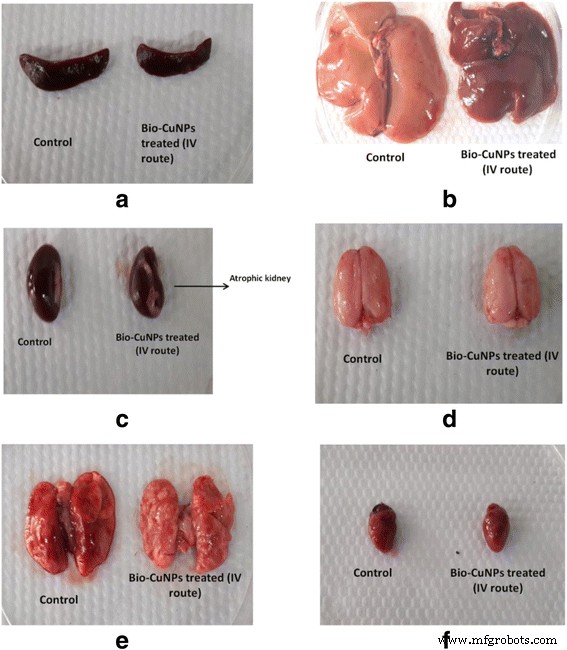
Veränderung der Organellenmorphologie. Wo a Milz, b Leber, c Niere, d Gehirn, e Lunge und f Herz, von männlichen Wistar-Ratten, die intravenös mit Bio-CuNPs behandelt wurden, im Vergleich zur Kontrolle am 28. Beobachtungstag
Bei i/v- und i/p-Bio-CuNPs-behandelten Gruppen wurden offensichtliche Auswirkungen auf den Organindex sowohl bei IC50 . beobachtet und DC-Dosen. Darüber hinaus zeigt die intraperitoneale Injektion von den zwei verschiedenen Verabreichungswegen die mäßige Toxizität in den mit Bio-ZnONPs behandelten Gruppen und die höchste Toxizität in den mit Bio-CuNPs behandelten Gruppen. Aufgrund der dichten Blutgefäße und der Lymphe im Peritoneum der Maus war bekannt, dass eine effiziente Arzneimittelaufnahme durch i/p-Injektion schnell ist [40]. Dementsprechend zeigt die intravenöse Injektion die geringste Toxizität in den mit Bio-ZnONPs behandelten Gruppen und die höchste Toxizität in den mit Bio-CuNPs behandelten Gruppen.
Toxikologische Veränderungen bei Ratten
Wir haben versucht, die Auswirkungen der Toxizität bei verschiedenen Dosen und Zeitintervallen von Bio-NPs zu untersuchen. Mit Bio-ZnONPs behandelte Gewebe (i/v-Pfad:Dosierungsbereich 11-16 µg/kg, i/p-Pfad:Dosierungsbereich 24-30 µg/kg) zeigten keine Veränderungen in Leber, Niere, Milz und Gehirn im Vergleich zu Kontrollgewebe (Abb. 4, 5, 6 und 7). Obduktionsbeobachtungen (Autopsie:Sezierende Untersuchung toter Ratten) ergaben, dass alle Organe von mit Bio-NPs behandelten Ratten die anatomischen Merkmale (z. B. Merkmale von Farbe, Form und Größe) aufwiesen, die aufgrund ihres Aussehens bei unbehandelten Tieren zu erwarten waren. Im Vergleich zu Bio-ZnONPs zeigten mit Bio-CuNPs behandelte Ratten signifikantere Veränderungen der anatomischen Merkmale von Nieren-, Leber-, Milz- und Hirngewebe im Gegensatz zur Kontrolle (Abb. 4, 5, 6 und 7).
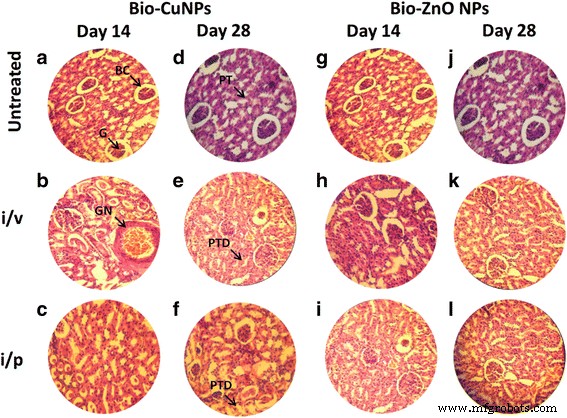
H&E-gefärbte Schnitte von Rattennieren. Ratten, die über die i/v- und i/p-Route mit Bio-Cu und ZnONPs behandelt wurden; unbehandelte Proben wurden als Kontrolle betrachtet. Wo mit Bio-CuNPs behandelte Schnitte an Tag 14 (A–C) und Tag 28 (D–F) beobachtet wurden. Behandelte Schnitte von Bio-ZnONPs an Tag 14 (G–I) und Tag 28 (J–L). BC Bowman-Kapsel, G glomerulär, PT proximaler Tubulus, GN glomeruläre Nekrose, PTD proximaler Tubulusschaden
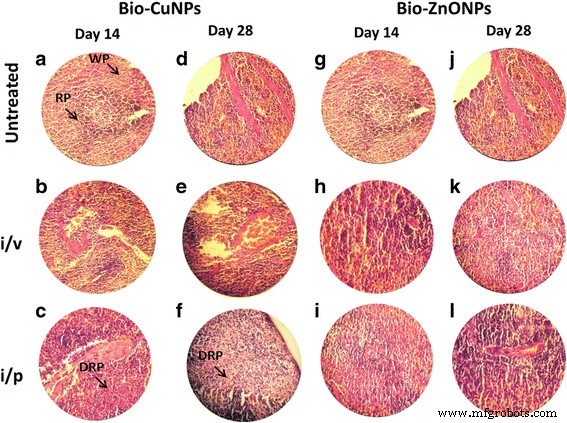
H&E-gefärbte Abschnitte der Rattenmilz. Ratten, die über die i/v- und i/p-Route mit Bio-Cu und ZnONPs behandelt wurden; unbehandelte Proben wurden als Kontrolle betrachtet. Schnitte, die mit Bio-CuNPs behandelt wurden, beobachtet an Tag 14 (A–C) und Tag 28 (D–F). Behandelte Schnitte von Bio-ZnONPs an Tag 14 (G–I) und Tag 28 (J–L). WP weißer Zellstoff, RP roter Zellstoff, DRP-Rückgang bei rotem Zellstoff
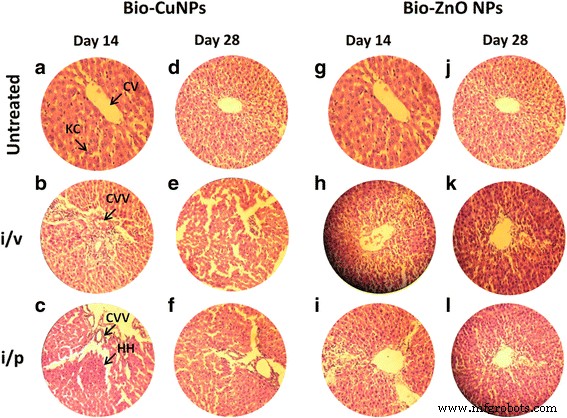
H&E-gefärbte Schnitte von Rattenleber. Ratten, die über die i/v- und i/p-Route mit Bio-Cu und ZnONPs behandelt wurden; unbehandelte Proben wurden als Kontrolle betrachtet. Schnitte, die mit Bio-CuNPs behandelt wurden, beobachtet an Tag 14 (A–C) und Tag 28 (D–F). Behandelte Schnitte von Bio-ZnONPs an Tag 14 (G–I) und Tag 28 (J–L). CV-Zentralvene, KC-Kupffer-Zellen, CVV-Zentralvenen-Vakuolisierung (zytoplasmatische Vakuolisierung), HH-Hepaterblutung
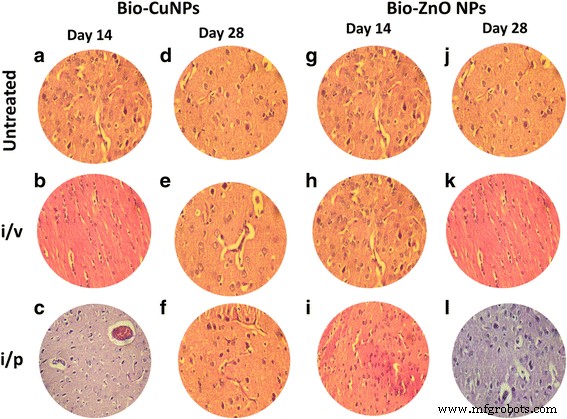
H&E-gefärbte Abschnitte des Rattenhirns. Ratten, die über die i/v- und i/p-Route mit Bio-Cu und ZnONPs behandelt wurden; unbehandelte Proben wurden als Kontrolle betrachtet. Schnitte, die mit Bio-CuNPs behandelt wurden, beobachtet an Tag 14 (A–C) und Tag 28 (D–F). Behandelte Schnitte von Bio-ZnONPs an Tag 14 (G–I) und Tag 28 (J–L). [Alle Objektträger werden unter × 40-Vergrößerung betrachtet, NIKON Eclipse E200 (Trinakularmikroskop)]
Bio-CuNPs induzierten Schäden über eine i/v-Verabreichung und zeigten einen dosisabhängigen Trend im Gewebe. Bei einer TLC-Konzentration (11,7 μg/kg) zeigten Bio-CuNPs schwere Schäden am Leber- und Nierengewebe von Wistar-Ratten. Darüber hinaus haben Bio-CuNPs, die sowohl über die i/v- als auch die i/p-Route behandelt wurden, eine Nekrose der glomerulären Zellen (glomeruläre Atrophie), der Bowman-Kapsel und des proximalen Tubulus bei den Ratten der Gruppen am 14. ) im Vergleich zur unbehandelten Kontrolle. Glomeruläre Nekrose ist auf immunologische Kostenerstattung zurückzuführen, aber Tubulusschäden sind meist auf die toxische Wirkung der NPs zurückzuführen. Die tubuläre Schädigung, die durch die toxischen Wirkungen von Bio-CuNPs sowohl über den i/v- als auch den i/p-Weg verursacht wurde, erhöhte auch den glomerulären Druck und verursachte eine glomeruläre Atrophie.
Die normale Kontrollgruppe zeigte eine normale histologische Struktur des Leberläppchens und der Zentralvene, die von normalen Hepatozyten umgeben ist (Abb. 6). Bio-CuNPs, die über die i/p-Route (19,82 μg/kg) behandelt wurden, zeigten leichte histologische Veränderungen, einschließlich der Kupffer-Zellaktivierung, sowohl am 14. als auch am 28. Tag der Beobachtung (Abb. 6b, e). Ratten, die mit Bio-CuNPs auf dem i/v-Weg behandelt wurden, zeigten schwere Veränderungen, einschließlich zytoplasmatischer Vakuolisierung von Hepatozyten, die die Zentralvene umgeben, und Leberblutung für die Beobachtung am 14. Tag (Abb. 6c). Überraschenderweise zeigte die Gruppe am 28. Tag mäßige Veränderungen, einschließlich fettiger Veränderungen der Hepatozyten und Pyknose der hepatozytischen Kerne (Abb. 6f). Mit Bio-ZnONPs behandeltes Lebergewebe zeigte am 14. Tag der i/p-verabreichten Gruppe mäßige Veränderungen, die durch fettige Veränderungen der Hepatozyten demonstriert wurden (Fig. 6i). Die mit Bio-ZnONPs behandelten Gruppen zeigten eine leichte Verbesserung und eine signifikante hepatoprotektive Aktivität wurde am 28. Tag im Vergleich zum 14. Tag beobachtet (Abb. 6l). Ab dem 14. Tag hat bei den mit Bio-ZnONPs behandelten Tieren die Wiederherstellung der normalen Leberarchitektur stattgefunden.
Es wurde ein Rückgang der Milzzellen (rote Pulpa), während eine Zunahme der Lymphozyten (weiße Pulpa) in Milzgewebe festgestellt, das aus Ratten extrahiert wurde, die mit Bio-CuNPs über die i/v-Route behandelt wurden (Abb. 5c, f). Bei der primären Beobachtung wurde eine Anlagerung von Bio-CuNPs in der Milz in der roten Pulpa festgestellt und war mit einem bescheidenen Verlust an Zellmasse verbunden; reduced cell mass was obvious on the 28th day time point when compared with 14th day of i/v administration (Fig. 5f), whereas minor changes were observed in red pulp depletion when rats were treated with Bio-CuNPs via i/p route on both 14th and 28th day time point. Structural changes were not seen in the white pulp or in splenic blood vessels (arteries or venous sinuses) and intravascular erythrocytes (Fig. 5b, e). No morphological changes have been found in spleen tissues treated with Bio-ZnONPs (Fig. 5). The H&E-stained brain sections of rats, treated (i/v and i/p) with NPs, showed no changes in brain region, olfactory bulb (perivascular localization) and the choroid plexus and ependyma of the lateral ventricles (Fig. 7).
Conclusion
Animal toxicity studies using 16- to 96-nm-ranged biosynthesized copper (Bio-CuNPs) and zinc oxide (Bio-ZnONPs) was assessed in male Wistar rat at the dose range of 6.1 to 19.82 μg/kg and 11.14 to 30.3 μg/kg respectively for both i/p and i/v routes on 14th and 28th day of observation. We observed no mortality and normal behaviour in the animals treated with Bio-CuNPs and Bio-ZnONPs in their specific dose range. The results also verified the Bio-CuNPs and Bio-ZnONPs at low concentrations do not cause identifiable toxicity even after their breakdown in vivo over time. Increased concentrations of these Bio-NPs induce weight reduction, but no significant statistical difference was observed for Bio-ZnONPs’ treated animals. In the case of i/v and i/p Bio-CuNPs’ treated groups, obvious effects on organ index have been observed at both IC50 and TLC doses. Moreover, of the two different administration routes, the intraperitoneal injection shows the modest toxicity in Bio-ZnONPs’ treated groups and highest toxicity in Bio-CuNPs’ treated groups. Correspondingly, the intravenous injection shows the least toxicity in Bio-ZnONPs’ treated groups and highest toxicity in Bio-CuNPs’ treated groups. Considering all the results of studies, targeting Bio-ZnONPs by intravenous injection is promising for possible biomedical application.
Abkürzungen
- ±:
-
Plus or minus
- ALP:
-
Alkaline phosphatase
- ALT:
-
Alanine aminotransferase
- AST:
-
Aspartate aminotransferase
- Bio-CuNPs:
-
Biogenic copper nanoparticles
- Bio-ZnONPs:
-
Biogenic zinc oxide nanoparticles
- BX :
-
Brain index
- CRE:
-
Creatinine
- Cu:
-
Copper
- FesEM:
-
Feldemissions-Rasterelektronenmikroskopie
- H&E:
-
Haematoxylin eosin
- Hb:
-
Haemoglobin
- HX :
-
Heart index
- i.e.:
-
That is
- i/p route:
-
Intraperitoneal route
- i/v route:
-
Intravenous route
- IC:
-
Inhibitory concentration
- KX :
-
Kidney index
- LiX :
-
Liver index
- LuX :
-
Lung index
- NOAEC:
-
No observable adverse effect concentration
- NPs:
-
Nanoparticles
- Ox :
-
Organ index
- RBC:
-
Red blood cell
- SD:
-
Standard deviation
- SX :
-
Spleen index
- TEM:
-
Transmissionselektronenmikroskopie
- TLC:
-
Total lethal concentration
- TX :
-
Thymus index
- WBC:
-
White blood cell
- ZnO:
-
Zinkoxid
Nanomaterialien
- Biokompatible FePO4-Nanopartikel:Wirkstofftransport, RNA-Stabilisierung und funktionelle Aktivität
- Biogene Synthese, Charakterisierung und Bewertung des antibakteriellen Potenzials von Kupferoxid-Nanopartikeln gegen Escherichia coli
- Resveratrol-beladene Albumin-Nanopartikel mit verlängerter Durchblutung und verbesserter Biokompatibilität für eine hochwirksame gezielte Pankreastumortherapie
- Neuartige biokompatible Au-Nanostars@PEG-Nanopartikel für die In-vivo-CT-Bildgebung und renale Clearance-Eigenschaften
- Biosicherheit und antibakterielle Wirkung von Graphen und Graphenoxid in vitro und in vivo
- Modifiziertes hyperverzweigtes Polyglycerin als Dispergiermittel zur Größenkontrolle und Stabilisierung von Goldnanopartikeln in Kohlenwasserstoffen
- Synthese und In-vitro-Leistung von polypyrrolbeschichteten Eisen-Platin-Nanopartikeln für die Photothermie und die photoakustische Bildgebung
- Grüne Kompetenz bei der Synthese und Stabilisierung von Kupfernanopartikeln:katalytische, antibakterielle, zytotoxische und antioxidative Aktivitäten
- Eine vergleichende In-vivo-Untersuchung biosynthetisierter Kupfer- und Zinkoxid-Nanopartikel durch intraperitoneale und intravenöse Verabreichungswege bei Ratten
- Grüne Synthese von Metall- und Metalloxid-Nanopartikeln und ihre Wirkung auf die einzellige Alge Chlamydomonas reinhardtii



