Stickstoffdotierte poröse Kohlenstoff-Nanoblätter, stark gekoppelt mit Mo2C-Nanopartikeln für eine effiziente elektrokatalytische Wasserstoffentwicklung
Zusammenfassung
Die Erforschung von erdreichen und edelmetallfreien Katalysatoren für die Wasserelektrolyse ist von zentraler Bedeutung für die erneuerbare Wasserstofferzeugung. Hier ein hochaktiver Elektrokatalysator aus stickstoffdotierten porösen Kohlenstoffnanoblättern gekoppelt mit Mo2 C-Nanopartikel (Mo2 .) C/NPC) wurde nach einer neuartigen Methode mit einer hohen BET-Oberfläche von 1380 m 2 . synthetisiert g −1 Verwendung von KOH zur Aktivierung von Kohlenstoffverbundwerkstoffen. Der KOH spielt eine Schlüsselrolle beim Herausätzen von MoS2 um Mo-Vorläufer herzustellen; gleichzeitig korrodiert es Kohlenstoff, um eine poröse Struktur zu bilden und reduzierende Gase wie H2 . zu produzieren und CO. Das resultierende Mo2 C/NPC-Hybrid zeigte eine überlegene HER-Aktivität in saurer Lösung mit einem Überpotential von 166 mV bei einer Stromdichte von 10 mA cm −2 , Einsetzende Überspannung von 93 mV, Tafel-Steigung von 68 mV dec −1 , und bemerkenswerte langfristige Zyklenstabilität. Die vorliegende Strategie könnte eine vielversprechende Strategie zur Herstellung anderer Metallcarbid/Kohlenstoff-Hybride zur Energieumwandlung und -speicherung darstellen.
Einführung
Heutzutage sind Umweltverschmutzung und Energiekrise zu den Schlüsselthemen für eine nachhaltige Entwicklung geworden [1, 2]. Der Schlüssel zur Lösung des Problems liegt in einer sauberen und erneuerbaren Energiequelle. Wasserstoff, der durch die Zersetzung von Wasser durch Katalysatoren erzeugt wird, gilt als vielversprechende Alternative zu fossilen Brennstoffen [3, 4]. Katalysatoren auf Platinbasis sind bis heute die effizientesten Katalysatoren für die Wasserstoffentwicklungsreaktion (HER), aber die Knappheit und die hohen Kosten begrenzen ihre großtechnischen Anwendungen. Als Ersatz für die edlen Metallkatalysatoren. Unter diesen Elektrokatalysatoren ist Mo2 C hat als effizienter HER-Elektrokatalysator großes Interesse auf sich gezogen, da seine elektronische d-Band-Struktur der von Pt ähnelt [11]. Die katalytischen Eigenschaften von Molybdäncarbid beruhen hauptsächlich auf der Freilegung aktiverer Zentren und der Verbesserung der Leitfähigkeit der Katalysatoren. Forscher tendieren zur Verbesserung der Zusammensetzung und Struktur von Mo2 C-Hybride; die aktuelle Synthese von Mo2 C-Hybride erfordern hauptsächlich eine hohe Temperatur, die zu einer Agglomeration der Partikel führt, was zu einer Abnahme der aktiven Oberflächen und einer Verringerung der HER-katalytischen Leistung führt [12]. Um die Agglomeration von Molybdäncarbid zu verringern, wird normalerweise leitfähiges Kohlenstoff-Trägermaterial aufgebracht, um die aktiven Oberflächen und die Leitfähigkeit zu erhöhen. Graphit mit zweidimensionaler Struktur erwies sich als hervorragendes Trägermaterial für Katalysatoren [13]. Andernfalls würde eine große Oberfläche der Katalysatoren mehr exponierte aktive Zentren bereitstellen, wodurch die HER-Leistung verbessert würde. Leider ist die neuere Methode zur Verbesserung der spezifischen Oberfläche des Katalysators immer noch begrenzt, und Forscher neigen dazu, die Größe des Katalysators zu reduzieren, wobei sie sich selten auf die Erhöhung der Porosität des Materials konzentrieren [14, 15]. Daher ist die Zunahme der spezifischen Oberfläche von Mo2 C/C-Komposit ist eingeschränkt. Die Herstellung von porösem Kohlenstoff mit hoher spezifischer Oberfläche (4196 m 2 .) g −1 ) aus Kaliumhydroxid-aktiviertem Polymerhydrogel [16] bietet eine neue Idee, das tragende leitfähige Graphitsubstrat mit einer porösen Struktur zu synthetisieren, die während der HER einen offenen Raum und kurze Diffusionskanäle für Reaktanten bereitstellen würde [17]. Ein früherer Bericht hat gezeigt, dass die synergistischen Effekte zwischen Mo2 C- und N-Dotierstoffe in Kohlenstoffmaterialien würden zu einer hohen elektrokatalytischen HER-Leistung führen [18]. Die kontrollierte Synthese von N-dotierten porösen Kohlenstoffnanoblättern als Trägersubstrat würde eine große Oberfläche, ausgezeichnete Leitfähigkeit, hohe Haltbarkeit, N-Dotierstoffe zur Verbesserung des Elektronentransfers und eine poröse Struktur zur Förderung der Masse-/Ladungsübertragung aufweisen. Darüber hinaus haben Berichte bewiesen, dass das β-Mo2 C mit hexagonaler Struktur ist die aktivste Phase der vier Phasen von Molybdäncarbid, da sie eine ähnliche Valenzbandform wie Pt aufweist [19]. Daher ist es eine Herausforderung, die stickstoffdotierten porösen Kohlenstoff-Nanoblätter gekoppelt mit β-Mo2 . zu synthetisieren C-Nanopartikel für eine hocheffiziente katalytische Wasserstoffproduktion.
Hier berichten wir über eine neuartige Methode der Selbsttemperierung, um einen hochaktiven und stabilen edelmetallfreien Elektrokatalysator mit großer Porosität zu erhalten. Kommerzielles MoS2 wurde als Mo-Quelle und Selbsttemplat verwendet und Dopamin wurde als C- bzw. N-Quelle verwendet. Da Dopamin auf der Oberfläche der Mo-Quelle leicht selbstpolymerisieren kann, um Polydopamin (PDA)-Mikrokügelchen zu bilden, ist es wichtig, Katalysatoren mit einer aktiveren Oberfläche zu synthetisieren, die der Luft ausgesetzt ist [20]. Reporter neigen dazu, Vorlagen wie SiO2 . zu verwenden [21] und NaCl [22] um Aggregation zu vermeiden und Strukturen mit hoher spezifischer Oberfläche zu bilden. Das Auflösen von Kieselsäure erfordert jedoch Flusssäure, die eine hochriskante Chemikalie ist, und das Entfernen des Salztemplats erfordert mehr Schritte. Wir haben uns für kommerzielles MoS2 entschieden als Mo-Quelle und Selbst-Templates seit MoS2 kann bei hoher Temperatur mit KOH reagieren. Die Entfernung des Templats und die Aktivierung von KOH, was zu porösem Kohlenstoff und reduzierendem Gas führte, synthetisierte das endgültige Mo2 C/NPC-Hybrid mit hoher katalytischer Aktivität. Unsere Synthesemethode legt eine vielversprechende Strategie zur Herstellung edelmetallfreier Hochleistungs-HER-Katalysatoren nahe.
Methoden
Vorbereitung von Mo2 C/NPC-Hybrid und der Referenz-NPC
Bei einer typischen Synthese werden 500 mg kommerzielles MoS2 wurde zuerst in 100 &mgr;ml entionisiertem Wasser mittels Beschallungsverfahren dispergiert. Dann wurden 120 mg Trizma®-Base und 200 mg Dopaminhydrochlorid in die Suspension gegeben. Die Mischung wurde 24 h bei Raumtemperatur gerührt und das Produkt nach dem Waschen mit entionisiertem Wasser durch Filter gesammelt. Nachdem es über Nacht in den Ofen gestellt wurde, wird das resultierende MoS2 @PDA wurde in einem Röhrenofen bei 600°C 2 h lang karbonisiert, um MoS2 . zu bilden @NC. Das karbonisierte MoS2 @NC wurde in 4 ml 7 M KOH eingeweicht, mit einem KOH zu MoS2 @NC-Massenverhältnis von 3:1. Das getrocknete KOH/MoS2 @NC-Gemisch wurde unter N2 . erhitzt bei 800 °C für 1 Stunde. Nach dem Abkühlen wurde die Probe filtriert und mit verdünnter Salzsäurelösung und entionisiertem Wasser gewaschen. Es wurde dann über Nacht bei 60 °C getrocknet. Das Endprodukt war Mo2 C/NPC und N-dotierter poröser Kohlenstoff (NPC) wurden nach einem ähnlichen Verfahren erhalten, außer dass kein kommerzielles MoS2 wurde hinzugefügt.
Charakterisierung
Röntgenbeugung (XRD) wurde an einem PANalytical X’Pert3 Powder unter Verwendung von Cu Kα-Strahlung (λ = 1,54056 Å). Die Morphologie wurde unter Verwendung einer Feldemissions-Rasterelektronenmikroskopie (REM, Hitachi SU8020) charakterisiert. Transmissionselektronenmikroskopie(TEM)-Bilder und entsprechende energiedispersive Röntgen(EDX)-Elementarkartierungsbilder wurden mit einem FEI Tecnai G2 F20 S-TWIN TMP durchgeführt. Das Raman-Spektrum wurde mit einem konfokalen Raman-Spektrometer (HORIBA LabRAM HR Evolution) aufgenommen. Röntgen-Photoelektronenspektren (XPS) wurden auf einem PHI Quantera-II-Röntgen-Mikrosonden-Röntgenspektrometer mit Al Kα-Strahlung (1486,6 eV) als Anregungsquelle durchgeführt. Die TGA/DSC-Kurve wurde mit einem TGA/DSC1-Thermoanalysator von Mettler-Toledo gemessen. Die spezifische Oberfläche der Probe wurde mit einem Micromeritices ASAP 2020 HD88 gemessen.
Elektrochemische Messungen
Alle elektrochemischen Tests werden mit einem Standard-Dreielektrodensystem auf einem CHI660E-Potentiostaten (CH Instruments, China) durchgeführt, und alle Potenziale in diesem Papier beziehen sich auf eine reversible Wasserstoffelektrode (RHE) gemäß E(RHE) = E(Ag/AgCl .). ) + 0,059 pH + 0,197 V. Als Gegenelektrode wurde ein Graphitstab und als Referenzelektrode Ag/AgCl (gesättigte KCl-Füllung) verwendet. Als Arbeitselektrode wurde eine Glaskohlenstoffelektrode mit einem Durchmesser von 5 mm verwendet, die mit 15 µl Katalysatortinte bedeckt war. Typischerweise werden bei der Vorbereitung einer Arbeitselektrode 4 mg des Mo2 C/NPC und 20 µl Nafion-Lösung werden in 1 µl 3:1 V/V Wasser/Ethanol durch Ultraschall für 1 µl dispergiert, um eine homogene Tinte zu bilden. Vor den elektrochemischen Tests wird die frische Arbeitselektrode 50 Zyklen durchlaufen, um den Strom zu stabilisieren, und die Linear-Sweep-Voltammetrie (LSV) wird in 0,5 M H2 . getestet SO4 bei einer Abtastrate von 5 mV s −1 ohne IR-Kompensation. Zusätzlich werden zyklische Voltammogramme (CV) von 0 bis 0,2 V (gegen RHE, in 0,5 M H2 SO4 ) mit Sweep-Raten von 20, 40, 60, 80, 100, 120 und 140 mV s −1 , bzw.
Ergebnisse und Diskussionen
Das Syntheseverfahren von Mo2 C/NPC-Hybrid ist in Abb. 1 dargestellt. Wir wählten Dopamin als Kohlenstoff- und Stickstoffquelle. Kommerzielle Massen-MoS2 wurde als Mo-Quelle und Selbsttemplate ausgewählt, wobei die Größe ~ 2 μm beträgt (Zusatzdatei 1:Abbildung S1a). Zunächst polymerisierte das Dopamin auf der Oberfläche von Bulk-MoS2 um ein MoS2 zu bilden @PDA Core-Shell-Struktur (Zusätzliche Datei 1:Abbildung S1b). Dann wird die Kern-Schale-Struktur MoS2 @PDA wurde karbonisiert, um einen N-dotierten Kohlenstofffilm zu bilden, der auf die Oberfläche von MoS2 . gewickelt war , die als MoS2 . signiert wurde @NC (Zusatzdatei 1:Bild S1c) [23, 24]. Schließlich wird die Mischung des so hergestellten MoS2 @NC und KOH wurden in einen Röhrenofen gegeben und umgesetzt, um das Endprodukt zu erhalten:Stickstoff-dotierte poröse Kohlenstoff-Nanoblätter gekoppelt mit Mo2 C-Nanopartikel (gespendet als Mo2 C/NPC) (Zusatzdatei 1:Abbildung S1d). Wenn MoS2 als Mo-Quelle abgetrennt wurde, bildet Dopamin einen PDA-Film auf der Oberfläche von MoS2 , das MoS2 diente als Selbsttemplat, um zu verhindern, dass Dopamin Mikrokügelchen bildet, und ein PDA-Film wurde erzeugt. Dies liegt daran, dass die Umwandlung von PDA zu N-dotiertem C weiterhin seine Morphologie behält [15]; wenn MoS2 mit KOH reagieren, können wir Kohlenstoff-Nanoblätter mit einer Länge von etwa 2 µm erhalten. Der Kohlenstoff in MoS2 @NC kann auch durch KOH aktiviert werden, um die porösen C-Nanoblätter zu erhalten. Die Bildung von Mo2 C/NPC kann basierend auf einer Reihe von Reaktionen vorgeschlagen werden. Der Prozess der KOH-Einfügung und Reaktion mit Kohlenstoff kann als KOH-Aktivierungsreaktion zusammengefasst werden, die chemische Reaktionsgleichung wird als 6KOH + 2C ↔ 2K + 3H2 . beschrieben + 2 K2 CO3 , und die K2 CO3 kann weiter in K2 . zerlegt werden O, CO2 , und CO [25]. Der Prozess der KOH-Aktivierungsreaktion kann nicht nur Kohlenstoffeinheiten korrodieren, um eine poröse Kohlenstoffstruktur zu erzeugen, sondern auch die Bildung von graphitischem Kohlenstoff fördern. Inzwischen könnte KOH MoS2 . ätzen Vorlage zur Herstellung von Mo2 C-Nanopartikel mit Diffusion von Schwefeldampf und Bildung von K2 S. Somit führen die Reaktionen zur Bildung von Mo2 C/NPC-Hybrid.
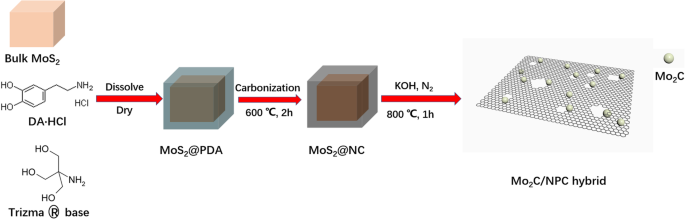
Schema des Verfahrens zur Herstellung von Mo2 C/NPC-Hybrid
Die kristalline Phasenzusammensetzung des Produkts wurde durch Röntgenbeugung untersucht (Fig. 2a). Ein breiter Peak bei 26° und der Peak bei 46,3° kann den (003)- und (012)-Ebenen des graphitischen Kohlenstoffs zugeschrieben werden. Die anderen Röntgenbeugungspeaks bei 34,3, 37,9, 39,39, 52,1, 61,5, 69,5,74,6 und 75,5° werden den Beugungen der (100), (002), (101), (102), (110 .) zugeschrieben ), (103), (112) und (201) Flächen des hexagonalen β-Mo2 C (JCPDS 35-0708). Darüber hinaus gibt es keine erkennbaren Verunreinigungen wie Molybdänmetall, Oxide, Sulfide oder andere Carbide, was auf die vollständige Umwandlung von kommerziellem MoS2 . hinweist bis Mo2 C. Die Ergebnisse der Raman-Spektroskopie in Fig. 2b bestätigten ferner, dass der so hergestellte Katalysator eine Mischung aus Molybdäncarbid und Graphit ist. Das Intensitätsverhältnis von G-Band zu D-Band, I G /Ich D> 1, legt nahe, dass der Kohlenstoff im Wesentlichen graphitisch ist [26]. Die Menge an Mo2 C im Endprodukt wurde basierend auf der thermogravimetrischen Analyse (TGA) in Luft zu ~~44 wt% gefunden (zusätzliche Datei 1:Abbildung S2). Die Stickstoffadsorptions-Desorptions-Isothermen wurden bei 77 K gemessen, um die spezifische Brunauer-Emmett-Teller (BET)-Oberfläche zu bewerten. Wie in Abb. 2c gezeigt, sind die Stickstoffadsorptions-Desorptions-Isothermen von Mo2 C/NPC zeigte eine Hystereseschleife vom H4-Typ, die für Materialien mit Mikromesoporen geeignet war. Darüber hinaus beträgt die durchschnittliche Porengröße der BJH-Desorption 3,23 nm und die spezifische BET-Oberfläche 1380 m 2 . g −1 , die die erfolgreiche Synthese der porösen Struktur offenbarte. Eine solche mikromeso-poröse Struktur aus Kohlenstoffmatrix mit ultrahoher Oberfläche soll ein ideales Elektrodenmaterial sein, das nicht nur einen offenen Raum und kurze Diffusionskanäle für Reaktanden bieten kann, sondern auch die Absorption von H +<. erleichtern kann /sup> und Desorption von H2 , was zu einer guten Masse-/Ladungsübertragungsfähigkeit führt.
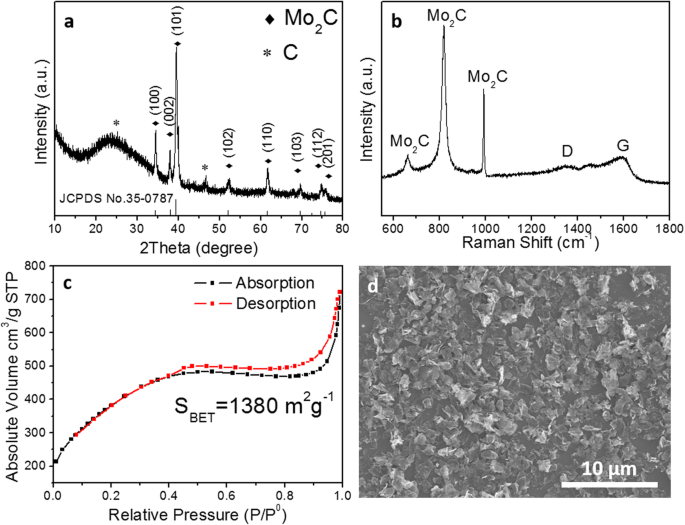
Die physikalische Charakterisierung von Mo2 C/NPC. a XRD-Muster, b Raman-Spektren, c N2 Adsorptions-Desorptions-Isotherme und d REM-Bild
Dann die Morphologie und Struktur des hierarchischen Mo2 C/NPC-Hybrid wurde durch SEM und TEM untersucht. Wie in Abb. 2d gezeigt, zeigt das REM-Bild mit geringer Vergrößerung diese zahlreichen gut dispergierten nanoblattartigen Strukturen mit einer durchschnittlichen Größe von 2 μm, was mit der Größe des Templats MoS2 . übereinstimmt . Die TEM-Bilder in Abb. 3a und c zeigten, dass das β-Mo2 C-Nanopartikel mit einer Größe von mehreren Nanometern bis 50 nm wurden auf Stickstoff-dotierten Kohlenstoff-Nanoblättern verankert. Die poröse Natur von Kohlenstoff-Nanoblättern ist aus TEM-Bildern in Abb. 3b ersichtlich [27]. Darüber hinaus zeigte das hochauflösende TEM-Bild in Fig. 3d die Gitterstreifen mit d-Abständen von 0,23 nm und 0,24 nm, die den (101) und (002) Ebenen von β-Mo2 . entsprechen C. Die poröse Struktur des tragenden Kohlenstoffs und die Kopplung von Mo2 C-Nanopartikel mit N-dotierten porösen C-Nanoblättern würden den Elektronentransfer von Molybdäncarbid auf Kohlenstoff erleichtern und dadurch die Effizienz des Katalysators erhöhen. Wie in Abb. 3e veranschaulicht, zeigte die energiedispersive Spektroskopie (EDS)-Analyse, dass die Nanoblätter aus Mo-, C- und N-Elementen bestanden, was die erfolgreiche Synthese von Mo2 . bestätigt C/NPC-Hybrid.
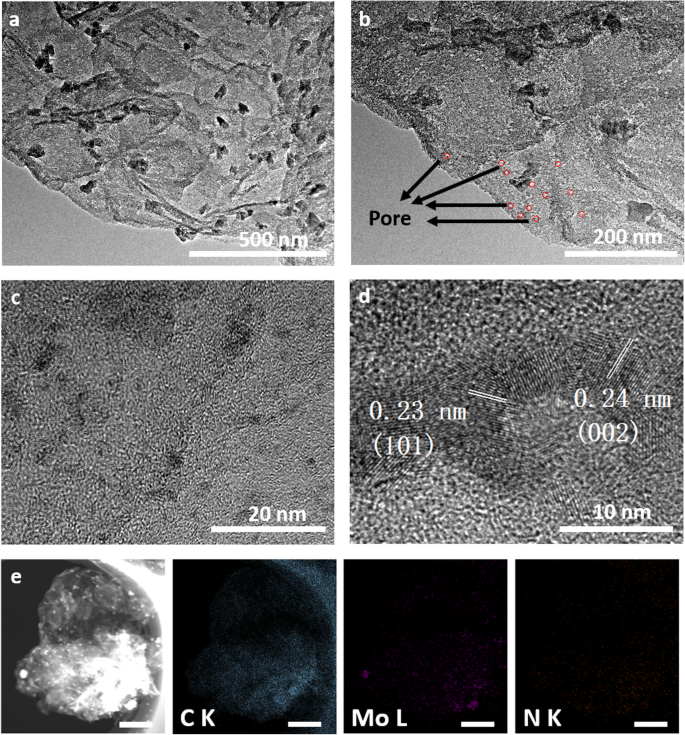
Die Morphologie von Mo2 C/NPC. a –d TEM- und HRTEM-Bilder in verschiedenen Vergrößerungen und e entsprechendes EDS-Element-Mapping von Mo2 C/NPC (Maßstab 500 nm)
Die Oberflächenzusammensetzung des so synthetisierten Mo2 C/NPC-Nanoblätter wurden durch XPS weiter aufgeklärt. Aus dem in Abb. 4a dargestellten Übersichtsspektrum können Elemente von Mo, C, N und O eindeutig identifiziert werden. Der C 1s XPS-Peak kann in drei Peaks mit den Zentren 284.6, 285.6 und 288.8 eV (Abb. 4b) eingepasst werden, die CC/C=C-, CN- bzw. C=O-Spezies zugeschrieben werden können [28, 29 ]. Der Mo 3d XPS-Peak kann in zwei Dubletts entfaltet werden (Abb. 4c). Einer ist bei einer Bindungsenergie von 228,6/231,6 eV zentriert und der andere ist 232,9/235,9 eV, was Mo2 . zugeschrieben werden kann C und oberflächenoxidiertes MoO3 , bzw. [14, 26, 29]. Die unvermeidliche Häufigkeit einer signifikanten Menge an Molybdänoxid kommt von der langsamen Oxidation an der Oberfläche von Molybdäncarbid an der Luft [30]. Darüber hinaus wurde berichtet, dass das auf der Oberfläche des Carbids gebildete Oxid die Aktivität des Carbids beibehalten kann. Der N 1s-Peak (Abb. 4d) bei Bindungsenergien von 398,4, 400,2 und 401,4 eV kann Pyridin-, Pyrrol- bzw. quartären N-Atomen zugeschrieben werden [24, 29]. Ein früherer Bericht hat bewiesen, dass die N-Dotierstoffe im Kohlenstoff den Elektronentransferprozess (Mo2 C→C→N), was zu einer Verstärkung der Synergie zwischen Mo2 . führt C- und N-Dotierstoffe in Kohlenstoff [18].
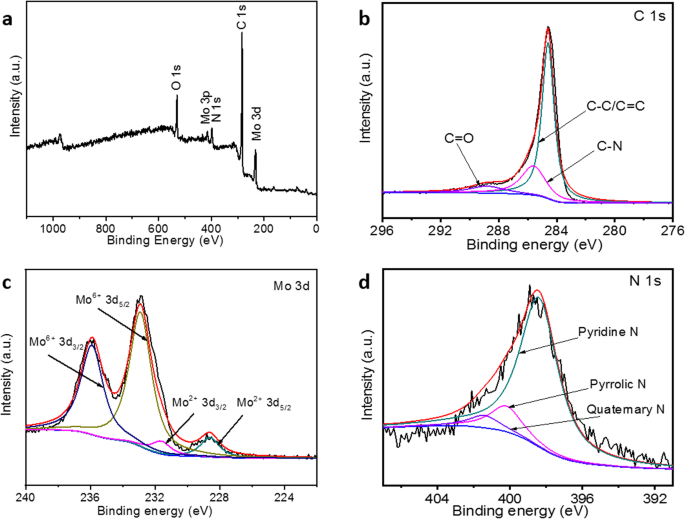
XPS-Umfragespektrum (a ) und hochauflösender XPS-Scan von C1s (b ), Mo3d (c ) und N1 s (d ) von Mo2 C/NPC
Die elektrokatalytische HER-Aktivität des Mo2 C/NPC wurde erstmals in 0,5 M H2 . untersucht SO4 . Zum Vergleich das ursprüngliche kommerzielle MoS2 (c-MoS2 ), N-dotiertes poröses C (NPC) und 20 Gew.-% Pt/C wurden ebenfalls unter Verwendung der gleichen Beladungsmenge getestet. Abbildung 5a vergleicht die entsprechenden Polarisationskurven. Wie erwartet, sowohl der NPC als auch das kommerzielle MoS2 zeigte eine sehr begrenzte HER-Aktivität mit einem beginnenden Überpotential von 354 mV bzw. 289 mV, während die Mo2 C/NPC hatte ein anfängliches Überpotential von 93 mV, viel niedriger als das von NPC und c-MoS2 . Das Überpotential des Mo2 C/NPC bei einer Stromdichte von 10 mA cm −2 ist 166 mV, viel niedriger als bei NPC und dem ursprünglichen c-MoS2 und vergleichbar mit dem des Mo2 C/C-Hybride in anderen Arbeiten [20, 31]. Um die HER-Kinetik der Katalysatoren zu untersuchen, wurden Tafel-Plots an die Tafel-Gleichung (η = a + b log (j )), wobei b ist die Tafel-Steigung. Wie in Fig. 5b gezeigt, ist die Tafel-Steigung von Mo2 C/NPC wurde mit 68 mV dec −1 . berechnet , viel niedriger als die von c-MoS2 (184 mV dez −1 ) und NPC (296 mV dez −1 ), was darauf hindeutet, dass der Desorptionsschritt auf den Oberflächen des Mo2 . effizient war C/NPC-Katalysatoren. Die Tafel-Steigung von Mo2 C/NPC-Hybrid liegt im Bereich von 40–120 mV dec −1 , was bedeutet, dass die HER auf der Mo2 . aufgetreten ist Die C/NPC-Oberfläche folgt einem Volmer-Heyrovsky-Mechanismus [32]. Basierend auf der Tafel-Analyse ist die Austauschstromdichte (j 0 ) von Mo2 C/NPC wurde mit 37,4 μA cm −2 . berechnet , das viele in der Literatur beschriebene unedle HER-Elektrokatalysatoren übertrifft (wie in Zusatzdatei 1:Tabelle S1 illustriert) [33,34,35]. Um die elektrochemisch aktive Oberfläche (ECSA) von Mo2 . abzuschätzen C/NPC unter den Arbeitsbedingungen berechneten wir die Doppelschichtkapazität (C dl ) aus zyklischen Voltammetrie (CV)-Kurven bei verschiedenen Abtastraten in Abb. 5c. Wie im Einschub von Fig. 5c gezeigt, zeigte die lineare Korrelation der Stromdichte bei 0,1 V gegenüber der Abtastrate, dass der C dl von Mo2 C/NPC beträgt 102,4 mF cm −2 . Wenn wir einen Standardwert von 60 μF/cm 2 . annehmen , die ECSA von Mo2 C/NPC wird auf ∼ 558 m 2 . geschätzt /g (die Berechnung ist in Zusatzdatei 1:Abbildung S3 dargestellt). Ein so hoher ECSA wird sowohl von Mo2 C und der Kohlenstoffträger. Da Kohlenstoff viel leichter ist, wird geschätzt, dass das N-dotierte poröse C die meisten ECSAs ausmacht [26] und es stimmt mit der spezifischen BET-Oberfläche überein, was somit belegt, dass der größte Teil des aktiven Mo2 C-Oberfläche ist elektrochemisch zugänglich.
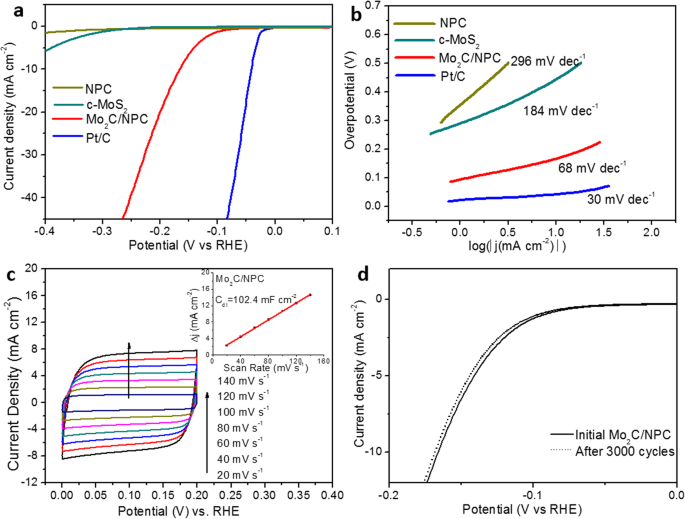
Elektrochemische Messungen von Mo2 C/NPC-Hybrid für die HER-Elektrokatalyse in 0,5 M H2 SO4 . a Polarisationskurven und b Tafel-Plots von Mo2 C/NPC im Vergleich mit Pt/C-Benchmark, c-MoS2 , und NPC. c CV-Kurven von Mo2 C/NPC unter verschiedenen Scanraten von 20 bis 140 mV/s. Der Einschub veranschaulicht die Auftragung des kapazitiven Stroms bei 0,1 V gegen die Abtastrate. d Polarisationskurven von Mo2 C/NPC vor und nach 3000 potentiellen Zyklen
Neben der HER-Aktivität ist die Stabilität ein weiterer entscheidender Faktor, um einen Katalysator zu bewerten. Es wurde eine zyklische Langzeitvoltammetrie durchgeführt, um die Stabilität des Mo2 . zu messen C/NPC in 0,5 M H2 SO4 . Die HER-Polarisationskurven in Abb. 5d für das Mo2 C/NPC zeigen nach 3000 Zyklen nur einen Verlust von 2 mV, was auf eine vernachlässigbare Stabilität des Katalysators hinweist. Die chronoamperometrische Reaktionskurve von Mo2 C/NPC bei der Überspannung von − 0,166 V gegenüber dem RHE wurde in der Zusatzdatei 1 dargestellt:Abbildung S4. Basierend auf der obigen elektrochemischen Studie ist die bemerkenswerte elektrokatalytische Leistung von Mo2 C/NPC-Nanoblätter können auf folgende Faktoren zurückgeführt werden:(1) Die hohe spezifische Oberfläche der Katalysatoren würde zu mehr aktiven Zentren für H + . führen Absorption und die gute Leitfähigkeit des Trägersubstrats würden die Elektronenübertragung verbessern; (2) die Kopplung von β-Mo2 C-Nanopartikel und N-dotierte poröse C-Nanoblätter würden den Kontakt des Katalysators mit dem Elektrolyten vergrößern und den Ladungs- und Massentransfer erleichtern; und (3) die dotierenden N-Atome können nicht nur besser mit H + . wechselwirken als C-Atome, sondern modifizieren auch die elektronischen Strukturen benachbarter Mo- und C-Atome, wodurch Mo2 C/NPC ein hocheffizienter Katalysator.
Schlussfolgerungen
Zusammenfassend lässt sich sagen, dass eine neuartige Strategie zur Herstellung von hierarchischem Mo2 C/NPC-Hybrid wurde durch eine KOH-Aktivierungsmethode entwickelt. Kommerzielles MoS2 wurde als Mo-Quelle und Selbsttemplat verwendet, während Dopamin als C- und N-Quelle verwendet wurde. MoS2 wurde mit KOH herausgeätzt, um einen Mo-Vorläufer herzustellen, und das carbonisierte PDA wurde durch KOH korrodiert, um ein poröses Graphitsubstrat zu bilden. Die ausgezeichnete HER-Aktivität von Mo2 C/NPC-Hybrid mit dem Überpotential von 166 mV bei 10 mA cm −2 , das beginnende Überpotential von 93 mV, Tafel-Steigung von 68 mV dec −1 , und die hervorragende Langzeit-Zyklusstabilität wird dem Stickstoff-Dotierungsgehalt, dem porösen leitfähigen Substrat, der Fülle an aktiven Zentren und der starken Wechselwirkung zwischen Mo2 . zugeschrieben C und graphitischer Kohlenstoff. Diese effektive Methode kann auf das Design und die Herstellung anderer Carbidverbindungen mit hoher spezifischer Oberfläche für verschiedene elektrokatalytische Anwendungen angewendet werden.
Verfügbarkeit von Daten und Materialien
Alle Daten sind uneingeschränkt verfügbar.
Abkürzungen
- c-MoS2 :
-
Kommerzielles MoS2
- IHR:
-
Wasserstoffentwicklungsreaktion
- HRTEM:
-
Hochauflösende Transmissionselektronenmikroskopie
- Mo2 C/NPC:
-
Stickstoffdotierte poröse Kohlenstoffnanoblätter gekoppelt mit Mo2 C-Nanopartikel
- MoS2 @NC:
-
Auf die Oberfläche von MoS2 . gewickelter Stickstoff-dotierter Kohlenstoffilm
- NPC:
-
Stickstoffdotierter poröser Kohlenstoff
- PDA:
-
Polydopamin
- Pt/C:
-
Platin/Kohlenstoff-Katalysator
- RHE:
-
Umkehrbare Wasserstoffelektrode
- TGA:
-
Thermogravimetrische Analyse
Nanomaterialien
- MoS2 mit kontrollierter Dicke für die elektrokatalytische Wasserstoffentwicklung
- S, N codotierte Graphen-Quantenpunkt/TiO2-Komposite für eine effiziente photokatalytische Wasserstofferzeugung
- Elektrogesponnene Polymer-Nanofasern, dekoriert mit Edelmetall-Nanopartikeln für die chemische Sensorik
- Kohlenstoff-Nanodots als Dual-Mode-Nanosensoren für den selektiven Nachweis von Wasserstoffperoxid
- Monodisperse Kohlenstoff-Nanosphären mit hierarchischer poröser Struktur als Elektrodenmaterial für Superkondensatoren
- Erforschung des Zr-Metall-organischen Gerüsts als effizienter Photokatalysator für die Wasserstoffproduktion
- Hierarchische Heterostruktur von ZnO@TiO2-Hohlkugeln für eine hocheffiziente photokatalytische Wasserstoffentwicklung
- PtNi-Legierungs-Cokatalysator-Modifikation des Eosin-Y-sensibilisierten g-C3N4/GO-Hybrids für eine effiziente photokatalytische Wasserstoffentwicklung mit sichtbarem Licht
- Verbesserte photokatalytische Wasserstoffentwicklung durch Laden von Cd0.5Zn0.5S-QDs auf poröse Ni2P-Nanoblätter
- Gut ausgerichtete TiO2-Nanoröhren-Arrays mit Ag-Nanopartikeln für den hocheffizienten Nachweis von Fe3+-Ionen



