Hierarchische Heterostruktur von ZnO@TiO2-Hohlkugeln für eine hocheffiziente photokatalytische Wasserstoffentwicklung
Zusammenfassung
Das rationale Design und die Herstellung hierarchischer Nanoarchitekturen sind entscheidend für eine verbesserte photokatalytische Wasserstoffentwicklungsreaktion (HER). Hierin gut integriertes hohles ZnO@TiO2 Heteroübergänge wurden durch eine einfache hydrothermale Methode erhalten. Diese einzigartige hierarchische Heterostruktur verursacht nicht nur Mehrfachreflexionen, die die Lichtabsorption verbessern, sondern verbessert auch die Lebensdauer und den Transfer photogenerierter Ladungsträger aufgrund der auf dem ZnO-TiO2 . erzeugten Potentialdifferenz Schnittstelle. Als Ergebnis im Vergleich zu blankem ZnO und TiO2 , das ZnO@TiO2 Komposit-Photokatalysator zeigte eine höhere Wasserstoffproduktion von bis zu 0,152 mmol h −1 g −1 unter simuliertem Sonnenlicht. Darüber hinaus wurde auch auf dem ZnO@TiO2 . eine stark wiederholte Photostabilität beobachtet Komposit-Photokatalysator auch nach einem Dauertest von 30 h. Es wird erwartet, dass dieses kostengünstige, ungiftige und leicht verfügbare ZnO@TiO2 Katalysator könnte vielversprechendes Potenzial in photokatalytischem H2 . aufweisen um den zukünftigen Kraftstoffbedarf zu decken.
Hintergrund
Wasserstoff (H2 .) ), eine der wichtigsten sauberen und nachhaltigen Energiequellen, gilt als vielversprechende alternative Energiequelle zur Deckung des zukünftigen Brennstoffbedarfs [1,2,3,4,5]. Seit der Entdeckung des photoelektrochemischen (PEC) Wasserspaltungssystems durch Fujishima und Honda in den 1970er Jahren [6] ist die Produktion von H2 basierend auf TiO2 Halbleiter-Photokatalysatoren, die Sonnenlicht verwenden, haben zunehmende Aufmerksamkeit auf sich gezogen. Die praktische Anwendung von einzelnem bloßem TiO2 in der Industrie ist aufgrund der schnellen Rekombination photogenerierter Elektronen und Löcher an der Oberfläche von TiO2 . immer noch eine Herausforderung führt zu einer geringen Quanteneffizienz. Bis heute wurden viele Anstrengungen unternommen, um TiO2 . zu entwickeln -basierte Komposit-Photokatalysatoren, um die oben genannten Probleme zu lösen, wie die Kopplung mit einem anderen Halbleiter, das Dotieren von Übergangsmetallionen oder Nichtmetallatomen usw. [7,8,9]. Insbesondere die Bildung von Halbleiter-Halbleiter-Heteroübergängen mit passenden Bandpotentialen ist ein effektiver Weg, um die Ladungsrekombination zu verhindern und die Lebensdauer der Ladungsträger zu erhöhen [10,11,12].
Unter den verschiedenen Halbleitern wird auch ZnO wegen seiner identischen Eigenschaften von TiO2 . intensiv untersucht mit Ungiftigkeit, Billigkeit, hoher Effizienz und chemischer Stabilität [13, 14]. Da das Leitungsband (CB) und Valenzband (VB) von ZnO über denen von TiO2 . liegen , werden die photogenerierten Elektronen in ZnO auf TiO2 . übertragen sobald ein Heteroübergang zwischen TiO2 . gebildet wurde und ZnO. Diese Art von ZnO@TiO2 Komposit-Heteroübergang wird von der Trennung photogenerierter Elektron-Loch-Paare profitieren, wodurch mehr Elektronen auf dem TiO2 . angesammelt werden die mit H2 . reagieren wird O um H2 . zu erzeugen [15,16,17].
Zusätzlich zu den oben besprochenen beeinflussen auch geometrische Formen und Morphologien der Photokatalysatoren die Leistung der Wasserstoffentwicklungsreaktion (HER) stark [18, 19, 20]. Es wurde berichtet, dass die Beugungen an den Hohlkugeln und die Mehrfachreflexionen aufgrund der Schalenstruktur die Effektivität der Lichtnutzung erhöhen würden [21]. Zum Beispiel stellte die Gruppe von Li hydrierte käfigartige Hohlkugeln aus Titanoxid her, die viel höhere HER-Aktivitäten aufwiesen als feste Strukturen [22]. Darüber hinaus haben die kugelförmigen Hohlstrukturen die Vorteile einer großen spezifischen Oberfläche, verkürzten Transportlängen für Ladungsträger und einer guten chemischen und thermischen Stabilität, die alle zu der ausgezeichneten photokatalytischen Fähigkeit beitragen [23]. Der Großteil der Forschung konzentrierte sich jedoch auf die Herstellung von Verbundhohlkugeln durch Dotieren von Übergangselementen wie Ce-ZnO [24], Ni-ZnO [25], Ag-TiO2 [26], Au-TiO2 [27] usw. Nach unserem besten Wissen haben nur wenige Studien über die Synthese geschlossener, vollständiger und intakter Hohlkugeln berichtet, die aus porösen Partikeln aus gemischten Metalloxiden bestehen. Trotzdem werden die meisten dieser Verbundwerkstoffe beim photokatalytischen Abbau organischer Schadstoffe eingesetzt, nicht jedoch bei der photokatalytischen Wasserstoffproduktion.
In diesem Artikel berichteten wir über eine einfache Methode zur Synthese von hierarchisch porösem ZnO@TiO2 zusammengesetzte Mikrohohlkugeln und applizierte sie in der photokatalytischen H2 . Die Hohlkugeln verbesserten die Lichtabsorption durch Mehrfachreflexionen, gleichzeitig wurden auch die Lebensdauer und Übertragungsrate photogenerierter Ladungsträger aufgrund der am ZnO-TiO2 . erzeugten Potentialdifferenz verbessert Schnittstelle. Das Ergebnis zeigte, dass das ZnO@TiO2 Komposit-Photokatalysator zeigte verbessertes H2 Entwicklungsrate, verglichen mit dem bloßen ZnO und TiO2 . Darüber hinaus ist der Mechanismus des photokatalytischen H2 auf dem ZnO@TiO2 Verbundhohlkugeln wurde ausführlich besprochen.
Methoden
Synthese des hierarchischen ZnO@TiO2 Hohlkugeln
Die Herstellung von ZnO@TiO2 Composites basierte auf einer sehr einfachen einstufigen templatfreien Hydrothermalmethode bei Umgebungsbedingungen. In einem typischen Verfahren werden 0,015 Mol Ti(SO4 )2 , 0,015 Mol Zn(NO3 )2 ·6H2 O, 0,015 Mol NH4 F und 0,06 Mol CO(NH2 .) )2 wurden mit 50 ml entionisiertem Wasser in ein Becherglas gegeben. Nach 60 Minuten Rühren wurde die Mischungslösung in einen mit Teflon ausgekleideten Edelstahlautoklaven überführt und in einem Elektroofen 12 h auf 180 °C erhitzt. Danach wurde der weiße Niederschlag viermal gründlich mit Ethanol gewaschen und dann 12 h bei 60 °C getrocknet, um ZnO@TiO2 . zu erhalten Heterostrukturen. Zum Vergleich blankes TiO2 und ZnO wurden unter den gleichen Bedingungen hergestellt.
Synthese von Pt–ZnO@TiO2 Proben
In einem typischen Syntheseprozess von Pt–ZnO@TiO2 Proben, das ZnO@TiO2 Hohlkugeln wurden in einen Behälter gegeben, der 10 Vol. % Triethanolamin und H2 . enthielt PtCl6 Lösung. Dann wurde das System 30 Minuten lang mit Stickstoff durchperlt, um die Luft zu entfernen. Schließlich wurde das Pt in situ auf dem ZnO@TiO2 . abgeschieden Hohlkugeln unter einer vollen Lichtbogenbestrahlung (λ> 300 nm) für 2 h. Der Pt-Gehalt kann durch die Konzentration von H2 . eingestellt werden PtCl6 und die Reaktionszeit, die durch induktiv gekoppeltes Plasma (ICP, PE5300DV) bestimmt wurde.
Charakterisierung
Die Morphologie von ZnO@TiO2 Heterostrukturen wurden mittels Feldemissions-Rasterelektronenmikroskop (FESEM, Hitachi, Japan), Transmissionselektronenmikroskopie (TEM, Tecnai F20), ringförmigem Hochwinkel-Dunkelfeld-Scanning-TEM (STEM, Tecnai F20) und hochauflösendem TEM (HRTEM, Tecnai F20). Die Abbildungsbilder der energiedispersiven Röntgenspektroskopie (EDS) wurden auf einem analytischen Mikroskop mit atomarer Auflösung vom Typ Tecnai G2 F20 S-TWIN aufgenommen. Die Kristallphaseneigenschaften der Proben wurden mit einem Röntgendiffraktometer mit Cu-K-Strahlung (XRD, M21X, MAC Science Ltd., Japan) charakterisiert. Die spezifischen BET-Oberflächen wurden mit einem Belsorp-mini II-Analysator (Japan) gemessen.
Photoelektrochemische Messungen
Photostromstudien wurden an einer elektrochemischen Arbeitsstation CHI 660D unter Verwendung einer Drei-Elektroden-Konfiguration durchgeführt, bei der fluordotierte Zinnoxid-(FTO)-Elektroden mit den Proben als Arbeitselektrode, Pt als Gegenelektrode und einer gesättigten Kalomelelektrode (SCE) als Referenz abgeschieden wurden . Der Elektrolyt war 0,35 M/0,25 M Na2 . S–Na2 SO3 wässrige Lösung. Zur Herstellung der Arbeitselektrode wurden 0,25 g der Probe mit 0,06 g Polyethylenglykol (PEG, Molekulargewicht 20.000) und 0,5 ml Ethanol gemahlen, um eine Aufschlämmung herzustellen. Dann wurde die Aufschlämmung auf ein 1 × 4 cm großes FTO-Glas durch die Rakeltechnik verteilt und dann an der Luft trocknen gelassen. Als simulierte Sonnenlicht-Bestrahlungsquelle diente eine 300 W-Xenon-Bogenlampe (Perfectlight, PLS-SXE 300C, Peking, China). Die einfallende Lichtintensität wurde auf 100 mW/cm 2 . eingestellt gemessen von NOVA Oriel 70260 mit einem Thermodetektor.
Photokatalytische Wasserstoffproduktionstests
Experimente zur photokatalytischen Wasserstofferzeugung wurden in einem verschlossenen Quarzkolben bei Umgebungstemperatur und unter Atmosphärendruck durchgeführt. Als Lichtquelle zum Auslösen der photokatalytischen Reaktion wurde eine 300 W-Xenonbogenlampe (Perfect Light, PLS-SXE 300C, Peking, China) verwendet. Das entwickelte H2 wurden von einem H2 . gesammelt und online analysiert -Solarsystem (Beijing Trusttech Technology Co., Ltd.) mit einem Gaschromatogramm, ausgestattet mit einem Wärmeleitfähigkeitsdetektor (WLD), einer 5A-Molekularsiebsäule und Stickstoff als Trägergas. Alle photokatalytischen Experimente mit mehr als 100 mg Photokatalysator wurden in einer wässrigen Lösung mit H2 . durchgeführt O (80 ml) und Alkohol (20 ml). Vor der Bestrahlung wurde das System durch Einperlen von Stickstoff für 15 Minuten entlüftet. Während der photokatalytischen Reaktion war der Reaktor dicht verschlossen, um einen Gasaustausch zu vermeiden.
Ergebnisse und Diskussion
Die Größe und Morphologie des so hergestellten ZnO@TiO2 Hohlkugeln wurden in Abb. 1 gezeigt. Abb. 1a zeigt, dass die Probe eine einheitliche kugelförmige Morphologie mit einem mittleren Durchmesser von etwa 1,45 μm gemäß der Nanopartikelgrößenverteilung (Einschub von Abb. 1a) hat. Abbildung 1b zeigt eine einzelne zerbrochene Kugel, was darauf hindeutet, dass die vorbereitete Probe eine hohle Struktur aus kleinen Partikeln ist. Ein TEM-Bild wurde außerdem verwendet, um die Struktur von ZnO@TiO2 . zu bestätigen Hohlkugeln. Der Farbwechsel des ZnO@TiO2 Kugeln in der Mitte und im äußeren Bereich waren dunkel bzw. hell, was das ZnO@TiO2 . bestätigte Kugeln hatten eine hohle Struktur (Abb. 2a). Eine stark vergrößerte Ansicht in Abb. 2b zeigt auch, dass die Oberfläche der Hohlkugeln rau war, die aus Untereinheiten von Nanopartikeln aufgebaut waren, was zur Bildung der hierarchischen Heterostruktur von ZnO@TiO2 . führte Hohlkugeln. Die Elementkarten in Abb. 2(d–f) wurden verwendet, um die Elementverteilung im ZnO@TiO2 . zu bestätigen Hohlkugeln. Es ist ersichtlich, dass Zn, Ti und O gleichmäßig in ZnO@TiO2 . verteilt waren Hohlkugeln.

a Ein schwach vergrößertes REM-Bild von ZnO@TiO2 Hohlkugeln; der Einschub zeigt die statistische Analyse der Durchmesserverteilung der Proben. b Ein stark vergrößertes SEM-Bild eines einzelnen gebrochenen ZnO@TiO2 Kugel
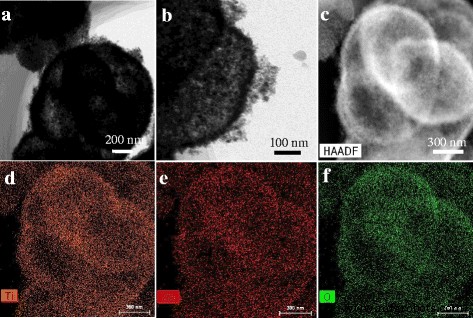
a TEM, b vergrößertes TEM und c STEM-Bilder von ZnO@TiO2 Hohlkugeln; Entsprechende EDS-Elementarabbildungen von c zeigt die gleichmäßige Verteilung von d . an Ti, e Zn und f O bzw.
HRTEM-Bilder in Abb. 3 bestätigten die Heteroübergangsstruktur von ZnO@TiO2 Hohlkugeln. Die ausgewählten Bereiche in Abb. 3a, die durch ein weißes Quadrat markiert sind, wurden in Abb. 3b–d vergrößert, entsprechend ZnO, TiO2 , und ZnO@TiO2 Heteroübergang. Die Gitterabstände von 0,28 und 0,35 nm entsprachen den (100)-Ebenen von Wurtzit ZnO und (101)-Ebenen von Anatas-TiO2 , wie in Abb. 3b, c gezeigt. Abbildung 3d zeigt einen deutlichen Übergang von der Wurtzit-ZnO-Phase zu Anatas-TiO2 Phase, die bestätigte, dass der Heteroübergang an der Grenzfläche zwischen ZnO und TiO2 . gebildet wurde . Eine solche Heteroübergangsstruktur kann den photoangeregten Elektronentransfer für eine verbesserte photokatalytische Aktivität stark fördern.

a HRTEM-Bilder von ZnO@TiO2 Hohlkugeln. b , c , und d sind verstärkte HRTEM-Bilder des angegebenen quadratischen Teils in a , was auf ZnO, TiO2 . hinweist , und ZnO@TiO2 Heterojunctions bzw.
Die Porenstruktureigenschaften von ZnO, TiO2 , und ZnO@TiO2 Proben wurden weiter durch die N2 . bestimmt Adsorptions-Desorptions-Isothermen und entsprechende Diagramme der Barrett-Joyner-Halenda (BJH)-Porengrößenverteilung (Abb. 4). Alle Proben zeigten eine Typ-IV-Isotherme mit Hystereseschleife bei hohem Relativdruck (P /P 0> 0.7), was die Existenz mesoporöser Strukturen gemäß der Klassifikation der International Union of Pure and Applied Chemistry (IUPAC) belegt. Der Einschub von Abb. 4 sind Diagramme der BJH-Porengrößenverteilung, die weiter darauf hindeuten, dass alle Proben mesoporöse Strukturen aufweisen. Die berechneten BET-Oberflächen des ZnO@TiO2 Mikrokugel war ungefähr 102 m 2 g −1 , das viel größer war als das von ZnO (23 m 2 g −1 ) und TiO2 (35 m 2 g −1 ). Daraus kann die Einführung von ZnO in TiO2 . geschlossen werden um das ZnO@TiO2 . zu bilden Hohlkugeln könnten die Oberfläche stark vergrößern, obwohl alle Proben mesoporöse Strukturen aufweisen. Die größeren Oberflächen von ZnO@TiO2 Hohlkugeln würden mehr Plätze für verbessertes katalytisches H2 . bieten Leistung.
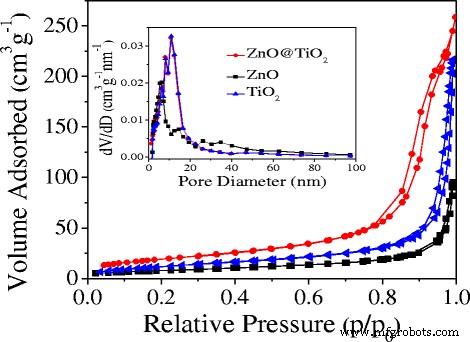
N2 Adsorptions-Desorptions-Isothermen und der Einschub zeigen die entsprechenden Porengrößenverteilungskurven
Die photokatalytische Fähigkeit der so hergestellten Proben wurde durch Photostrom und photokatalytisches H2 . bewertet testet. Wie in Abb. 5a gezeigt, ist das ZnO@TiO2 Hohlkugeln lieferten die höchste Photostromdichte von 3,38 mA/cm 2 , das mehr als 2,61 war, 2,17-mal höher als das von ZnO und TiO2 , bzw. Diese Ergebnisse bedeuten die stärkere Fähigkeit zur Erzeugung von Ladungsträgern und eine verbesserte Trenneffizienz von ZnO@TiO2 Hohlkugeln. Mit Ausnahme der Wasserstoffproduktionsrate von ZnO@TiO2 Hohlkugeln erreichten 0,152 mmol h −1 g −1 , höher als 0,039 mmol h −1 g −1 von ZnO und 0,085 mmol h −1 g −1 von TiO2 (Abb. 5b). Pt als hocheffizienter Edelmetall-Cokatalysator wird häufig für H2 . verwendet Evolutionsreaktion in der Literatur [8, 11]. Eine Reihe von Pt–ZnO@TiO2 mit unterschiedlichen Pt-Gehalten hergestellt und in Abb. 5c verglichen. Es wurde gezeigt, dass das Laden von Pt auf ZnO@TiO2 Hohlkugeln könnten das H2 . deutlich verbessern Evolutionsaktivität und die Probe mit 1,5 Atom-% Pt zeigt den höchsten H2 Evolutionsrate. Abbildung 5d zeigt, dass ZnO@TiO2 Hohlkugeln behielten in den fünf Reaktionszyklen 30 h lang ihre ursprüngliche photokatalytische Aktivität ohne merklichen Abbau bei, was die außergewöhnliche photokatalytische Stabilität demonstriert.
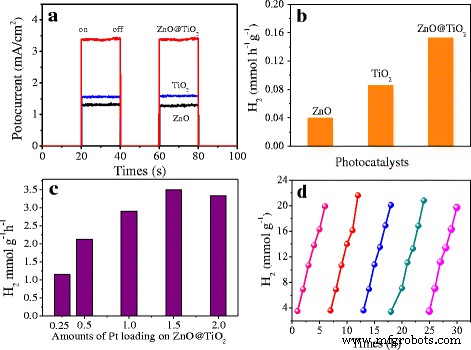
a Photostrom-Antworten und b photokatalytisches H2 Entwicklung von nacktem ZnO, nacktem TiO2 , und ZnO@TiO2 Heterojunctions. c Photokatalytisches H2 Entwicklung über Pt–ZnO@TiO2 Heterojunctions-Komposite mit unterschiedlichen Gewichtsverhältnissen von Pt. d Photokatalytische Stabilität von ZnO@TiO2 Hohlkugeln. Alle Messungen wurden unter einer simulierten Sonnenlicht-Bestrahlungsquelle mit einer Intensität von 100 mW/cm 2 . durchgeführt
Für die verbesserte HER-Aktivität von ZnO@TiO2 . wurde ein photokatalytischer Mechanismus vorgeschlagen Hohlkugeln, wie in Abb. 6 gezeigt. Unter simulierter Sonneneinstrahlung werden die Elektronen von ZnO und TiO2 wurden von ihren Valenzbändern (VB) zu ihren Leitungsbändern (CB) angeregt. Da das Leitungsband (CB) und Valenzband (VB) von ZnO positiver waren als die von TiO2 , die von ZnO auf TiO2 übertragenen photogenerierten Elektronen durch die intimen Grenzflächenkontakte [16]. Dann, je mehr akkumulierte Elektronen auf dem TiO2 reagiert mit H2 O zum Erzeugen von H2 für das höhere photokatalytische H2 Rate (wie rechts in Abb. 6 gezeigt). Gleichzeitig werden die photogenerierten Löcher in der VB von TiO2 wanderten zu ZnO, die vom Opfermittel eingefangen wurden, um das thermodynamische Gleichgewicht aufrechtzuerhalten. Darüber hinaus profitieren die hierarchischen Hohlkugeln von Lichtstreuung und Mehrfachreflexionen unter ZnO@TiO2 Komposit-Photokatalysator, der die Effektivität der Lichtnutzung erhöhen würde [10, 21, 22]. Somit würden aufgrund der erhöhten effektiven Photonenpfadlänge mehr freie Elektronen und Löcher erzeugt [21, 22], was zu einer höheren HER-Effizienz führt (wie in Abb. 6 links gezeigt).
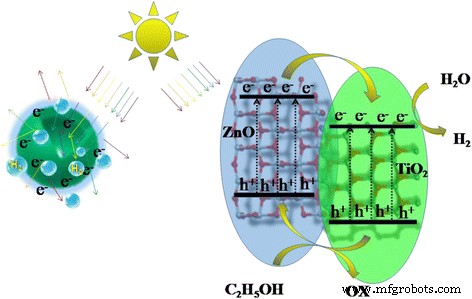
Schematische Darstellung des vorgeschlagenen HER-Mechanismus von ZnO@TiO2 Hohlkugeln
Schlussfolgerungen
Zusammenfassend lässt sich sagen, dass die hierarchische Heterostruktur von ZnO@TiO2 Hohlkugeln wurde erfolgreich über ein einfaches hydrothermales Verfahren hergestellt. Im Vergleich zu blankem ZnO und TiO2 , das ZnO@TiO2 Komposit-Photokatalysator zeigte eine hohe Wasserstoffproduktion von bis zu 0,152 mmol h −1 g −1 unter simuliertem Sonnenlicht. Es wird angenommen, dass eine hierarchische Heterostruktur die Oberfläche vergrößert, was mehr aktive Zentren für eine effektive HER belegt und gleichzeitig die Lebensdauer und den Transfer von photogenerierten Ladungsträgern aufgrund der auf dem ZnO-TiO2 . erzeugten Potentialdifferenz verbessert Schnittstelle. Darüber hinaus ist das ZnO@TiO2 Der zusammengesetzte Photokatalysator zeigte selbst nach fünfmaliger Wiederverwendung eine gute Haltbarkeit. Diese Arbeit zeigte gute Aussichten für photokatalytisches H2 Evolution aus Wasser basierend auf der rationellen Nutzung und Herstellung von hochaktiver, kostengünstiger und chemischer Stabilität von ZnO und TiO2 .
Nanomaterialien
- Hocheffizientes Spülmittel zum Blasformen von Polyolefinen
- Hochreflektierende Dünnschicht-Optimierung für Vollwinkel-Mikro-LEDs
- MoS2 mit kontrollierter Dicke für die elektrokatalytische Wasserstoffentwicklung
- S, N codotierte Graphen-Quantenpunkt/TiO2-Komposite für eine effiziente photokatalytische Wasserstofferzeugung
- Erforschung des Zr-Metall-organischen Gerüsts als effizienter Photokatalysator für die Wasserstoffproduktion
- PtNi-Legierungs-Cokatalysator-Modifikation des Eosin-Y-sensibilisierten g-C3N4/GO-Hybrids für eine effiziente photokatalytische Wasserstoffentwicklung mit sichtbarem Licht
- Verbesserte photokatalytische Wasserstoffentwicklung durch Laden von Cd0.5Zn0.5S-QDs auf poröse Ni2P-Nanoblätter
- Herstellung hierarchischer ZnO@NiO-Kern-Schale-Heterostrukturen für verbesserte photokatalytische Leistung
- Einbau nanostrukturierter Kohlenstoff-Verbundmaterialien in Gegenelektroden für hocheffiziente farbstoffsensibilisierte Solarzellen
- Ein neuartiger magnetoelastischer Nanobiosensor für den hochempfindlichen Nachweis von Atrazin



