Grüne Kompetenz bei der Synthese und Stabilisierung von Kupfernanopartikeln:katalytische, antibakterielle, zytotoxische und antioxidative Aktivitäten
Zusammenfassung
Kupfer-Nanopartikel (CuNPs) sind aufgrund ihrer außergewöhnlichen Eigenschaften wie hohes Oberflächen-Volumen-Verhältnis, hohe Streckgrenze, Duktilität, Härte, Flexibilität und Steifigkeit von großem Interesse. CuNPs zeigen katalytische, antibakterielle, antioxidative und antimykotische Aktivitäten zusammen mit Zytotoxizität und Antikrebseigenschaften in vielen verschiedenen Anwendungen. Viele physikalische und chemische Methoden wurden verwendet, um Nanopartikel zu synthetisieren, einschließlich Laserablation, Mikrowellen-unterstützter Prozess, Sol-Gel, Co-Präzipitation, gepulste Drahtentladung, Vakuumdampfabscheidung, Hochenergiebestrahlung, Lithographie, mechanisches Fräsen, photochemische Reduktion, Elektrochemie , Elektrospray-Synthese, hydrothermale Reaktion, Mikroemulsion und chemische Reduktion. Die Phytosynthese von Nanopartikeln wurde aufgrund der geringen Zytotoxizität, der wirtschaftlichen Aussichten, der Umweltfreundlichkeit, der verbesserten Biokompatibilität und der hohen antioxidativen und antimikrobiellen Aktivität als wertvolle Alternative zu physikalischen und chemischen Methoden vorgeschlagen. Die Übersicht erklärt Charakterisierungstechniken, ihre Hauptrolle, Einschränkungen und Empfindlichkeit bei der Herstellung von CuNPs. Ein Überblick über Techniken, die bei der Synthese von CuNPs verwendet werden, Syntheseverfahren, Reaktionsparameter, die die Eigenschaften synthetisierter CuNPs beeinflussen, und eine Screening-Analyse, die verwendet wird, um sekundäre Pflanzenstoffe in verschiedenen Pflanzen zu identifizieren, wird aus der kürzlich veröffentlichten Literatur gegeben, die überprüft und zusammengefasst wurde . Hypothetische Mechanismen der Reduktion des Kupferions durch Quercetin, Stabilisierung von Kupfer-Nanopartikeln durch Santin, antimikrobielle Aktivität und Reduktion von 4-Nitrophenol werden mit schematischen Illustrationen angegeben. Der Hauptzweck dieser Übersicht bestand darin, die Daten von Pflanzen, die für die Synthese von CuNPs verwendet wurden, zusammenzufassen und Forschern einen neuen Weg zu eröffnen, um Pflanzen zu untersuchen, die in der Vergangenheit nicht verwendet wurden.
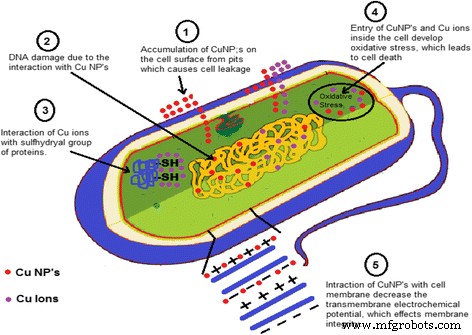
Vorgeschlagener Mechanismus für die antibakterielle Aktivität von Kupfer-Nanopartikeln.
Hintergrund
Nanopartikel (NPs) haben eine Reihe interessanter Anwendungen im industriellen Bereich wie Raumfahrttechnologie, Magnetismus, Optoelektronik und Elektronik, Kosmetik sowie katalytische, pharmazeutische, biomedizinische, Umwelt- und Energieanwendungen [1, 2]. Die außergewöhnlichen Eigenschaften von Nanopartikeln wie Duktilität, hohe Streckgrenze, Härte, Flexibilität, Steifigkeit, hohes Oberflächen-Volumen-Verhältnis, Makroquantentunneleffekt und Quantengröße sind im Vergleich zu den Eigenschaften von Schüttgütern gleicher chemischer Zusammensetzung zurückzuführen [3 ]. Tatsächlich sind die Eigenschaften von NPs, die sich erheblich von denen feiner Partikel unterscheiden können, eine höhere spezifische Oberfläche, spezifische optische Eigenschaften, niedrigere Schmelzpunkte, spezifische Magnetisierungen, mechanische Festigkeit und zahlreiche industrielle Anwendungen [4]. Kupfernanopartikel (CuNPs) sind aufgrund ihrer leichten Verfügbarkeit, geringen Kosten und ihrer ähnlichen Eigenschaften wie Edelmetalle von großem Interesse [5,6,7,8,9]. CuNPs können auch in Sensoren, Wärmeübertragungssystemen [10,11,12] und Elektronik (Brennstoffzelle und Solarzelle), als Katalysatoren in vielen Reaktionen und als bakterizide und antimikrobielle Mittel zur Beschichtung von Krankenhausgeräten verwendet werden [13,14, 15,16,17,18,19].
Viele physikalische und chemische Methoden wie Laserablation [20], Mikrowellen-unterstützte Verfahren, Sol-Gel [21], Co-Präzipitation [22], gepulste Drahtentladung [23], Vakuumdampfabscheidung [24], Hochenergiebestrahlung [ 25], Lithographie [26], mechanisches Mahlen [27], photochemische Reduktion, Elektrochemie [28,29,30,31,32], Elektrospray-Synthese [33], hydrothermale Reaktion [34], Mikroemulsion [35] und chemische Reduktion werden zur Synthese von Nanopartikeln verwendet. Physikalische und chemische Verfahren erzeugen zwar genau definierte und reine Nanopartikel, diese Verfahren sind jedoch aufgrund des Einsatzes giftiger Chemikalien weder kostengünstig noch umweltfreundlich. Eines der wichtigsten Kriterien der Nanotechnologie ist die Entwicklung umweltfreundlicher, ungiftiger und sauberer Green-Chemie-Verfahren [36]. Daher enthält die Biosynthese von Nanopartikeln eine auf der grünen Chemie basierende Methode, die verschiedene biologische Körper wie Pflanzen [37, 38], Actinomyceten [39, 40], Pilze [41, 42, 43, 44], Bakterien [45, 46, 47,48,49], Hefe [50,51,52] und Viren [53, 54]. Biologische Einheiten bieten einen ungiftigen, sauberen und umweltfreundlichen Ansatz zur Synthese von NPs mit einer breiten Palette von Größen, physikalisch-chemischen Eigenschaften, Formen und Zusammensetzungen [55].
Kupfer-Nanopartikel wurden in der Literatur unter Verwendung verschiedener Pflanzen wie Euphorbia esula . synthetisiert und stabilisiert [56], Punica granatum [57], Ocimum sanctum [58], Ginkgo biloba [59], Calotropis procera [60], Lawsonia inermis [61], Citrus medicalinn [62], Camellia sinensis [63], Datura innoxia [64], Syzygium aromaticum [65], Sesamum-Indicum [66], Zitruslimon , Kurkuma-Curcumin [67], Gloriosa superba L. [68], Ficus carica [69], Aegle Marmelos [70], Caesalpinia pulcherrima [71], Cassia-Fistel [72], Leucas aspera , Leucas chinensis [73], Delonix elata [74], Aloe barbadensis Miller [75], Thymus vulgaris [76], Phyllanthus emblica [77], Magnolienkobus [78], Eukalyptus [79], Artabotrys odoratissimus [80], Capparis zeylanica [81], Vitis vinifera [82], Hibiscus rosa-sinensis [83], Zingiber officinale [84], Datura metel [85], Zea mays [86], Urtica , Matricaria chamomilla , Glycyrrhiza glabra , Schisandra chinensis , Inula Helenium , Zimt [87], Dodonaea viscosa [88], Cassia auriculata [89], Azadirachta indica , Lantana-Kamera , Tridax Procumbens [90], Allium sativum [91], Spargel adscendens , Bacopa monnieri , Ocimum bacilicum , Withania somnifera [92], Smithia sensitiva , Colocasia esculenta [93], Neriumoleander [94] und Psidium Guajava [95]; durch Verwendung verschiedener Algen/Pilze wie Phaeophyceae [96], Stereum hirsutum [97] und Hypocrea lixii [98]; und durch die Verwendung einiger Mikroorganismen wie Pseudomonas fluorescens [99] und Enterococcus faecalis [100] Kulturen.
Biosynthese von Kupfer-Nanopartikeln
Pflanzenteile, die für den Extrakt verwendet werden
Zur Herstellung von Pflanzenextrakten werden verschiedene Pflanzenteile wie Blätter, Samen, Rinde, Früchte, Schalen, Kokos, Wurzeln und Gummi verwendet. Blätter und Wurzeln werden auf zwei Arten verwendet. Zum einen werden frische Blätter und Wurzeln zur Herstellung von Pflanzenextrakten verwendet, zum anderen werden trockene Blätter und Wurzeln in Pulverform verwendet.
Verfahren zur Synthese von CuNPs
Für die Synthese von CuNPs wurde Pflanzenextrakt unter Verwendung verschiedener Teile verschiedener Pflanzen hergestellt. Zur Synthese des Extraktteils der interessierenden Pflanze werden die Blätter gesammelt und mit Leitungswasser und dann mit destilliertem Wasser gewaschen, um Staubpartikel zu entfernen. Die gewaschenen Blätter werden auf zwei Arten weiterverwendet. Zuerst werden diese Blätter 1–2 h in der Sonne getrocknet, um die Restfeuchtigkeit zu entfernen. Bekannte Gewichte dieser sonnengetrockneten Blätter werden in kleine Teile geteilt und in entionisiertem Wasser oder Ethanollösung eingeweicht. Diese Mischung wird 24 h bei Raumtemperatur mit einem Magnetrührer gerührt und dann zur weiteren Verwendung filtriert. Zweitens werden diese Blätter 4–7 Tage lang in der Sonne getrocknet oder 1 Tag lang in einem Ofen bei 50 °C getrocknet und mit einem Haushaltsmixer pulverisiert. Pflanzenpulver mit bekanntem Gewicht wird in Wasser oder Ethanollösung gemischt und dann gerührt und gefiltert.
Für die Synthese von CuNPs werden wässrige Lösungen von Vorläufersalzen wie Kupfersulfat, Kupferchlorid, Kupferacetat und Kupfernitrat mit unterschiedlichen Konzentrationen mit Pflanzenextrakt vermischt. Eine wässrige Lösung von Natriumhydroxid wird ebenfalls hergestellt und dem Reaktionsgemisch zugesetzt, um den pH-Wert des Mediums zu kontrollieren. Das Reaktionsgemisch wird in einem elektrischen Schüttler für unterschiedliche Zeitintervalle stark geschüttelt und in unterschiedlichen Zeitintervallen und bei unterschiedlichen Temperaturen in einem Ofen erhitzt. Die Bildung von CuNPs kann auch bei Raumtemperatur erfolgen und wird durch eine Farbänderung der Reaktionsmischung bestätigt. Am Ende wurden Nanopartikel zentrifugiert und bei verschiedenen Temperaturen getrocknet. Reaktionsoptimierungen erfolgen durch Änderung des pH-Werts der Mischung, der Konzentration des Vorläufersalzes, der Erwärmungszeit und der Temperatur der Reaktionsmischung. In der Literatur wurden verschiedene Anlagen zur Bildung von Kupfernanopartikeln unter Verwendung verschiedener Vorläufersalze mit unterschiedlichen Reaktionsbedingungen verwendet, wie in Tabelle 1 gezeigt. Aus der Tabelle ist ersichtlich, dass die unterschiedlichen Reaktionsbedingungen die Form und Größe von Kupfer beeinflussen Nanopartikel.
Einfluss von Reaktionsparametern auf Eigenschaften von NPs
Die Konzentration des Pflanzenextrakts spielt eine Hauptrolle bei der Reduzierung und Stabilisierung der CuNPs. Es wurde berichtet, dass durch die Erhöhung der Konzentration des Pflanzenextrakts die Anzahl der Partikel zunahm [88]. Durch die Erhöhung der Konzentration des Pflanzenextrakts stieg die Konzentration an sekundären Pflanzenstoffen und die Reduktion von Kupfersalz nahm ebenfalls zu. Aufgrund der schnellen Reduktion des Metallsalzes nahm auch die Größe der Nanopartikel ab [101].
Größe und Struktur von CuNPs werden stark durch das Kupfersalz beeinflusst. Die Morphologie von Nanopartikeln ändert sich, wenn das Salz (z. B. Kupferchlorid, Kupferacetat, Kupfernitrat oder Kupfersulfat) in Gegenwart von Natriumhydroxid verwendet wird. Es wurde berichtet, dass die Form bei Kupferchlorid dreieckig und tetraedrisch, bei Kupferacetat stäbchenförmig und bei Kupfersulfat kugelförmig war [102]. Durch Erhöhung der Konzentration des Vorläufersalzes nahm auch die Größe der CuNPs zu.
Die Synthese von CuNPs liefert die besten Ergebnisse, indem der pH-Wert des Reaktionsmediums innerhalb des bevorzugten Bereichs variiert wird. Die Größe der Nanopartikel wurde durch Veränderung des pH-Wertes der Reaktionsmischung kontrolliert. Bei einem höheren pH-Wert wurden kleinere Nanopartikel erhalten, verglichen mit denen, die bei einem niedrigen pH-Wert erhalten wurden. Dieser Unterschied kann auf die unterschiedliche Reduktionsrate der Metallsalze durch Pflanzenextrakt zurückgeführt werden. Die umgekehrte Beziehung zwischen dem pH-Wert und der Größe der Nanopartikel zeigte, dass eine Erhöhung des pH-Wertes es uns ermöglicht, kleine kugelförmige Nanopartikel zu erhalten, während eine Verringerung des pH-Wertes große (stäbchenförmige und dreieckige) Nanopartikel ergibt. Der Einfluss verschiedener pH-Werte (4, 6, 8, 10 und 12) auf die Absorptionsspektren ist in Abb. 1 dargestellt [36]. Es wurde berichtet, dass die Zugabe von Pflanzenextrakt zu CuCl2 führten nicht zur Bildung von CuNPs, sondern wurden stattdessen durch Ändern des pH-Werts der Reaktionsmischung in ein basisches Medium erhalten. Das gleiche Verhalten wurde von Wu und Chen beobachtet, und es wurde geschlussfolgert, dass der pH-Wert eine wichtige Rolle bei der Synthese von CuNPs spielt [103].
Pflanzenteile zur Herstellung von Pflanzenextrakt
Mechanismus für die Phytosynthese von Kupfer-Nanopartikeln
Phytochemisches Screening:eine qualitative Analyse
Die phytochemische Screening-Analyse ist eine chemische Analyse, die zum Nachweis von sekundären Pflanzenstoffen in verschiedenen Pflanzen durchgeführt wird. Für diese Analyse wird Frischpflanzenextrakt mit Chemikalien oder chemischen Reagenzien verwendet [77], wie in Tabelle 2 gezeigt.
Phytochemikalien zur Metallreduktion und Stabilisierung der NPs
Die grüne Synthese von CuNPs unter Verwendung von sekundären Pflanzenstoffen bietet eine flexiblere Kontrolle über die Form und Größe der NPs (d. h. durch Änderung der Reaktionstemperatur, Konzentration des Pflanzenextrakts, Metallsalzkonzentration, Reaktionszeit und pH-Wert der Reaktionsmischung). Die Farbänderung des Reaktionsmediums weist auf eine Reduktion des Metallions und die Bildung von NPs hin. Die Grünreduktion der Kupfersalze setzt sofort ein und die Bildung von Kupfer-Nanopartikeln wird durch den Farbumschlag der Reaktionsmischung angezeigt. Phytochemikalien spielen eine Hauptrolle dabei, zuerst die Metallionen zu reduzieren und dann die Kerne des Metalls in Form von Nanopartikeln zu stabilisieren, wie in Abb. 2 gezeigt. Die Wechselwirkung von sekundären Pflanzenstoffen mit Metallionen und die Konzentration dieser sekundären Pflanzenstoffe steuern die Form und Größe von CuNPs.
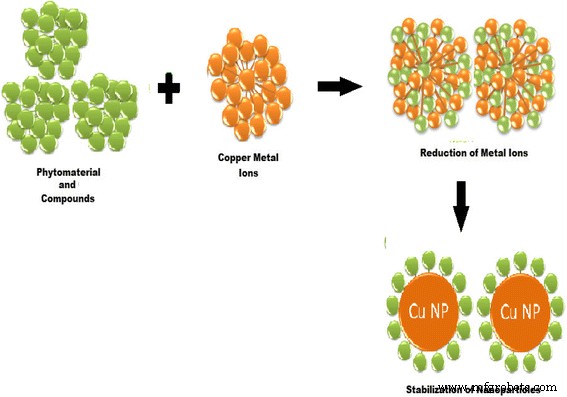
Ein Protokoll zum Reduzieren der Metallionen und anschließenden Stabilisieren der Metallkerne
Flavonoide enthalten polyphenolische Verbindungen, z. B. Quercetin, Katechine, Flavanone, Isoflavone, Santin, Penduletin, Alizarin, Pinocembrin, Anthocyane, Flavone, Tannine und Saponine, die in verschiedenen Pflanzen wie Ginkgo biloba vorkommen [59], Citrus medicalinn [62], Phyllanthus emblica [77], Hibiscus rosa-sinensis [83] und Dodonaea viscosa [93]. Diese Verbindungen spielen eine Hauptrolle bei der Reduktion und Chelatisierung des Metalls. Für die Reduktion des Kupferions sind verschiedene funktionelle Gruppen der Flavonoide verantwortlich. Es wurde angenommen, dass während der tautomeren Umwandlung der Enolform in die Ketoform ein reaktives Wasserstoffatom in den Flavonoiden freigesetzt werden kann, das Kupferionen zu Kupferkernen oder CuNPs reduzieren kann. Es wird beispielsweise angenommen, dass im Fall von Ginkgo biloba Pflanzenextrakten spielt die Umwandlung von Quercetin (Flavonoid) eine Hauptrolle bei der Reduktion von Kupfermetallionen in Kupferkerne oder CuNPs aufgrund der Umwandlung der Enolform in die Ketoform, wie in Abb. 3 gezeigt.
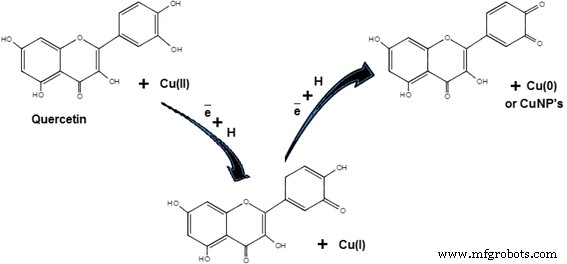
Reduktion von Kupferionen durch Quercetin
Während des Syntheseprozesses von CuNPs werden Metallionen mit ein- oder zweiwertigen Oxidationsstufen in Kupferkerne ohne Oxidation umgewandelt und diese Kerne werden zu unterschiedlichen Formen verschmolzen. Während der Keimbildung aggregieren Kerne zu verschiedenen Formen wie Drähten, Kugeln, Würfeln, Stäben, Dreiecken, Fünfecken und Sechsecken. Einige Flavonoide haben die Fähigkeit, die CuNPs mit ihrem π . zu chelatisieren Elektronen und Carbonylgruppen. Quercetin und Santin sind Flavonoide mit starker chelatisierender Aktivität aufgrund der Anwesenheit von zwei funktionellen Gruppen, die die Hydroxyle und Carbonyle umfassen. Diese Gruppen bilden mit Kupfernanopartikeln eine Chelatbildung, indem sie dem vorherigen Mechanismus folgen, und erklären auch die Fähigkeit zur Adsorption von Santin (Flavonoid) auf der Oberfläche von CuNPs, wie in Abb. 4 gezeigt.
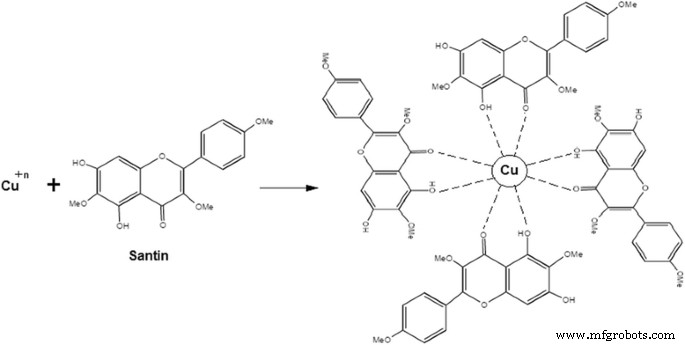
Stabilisierung von Kupfer-Nanopartikeln durch Santin
Es wurde angenommen, dass die Proteinmoleküle (Superoxiddismutase, Katalase, Glutathion) in verschiedenen Pflanzen wie Hibiscus rosa-sinensis [83] und Camellia sinensis [104] zeigen eine hohe reduzierende Aktivität für die Bildung von Nanopartikeln aus Metallionen, ihre chelatbildende Aktivität ist jedoch nicht übermäßig. Zucker wie Monosaccharide (Glukose), Disaccharide (Maltose und Laktose) und Polysaccharide in Camellia sinensis Pflanze [63] kann als Reduktionsmittel oder Antioxidans wirken und eine Reihe von tautomeren Umwandlungen von Keton zu Aldehyd aufweisen.
Andere sekundäre Pflanzenstoffe wie Polyphenole (z. B. Ellagsäure und Gallussäure), die in Hibiscus rosa-sinensis vorhanden sind [40], Phenylpropanoide (Phenylalanin, Tyrosin) in Aegle Marmelos [70], Terpenoide im Ocimum sanctum und Spargel-Adscendens [58, 92], Cysteinproteasen in Calotropis procera [60], Curcuminanilineazomethin in Kurkuma-Curcumin [67], Ascorbinsäure in Citrus medicalinn [62], Eugenol in Syzygium aromaticum [65] und Alkaloide in Aegle marmelos [70] spielen die gleiche Rolle bei der Reduktion der Kupferionen und der Stabilisierung der Kupfernanopartikel. Kohlenhydrate, Anthrachinon, Chinon und Anthocyanosid in Phyllanthus emblica [77]; Lignine und Xanthone in Hibiscus rosa-sinensis [83]; und Herzglykosid, Triterponoid, Carotinoidglykosid und Anthrachinonglykosid bei Colocasia esculenta plant [93] sind ebenfalls sekundäre Pflanzenstoffe, die in Extrakten verschiedener Pflanzen enthalten sind und als Reduktions- und Stabilisierungsmittel wirken. Beispiele für bestimmte sekundäre Pflanzenstoffe mit Strukturen sind in Abb. 5 dargestellt.
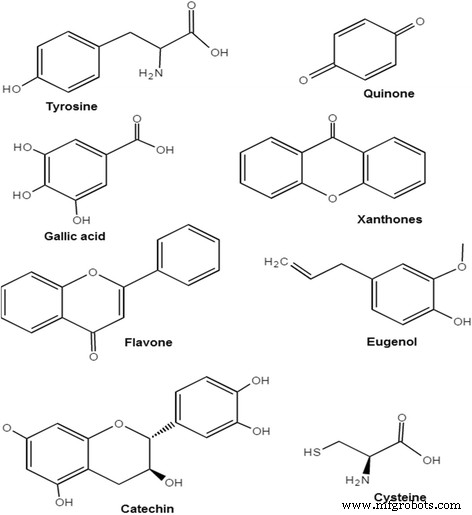
Phytochemikalien mit ihren Strukturen
Charakterisierungstechniken
Zur Charakterisierung synthetisierter Nanopartikel wurden verschiedene Techniken verwendet, wie Ultraviolett-Vis-Spektroskopie (UV-vis), Transmissionselektronenmikroskopie (TEM), Kleinwinkel-Röntgenstreuung (SAXS), Fourier-Transformations-Infrarotspektroskopie (FTIR), Röntgen- Röntgenfluoreszenzspektroskopie (XRF), Röntgenbeugung (XRD), Röntgenphotoelektronenspektroskopie (XPS), Rasterelektronenmikroskopie (REM), Feldemissionsrasterelektronenmikroskopie (FESEM), Partikelgrößenanalyse (PSA), Malvern Zetasizer ( MZS), energiedispersive Röntgenspektroskopie (EDX/EDS), Nanopartikel-Tracking-Analyse (NTA), Röntgenreflektometrie (XRR), Brunauer-Emmett-Teller-Analyse (BET), Selected Area Electron Beugung (SAED) und Rasterkraftmikroskopie (AFM) (Tabelle 3).
Anwendungen von Kupfer-Nanopartikeln
Aufgrund ihrer hervorragenden chemischen und physikalischen Eigenschaften, ihres großen Oberfläche-zu-Volumen-Verhältnisses, ihrer ständig erneuerbaren Oberfläche, ihrer geringen Kosten und ihrer ungiftigen Herstellung sind CuNPs für Anwendungen in verschiedenen Bereichen von großem Interesse. Kupfernanopartikel zeigen katalytische Aktivität, antibakterielle Aktivität, Zytotoxizität oder Antikrebsaktivität, antioxidative Aktivität und antimykotische Aktivität in verschiedenen Anwendungen. In katalytischer Aktivität werden Kupfer-Nanopartikel für die Huisgen [3 + 2]-Cycloaddition von Alkinen und Aziden in vielen Lösungsmitteln unter ligandenfreien Bedingungen verwendet [59], 1-Methyl-3-phenoxybenzol, 3,3-Oxybis(methylbenzol) [94], Synthese von 1-substituiertem 1H -1,2,3,4-Tetrazol [76], Adsorption von Stickstoffdioxid und Adsorption von Schwefeldioxid [66]. Bei den meisten der katalysierten Übergangsmetalle werden Ullmann-Kupplungsreaktionsliganden, wie Phosphine, in der Literatur beschrieben, und die meisten Liganden sind teuer, schwierig herzustellen und feuchtigkeitsempfindlich. Für diese Arbeit werden synthetisierte Kupfer-Nanopartikel für die ligandenfreie Ullmann-Kupplung von Diphenylether verwendet. Verschiedene Farbstoffe und giftige organische Verbindungen und Pestizide in Industrieabfällen sind sehr schädlich für die Umwelt und lebende Organismen. Kupfernanopartikel werden zum Abbau verschiedener Farbstoffe wie Methylenblau [73], Abbau von Atrazin [86] und Reduktion von 4-Nitrophenol [76] verwendet.
Unter den antimikrobiellen Wirkstoffen werden Kupferverbindungen häufig in der Landwirtschaft als Herbizide [105], Algizide [106], Fungizide [107] und Pestizide sowie in der Tierhaltung als Desinfektionsmittel [108] eingesetzt (siehe Tabelle 4). Die biogenen Kupfer-Nanopartikel zeigten eine starke antibakterielle Aktivität gegen grampositive und gramnegative Krankheitserreger wie Pseudomonas aeruginosa (MTCC 424), Micrococcus luteus (MTCC 1809), Enterobacter aerogenes (MTCC 2832) [57], Salmonella enterica (MTCC 1253), Rhizoctonia solani , Xanthomonas axonopodis pv. Citri , Xanthomonas axonopodis pv. punicea [58], Escherichia coli (ATCC 14948) [62], Staphylococcus aureus (ATCC 25923), Bacillus subtilis (ATCC 6633), Pediococcus acidilactici [69] und Klebsiella pneumoniae (MTCC 4030). Bei der antimykotischen Wirkung werden Kupfer-Nanopartikel gegen Alterneria carthami . verwendet , Colletotrichum gloeosporioides , Colletotrichum lindemuthianum , Drechslera sorghicola , Fusarium oxysporum f.sp. carthami , Rhizopus stolonifer , Fusarium oxysporum f.sp. ciceris , Macrophomina phaseolina , Fusarium oxysporum f.sp. udum , Rhizoctonia bataticola [58], Candida albicans , Kurvularia , Aspergillus niger , und Trichophyton simii [67]. In der Zytotoxizität werden Kupfer-Nanopartikel für eine Studie an HeLa-, A549-, MCF7-, MOLT4- und BHK21-Zelllinien (Krebstumoren) verwendet [60, 104].
Hypothetischer Mechanismus der antimikrobiellen Aktivität
Es wurde beobachtet, dass CuNPs eine ausgezeichnete antimikrobielle Aktivität aufweisen, und nur wenige Berichte präsentierten den Mechanismus der antibakteriellen Aktivität von Kupfernanopartikeln in der Literatur, aber diese Mechanismen waren hypothetisch. Es wurde beobachtet, dass Bakterien und Enzyme/Proteine durch die Interaktion von CuNPs mit der –SH (Sulfhydryl)-Gruppe zerstört wurden [109, 110]. Es wurde auch berichtet, dass die helikale Struktur von DNA-Molekülen durch die Wechselwirkung von CuNPs gestört wird [111]. Die Wechselwirkung von CuNPs mit der Zellmembran von Bakterien verringerte das elektrochemische Transmembranpotential und beeinflusste aufgrund der Abnahme des elektrochemischen Transmembranpotentials die Membranintegrität [112]. Es wurde angenommen, dass Metall-NPs ihre jeweiligen Metallionen freisetzen. Kupfernanopartikel und Kupferionen reichern sich auf der Zelloberfläche der Bakterien an und bilden Grübchen in der Membran, wodurch die Zellkomponente aus der Zelle und in das Zellinnere austritt, wodurch oxidativer Stress verursacht wird, der zum Zelltod führt [112,113,114]. Ein hypothetischer Mechanismus der antibakteriellen Aktivität, der die obigen Möglichkeiten darstellt, ist in Abb. 6 gezeigt.
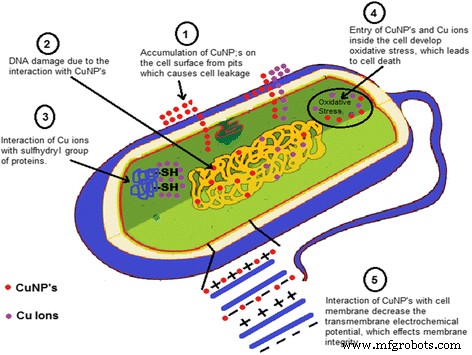
Mechanismus der antibakteriellen Aktivität von Kupfer-Nanopartikeln
katalytische Aktivität zur Reduktion von 4-Nitrophenol
4-Nitrophenol (4-NP), das normalerweise in landwirtschaftlichen Abwässern und Industrieprodukten vorkommt, ist gefährlich und nicht umweltfreundlich. Die Hydrierung oder Reduktion von 4-NP, das in 4-Aminophenol (4-AP) umgewandelt wird, findet in Gegenwart von CuNPs statt. CuNPs können die Reaktion katalysieren, um die kinetische Barriere zu überwinden, indem sie den Elektronentransfer von den Donor-Borhydrat-Ionen auf den Akzeptor 4-NP unterstützen.
Die katalytische Aktivität der synthetisierten CuNPs wurde bei der Reduktion von 4-Nitrophenol in wässrigem Medium bei Raumtemperatur in Gegenwart einer wässrigen Lösung von Natriumborhydrid untersucht [56]. Die Reduktion von 4-NP durch Verwendung von CuNPs ist ein einfacher und umweltfreundlicher Prozess. Die katalytische Effizienz von CuNPs für die Reduktion von 4-NP wurde unter Verwendung eines UV-Vis-Spektrometers untersucht. Es wurde beobachtet, dass der maximale Absorptionspeak für 4-NP in wässrigem Medium bei 317 nm lag und der Adsorptionspeak durch Zugabe von Natriumborhydrid aufgrund der Bildung von 4-Nitrophenolationen auf 403 nm verschoben wurde. Ein Peak bei 403 nm blieb auch nach 2 Tagen unbeeinflusst, was darauf hinwies, dass die Reduktion von 4-NP ohne Katalysator nicht stattfinden kann. Nach Zugabe der CuNPs verschob sich der Absorptionspeak der Lösung auf 300 nm und der Peak bei 403 nm verschwand vollständig, was die Reduktion von 4-NP zu 4-AP ohne Nebenprodukt anzeigte. Ein hypothetischer Mechanismus für die Reduktion von 4-NP ist in Abb. 7 dargestellt. Bei dem Mechanismus liegen 4-NP und Natriumborhydrid in Form von Ionen in der Lösung vor. Die Protonen des Borhydrid-Ions adsorbieren an der Oberfläche der Kupfer-Nanopartikel und BO2 produziert. 4-Nitrophenolat-Ionen adsorbieren ebenfalls an der Oberfläche der CuNPs. Aufgrund der Adsorption von Protonen und 4-Nitrophenolat-Ion überwinden CuNPs die kinetische Barriere der Reaktanten und 4-Nitrophenolat-Ion wird in 4-Aminophenolat-Ion umgewandelt. Nach der Umwandlung findet die Desorption des 4-Aminophenolat-Ions statt und es wird in 4-Aminophenol umgewandelt.
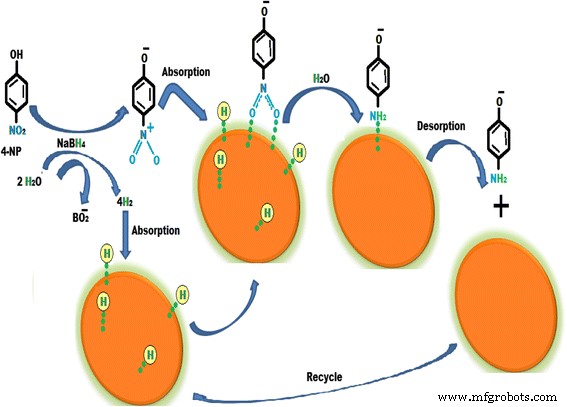
Mechanismus zur Reduktion von 4-Nitrophenol
Schlussfolgerungen
In diesem Artikel wurden aktuelle Informationen zu biologischen Methoden zur Synthese von Kupfer-Nanopartikeln (CuNPs) unter Verwendung verschiedener Pflanzen überprüft und zusammengefasst. Die grüne Synthese von CuNPs wurde als wertvolle Alternative zu physikalischen und chemischen Methoden mit geringer Zytotoxizität, wirtschaftlichen Aussichten, umweltfreundlicher, verbesserter Biokompatibilität, Machbarkeit und hoher antioxidativer Aktivität und hoher antimikrobieller Aktivität von CuNPs vorgeschlagen. Der Mechanismus der Biosynthese von NPs ist noch unbekannt, und mehr Forschung muss auf den Mechanismus der Bildung von Nanopartikeln und das Verständnis der Rolle von sekundären Pflanzenstoffen bei der Bildung von NPs konzentriert werden. Dieser Aufsatz enthält Daten zu Pflanzen, die bei der Synthese von Kupfernanopartikeln verwendet werden, Syntheseverfahren und die Reaktionsparameter, die die Eigenschaften synthetisierter CuNPs beeinflussen. Eine phytochemische Screening-Analyse ist eine chemische Analyse, die verwendet wird, um die sekundären Pflanzenstoffe wie den Nachweis von Kohlenhydraten, Tanninen, Saponinen, Flavonoiden, Alkaloiden, Anthrachinonen und Anthocyanosiden in verschiedenen Pflanzen zu identifizieren. Der Mechanismus der Reduktion von Kupferionen durch Quercetin und die Stabilisierung von Kupfernanopartikeln durch Santin wird in diesem Artikel beschrieben. In der Literatur verwendete Charakterisierungstechniken für Kupfernanopartikel sind UV-Vis, FTIR, XRD, SEM, FESEM, TEM, PSA, MZS, EDX, NTA, SAXS, XRR, XRF, XPS, BET, SAED und AFM. Kupfernanopartikel zeigen katalytische Aktivität, antibakterielle Aktivität, Zytotoxizität oder Antikrebsaktivität, antioxidative Aktivität und antimykotische Aktivität in verschiedenen Anwendungen. Hypothetische Mechanismen der antimikrobiellen Aktivität und Reduktion von 4-Nitrophenol mit Diagrammen werden in diesem Papier gezeigt.
CuNPs mit unterschiedlichen strukturellen Eigenschaften und effektiven biologischen Wirkungen können in den kommenden Tagen mit neuen grünen Protokollen hergestellt werden. Die Kontrolle über die Partikelgröße und wiederum die größenabhängigen Eigenschaften von CuNPs werden neue Türen für ihre Anwendungen öffnen. Diese Studie bietet einen Überblick über die Synthese von CuNP unter Verwendung von Pflanzenextrakt, mikrobiellem Extrakt und natürlich vorkommenden Biomolekülen. Obwohl alle diese grünen Protokolle für die CuNP-Synthese ihre eigenen Vorteile und Einschränkungen haben, ist die Verwendung von Pflanzenextrakt als Reduktionsmittel im Vergleich zur Verwendung von mikrobiellem Extrakt aufgrund der schnellen Produktion von Nanopartikeln mit dem ehemaligen grünen Reduktionsmittel vorteilhafter.
Nanomaterialien
- Biogene Synthese, Charakterisierung und Bewertung des antibakteriellen Potenzials von Kupferoxid-Nanopartikeln gegen Escherichia coli
- Einfache Synthese und optische Eigenschaften kleiner Selen-Nanokristalle und -Nanostäbe
- Herstellung und verbesserte katalytische Hydrierungsaktivität von Sb/Palygorskit (PAL)-Nanopartikeln
- Grüne Eintopf-Synthese von Ag-dekorierten SnO2-Mikrosphären:ein effizienter und wiederverwendbarer Katalysator für die Reduktion von 4-Nitrophenol
- Einfache Synthese von farbigen und leitfähigen CuSCN-Kompositen, die mit CuS-Nanopartikeln beschichtet sind
- Hydrothermale Synthese von In2O3-Nanopartikel-Hybrid-Zwillingen hexagonalen Scheiben-ZnO-Heterostrukturen für verbesserte photokatalytische Aktivitäten und Stabilität
- Nachbehandlungsmethode zur Synthese monodisperser binärer FePt-Fe3O4-Nanopartikel
- Platycodon-Saponine aus Platycodi Radix (Platycodon grandiflorum) für die grüne Synthese von Gold- und Silber-Nanopartikeln
- Grüne Synthese von Metall- und Metalloxid-Nanopartikeln und ihre Wirkung auf die einzellige Alge Chlamydomonas reinhardtii
- Einfache Synthese von Liganden-freien Iridium-Nanopartikeln und ihre In-vitro-Biokompatibilität



