Kovalent modifiziertes Graphenoxid und Polymer mit intrinsischer Mikroporosität (PIM-1) in Mischmatrix-Dünnschicht-Verbundmembranen
Zusammenfassung
In dieser Studie wurden Mixed-Matrix-Membranen (MMMs) bestehend aus Graphenoxid (GO) und funktionalisiertem Graphenoxid (FGO), die in ein Polymer mit intrinsischer Mikroporosität (PIM-1) eingebaut sind, das als Polymermatrix dient, durch Tauchbeschichtungsverfahren hergestellt. und ihre einzelnen Gastransporteigenschaften wurden untersucht. Erfolgreich oberflächenmodifizierte GOs wurden durch Fourier-Transformations-Infrarotspektroskopie (FTIR), UV-Vis-Spektroskopie, Raman-Spektroskopie, Rasterelektronenmikroskopie (REM) und thermogravimetrische Analyse (TGA) charakterisiert. Die Wirkung der FGO-Beladung auf die MMM-Morphologie und -Leistung wurde untersucht, indem der FGO-Gehalt in der Polymermatrix von 9 bis 84 Gew.-% variiert wurde. Die Verwendung eines hohen FGO-Gehalts in der Polymermatrix half dabei, Unterschiede in der Wechselwirkung funktionalisierter Füllstoffe mit PIM-1 aufzudecken und sogar die Änderung der FGO-Steifigkeit und der Füllstoffausrichtung zur Membranoberfläche in Abhängigkeit von der Natur der funktionellen Gruppe zu diskutieren.
Einführung
Graphen ist ein vielversprechendes Kohlenstoff-Nanomaterial für zukünftige Anwendungen. Als zweidimensionale allotrope Modifikation von Kohlenstoff kann Graphen effektiv als potenzielles Material in molekularen Trenntechnologien verwendet werden. Defektfreies Graphen wirkt als undurchlässiges Material für alle Moleküle. Dank der zweidimensionalen Morphologie hilft bereits der Einbau kleiner Mengen dieses Materials in Polymermembranen, den Transport von Gasen und Flüssigkeiten effektiv zu behindern, da beispielsweise in PIM-1 dispergierte Graphen-Nanoplättchen (weniger als 0,0075 Gew.%) die Permeabilitätskoeffizienten von Gasen um den Faktor drei [1, 2]. Bei PET, das mit einem geringen Graphen-Anteil (0,4 Gew.%) beschichtet war, war die Sauerstoffdurchlässigkeit um das Vierfache reduziert [3]. APTS-funktionalisiertes Graphenoxid (GO) inkorporierte PVDF-Membran zeigte eine perfekte Salzabweisung (> 99,9%), während PBI-GO-Mischmatrixmembranen für die organische Lösungsmittel-Nanofiltration in den vorherigen Arbeiten entwickelt wurden [4, 5]. Aktuelle Forschungen zu thermisch umgelagerten (TR) Polymeren haben gezeigt, dass der Einbau von reduziertem Graphenoxid (rGO) die Durchlässigkeit von CO2 . um das 482-fache erhöht während die Selektivität der Mischmatrixmembran bei 35 wie bei der reinen Membran blieb [6].
Bisher konzentrierte sich die Forschung zur Herstellung von Dünnschicht-Verbundmembranen auf die Verwendung geringer Mengen an Füllstoffen, oft 0,1 Gew.-% Graphen oder seiner Derivate in einem Polymer [7]. Dieser Ansatz verwendet hauptsächlich eine zweidimensionale Form von Graphenpartikeln und eine entsprechende niedrige Perkolationsschwelle [8], bei der abgeblätterte flockenartige Partikel eine kontinuierliche Phase bilden. Berichtete Membranen aus reinem Graphen oder Graphenoxid enthalten Hunderte von einzelnen Schichten, die als Trennfaktor für Moleküle dienen [9].
Die Herausforderung bei der Herstellung eines einschichtigen Graphens ist der hohe Energieverbrauch während der Herstellung und die Wechselwirkungen zwischen den Schichten (Van-der-Waals-Wechselwirkungen und π-π-Stapelung), die eine starke Agglomeration der Graphenschichten verursachen. Dieses Problem kann durch chemische Anlagerung funktioneller Gruppen, kleiner Moleküle und sogar Polymerketten an eine Graphenschicht über „Grafting-to“- oder „Grafting from“-Methoden gelöst werden [10].
Die Graphenoxidation erhöht den Zwischenschichtabstand zwischen den einzelnen Blättern und macht sie widerstandsfähiger gegen Agglomeration oder Stapeln. Oxidiertes Graphen enthält mehrere funktionelle Sauerstoffgruppen wie Epoxid (C–O–C), phenolisches Hydroxy (–OH) und Carboxyl (–COOH).
Aufgrund der Anwesenheit von Sauerstofffunktionalitäten an den Kanten (–COOH) und in der Grundebene (C–O–C und –OH) ist Graphenoxid (GO) in verschiedenen Lösungsmitteln gut dispergierbar [11, 12]. Als gut dispergierbares Material ist GO leicht chemisch modifizierbar. Die chemische Funktionalisierung von GO dient als faszinierendes Mittel, um die Affinität von Graphen zu verschiedenen gasförmigen und flüssigen Substanzen zu erhöhen. Sowohl nicht-oxidierte graphitische Domänen als auch sauerstoffhaltige Gruppen von GO können entweder durch nicht-kovalente oder kovalente Funktionalisierung modifiziert werden. Die nicht-kovalente Funktionalisierung beinhaltet starke π-π-Wechselwirkungen zwischen graphitischen Domänen und funktionalisierenden Gruppen, wie von Dubey et al. [13] und Yang et al. [14].
In dieser Arbeit führten wir eine kovalente chemische Funktionalisierung von GO durch und führten verschiedene funktionelle Gruppen, Amine, Oxime, modifizierte Ferrocene, Thionylchlorid und Phosphortrichlorid in die Graphenstruktur ein Bereich der Graphenoxidgehalte. Die Forschung konzentrierte sich auf die einzelnen Gastransportexperimente von drei verschiedenen FGOs mit eingebautem Polymer mit intrinsischer Mikroporosität (PIM-1) (Abb. 1), das sich durch eine hohe Gasdurchlässigkeit, aber relativ geringe Selektivität auszeichnet. Graphenoxidschichten wurden modifiziert, um die Natur der Nanopartikel zu verändern, um die Einzelgastransporteigenschaften der PIM-1-Membran zu verbessern. Zu diesem Zweck wurde GO aufgrund einer möglichen Affinität funktioneller Gruppen zu Sauerstoff mit Ferrocenderivaten (GO-AEDPPF und GO-dClpf) modifiziert; zu Kohlendioxid, mit Amin- und Oximderivaten (GO-DMPPA und GO-DClBAO) und um den Transport der Gasmoleküle mit großem kinetischen Durchmesser mit Phosphortrichlorid (PhChGO) zu behindern. Unter diesen Modifikationen wurden GO-AEDPPF und GO-DClBAO für Einzelgastransportexperimente als potenzielle Kandidaten für die Verbesserung der PIM-1-Permeanz und der Selektivitätsstabilität aufgrund der kovalent an GO-Nanopartikel gebundenen großen sperrigen Gruppen ausgewählt. Gleichzeitig sollte die Wirkung einer hohen Partikelbeladung auf die MMM-Gastransporteigenschaften beobachtet werden, um die Membranleistungen mit modernsten Polymeren (Tabelle 3 und zusätzliche Datei 1:Tabelle S1) und Graphen zu vergleichen. beladenen PIM-1-Membranen aus den Gastransportexperimenten, um Rückschlüsse auf folgende Fragen zu ziehen:
-
Was ist der maximale Gehalt eines Füllstoffs, bei welcher selektiven Schicht noch nach dem Lösungs-Diffusions-Mechanismus arbeitet?
-
Ist die Ausrichtung der plattenförmigen Partikel entlang der Oberfläche der Membran mit der Tauchbeschichtungstechnik erreichbar?
-
Gibt es einen Unterschied in den Eigenschaften eines Füllstoffs, der zum Bruch der selektiven Schicht führt?
-
Jeder Hinweis auf eine Membranaffinität gegenüber Gasen, die theoretisch mit funktionellen Gruppen interagieren können.
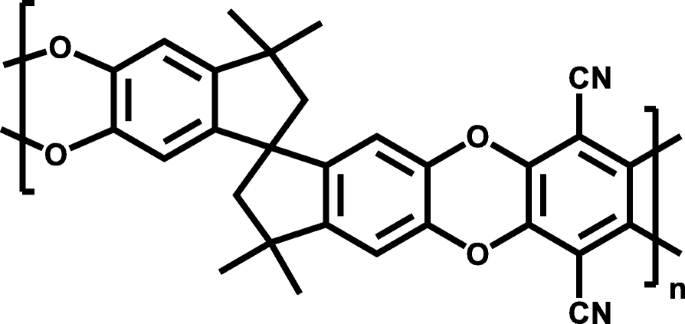
Chemische Struktur des Polymers mit intrinsischer Mikroporosität (PIM-1)
Methoden
Materialien
Graphit (Alfa Aesar, natur, Brikettierqualität, ~ 100 mesh, 99,9995%), 2,4-Dichlorbenzamidoxim (DClBAO, 97%) und Tetrahydrofuran (THF) „zur Synthese“-Qualität wurden von Alfa Aeser (Karlsruhe, Deutschland) bezogen. . Natriumnitrat (NaNO3 .) , 99,5%) und N ,N -Dimethylformamid (DMF) „zur Synthese“-Qualität wurden von Merck (Darmstadt, Deutschland) bezogen, Triethylamin (Et3 N, 99%) von ABCR (Karlsruhe, Deutschland), H2 O2 (Ph. Eur. Stabilized, 30%) von Roth, 2,5-Dimethyl-6-phenylpyrazolo(1a)-pyrimidin-7-amin (DMPPA, 98%), (Rp )-1-[(1S)-(1-aminoethyl)]-2-(diphenylphosphino)ferrocen (AEDPPF, 97%), 1,1-Bisdichlorphosphino-ferrocen (dClpf, ≥ 96%), Kaliumpermanganat (KMnO4 , 99,0%), Schwefelsäure (H2 SO4 , 95,0–98,0 %), Thionylchlorid (SOCl2 , 99%), Phosphortrichlorid (PCl3 .) , 99%) und N -Methyl-2-pyrrolidon (NMP,> 99%) von Sigma-Aldrich (Steinheim, Deutschland) und Benzol „zur Synthese“-Qualität von AppliChem (Darmstadt, Deutschland). Alle Materialien wurden wie erhalten verwendet.
Synthese von Graphenoxid
Graphenoxid wurde aus natürlichem kristallinem Graphitpulver nach der Hummers-Methode hergestellt [15]. Also 2 g Graphitpulver, 1 g NaNO3 , und 46 ml konzentriertes H2 SO4 wurden in einem Rundkolben, der in ein Eisbad gestellt wurde, zusammengemischt und 30 Minuten gerührt. Dann 6 mg KMnO4 wurde portionsweise in die Mischung gegeben, um einen Temperaturanstieg über 20 °C zu verhindern, und 2 h gerührt. Anschließend wurde die Temperatur der Suspension auf 35 °C gebracht und eine Stunde auf diesem Niveau gehalten. Dann wurden 92 ml destilliertes Wasser bei Umgebungstemperatur in die bräunlich-graue Paste gegeben, was ein heftiges Aufschäumen und einen Temperaturanstieg auf 98 °C verursachte. Die erhaltene verdünnte, braune Farbsuspension wurde mehrere Minuten bei dieser Temperatur gehalten; während dieser Zeit änderte die Lösung ihre Farbe zu leuchtendem Gelb; und danach wurde die Suspension mit 250 ml warmem destilliertem Wasser weiter verdünnt und mit 20 ml H2 . behandelt O2 um das restliche Permanganat und Mangandioxid zu reduzieren. Während die Suspension noch warm war, wurde sie vakuumfiltriert, um die Ausfällung von Nebenprodukten zu vermeiden [16]. Der Filterkuchen wurde mit warmem Wasser gewaschen und auf einer Sigma 6-16 K Zentrifuge (SciQuip, USA) zentrifugiert. Das erhaltene Sediment wurde auf einer Gamma 1-16 LSC plus Maschine (Martin Christ Gefriertrocknungsanlagen GmbH) gefriergetrocknet.
Synthese von funktionalisiertem Graphenoxid (FGO)
Synthese von chloriertem Graphenoxid (GO-Cl)
Chloriertes Graphenoxid wurde nach dem an anderer Stelle beschriebenen Verfahren synthetisiert [17]. Kurz gesagt, 0,5 g GO, 10 ml Benzol und 50 ml SOCl2 wurden in einem 50-ml-Rundkolben vermischt und 24 h bei 70 °C gerührt. Danach wird der Überschuss an SOCl2 durch Vakuumdestillation entfernt und der Feststoff in Aceton dispergiert. Dann wurde die Suspension filtriert, zweimal mit Aceton gewaschen und 24 h bei 60 °C vakuumgetrocknet.
Synthese von (Rp )-1-[(1S)-(1-Aminoethyl)]-2-(Diphenylphosphino)Ferrocen-modifiziertes GO (GO-AEDPPF)
In Gegenwart von 60 ml DMF ließ man 0,2 g GO-Cl und 3 ml Triethylamin mit 0,02 g (Rp )-1-[(1S)-(1-aminoethyl)]-2-(diphenylphosphino)ferrocen (AEDPPF) bei 130 °C für 3 Tage, um GO-AEDPPF zu erhalten [18]. Nach der Reaktion wurde die Lösung auf Umgebungstemperatur abkühlen gelassen und vakuumfiltriert. Der Filterkuchen wurde mit DMF und einer kleinen Menge destilliertem Wasser gewaschen (um Et3 . zu entfernen N·HCl) und Aceton und bei 60 °C für 24 h vakuumgetrocknet.
Synthese von 2,4-Dichlorbenzamidoxim-modifiziertem GO (GO-DClBAO)
0,2 g GO-Cl wurden in 50 ml NMP in einem 500-ml-Rundkolben dispergiert. Dann wurden in die Suspension in Gegenwart von 3 ml Trimethylamin 0,02 g 2,4-Dichlorbenzamidoxim (DClBAO) zugegeben, die Reaktionstemperatur auf 157 °C eingestellt und 72 h lang gehalten, um GO-DClBAO zu erhalten. Nach der Reaktion wurde die Suspension unter Vakuum filtriert, mit NMP und einer kleinen Menge destilliertem Wasser gewaschen (um Et3 . zu entfernen N·HCl) und 24 h bei 40 °C vakuumgetrocknet.
Synthese von Polymer mit intrinsischer Mikroporosität
Polymer mit intrinsischer Mikroporosität (PIM-1) wurde auf dem in den Referenzen [19, 20, 21, 22, 23] beschriebenen Weg synthetisiert. Das synthetisierte Polymer wurde 2 Tage bei 70 °C unter Vakuum getrocknet, bevor es zur Charakterisierung und Herstellung von TFCMs verwendet wurde. Das Molekulargewicht und die Polydispersität von PIM-1 betrugen 200 kg/mol bzw. 4–5, bestimmt durch Größenausschlusschromatographie.
Vorbereitung der Dünnschicht-Verbundmembran
Die Dünnschicht-Verbundmembranen mit der hybriden selektiven Schicht aus Graphenverbindungen und PIM-1 wurden auf einem mikroporösen Polyacrylnitril (PAN)-Träger hergestellt (eigene Herstellung, durchschnittliche Porengröße 22 nm und 15 % Oberflächenporosität) [24] unter Verwendung einer Membrangießmaschine im Labormaßstab [25]. Die Nanopartikel von GO, GO-AEDPPF und GO-DClBAO wurden in der PIM-1-Lösung (1 Gew. % in THF) mit Beladungen von 9, 33, 50, 76 und 84 Gew. % in Bezug auf das Trockenpolymergewicht dispergiert . Vor dem Gießen wurden alle Lösungen 1 h lang mit der Spitze beschallt (mit dem Bandelin Sonoplus-Sonicator).
Die selektive Schichtabscheidung erfolgte durch ein modifiziertes Tauchbeschichtungsverfahren, bei dem der poröse Träger zunächst mit der Polymerlösung in Kontakt gebracht wurde und dann für 1–2 mm angehoben wurde, um einen Meniskus der Polymerlösung zwischen der porösen Membran und der Lösung zu bilden Oberfläche. Die selektive Schicht wurde bei Umgebungsbedingungen gebildet, indem die Polymerlösung (mit einer Geschwindigkeit von 1,56 m/min) aus dem Meniskus gezogen wurde, wodurch eine gleichmäßige, reproduzierbare Beschichtung erzielt wurde. Die Verdampfung des Lösungsmittels wurde nicht kontrolliert oder beeinflusst. Die gebildete Membran wurde bei Umgebungsbedingungen trocknen gelassen.
Charakterisierungen
Fourier-Transformations-Infrarot(FTIR)-Spektren wurden im abgeschwächten Totalreflexions(ATR)-Modus auf einem Bruker ALPHA FT-IR-Spektrometer (Ettlingen, Deutschland) aufgezeichnet. Die Absorptionsmessungen wurden bei Umgebungstemperatur in einem Spektralbereich von 400–4000 cm −1 . durchgeführt mit einer Auflösung von 4 cm −1 und durchschnittlich 64 Scans. UV-Vis-Spektroskopieuntersuchungen wurden an einem Specord 210 Plus Spektrophotometer (Überlingen, Deutschland) im Absorptionsmodus mit einem 2-nm-Spalt im Wellenlängenbereich von 190–1100 nm unter Verwendung einer Ulbrichtkugel durchgeführt. Raman-Spektren wurden unter Verwendung eines Raman-Spektrometers von Senterra (Bruker, Ettlingen, Deutschland) mit einem 532-nm-Anregungslaser und einer 10-fach-Objektivlinse erhalten. Das Ergebnis wurde geschätzt, indem jedes einzelne Spektrum und die Bereiche extrahiert wurden, die dem D (störungsinduzierter Modus, zentriert um 1300 cm −1 .) entsprechen ) und die G-Bänder (Graphitmodus, ca. 1550 cm −1 .) ) wurden durch zwei Gauß-Anpassungen ausgewertet. Die thermogravimetrische Analyse (TGA) wurde verwendet, um den Massenverlust von funktionalisierten GO-Proben als Funktion der Temperatur zu untersuchen. Die Analyse wurde auf einem Netzsch TG209 F1 Iris Instrument (Selb, Deutschland) unter Argonfluss (50 ml min −1 .) durchgeführt ) von 25 bis 900 °C bei 10 K min −1 . Ein Rasterelektronenmikroskop Merlin (Zeiss, Oberkochen, Deutschland), ausgestattet mit einem energiedispersiven Röntgenanalysesystem (EDX) (Oxford, Wiesbaden, Deutschland) wurde verwendet, um sowohl die Oberflächen- als auch die Querschnittsmorphologie der Proben zu charakterisieren. Die Proben wurden auf einem elektrisch leitfähigen Klebeband fixiert und mit ca. 6 nm Kohlenstoff. Sekundärelektronen(SE)-Bilder und die EDX-Spektren wurden bei Beschleunigungsspannungen von 2–3 kV bzw. bei 10 kV aufgenommen. Die GPC-Messung wurde bei Raumtemperatur in THF auf einem Waters-Instrument (Waters GmbH, Eschborn, Deutschland) unter Verwendung eines Brechungsindex-Detektors und Polystyrol-Polymer-Standards mit unterschiedlichen Molekulargewichten (Polymer Labs GmbH) durchgeführt. Die Elementaranalyse (EA) wurde mit einem EuroEA Elementar CHNSO Analyzer (EuroVector, Italien) durchgeführt. Gesamtkohlenstoff, Wasserstoff, Stickstoff und Sauerstoff wurden durch die Trockenverbrennungsmethode bestimmt.
Nach der Membranpräparation wurden die Proben mit einem Durchmesser von 75 mm geschnitten und in die Messzelle der Membrantestanlage und der Gastransporteigenschaften für CH4, . gegeben N2 , O2 , und CO2 wurden bei 30 °C und 500 mbar Speisedruck bestimmt. Der Feeddruck von maximal 500 mbar und der Permeatdruck von maximal 10 mbar geben die Möglichkeit, alle oben genannten Gase als ideal für die Berechnung der Membranpermeanz zu betrachten. Die Versuchsanlage zur Gaspermeation wird an anderer Stelle ausführlicher beschrieben [26]. Die Membranpermeanz (L ) eines Gases kann mit der Gleichung berechnet werden:
$$ L=\frac{V\bullet 22,41\bullet 3600}{RTAt}\ln \frac{\left({p}_F-{p}_0\right)}{\left({p}_F- {p}_{P(t)}\right)} $$ (1)wo L ist die Gaspermeanz (m 3 (STP) m −2 h −1 bar −1 ), V ist das Permeatvolumen (m 3 ), 22,41 ist das Molvolumen (m 3 (STP) kmol −1 ), 3600 ist der Umrechnungsfaktor (s h −1 ), R ist die ideale Gaskonstante (0,08314 m 3 Balken K −1 kmol −1 ), T ist die Temperatur (K), t ist die Messzeit zwischen Permeatdruckpunkten p 0 und p P(t) (s), A ist die Membranfläche (m 2 ) und p F , p 0 , und p P(t) sind die Drücke auf der Feed-, Permeatseite zu Beginn bzw. zum Ende der Messung (mbar). Die ideale Selektivität für ein Gaspaar A und B (αA/B ) kann durch die Gleichung berechnet werden:
$$ {\alpha}_{A/B}=\frac{L_A}{L_B} $$ (2)Ergebnisse und Diskussion
Synthese und Charakterisierung von GO und FGO
Die Synthese von GO aus kristallinem Naturgraphitpulver nach der Hummers-Methode wird im experimentellen Abschnitt beschrieben. In dieser Arbeit werden die Modifizierung von Graphenoxid durch Einführung verschiedener funktioneller Gruppen und Eigenschaften der resultierenden Materialien diskutiert. Synthetisiertes GO ergibt ein nicht-stöchiometrisches Material, das verschiedene sauerstoffhaltige funktionelle Gruppen enthält, wie phenolische –OH-, Epoxy- (C-O-C) und Carboxyl- (-COOH)-Gruppen, die sowohl in der Grundebene als auch entlang der Kanten [27]. GO wurde durch Einführung verschiedener funktioneller Gruppen chemisch modifiziert.
Schema 1 und zusätzliche Datei 1:Schema S1 repräsentiert die GO-Synthese und ihre Modifikation zu GO-Cl und 1,1-Bisdichlorphosphinoferrocen-modifiziertes Graphenoxid (GO-dClpf) bzw. phosphochloriertes Graphenoxid (PhChGO), während Schema 2 GO beschreibt -Cl-Modifikation zu GO-DMPPA, GO-DClBAO und GO-AEDPPF mit 2,5-Dimethyl-6-phenylpyrazolo[1,5-a]-pyrimidin-7-amin, 2,4-Dichlorbenzamidoxim und (R p )-1-[(1S)-(1-Aminoethyl)]-2-(diphenylphosphino)ferrocen. Das Syntheseverfahren für GO-dClpf, PhChGO und für GO-DMPPA ist in den Begleitinformationen beschrieben.
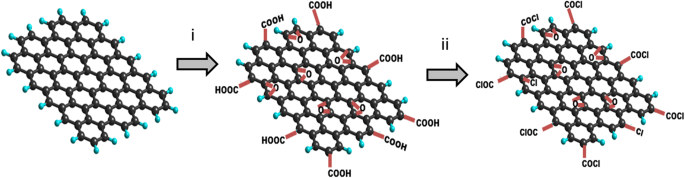
Synthese von chloriertem Graphenoxid (GO-Cl) nach der Hummers-Methode wobei (i) KMnO4 , NaNO3 , H2 SO4 , H2 O2; (ii) SOCl2
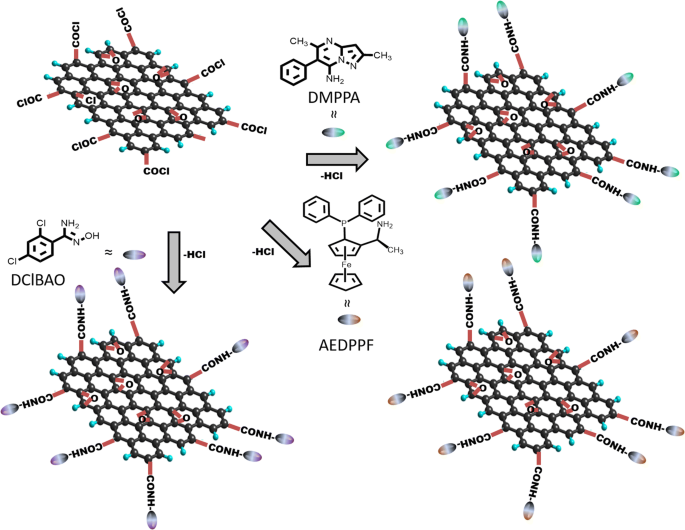
Synthese von GO-DMPPA, GO-AEDPPF und GO-DClBAO aus GO-Cl
Frühere Berichte zeigten, dass GO sowohl in den Basalebenen als auch an den Kanten funktionelle Sauerstoffgruppen enthält, die nukleophile Substitutionsreaktionen beispielsweise mit Aminen [28, 29] und Ferrocen [30] eingehen können. In der vorliegenden Studie werden nukleophile Substitutionen von Graphenoxid durch modifiziertes Ferrocen und verschiedene Amine diskutiert.
Die elementare Zusammensetzung von Graphenoxid und Produkten seiner Modifikationen wurde durch Elementaranalyse analysiert und die Ergebnisse sind in Tabelle 1 aufgeführt.
Die Elementaranalyse gibt Aufschluss über die Massenzusammensetzung der präparierten graphenbasierten Proben. Wie aus Tabelle 1 ersichtlich, beträgt das C/O-Verhältnis für Graphenoxid nach der Synthese 1,42, was auf einen hohen Oxidationsgrad hinweist, der mit dem größten Zwischenschichtabstand einhergeht [31]. GO-DMPPA- und GO-AEDPPF-Proben haben ein C/O-Verhältnis von 5,61 bzw. 5,12, was zusammen mit dem reduzierten Sauerstoffgehalt auf eine erfolgreiche Pfropfung von Aminverbindungen auf das GO-Blatt hindeutet.
Folglich untersuchten wir Graphit und GO durch REM- und EDX-Analyse. Die REM-Bilder in Abb. 2 zeigen den Unterschied in der Graphitmorphologie vor und nach dem Oxidationsprozess.
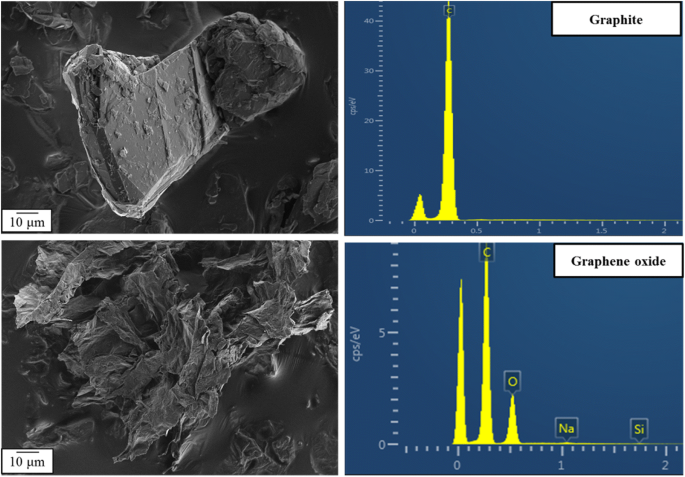
REM-Bilder und EDX-Spektren zeigen die Morphologie (links) und die detektierten Elemente (rechts) von Graphit (oben) und GO-Partikeln (unten)
Die EDX-Analyse (Abb. 2) bestätigte die Änderung der elementaren Zusammensetzung des Graphits nach seiner Modifikation zu GO. Ein Anstieg der Sauerstoffmenge zeigt den erfolgreichen Oxidationsprozess an. Andere Elemente in den EDX-Spektren chemisch modifizierter Proben zeigen das Aufpfropfen kleiner Verbindungen auf Graphenschichten (zusätzliche Datei 1:Abbildung S1).
Chemische Modifikation und erfolgreiches Pfropfen verschiedener Verbindungen auf GO wurden durch spektroskopische Methoden wie FTIR, UV-Vis und Raman-Spektroskopie bewertet. Abbildung 3 zeigt die FTIR-Spektren von GO, chloriertem GO und chemisch modifiziertem GO, die Informationen über chemische Wechselwirkungen zwischen GO und anderen chemischen Verbindungen liefern. Das FTIR-Spektrum von Graphit (Abb. 3) erscheint im IR-Bereich flach und strukturlos. Pristine GO zeigte starke FTIR-Streckschwingungen bei 3000–3700, 1725, 1628, 1226 und 1055 cm −1 entsprechend den intermolekular gebundenen –OH-Streckschwingungen der Hydroxylgruppe, –C=O-Streckung (–COOH-Gruppe), nicht oxidierte graphitische Domänen, C–O-Streckung (–COOH-Gruppe) und C–O–C-Oxiranstreckung (Epoxidgruppe) Vibrationen (Abb. 3). Nach der Thionylchloridbehandlung wurden die Carboxylstellen von GO in Säurechloride umgewandelt. Dies wurde durch Peakverschiebungen im FTIR-Spektrum und das fast Verschwinden des breiten Peaks bei 3000–3700 cm −1 . angezeigt . Somit verschiebt sich das Band, das –C=O Streckschwingungen darstellt, von 1725 auf 1717 cm −1 was auf den negativen induktiven Effekt des Chloratoms in der –COCl-Gruppe und die Anwesenheit von Chinonen hindeutet [32, 33], was zu Fehlstellendefekten [34] auf dem GO-Faltblatt führt. Ein neues Band bei etwa 1800 cm −1 zeigt die Reaktion zwischen –COOH und SOCl2 . Absorptionsbanden bei 1210 cm −1 und 717 cm −1 beschreiben die C–O-Streckschwingungen in der –COCl-Gruppe bzw. die C–Cl-Bildung in GO. Streckschwingungen von C–O–C bei 1050 cm −1 werden immer noch beobachtet.
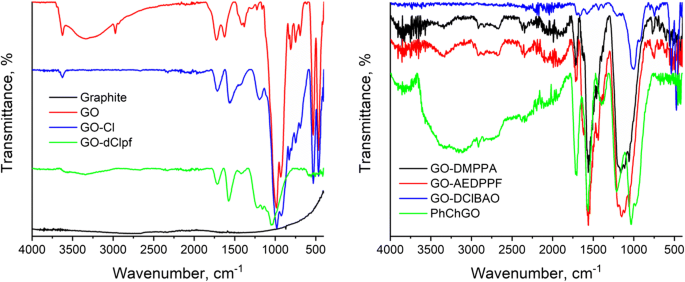
FTIR-Spektren von GO und seinen Modifikationen
Im Vergleich zu reinem GO und GO-Cl zeigte Amin- und Imin-modifiziertes GO (GO-DMPPA, GO-AEDPPF und GO-DClBAO) die neuen Peaks zwischen 1500 und 1650 cm −1 entsprechend Reaktionsprodukten zwischen GO und Amin und Iminverbindungen. Auftreten von Peaks bei etwa 1560 cm −1 zeigen N–H-Biegeschwingungen in der –CONH-Gruppe und bei 1240 cm −1 stehen für C-N-Streckung (Pfropfen auf den aromatischen Ring). Dies bestätigt Amidbindungen während des Pfropfens. Ein leichter breiter Peak bei 3200–3600 cm −1 gehört zu N-H-Streckschwingungen, während Spitzen bei 1700, 1717 und 1734 cm −1 . liegen zeigen das Vorhandensein von Chinonen und Lactonen.
Bei GO-dClpf und PhChGO liegen die Streckschwingungen für die C–O–P-Gruppe (verbunden mit aromatischen Ringen) bei 1054 cm −1 . Dehnungsband bei 644 cm −1 zeigt eine P-Cl-Bindung an, wenn der Peak bei 1232 cm −1 . liegt zeigt eine P=O-Streckschwingung, die das Vorhandensein von –OH-Gruppen in der Phosphoreinheit beschreibt.
Zusätzliche Datei 1:Abbildung S2 zeigt die UV-Vis-Spektren von GO und seinen Modifikationen. π-π * Übergang der Carbonylgruppe wurde zwischen ~ 190 und ~ 200 nm beobachtet, während n-π * Der Übergang dieser Gruppe kann bei ~ 265 und ~ 273 nm in GO und seinen Modifikationen beobachtet werden. Der Absorptionspeak bei etwa ~ 248 nm wird auf π-π * . zurückgeführt Übergang von C=C-Bindungen aus der ursprünglichen Graphitstruktur. Der bei UV-Vis-Messungen beobachtete Bereich von ~ 295–310 nm wird dem n-π * . zugeordnet Übergänge aufgrund von C-O-C- und C-O-P-Verknüpfungen (zusätzliche Datei 1:Abbildung S2).
Als leistungsfähige Technik wurde die Raman-Spektroskopie zur Charakterisierung von sp . verwendet 3 und sp 2 Hybridisierung der Kohlenstoffatome und Untersuchung von geordneten vs. ungeordneten Kristallstrukturen [35]. Die Raman-Spektren von GO und seinen Modifikationen zeigen (Abb. 4) die D-Banden bei ~ 1340 und ~ 1350 cm −1 , charakteristische Lorentzsche G-Bande bei ~ 1580 und ~ 1585 cm −1 und 2D-Peaks bei ~ 2700 cm −1 . Die Daten sind in Tabelle 2 zusammengefasst.
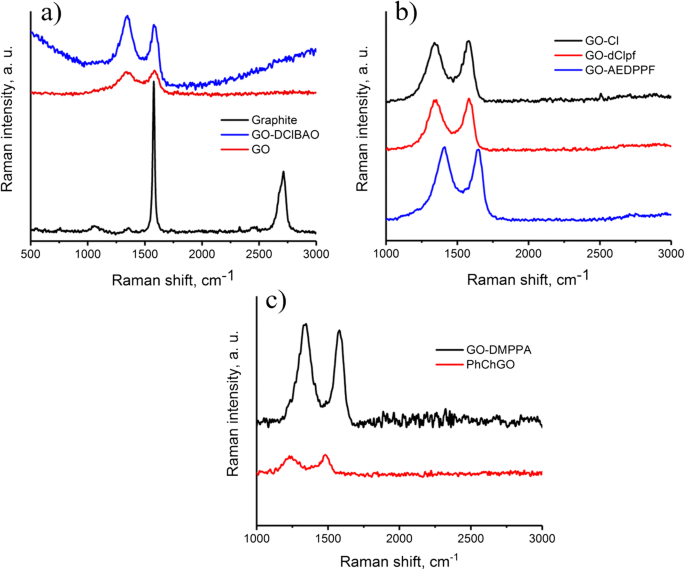
Raman-Spektren von a Graphit, GO und GO-DClBAO; b GO-Cl, GO-dClpf und GO-AEDPPF; und c GO-DMPPA und PhChGO
Das D-Band wird lokalen Defekten und Störungen zugeschrieben, während das G-Band dem E zugeordnet wird 2g Phonon des Kohlenstoffs sp 2 Atome des Graphitgitters. Das 2D-Band gibt Auskunft über die Graphenschichten [35]. Die 2D-Bande von Monolayer-Graphen zeigt jedoch einen einzelnen scharfen Peak. Das Intensitätsverhältnis der D- und G-Bande wird häufig zur Bestimmung der Schichtanzahl verwendet:I D /Ich G für alle Proben war ~ 1, was darauf hindeutet, dass GO-Schichten mehrschichtig sind (Abb. 4).
Um die thermische Stabilität von GO und seinen Modifikationen zu untersuchen, wurde die thermogravimetrische Analyse durchgeführt (Zusatzdatei 1:Abbildung S3). Das makellose GO wurde in zwei Hauptschritten abgebaut. Der erste Schritt (25–140 °C) um 15 % Gewichtsverlust lässt sich durch die Verdunstung des aufgenommenen Wassers erklären. Ein ähnliches Verhalten findet sich für GO-Cl mit einem Gewichtsverlust von 6%, GO-AEDPPF, 2%; GO-DMPPPA, 1%; GO-DClBAO und GO-dClpf, 7%; und PhChGO—11 %. Ein weiterer großer Gewichtsverlust von etwa 33 % tritt im Temperaturbereich von 140–350 °C auf und entspricht der Zersetzung labiler sauerstoffhaltiger Funktionalitäten. Das Pfropfen von Aminen und Iminen erhöhte die thermische Stabilität von GO im Temperaturbereich von 200–500 °C [28]. Der Gewichtsverlust für diese GO-Modifikationen liegt bei etwa 35%. Die größten Gewichtsverluste für GO-Cl, GO-dClpf und PhChGO werden im zweiten Schritt gesehen:100–240 °C für GO-Cl um 28 %, 120–360 °C für GO-dClpf um 32 % und 150 –280 °C für PhChGO um 25 %. Der geringere Gewichtsverlust von modifiziertem GO unter 100 °C weist auf eine verbesserte Hydrophobie hin, die die Menge an absorbiertem Wasser im Vergleich zu reinem GO minimiert.
Zusätzliche Datei 1:Abbildung S4 zeigt die SEM-Bilder von GO und seinen modifizierten Derivaten. Nach der Funktionalisierung wurde die Morphologie von Graphen (zusätzliche Datei 1:Abbildung S4) erheblich verändert, und es sollte erwähnt werden, dass die Morphologie der vom REM beobachteten Graphenschichten nicht annähernd der Ebene entspricht. Diese Beobachtung ist wichtig für die Bildung einer Dünnschicht-Verbundmembran, bei der die selektive Schicht oft im Bereich von 100 nm liegt [36]. Bei diesem Verfahren können Graphenoxidschichten in der Polymermatrix unter den Scherkräften falten und den Gastransport behindern. Die REM-Bilder von modifizierten Graphenoxidproben zeigen, dass ihre Morphologie nicht eben ist, was uns Informationen darüber gibt, dass diese Modifikationen den oben genannten Kräften widerstehen können.
TFC-Membranmorphologie
Oberflächenmorphologie der TFC-Membranen
Um den Einfluss von plättchenförmigen Füllstoffen mit unterschiedlichen funktionellen Oberflächengruppen auf die Morphologie der TFC-Membran und die Gastransportleistung zu bewerten, wurden die drei synthetisierten graphenbasierten Proben GO, GO-AEDPPF und GO-DClBAO als Füllstoffe für PIM-1 dient als Matrixpolymer der selektiven Schicht der TFC-Membran. TFC-Membranen wurden unter Verwendung von PIM-1/GO-, PIM-1/GO-AEDPPF- und PIM-1/GO-DClBAO-Dispersionen mit unterschiedlichen Füllstoff-zu-Polymer-Verhältnissen (9 Gew. %, 33 Gew. %, 50 Gew. %, 76 Gew. % und 84 Ge %. Das Vorhandensein der Füllstoffe in PIM-1-Lösungen änderte je nach Füllstofftyp die Farbe von gelbgrün zu braun oder dunkelschwarz. Zusätzliche Datei 1:Abbildung S5 zeigt die Bilder von TFC-Membranen, die aus PIM-1- und PIM-1/GO-Derivaten hergestellt wurden.
Zusätzliche Datei 1:Abbildung S6 zeigt die SEM-Oberflächenbilder der TFC-Membranen mit der selektiven Schicht aus reinem und Füllstoff, die PIM-1 enthält. Die Oberfläche der reinen PIM-1-TFC-Membran ist glatt und weist keine Merkmale auf, mit Ausnahme einer für Fokussierungszwecke ausgewählten, die das Vorhandensein von Defekten in der selektiven Schicht anzeigen würde. Eine Erhöhung der Beladungsmenge von GO und seinen Modifikationen in PIM-1 verändert das Aussehen der Membranoberfläche. Bei 76 Gew. % und 84 Gew. % Lösungsladungen von GO (Zusatzdatei 1:Abbildung S6e und f) und bereits bei 50 Gew.-% GO-AEDPPF (Zusatzdatei 1:Abbildung S6i-k) und GO-DClBAO ( Zusätzliche Datei 1:Abbildung S6n-p) Es wurden agglomerierte GO-Partikel beobachtet. Da bis zu einer Lösungsmenge von 50 Gew.% keine sichtbaren Brüche zwischen Polymer- und Füllstoffpartikeln zu beobachten sind, kann man davon ausgehen, dass PIM-1 eine gute Haftung an den synthetisierten Graphenoxidmaterialien aufweist und der Füllstoff relativ gleichmäßig entlang der Membranoberfläche. Um jedoch die Homogenität der Füllstoffverteilung innerhalb der Polymermatrix wirklich zu kennen, wurde auch der Querschnitt der Membranen untersucht.
Querschnittsmorphologie der Membranen
In zusätzlicher Datei 1:Abbildung S7 werden die Querschnittsmorphologien der vorbereiteten TFC-Membranen gezeigt. Die Bilder zeigen, dass die für die TFC-Membranherstellung verwendeten Partikel trotz der chemischen Behandlung des Graphens Agglomerate bilden.
Das Bild der TFC-Membran mit reiner PIM-1-Selektivschicht zeigt, dass das Verfahren zur Beschichtung eines porösen Trägers eine gleichmäßige Polymerschicht mit einer Dicke von ca. 200 nm unter Verwendung einer Polymerlösung mit einer Konzentration von 50 Gew.-%. At 9 wt.% of filler in the solution (9 wt.% to GO/polymer composition) GO particles are oriented along the membrane surface, which is expected due to the presence of shear force applied to the forming selective layer during TFC membrane preparation. A competing additional force orienting the particles parallel to the membrane surface may arise from a strong suction of the solvent into the porous support by capillary force resulting in a complete wetting of the porous PAN sublayer. However, due to the high molecular weight of PIM-1, no significant penetration of polymer into the PAN pores was observed, as it can be seen by a border line between continuous polymer layer and porous substrate in the SEM images of pure PIM-1 and PIM-1 with 9 wt.% of GO. At filler concentrations higher than 50 wt.% for GO and 33 wt.% for GO-AEDPPF and GO-DClBAO strong agglomerations of particles were observed with voids within the graphene agglomerates, which were not filled with the polymer. The presence of voids had led to the Knudsen type of gas flow through the membrane at filler loadings of ≥ 50 wt.%. An increase in permeance in case of GO-AEDPPF and GO-DClBAO incorporation can be explained by this phenomenon.
Gas Transport Performance of Prepared Membranes
Pure gas permeances of TFC membranes for CH4 , N2 , O2 , and CO2 with pure PIM-1 and PIM-1 containing FGO such as PIM-1/GO, PIM-1/GO-AEDPPF, and PIM-1/GO-DClBAO were determined at 30 °C on the home-built gas permeation facility. The data of single gas permeance and ideal selectivity according to Eq. 2 were obtained for at least four stamps of the same batch of each TFC membrane; the permeance was calculated as an average value from at least 10 experimental points. The experimental error was determined from the accuracy of the measurement systems permeate volume calibration, from accuracy of pressure sensors, and from the standard deviation of experimental points. The error of the ideal selectivity was taken as a multiplication of experimental errors of corresponding gas permeances (Additional file 1:Table S1). The data for the selectivities and the comparison of the achieved results with the state-of-the-art polymer membranes are presented in Table 3.
Figure 5 demonstrates that the permeance of all gases decreases drastically when graphene-based nanoparticles are incorporated into the selective layer of the TFC membrane. It can be seen that integrity of the selective layer is lost in cases of all three filler materials when the filler concentration exceeds 50 wt.%. At the same time at filler content lower than 50 wt.%, differences in gas transport properties can be observed.
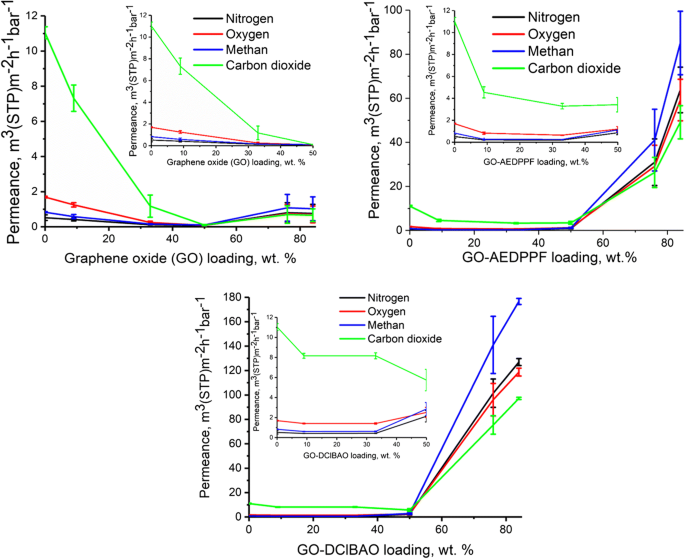
Gas permeances of different gases as a function of GO and its modifications content in PIM-1
In case of GO containing TFC membranes, due to the presence of flat particles in the PIM-1 oriented along the membrane surface a significant decrease of permeances is observed already at 9 wt.% loading and the most significant permeance loss was observed for CO2 . The lowering trend is continued until filler loading 50 wt.% and at higher loadings the selective layer become strongly damaged by GO agglomerates, the permeance of all gases increases and the selectivity does not differ from the Knudsen selectivity (Additional file 1:Table S2; Additional file 1:Figure S11).
According to the Additional file 1:Figure S8, which supports Fig. 5, the permeance loss increased in the line CH4 –O2 –CO2 meaning that “fastest” gases are the most affected by the presence of non-selective graphene based particles. Correspondingly, the selectivity of CO2 und O2 over N2 decreased with the increase of filler content in the polymer.
In comparison to the GO, GO-AEDPPF nanosheets influenced diversely the gas transports properties of MMM. In this case gas permeances were at lowest point at already 33 wt.% loading, remained the same at 50 wt.% and above this filler content the integrity of the selective layer was lost and permeances of all gases increased tremendously due to the presence of non-selective defects as it is shown in Fig. 5.
At 9 wt.% as well as at 33 wt.% loadings of (Rp )-1-[(1S)-(1-aminoethyl)]-2-(diphenylphosphino) ferrocene modified graphene oxide (GO-AEDPPF), selectivities of carbon dioxide and oxygen over nitrogen were higher than those of pure PIM-1 membrane, which indicates the better interaction of the GO-AEDPPF with PIM-1 (Additional file 1:Figure S9).
It was revealed that 2,4-dichlorobenzamidoxime containing graphene oxide (GO-DClBAO) showed the same performance as it was found in GO-AEDPPF case. The incorporation of 9 wt.% GO-DClBAO decreased gas transport through the PIM-1 based selective layer and it stood at the same level up to 33 wt.% loading (Table 3). The selectivity of CO2 und O2 over N2 was lower at these GO-DClBAO loadings when compared with the results for the GO-AEDPPF containing membranes and was almost the same as of pure PIM-1 membrane (Additional file 1:Figure S10).
An increase in permeance after 33 wt.% loading can be explained by loose aggregation of modified graphene oxide nanosheets those allow to permeate gaseous molecules without any hindrance.
Figure 5 proves that up to 33 wt.% incorporation permeance performance for all gases was leveled off at the same point after 9 wt.% loading. An increase in permeance after 33 wt.% loading an increase for methane, oxygen and nitrogen can be explained by the influence of defects on the modified graphene oxide monolayers. Other increases indicate an aggregation of nanosheets.
Figure 6 shows the effect of nanoparticle loading on CO2 permeance and CO2 /N2 selectivity for three types of MMMs. The effect of the GO modification on the membrane performance when the selective layer is loaded with more than 50 wt.% of filler can be observed. The GO nanoparticles appear to have a strong agglomeration tendency accompanied by the ability of these particles to effectively cover the surface of the membrane, creating an effective barrier for gas transport, when compared to other two compounds resulting in mostly non changing CO2 permeance at 50 wt.% and 84 wt.% loadings. The GO-AEDPPF and especially GO-DClBAO containing membranes showed a strong permeance increase at 76 and 84 wt.% loadings indicating properties of the modified GO particles much different from properties of pure GO. The modification of GO with AEDPPF and DClBAO lead to improved particle affinity toward PIM-1 matrix at a particle content below 50 wt.% and to high membrane permeances at 76 and 84 wt.% loadings. Taking into account low permeance of the GO containing PIM-1 TFC membrane at 84 wt.% GO loading and high permeances of both other membranes one can come to the conclusion that modification of the GO with bulky functional groups able to increase polymer-filler compatibility at low filler loadings can change the rigidity of the graphene sheets, which prevents effective alignment of particles along the membrane surface at chosen conditions of TFC membrane preparation. The hypothesis of the particle rigidity change dependent on the functional groups attached to the graphene sheet is to be studied further by e.g. nanoindention method able to characterize mechanical properties of nanometer sized objects [37].
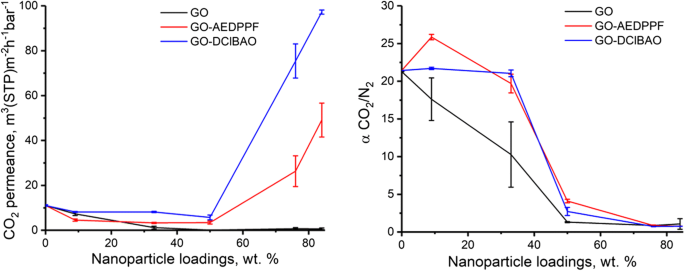
Effect of different FGO incorporation on permeance and selectivity of MMMs
Conclusions
In this study, different functionalizing agents were used to graft them onto graphene sheets. By EDX and elemental analysis, elemental compositions of the samples are confirmed. Thermogravimetric analysis revealed that the grafting of amines and imines on graphene sheets increased their thermal stability. Raman investigations showed that functionalization leads to multilayer flakes formation. TFC mixed matrix membranes containing PIM-1 as a matrix polymer and three different graphene based fillers synthesized in the course of the current work have demonstrated difference of filler materials properties. The pristine GO acts as an effective barrier material for single gas transport through the PIM-1/GO selective layer with both permeance and ideal selectivity decreasing with an increase of the GO loading. The PIM-1/GO TFC membranes with the filler loading 76 and 84 wt.% have shown low gas permeance indicating that GO can be aligned along the membrane surface under the influence of forces available during the casting solution penetration into the porous support. Gas transport properties of the GO embedded into the PIM-1 matrix are much different from properties of the GO-AEDPPF and GO-DClBAO, which have good compatibility to the PIM-1 at 9 and 33 wt.% loading the MMMs show ideal selectivities overpassing those of the pure PIM-1 TFC membrane. When the loading of these two GO fillers is above 50 wt.% the TFC membranes show significant increase of the permeance compared to GO-PIM-1 MMM, indicating that the matrix PIM-1 polymer and forces available during the membrane formation are not able to effectively align these particles along the membrane surface. The observation of high membrane permeance, which is similar to the permeance of the porous PAN membrane, has lead us to the conclusion that introduction of large amounts of bulky functional groups onto the surface of graphene sheet is leading to increase of the graphene rigidity; this effect is to be studied further with methods able to investigate mechanical properties of nanometer-sized objects.
Abkürzungen
- AEDPPF:
-
(Rp )-1-[(1S)-(1-Aminoethyl)]-2-(diphenylphosphino) ferrocene
- DClBAO:
-
2,4-Dichlorobenzamidoxime
- dClpf:
-
1,1-Bisdichlorophosphino-ferrocene
- DMPPA:
-
2,5-Dimethyl-6-phenylpyrazolo(1a)-pyrimidin-7-amine
- FGO:
-
Functionalized graphene oxide
- FTIR:
-
Fourier-Transformations-Infrarotspektroskopie
- GO:
-
Graphenoxid
- GO-AEDPPF:
-
(Rp )-1-[(1S)-(1-aminoethyl)]-2-(diphenylphosphino)ferrocene-modified GO
- GO-Cl:
-
Chlorinated graphene oxide
- GO-DClBAO:
-
2,4-Dichlorobenzamidoxime-modified GO
- GO-dClpf:
-
1, 1-Bisdichlorophosphinoferrocene-modified GO
- GO-DMPPA:
-
2, 5-Dimethyl-6-phenylpyrayolo [1, 5-a]-pyrimidin-7-amine-modified GO
- GPC:
-
Gel permeation chromatography
- PhChGO:
-
Phosphochlorinated GO
- SEM:
-
Rasterelektronenmikroskopie
- TFC:
-
Thin-film composite
- TGA:
-
Thermal gravimetric analysis
Nanomaterialien
- Graphen in Lautsprechern und Ohrhörern
- Graphen- und Polymerverbundstoffe für Superkondensatoranwendungen:ein Rückblick
- Hohe photokatalytische Leistung von zwei Arten von Graphen-modifizierten TiO2-Komposit-Photokatalysatoren
- Mit Titanat-Nanoröhren dekorierte Graphenoxid-Nanokomposite:Vorbereitung, Flammhemmung und Photoabbau
- Biosicherheit und antibakterielle Wirkung von Graphen und Graphenoxid in vitro und in vivo
- Synergetischer Effekt von Graphen und MWCNTs auf die Mikrostruktur und die mechanischen Eigenschaften von Cu/Ti3SiC2/C-Nanokompositen
- Synthese und CO-Oxidationsaktivität von 1D gemischten binären Oxid-CeO2-LaO x -Trägern
- Festkörper-Heizsynthese von Poly(3,4-Ethylendioxythiophen)/Gold/Graphen-Komposit und seine Anwendung für die amperometrische Bestimmung von Nitrit und Iodat
- Bewertung von Graphen/WO3- und Graphen/CeO x -Strukturen als Elektroden für Superkondensatoranwendungen
- Einstufige Kugelmahlvorbereitung von nanoskaligem CL-20/Graphenoxid für deutlich reduzierte Partikelgröße und Empfindlichkeit



