Horizontale Aggregation von Monolayer-reduziertem Graphenoxid unter tiefer UV-Bestrahlung in Lösung
Zusammenfassung
Graphen wird seit Jahrzehnten häufig in neuartigen optoelektronischen Geräten verwendet. Heutzutage wird die Herstellung von großformatigem Monolayer-Graphen mit spektraler Selektivität stark nachgefragt. Hier berichten wir über eine einfache Methode zur Synthese von großformatigen Monolayer-Graphen mit chemisch funktionalisierten Gruppen in Lösung. Das Nano-Graphen mit wenigen Schichten kann unter kurzzeitiger UV-Bestrahlung in protischer Lösung zu einschichtigem Nano-Graphen abgeblättert werden. Das abgeblätterte Monolayer-Nano-Graphen könnte bei längerer UV-Exposition eine Desoxygenierung erfahren. Gleichzeitig konnte die Kante von Nano-Graphen unter tiefer UV-Bestrahlung aktiviert werden und kleine Nano-Graphen-Blätter weiter horizontal in Lösung aggregieren. Die Größe des aggregierten rGO steigt von 40 nm auf maximal 1 μm. Dieser Ansatz könnte in Zukunft eine vielversprechende kostengünstige Methode zur Synthese von großformatigen, monoschichtreduzierten Graphenoxiden sein.
Hintergrund
Graphen ist aufgrund seiner hohen Trägermobilität und hohen optischen Transparenz ein potenzielles Material für ultradünne optoelektronische und Photodetektionsgeräte [1, 2]. Der Schlüssel zur hohen Photoreaktion von Geräten auf Graphenbasis ist die Verschiebung des Fermi-Niveaus, die durch die Anordnung von Ladungsträgern induziert wird [3]. Mit der Entwicklung der chemischen Gasphasenabscheidung (CVD) wird das Wachstum von großformatigem Graphen sowie die Herstellung von Geräten auf Graphenbasis bequem. Jedoch weist ein auf Graphen basierendes Photoreaktionsgerät normalerweise eine schwache Absorption und eine schlechte spektrale Selektivität auf. Die übliche Methode zur Überwindung dieses Nachteils ist die Hybridisierung von Graphen mit Quantenpunkten [4], plasmonischer Nanostruktur [5] oder anderen 2D-Materialien mit Energielücken [6], um eine photoinduzierte Ladungsträgerinjektion zu erreichen. Obwohl das CVD-Verfahren die Herstellung des Wachstums von Graphen mit großer Größe fördert, findet der Abscheidungsprozess gewöhnlich in extremen Umgebungen statt, wie beispielsweise Hochvakuum, hochselektierte Substrate usw. Dies schränkt die Vergrößerungsherstellung für die kommerzielle Herstellung ein. Neue und kostengünstige Methoden müssen dringend entwickelt werden. Die lösungsmittelvermittelte Exfoliation für wenige Schichtflocken ist eine der effizienten und kostengünstigen Methoden bei der Graphenherstellung [7,8,9,10,11,12,13,14,15]. Die am weitesten verbreitete Methode ist die modifizierte Hummer-Methode. Der Graphit kann oxidiert und zu Graphen mit wenigen Schichten abgeblättert werden. Inzwischen enthält Graphen, das durch chemisch oxidierte Exfoliation hergestellt wird, normalerweise verschiedene funktionelle Gruppen, die die optische Absorption und spektrale Selektivität verbessern können. Andererseits schädigt der oxidierte Peeling-Prozess normalerweise die Kristallinität von sp 2 Domäne [16], die eine extrem hohe Temperatur zur Wiederherstellung erfordert. Obwohl der thermische Reaktionsprozess das sp 2 Domäne werden auch fast alle funktionellen Gruppen entfernt, was wiederum zu schwacher Absorption und schlechter spektraler Selektivität führt. Hier berichten wir über eine neue Strategie zur Herstellung großformatiger chemisch funktionalisierter Monolayer-Graphen durch tiefe UV-Bestrahlung. Das geschichtete Nano-Graphen kann unter kurzzeitiger UV-Bestrahlung zu einer Monoschicht abgeblättert werden. Die neue sp 2 Die Domäne kann während einer Langzeit-UV-Exposition wiederhergestellt werden. Darüber hinaus kann das Rand-Kohlenstoffatom während der UV-Bestrahlung aktiviert werden, was dazu führt, dass mehrere Monolayer-Nano-Graphen-Schichten horizontal aggregieren, um große Monolayer-Graphen zu bilden.
Experimentelle Methode
Herstellung von Graphenoxid
Graphenoxid (GO) wurde aus natürlichem Graphit synthetisiert, indem die Hummer-Methode modifiziert wurde, wie in unserer früheren Arbeit beschrieben [17]. Die resultierende Mischung wurde dutzende Male mit 5% HCl-Lösung und DI gewaschen. Schließlich wurde GO-Feststoff nach Gefriertrocknung erhalten.
Synthese von Nano-Graphen mit wenigen Schichten und Wachstum für großformatiges reduziertes Graphenoxid
4,4 mg GO-Feststoff wurden in einen mit Teflon ausgekleideten Autoklaven und 12 ml Ethanol (oder N ,N -Dimethylformamid (DMF)) wurde zugegeben. Die Mischung wurde 5 h auf 176 °C erhitzt. Der Überstand wurde durch eine 0,22 µm mikroporöse Membran filtriert. Schließlich war die kolloidale Lösung die Nano-Graphen-Lösung mit wenigen Schichten.
4,4 mg GO-Feststoff wurden in einen mit Teflon ausgekleideten Autoklaven überführt und 15 ml DI zugegeben. Die Mischung wurde 5 h auf 176 °C erhitzt. Anschließend wurde der Überstand durch eine 0,22 µm mikroporöse Membran filtriert. Die kolloidale Lösung war die Monolayer-Nano-Graphen-Lösung.
Die Exfoliation von Nanographen mit wenigen Schichten und das Wachstum von großformatigem reduziertem Graphenoxid (rGO) wurden durch Bestrahlung mit tiefem UV-Licht (3 W, 254 nm) erreicht, wie in Schema 1 dargestellt.
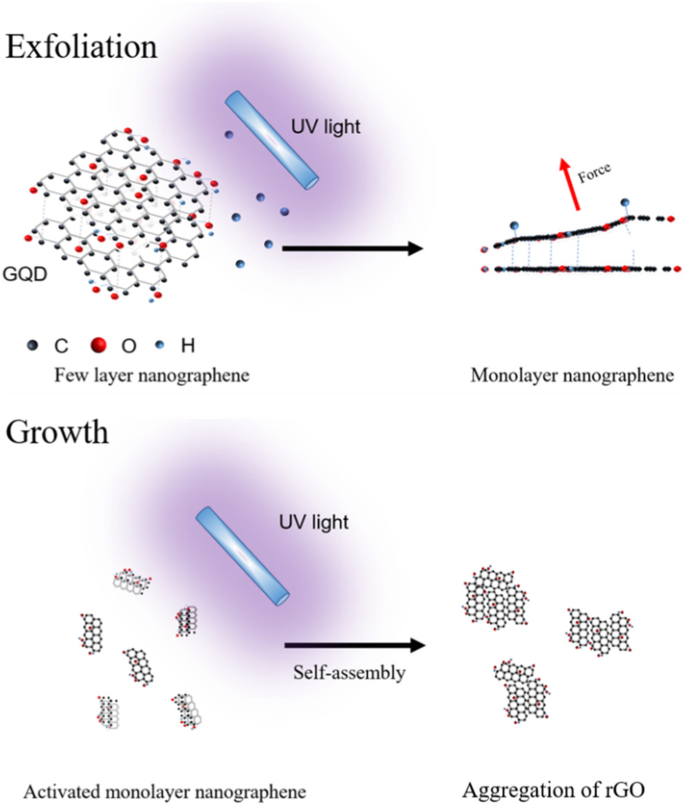
Schematische Darstellung der Exfoliation von Nanographen mit wenigen Schichten zu einer Monoschicht und Aggregation von rGO unter UV-Bestrahlung
Beispielcharakterisierung
Die Photolumineszenz (PL) und das Fourier-transformierte Infrarot (FTIR) wurden auf einem stationären Fluoreszenzspektrometer (FluoroMax-4, Horiba, Jobin Yvon) bzw. einem FTIR-Spektrometer (Nicolet 8700, Thermo Scientific) gemessen. Morphologie und Höhe wurden durch Rasterkraftmikroskopie (AFM) im Tapping-Modus bei Raumtemperatur auf Si-Substrat (NT-MDT Prima) charakterisiert. Die Kristallinität der Probe wurde durch ein hochauflösendes Transmissionselektronenmikroskop (HRTEM) (JEM-2100F, JEOL) bestimmt
Ergebnis und Diskussion
AFM wurde verwendet, um die Morphologie und Größe von Nanographen zu charakterisieren. Die Ergebnisse von Nano-Graphen unter verschiedenen UV-Bestrahlungszeiten sind in Abb. 1 dargestellt. Für das frische Nano-Graphen verteilen sich die Durchmesser hauptsächlich im Bereich von 30–60 nm und die Höhe beträgt> 2,5 nm (Abb. 1a). Die Höhe unseres Nano-Graphen ist ähnlich wie bei chemisch gruppenfunktionalisiertem Nano-Graphen mit 2–3 Schichtdicken [10, 18, 19]. Aus AFM-Daten bestimmen wir, dass mehr als 85% Nano-Graphen durch Stapeln von 2–3 Schichten Nano-Graphen-Monomer durch Van-der-Waals-Kraft (vdW) gebildet werden. Daher benennen wir sie als Nano-Graphen mit wenigen Schichten. Das Nano-Graphen mit wenigen Schichten konnte unter Bestrahlung mit einer 254-nm-UV-Lampe (3 W) zu einschichtigem Nano-Graphen abgeblättert werden. Abbildung 1b–d zeigen die Morphologie von Nanographen mit wenigen Schichten unter 30 s, 50 s bzw. 240 s UV-Bestrahlung. Nach kurzer UV-Belichtung ändert sich die Größe kaum. Die Höhenverteilung für Nano-Graphen unter verschiedenen UV-Belichtungszeiten zeigt jedoch deutlich, dass die Höhe von Nano-Graphen mit wenigen Schichten von> 2,5 nm auf < 1,0 nm nach mehreren Minuten UV-Bestrahlung abnimmt, was darauf hindeutet, dass die wenigen Nano-Graphen-Schichten zu einschichtigen exfoliert.
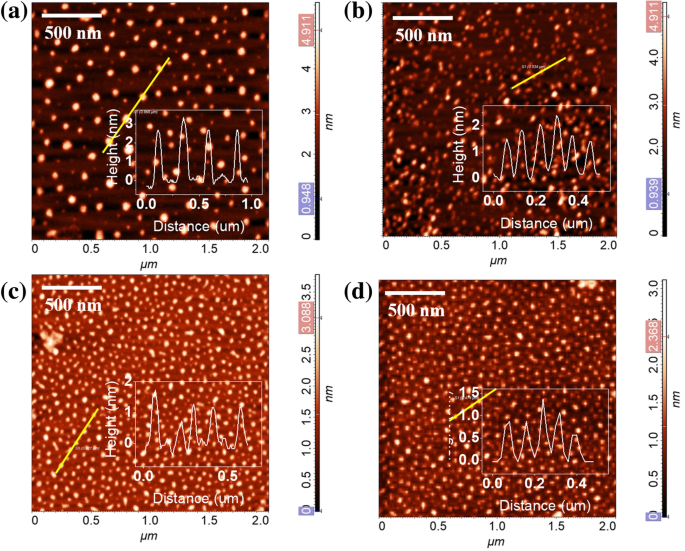
AFM-Bilder von Nano-Graphen mit wenigen Schichten mit verschiedenen UV-Belichtungszeiten a –d :0, 30 s, 50 s, 240 s, Insert ist die Höhenverteilung von Nanographen
Abbildung 2a ist ein hochauflösendes Transmissionselektronenmikroskop (HRTEM)-Bild von einschichtigem Nanographen, das durch UV-Bestrahlung hergestellt wurde. Das Kristallgitter von Nano-Graphen ist deutlich zu erkennen. Die schnelle Fourier-Transformation (FFT) des ausgewählten Bereichs ist im Einschub von Fig. 2a gezeigt und spiegelt die hexagonale Kristallstruktur wider. Der Gitterabstand in der Ebene beträgt 0,219 nm, was mit dem Gitter der [001]-Ebene [20] übereinstimmt.
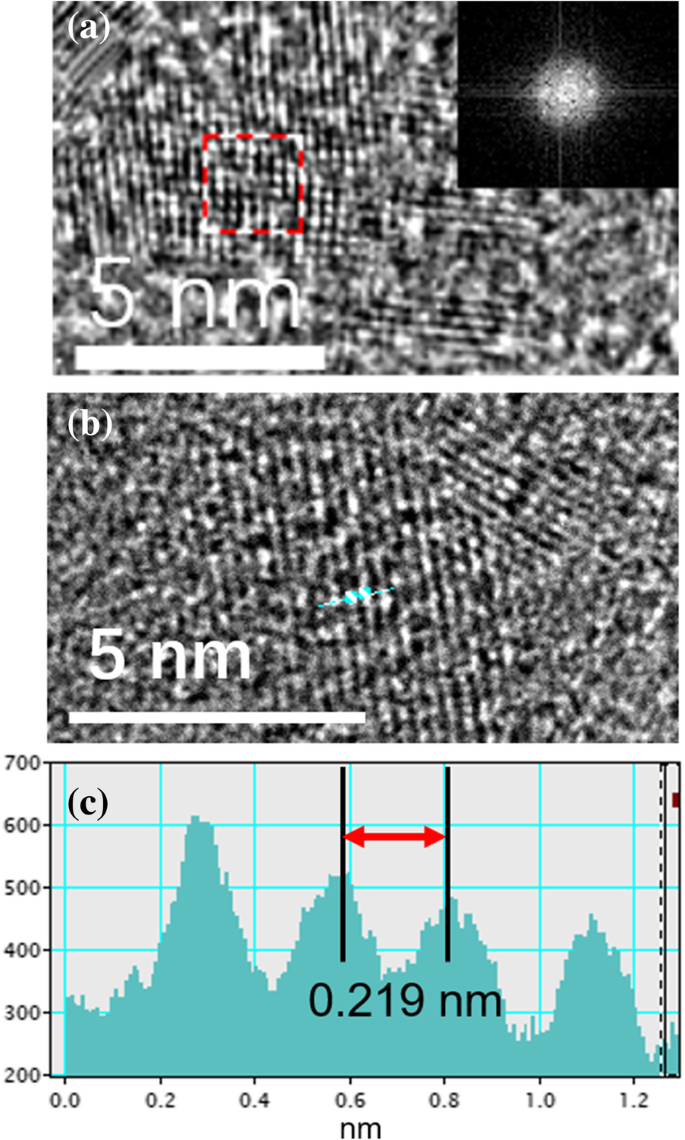
a HRTEM-Bilder von Nano-Graphen. Einschub:FFT-Bild eines ausgewählten Bereichs. b HRTEM und c Linienprofil des ausgewählten Nanographens
Wie von Lee et al. [21] Wasserstoffatome binden an die Oberfläche von Graphen und können Kohlenstoff(C)-Atomen eine Kraft aus der Ebene bringen. Diese Kraft verändert die Konfiguration der Kohlenstoffatome im Graphen und kann die vdW-Kraft zwischen verschiedenen Graphenschichten zerstören. Daher wird das gestapelte Graphen unter der Wirkung von Wasserstoffbrücken zu einer einzigen Schicht abgeblättert. Laut Literatur kann die Raman-Spektroskopie von Graphen wichtige Informationen für die planare Hydrierung in Graphen liefern [21, 22]. Das Intensitätsverhältnis zwischen D und G (Ich D /Ich G ) Modell der Raman-Streuung kann widerspiegeln, wie ein Wasserstoffatom an das Graphen gebunden ist. Um den Exfoliationsmechanismus zu untersuchen, wurden die Raman-Spektren von Nano-Graphen mit wenigen Schichten unter verschiedenen UV-Belichtungszeiten gemessen. Die Ergebnisse sind in Abb. 3 dargestellt. Die Raman-Spektren wurden durch das Lorenz-Modell angepasst, um das Peakintensitätsverhältnis genau zu berechnen. Die Daten zeigen, dass ich D /Ich G steigt von 1.21 auf 1.43 an, was auf das Vorhandensein von bindenden Wasserstoff auf der Nano-Graphen-Oberfläche mit wenigen Schichten nach UV-Bestrahlung hinweist. Das C-Atom bewegt sich in Richtung außerhalb der Ebene und führt zum Brechen der vdW-Kraft zwischen den Graphenschichten [21]. Wie in Schema 1 veranschaulicht, kann sich ein Wasserstoffatom an die Oberfläche von Nanographen mit wenigen Schichten binden, und die durch die Neuordnung des C-Atoms induzierte Kraft außerhalb der Anlage kann das Nanographen mit wenigen Schichten zu Nanographen einschichtig abblättern.
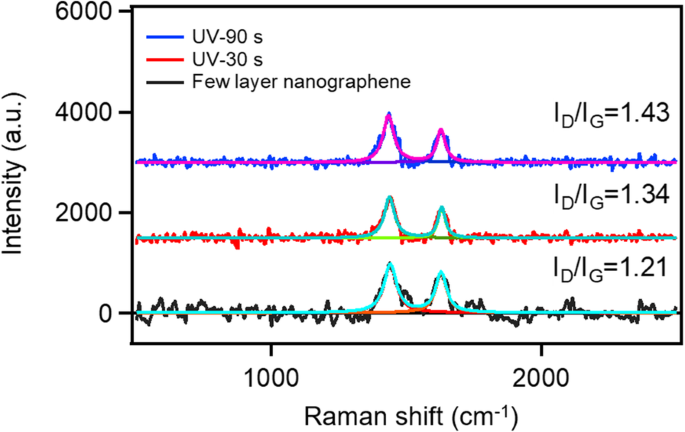
Raman-Spektren von Nano-Graphen mit wenigen Schichten unter verschiedenen UV-Belichtungszeiten
Die Oberfläche des Graphenoxids ist im Allgemeinen reich an sauerstoffhaltigen funktionellen Gruppen wie -COOH, C-OH, C-O-C usw. Diese sauerstoffhaltigen funktionellen Gruppen führen Defektzustände ein, die wichtige Quellen der Graphenoxidlumineszenz sind. Daher ist es sehr wichtig, die Veränderungen der funktionellen Gruppe von Nanographen während der UV-Bestrahlung zu untersuchen. Infrarotabsorption ist eine sehr effektive Methode zur Untersuchung chemischer Veränderungen funktioneller Gruppen. Der Abblätterungsmechanismus kann durch Messung der Veränderungen in den Infrarotabsorptionsspektren des mit ultraviolettem Licht bestrahlten Nanographens besser verstanden werden. Abbildung 4 zeigt die Fourier-Transform-Infrarot(FTIR)-Spektren von Nanographen mit wenigen Schichten bei unterschiedlichen UV-Bestrahlungszeiten. Für die wenigen Nanographenschichten werden Schwingungsmoden für Epoxide gezeigt (C-O-C, 900-1260 cm −1 ). Der Absorptionspeak bei 1740 cm −1 und 3129 cm −1 entsprechen dem Streckmodus von C-Atom-gebundenem Carboxyl (-COOH). Die Absorption bei 2850 cm -1 und 2920 cm −1 offenbaren die Existenz von C-H. Die Breitbandabsorption (3100–3700 cm −1 .) ) mit einem Höchststand von 3450 cm −1 wird auf die Hydroxylgruppen (-C-OH) zurückgeführt. Die C=C-Absorption von intrinsischem sp 2 Domain bei 1641 cm −1 wird ebenfalls präsentiert. Nach kurzer Zeit (240 s) mit UV-Bestrahlung änderten sich die Peaks der Epoxygruppe, Hydroxylgruppe, Carboxylgruppe und C=C nicht signifikant. Der Absorptionspeak von C-H wird jedoch ausgeprägter. Dies stimmt mit dem von Raman erhaltenen Ergebnis überein, das darauf hinweist, dass das H-Atom an das C-Atom bindet und die Absorption von C-H verstärkt. Es zeigt auch, dass eine kurzzeitige UV-Bestrahlung nicht zur Reduktion von Nano-Graphen führt und funktionelle Sauerstoffgruppen in Nano-Graphen sich während des Peeling-Prozesses nicht ändern.
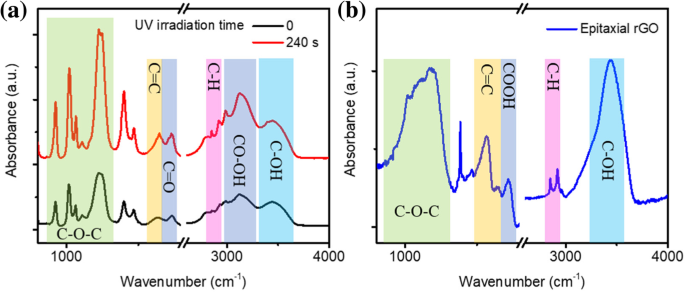
FTIR von (a ) Nanographen mit wenigen Schichten (schwarze Linie), Nanographen mit wenigen Schichten (rote Linie) und (b) epitaktisches Nanographen
Andererseits ändern sich die FTIR-Spektren von Nano-Graphen nach einer langen UV-Bestrahlung (2 h) signifikant (Abb. 4b). Die erste Änderung ist die Absorption von -COOH bei 3150 cm −1 wird deutlich reduziert. Gleichzeitig tritt eine neue C-O-C-Absorption auf, die sich mit der vorherigen C-O-C-Absorption überlappt, was zu einer umfangreichen C-O-C-Absorption führt. Zweitens bewegt sich die Absorption von C=O von 1740 cm −1 in Richtung niedriger Wellenzahl (1720 cm −1 .) ). Dies ist auf die Zunahme des Konjugatsystems zurückzuführen. Die dritte große Änderung ist das Auftreten eines neuen C=C-Absorptionspeaks in der Ebene bei 1562 cm −1 . Dies liegt daran, dass dieser Photoreduktionsprozess von GO eine Desoxygenierung induzieren und das sp 2 . wiederherstellen kann Domäne [16, 23, 24]. Schließlich wird eine weitere Verbesserung der C-H-Absorption beobachtet, da sich mehr H-Atome mit C-Atomen verbinden.
Um den Effekt von Schichtänderungen auf die optischen Eigenschaften zu untersuchen, messen wir die stationäre Fluoreszenz von Nano-Graphen unter verschiedenen UV-Belichtungszeiten. Abbildung 5a zeigt die PL-Spektren von Nano-Graphen bei unterschiedlicher UV-Bestrahlung. Das so hergestellte Nanographen mit wenigen Schichten emittiert reines tiefes UV-Licht mit einem Spitzenwert von 307 nm und die Intensität nimmt mit zunehmender UV-Bestrahlungszeit schnell ab. In der Zwischenzeit nimmt die PL-Intensität bei 500 nm zu. Die Kurven in Abb. 5b zeigen die Beziehung zwischen den UV-Bestrahlungszeiten und der PL-Intensität bei 307 nm und 500 nm. Mit zunehmender UV-Bestrahlungszeit verschwindet die 307-nm-Emission fast und die 500-nm-Emission des sichtbaren Lichts dominiert das PL-Spektrum während des Peeling-Prozesses.
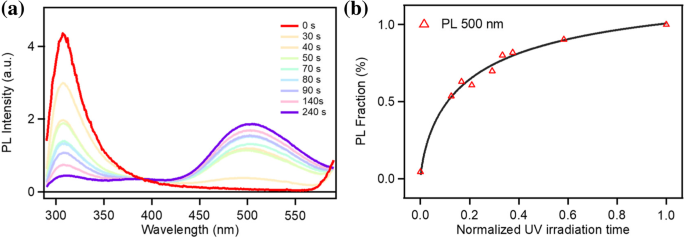
Stetige PL-Spektren von Nano-Graphen mit wenigen Schichten mit verschiedenen UV-Belichtungszeiten, angeregt bei 270 nm
Die Fluoreszenz von Graphen wurde systematisch untersucht. Der Ursprung der Lumineszenz wird hauptsächlich der Eigenzustands-induzierten Fluoreszenz zugeschrieben, die durch das sp 2 . verursacht wird Domain (302–380 nm) und sp 3 Defektlumineszenz verursacht durch die sauerstoffhaltige funktionelle Gruppe [19, 25, 26, 27]. Für die wenigen Schichten Nano-Graphen bildet sich der Van der Waals (vdW) Heteroübergang aufgrund der Stapelung von wenigen Schichten Nano-Graphen. Der vdW-Heteroübergang führt eine hohe Ladungstrennung durch. Das angeregte Elektron in Oberflächendefektzuständen, die durch funktionelle Sauerstoffgruppen induziert werden, würde in durch C=C sp 2 . induzierte intrinsische Zustände übergehen Domäne aufgrund der durch das Stapeln induzierten Bandverbiegung. Die wenigen Nano-Graphen-Schichten emittieren reines UV-Licht. Wir ordnen Lumineszenz mit Peak bei 307 nm der Fluoreszenz des Eigenzustands von sp 2 . zu Domain. Der sichtbare Anteil (Peak bei 500 nm) wird hingegen aus der Lumineszenz der Defektzustände abgeleitet, wie Literaturberichte [19, 25]. Es ist klar, dass die Fluoreszenz des Eigenzustands von sp 2 Die Domäne verschwindet allmählich, wenn das Nano-Graphen zu einer Monoschicht abgeblättert wird, und wir glauben, dass die Dickenänderung des Nano-Graphen der Hauptgrund für die Fluoreszenzänderung ist.
Für eine klarere, intuitive Darstellung der Änderung der funktionellen Graphenoxidgruppen während des Reduktionsprozesses haben wir die stationäre Fluoreszenz während des Reduktionsprozesses gemessen (Abb. 6). Die Fluoreszenz des sichtbaren Teils von Nanographen wird von Oberflächendefekten abgeleitet, die durch sauerstoffhaltige funktionelle Gruppen verursacht werden. Unterschiedliche funktionelle Gruppen verursachen unterschiedliche Tiefen von Defektzuständen, die auch zu unterschiedlicher Fluoreszenzemission führen [26, 27]. Konkenaet al. untersuchten im Detail die Beziehung zwischen funktionellen Gruppen und Fluoreszenz. Die Fluoreszenz unseres Nanographens bei 500 nm leitet sich von der deprotonierten Carboxylgruppe ab. Wie in Abb. 6 gezeigt, führt eine Verlängerung der UV-Belichtungszeit zu einer allmählichen Abnahme der PL-Intensität bei 500 nm und der Emissionspeak verschiebt sich von 500 nm auf ungefähr 475 nm nach 2 Stunden UV-Bestrahlung. Die Entwicklung der Spektren im sichtbaren Bereich ähnelt derjenigen, die beim chemischen Reduktionsprozess von Graphen beschrieben wurde [16, 28]. Die charakteristische Emission bei 500 nm ist das Symbol für Carboxylgruppen in ihren Deprotonierungszuständen. Die blaue (475 nm) Emission stammt von den dissoziierten Carboxylgruppen [28]. Mit zunehmender UV-Bestrahlungszeit wurden die Carboxylgruppen dissoziiert, was mit dem Verschwinden der IR-Absorption von C=O bei 1730 cm –1 . übereinstimmt (Abb. 4). Somit zeigen die PL-Spektren eine Abnahme und eine Blauverschiebung der sichtbaren Emission.
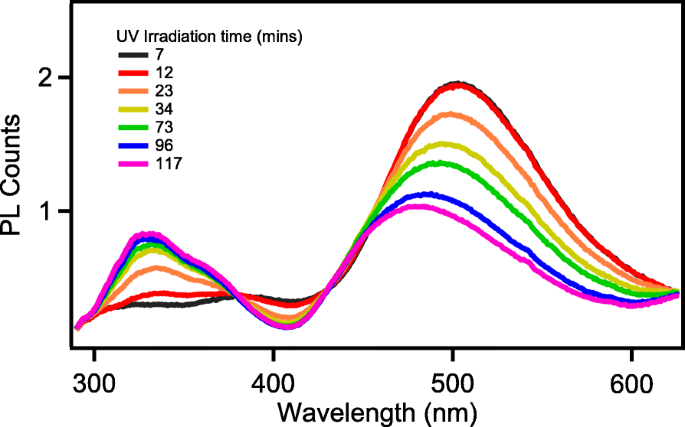
Konstanter PL von Monolayer-Nanographen nach unterschiedlichen UV-Expositionszeiten
Begleitet von der sichtbaren Emissionsänderung wird ein überraschendes Phänomen gezeigt, die UV-Emission zentriert bei 326 nm mit einer Schulter bei 360 nm und nimmt mit der Reduktionszeit zu. Die Reduktion von Graphenoxid wird normalerweise von der Bildung eines neuen sp 2 . begleitet Domäne [29]. Wir vermuten, dass dies an der Aggregation von Nano-Graphen liegt, die eine Zunahme der ultravioletten Fluoreszenz verursacht.
Um die Veränderungen der physikalischen Struktur von Nano-Graphen nach längerer UV-Bestrahlung weiter zu untersuchen, haben wir die Morphologie von rGO mit AFM gemessen. Wie in Abb. 7 dargestellt, wurden nach 2 Stunden UV-Bestrahlung viele große Nanoblätter beobachtet. Die Größenverteilung von rGO ist viel breiter (300–750 nm) im Vergleich zu der von Nanographen im präparierten Zustand. Die erhöhte Größe kann auf die horizontale Aggregation von Monolayer-Nanographen zurückgeführt werden. Das vergrößerte AFM-Bild zeigt deutlich, dass die größeren Nanoblätter von vielen kleinen Nanographenblättern mit einer durchschnittlichen Höhe von 0,7 nm umgeben sind. Nach dem Desoxygenierungsprozess sind die O-Atome am Rand des Nano-Graphen aktiv und könnten sich mit dem Rand-C-Atom eines anderen Nano-Graphen verbinden, um neue Epoxide zu bilden. Wie in Schema 1 dargestellt, nimmt mit zunehmender Reduktion die Zahl der aktivierten Nanographene zu und die Größe würde weiter zunehmen. In Anbetracht dessen, dass mit verlängerter UV-Bestrahlungszeit der ultraviolettes Licht emittierende Abschnitt verstärkt wird. Wir glauben, dass die UV-Lumineszenz bei 326 nm auf die Aggregation von Nanographen zurückzuführen ist. Mit zunehmender Anzahl der Agglomerate nimmt auch die Intensität der ultravioletten Fluoreszenz zu. Das einschichtige Nanographen ist stabil und selbst nach 2 Stunden UV-Bestrahlung wurde kein Niederschlag beobachtet (Abb. 7).
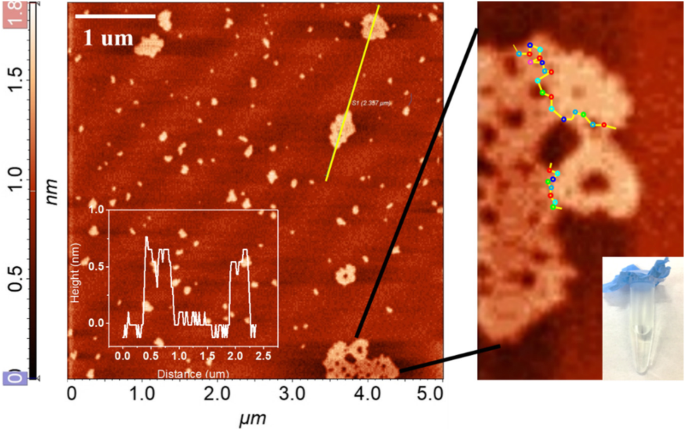
AFM von Monolayer-Nanographen unter übermäßiger UV-Belichtung, Einschub:Digitalfotos von aggregiertem rGO
Da die Intensität direkt mit der Aggregation zusammenhängt, untersuchen wir die Aggregationsdynamik von Nano-Graphen, indem wir den PL im UV-Bereich analysieren. Die UV-Belichtungszeit wurde auf die Konzentration von aneinander gebundenem Nanographen normiert. Abbildung 8 zeigt die Konzentrationskorrelation mit der UV-Intensität. Die experimentellen Daten wurden durch das Langmuir-Adsorptionsisothermenmodell angepasst. Mit zunehmender UV-Belichtungszeit nimmt auch die Zahl des aggregierten Nanographens sowie die Größe zu. Die Zahl des adsorbierten Nanographens kann als N . ausgedrückt werden und die Langmuir-Adsorptionsisotherme kann geschrieben werden als
$$ N=\frac{N_0k{(nx)}^{\left(1-c\right)}}{1+k{(nx)}^{\left(1-c\right)}} $$ (1)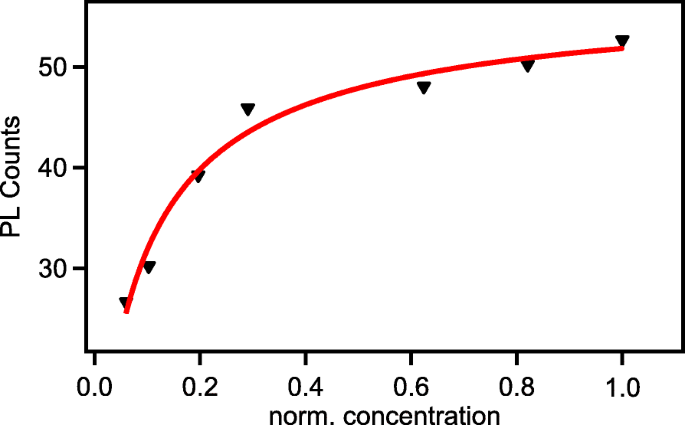
UV-PL-Intensität vs. normalisierte Konzentration
Hier, N 0 ist die anfängliche UV-Intensität. Die zugehörige Gleichgewichtskonstante k kann durch Anpassen der experimentellen Daten erhalten werden. Für ein System im chemischen Gleichgewicht ist die freie Gibbs-Energie gegeben
$$ \Updelta G=- RT1\mathrm{n}(k) $$ (2)Als wir k angewendet haben zur Gl. 2 erhalten wir die freie Gibbs-Energie ∆G ≈ − 4,43 kJ/mol. Das ∆G < 0 zeigt an, dass diese Reaktion bei Raumtemperatur thermodynamisch begünstigt ist [30]. Somit könnten sich mehrere Nanographene horizontal miteinander verbinden, um große Agglomerate zu bilden. Es ist erwähnenswert, dass durch CVD hergestelltes großes Graphen feines sp 2 . besitzt Struktur, enthält aber kaum funktionelle Gruppen für die spektrale Selektivität. Unsere UV-induzierte Nano-Graphen-Aggregation könnte verschiedene funktionelle Gruppen enthalten, die einzigartige optische Eigenschaften aufweisen und als Identifizierungsstellen für den selektiven Nachweis verwendet werden können.
Um die Wirkung von Lösungsmitteln auf die Struktur von Nano-Graphen zu untersuchen, haben wir Nano-Graphen in aprotischem Lösungsmittel DMF und protischem Lösungsmittel H2 . hergestellt O. Abbildung 9 zeigt PL und AFM von Nanographen, das in DMF und H2 . hergestellt wurde O. Die PL von Nano-Graphen in DMF führt eine tiefe UV-Emission durch, die aus der Stapelung der Nano-Graphen-Schicht stammt. Auch nach 115-minütiger UV-Bestrahlung gibt es nur eine geringe Veränderung. Es weist darauf hin, dass nach längerer Einwirkung von ultraviolettem Licht keine Abblätterung oder Aggregation auftritt. Die Höhenverteilung von Nanographen in DMF ist in Abb. 9b dargestellt. Die durchschnittliche Höhe beträgt> 15 nm. Der PL von Nanographen in H2 O ist bei ~ 475 nm zentriert (Abb. 9c). Es gibt eine UV-Emission und eine Spitzenverschiebung bei unterschiedlicher UV-Bestrahlung. Diese sichtbare Emission von Nanographen wird sauerstofffunktionell induzierten Defektzuständen zugeschrieben. Die Höhe von Nanographen in H2 O ist < 1,0 nm (Abb. 9d) und deutet darauf hin, dass das Nanographen eine Monoschicht in H2 . ist O. Die obigen Ergebnisse zeigen, dass die Stapelung von Nanographen durch die Verwendung verschiedener Lösungsmittel kontrolliert werden kann.
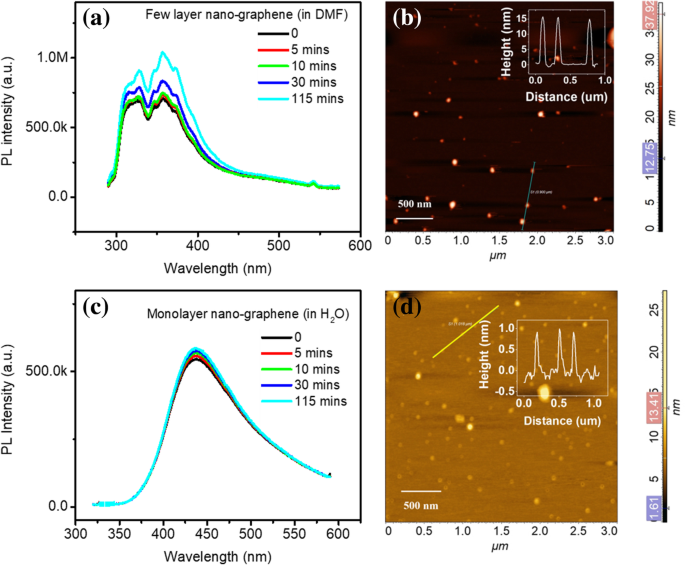
PL- und AFM-Aufnahme von Nanographen in DMF (a , b ) und H2 O (c , d )
Schlussfolgerungen
Zusammenfassend stellten wir fest, dass aufgrund des gebundenen H-Atoms an der Oberfläche unter kurzzeitiger tiefer UV-Bestrahlung in protischer Lösung nur wenige Nano-Graphen-Schichten zu Monoschichten-Nano-Graphen abgeblättert werden können. Das Monolayer-Nanographen könnte unter UV-Bestrahlung im Überschuss zu einer großen Monolayer-rGO aggregieren. Die AFM-Ergebnisse zeigen deutlich, dass eine große Monoschicht rGO durch Aggregation mehrerer kleiner Nanographenschichten gebildet wird. Die Aggregation von kleinem Nano-Graphen stimmt mit dem Langmuir-Adsorptionsisothermenmodell überein, das darauf hinweist, dass die Kante von Nano-Graphen aktiviert werden kann und sich mit anderem Nano-Graphen verbinden kann. Diese UV-induzierte Wachstumsmethode könnte in Zukunft die kostengünstige Herstellung von Monolayer-Graphen in großem Maßstab fördern.
Abkürzungen
- AFM:
-
Rasterkraftmikroskopie
- Lebenslauf:
-
Chemische Gasphasenabscheidung
- FTIR:
-
Fourier-Transformations-Infrarot
- GO:
-
Graphenoxid
- PL:
-
Photolumineszenz
- TEM:
-
Transmissionselektronenmikroskop
Nanomaterialien
- Mit Titanat-Nanoröhren dekorierte Graphenoxid-Nanokomposite:Vorbereitung, Flammhemmung und Photoabbau
- Biosicherheit und antibakterielle Wirkung von Graphen und Graphenoxid in vitro und in vivo
- Graphenoxid-hybridisierte nHAC/PLGA-Gerüste erleichtern die Proliferation von MC3T3-E1-Zellen
- Bewertung von Graphen/WO3- und Graphen/CeO x -Strukturen als Elektroden für Superkondensatoranwendungen
- Eingebetteter Si/Graphen-Verbundstoff, hergestellt durch thermische Magnesiumreduktion als Anodenmaterial für Lithium-Ionen-Batterien
- Einstufige Kugelmahlvorbereitung von nanoskaligem CL-20/Graphenoxid für deutlich reduzierte Partikelgröße und Empfindlichkeit
- Photokatalytische Aktivität des ternären Nanokomposits Attapulgit–TiO2–Ag3PO4 für den Abbau von Rhodamin B unter simulierter Sonneneinstrahlung
- Niedrigtemperatur-Reduktion von Graphenoxid:Elektrische Leitfähigkeit und Rasterkraftmikroskopie mit Kelvin-Sonde
- Das anionische Tensid/ionische Flüssigkeiten mit interkaliertem reduziertem Graphenoxid für Hochleistungs-Superkondensatoren
- Millstone-Peeling:ein echtes Scher-Peeling für großflächiges, wenige Schichten Graphenoxid



