Poröse Kohlenstoffnetzwerke aus Graphitkohlenstoffnitrid für eine effiziente Sauerstoffreduktionsreaktion
Zusammenfassung
Es wurden große Anstrengungen unternommen, um eine wirtschaftliche und effiziente Sauerstoffreduktionsreaktion (ORR) für die Brennstoffzellentechnologie zu finden. Unter verschiedenen Katalysatoren haben N-dotierte kohlenstoffbasierte Nanomaterialien aufgrund ihrer geringen Kosten, Edelmetallfreiheit und guten Haltbarkeit viel Aufmerksamkeit auf sich gezogen. Hier haben wir eine einfache und wirtschaftliche Strategie entwickelt, um stickstoffdotierte Kohlenstoffnetzwerke für eine effiziente ORR-Anwendung vorzubereiten. Die g-C3 N4 wird als Matrize und N-Quelle verwendet, und Dopamin wird als Kohlenstoffquelle verwendet. Durch einfache hydrothermale Behandlung und Sintern konnten N-dotierte Kohlenstoffnetzwerkstrukturen mit hoher spezifischer Oberfläche, effektiver ORR-Aktivität und überlegener Haltbarkeit erhalten werden. Die vorliegende Strategie ist frei von im Allgemeinen mehrstufigen, giftigen Reagenzien und der Komplikation der Entfernung von Templaten für die Herstellung von 3D-Kohlenstoffstrukturen.
Hintergrund
Die Sauerstoffreduktionsreaktion (ORR) ist ein entscheidender Schritt für die Weiterentwicklung sauberer Energieumwandlungsstrategien wie Brennstoffzellen und Metall-Luft-Batterien [1,2,3]. Die traditionellen Kathodenmaterialien auf Pt-Basis für die ORR leiden im Allgemeinen unter hohen Kosten, begrenzter Stabilität und geringer Toleranz gegenüber Methanol [1, 4, 5, 6, 7 8]. Daher hat die Entwicklung eines kostengünstigen, hochaktiven und haltbaren Materials für die ORR große Aufmerksamkeit auf sich gezogen [9, 10]. Es wurden zahlreiche Anstrengungen unternommen, um einen Ersatz für Pt-basierte Elektrokatalysatoren wie Übergangsmetallkatalysatoren [5, 11,12,13] und kohlenstoffbasierte Nanomaterialien [4, 8, 13,14,15,16] zu suchen.
Als metallfreie Elektrokatalysatoren sind kohlenstoffbasierte Nanomaterialien aufgrund ihrer guten Haltbarkeit, Edelmetallfreiheit und geringen Kosten vielversprechende Materialien für die ORR [17]. Durch elegantes Design des Materialsystems konnten 3D-poröse Kohlenstoffstrukturen erreicht werden und eine hohe spezifische Fläche und ein hohes Porenvolumen bereitgestellt werden, was für eine effiziente ORR äußerst wichtig ist [7, 18]. Erwünschte dreidimensionale Kohlenstoffstrukturen, die im Allgemeinen von verschiedenen Templaten abgeleitet sind, einschließlich Eis, Siliciumdioxid und Polystyrol [19]. Die Herstellung der 3D-Kohlenstoffstruktur umfasste im Allgemeinen mehrstufige, giftige Reagenzien und die Komplikation der Entfernung des Templats [6, 20, 21]. Daher ist eine einfache Vorbereitungsstrategie immer noch ein Haupthindernis. Darüber hinaus erhöht die Einführung von N-Atomen in Kohlenstoffmaterialien die elektrokatalytische Aktivität signifikant und führt so zu einer effizienten ORR [22, 23]. Große Anstrengungen haben über N-dotierte Kohlenstoffmaterialien berichtet, indem man stickstoffreiche Quellen wie Melamin [24, 25], Harnstoff [26], Dopamin [27] und Pyrrol einführte, gefolgt von Sintern. Für ORR-Anwendungen ist ein einfacher Weg zur Realisierung einer porösen Struktur und einer effizienten N-Dotierung immer noch sehr erwünscht.
Hier haben wir eine Strategie entwickelt, um stickstoffdotierte Kohlenstoffnetzwerke für eine effiziente ORR-Anwendung unter Verwendung von metallfreiem graphitischem Kohlenstoffnitrid (g-C3 N4 ) und Dopamin (DA) als N-Quelle bzw. C-Quelle. Metallfreies g-C3 N4 wurde aufgrund seiner potentiellen Anwendung für Photokatalyse [9, 28,29,30] und ORR [30,31,32,33] usw. intensiv untersucht. Die N-dotierten Materialien konnten mit gC3 N4 als N-Quelle aufgrund seines hohen N-Gehalts [20, 23, 34, 35]. Die g-C3 N4 ist ein typisches zweidimensionales konjugiertes Polymermaterial [36, 37]. Er hat als kostengünstiger, metallfreier, auf sichtbares Licht ansprechender Photokatalysator große Aufmerksamkeit erregt [38, 39]. Die g-C3 N4 hat eine ausgezeichnete elektronische Bandstruktur, Oberflächenfunktionalisierungsmodifikation und eine hohe physikalische und chemische Stabilität und ist ungiftig und reich an Rohstoffen [40,41,42]. Zudem ist der Stickstoffgehalt hoch und zählt damit zu den bekannten N-reichen Verbindungen [43]. Das Wichtigste ist, dass es eine Vielzahl von 2D- oder 3D-Strukturen aufweist, die durch Kontrolle der Synthesebedingungen erhalten werden können [44,45,46]. Stickstoffdotierte Kohlenstoffmaterialien weisen in der Regel eine Synthesetemperatur von über 800 °C auf, was die Voraussetzungen für die Entfernung des Templats erfüllt [47]. Daher ist es möglich, g-C3 . zu verwenden N4 die nur Kohlenstoff- und Stickstoffelemente enthält, um N-dotierte Kohlenstoffmaterialien zu synthetisieren [48]. In der vorliegenden Arbeit g-C3 N4 wird gleichzeitig als Templat und N-Quelle verwendet, um poröse Kohlenstoffstrukturen mit hoher spezifischer Oberfläche (954 m 2 .) herzustellen g −1 ) und ein N-Gehalt von 5,71% erreicht, was eine vergleichbare ORR-Aktivität, überlegene Haltbarkeit und Methanoltoleranz gegenüber dem Pt/C-Referenzelektrokatalysator aufweist.
Methoden
Materialien
Kaliumhydroxid (KOH) und Kaliumchlorid (KCl) wurden von Sinopharm Chemical Reagent Co., Ltd. bezogen. Kaliumhexacyanoferrat (K3 [Fe(CN)6 ]) wurden von Tianjin Yongsheng Fine Chemical Co., Ltd. bezogen. Harnstoff wurde von Beijing Chemical Corp. bezogen. Alle obigen Arzneimittel sind analytisch rein. Naifon® perfluorierte Lösung (5 Gew.-% in einer Mischung aus niederen aliphatischen Alkoholen und Wasser, enthält 45% Wasser) wurde von Sigma-Aldrich bezogen.
Synthese von g-C3 N4 Vorlage
Typischerweise wurden 15 g Harnstoff in einem 100-ml-Tiegel 4 h bei 550 °C gehalten. Die g-C3 N4 wurde erworben und nach dem Abkühlen auf Raumtemperatur zu hellgelbem Pulver zur späteren Verwendung gemahlen.
Synthese von g-C3N4@Dopamin-Vorstufen
0,5 g g-C3 N4 wurde in 20 ml DA-Lösung dispergiert. Die Konzentration an DA betrug 0,3 M. Die Mischung wurde 2 h mit Ultraschall behandelt und in einen Autoklaven überführt, gefolgt von 10 h Erhitzen auf 120°C. Die resultierende Probe wurde zentrifugiert und gewaschen, gefolgt von Trocknen bei 80 °C über Nacht. Zur Herstellung von g-C3 . wurden drei Heiztemperaturen von 120 °C, 140 °C und 160 °C verwendet N4 /PDA-Vorläufer und die entsprechenden Proben wurden g-C3 . genannt N4 /PDA-120, g-C3 N4 /PDA-140 und g-C3 N4 /P DA-160.
Herstellung von Stickstoff-dotierten 2D-Kohlenstoffmaterialien
Die Vorläufer von g-C3 N4 /PDA-120, g-C3 N4 /PDA-140 und g-C3 N4 /PDA-160 wurden 2 h in Stickstoffatmosphäre auf 900 °C erhitzt. Nach dem Abkühlen auf Raumtemperatur wurden mit Stickstoff dotierte poröse Kohlenstoffproben mit den Namen NC-120, NC-140 und NC-160 (NC-T) synthetisiert. Der Versuch, die Heiztemperatur weiter auf 100 °C zu senken, führte jedoch zu einer sehr schlechten Beschichtung von DA auf g-C3 N4 , was nach dem Sintern bei 900 °C zu einer geringen Ausbeute führte. Daher wurden drei Temperaturen von 120 °C, 140 °C und 160 °C für weitere Untersuchungen ausgewählt. Der Syntheseprozess von Stickstoff-dotierten porösen Kohlenstoffproben ist in Schema 1 dargestellt.
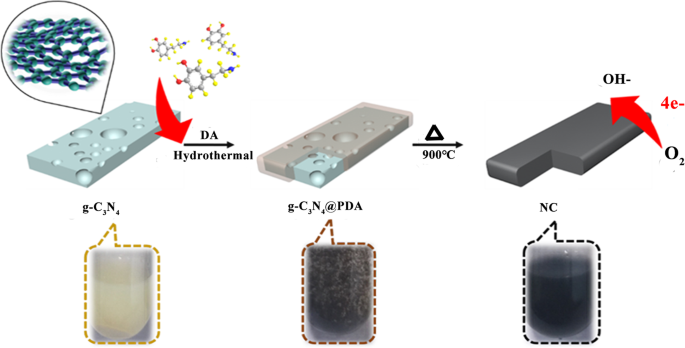
Der Syntheseprozess von NC-T-Elektrokatalysatoren
Elektrochemische Messung
Die elektrochemische Analyse wurde von der elektrochemischen Workstation DyneChem durchgeführt, wobei Ag/AgCl und Platin als Referenzelektrode bzw. Gegenelektrode verwendet werden. Das zyklische Voltampis wurde in 0,1 µM Kaliumhydroxidlösung getestet. Die Glaskohlenstoffelektrode (GCE) wurde vor der Verwendung poliert und gewaschen. Um die Arbeitselektroden vorzubereiten, wurden Aliquots von 5 μl und 2,5 mg/ml NC-120, NC-140, NC-160, Pt/C-Lösungen für weitere Tests auf GCE getaucht.
Charakterisierung
Die Struktur und chemische Zusammensetzung des NC-T wurde durch Röntgenbeugung (XRD) (D-MAX II A Röntgendiffraktometer), Transmissionselektronenmikroskopie (TEM) (Tecnai F20), Rasterelektronenmikroskop (REM) ( JEOL7610), Fourier-Transformations-Infrarot (FT-IR) (Nicolet iS50)-Spektren, Röntgen-Photoelektronen-Spektroskopie (XPS) (Kratos Axis UltraDLD) und Raman (Horiba, Japan); N2-Adsorptions-Desorptions-(77 K)-Isothermen wurden auf einem Micromeritics ASAP 2020-Instrument (MICROSENSOR, USA) durchgeführt.
Ergebnisse und Diskussion
SEM- und TEM-Charakterisierung
Um die Morphologie der synthetisierten Proben zu bestimmen, werden SEM und TEM zur Strukturbeobachtung verwendet, wie in Abb. 1 gezeigt. Abb. 1a zeigt die Blattstruktur von g-C3 . wie synthetisiert N4 . Die 2D-Struktur von g-C3 N4 wird weiter durch Abb. 1b bestätigt, die dem vorherigen Bericht ähnlich ist [48]. Für g-C3 N4 /PDA-120 wie in Abb. 1c, d gezeigt, ist das REM-Bild ähnlich dem von g-C3 N4 . Das TEM-Bild von g-C3 N4 /PDA-120 zeigt eine gut dispergierte blattartige Morphologie im Vergleich zu g-C3 . wie synthetisiert N4 . Bei steigender Heiztemperatur von 120 auf 160 °C konnte die dünne Lamellenstruktur der karbonisierten Schicht beobachtet werden (Zusatzdatei 1:Abbildung S1). Nach dem Sintern bei 900 °C erscheinen die REM-Bilder aufgrund der Pyrolyse von g-C3 . wie in Abb. 1e gezeigt wabenartige Strukturen N4 Vorlage, die poröse Kohlenstoffstrukturen induziert, wie in Abb. 1f und Zusatzdatei 1:Abbildung S2 gezeigt. Der Thermogravitationstest von g-C3 N4 wurde durchgeführt, um den Rückstand von g-C3 . zu bestimmen N4 , und g-C3 N4 beginnt sich bei 520 °C zu zersetzen. Unter Stickstoffschutz wird die vollständige Zersetzung bei 760 °C bestätigt, wie in Zusatzdatei 1:Abbildung S3 gezeigt. Zwischen 80 und 100 °C, g-C3 N4 wird durch die Verdunstung von Feuchtigkeit leicht an Qualität verlieren und das Forschungsergebnis stimmt mit früheren Berichten überein [47]. Dies weist darauf hin, dass g-C3 N4 als effiziente Vorlage für die Herstellung poröser Kohlenstoffstrukturen verwendet werden könnte.

Strukturelle Charakterisierung von Proben wie Kohlenstoff-Nanoblättern. a SEM und b TEM-Bilder von g-C3 N4 , c SEM und d TEM-Bilder von g-C3 N4 /PDA-120, e SEM und f TEM-Bilder von NC-120
XRD-, FT-IR- und Raman-Charakterisierung
Die hydrothermale Temperatur beeinflusst nicht nur die Struktur der Proben, sondern verändert auch den XRD-Peak. Die drei DA-beschichteten g-C3 N4 Proben zeigen alle zwei Beugungspeaks bei 13,0° und 27,4°, die auf (100) und (002) Kristallebenen von g-C3 . zurückzuführen sind N4 Schablone wie in Abb. 2a gezeigt. Nach der Kalzinierung bei 900 °C konnte die offensichtliche Abweichung für alle drei Proben festgestellt werden. Der Peak bei 13,0° verschwand, und zwei neue Peaks treten bei 26,3° und 44,1° auf, die für die (002)- und (100)-Ebenen von Graphen relevant sind, was auf die Bildung einer neuen graphitischen Kohlenstoffstruktur hindeutet, wie in Zusatzdatei 1 gezeigt:Abbildung S4 [4]. Mit steigender Hydrothermaltemperatur nimmt der Grad der Graphitisierung und der Kristallinität allmählich zu. Dies wird durch Raman- und FT-IR-Test weiter bestätigt.
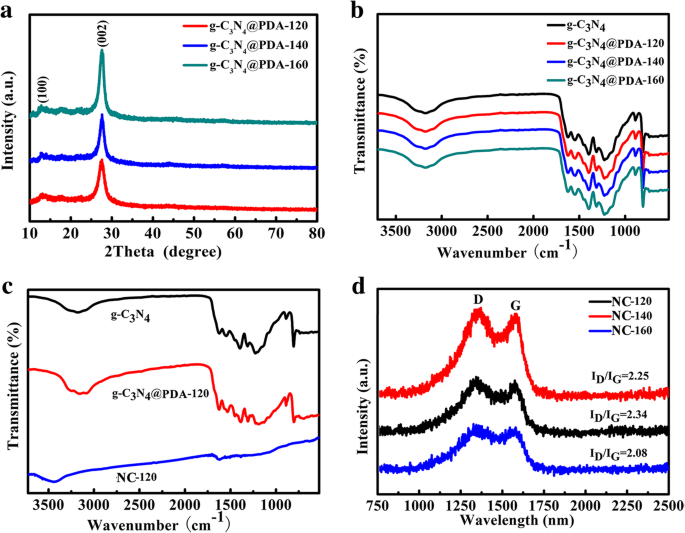
a XRD-Muster von g-C3 N4 @PDA-120, g-C3 N4 @PDA-140 und g-C3 N4 @PDA-160; b FT-IR-Spektren von g-C3 N4 , g-C3 N4 @PDA-120, g-C3 N4 @PDA-140 und g-C3 N4 @PDA-160; c FT-IR-Spektren von g-C3 N4 , g-C3 N4 /PDA-120 und NC-120; d Raman-Spektren von NC-120, NC-140 und NC-160
FT-IR-Spektrometrie wurde durchgeführt, um die auf den Oberflächen von NC-T-Hybriden vorhandenen funktionellen Gruppen zu analysieren. FT-IR-Spektren von g-C3 N4, g-C3 N4 /PDA-120, g-C3 N4 /PDA-140 und g-C3 N4 /PDA-160 zeigen an, dass diese Proben ähnliche kohlenstoff- und sauerstoffhaltige funktionelle Gruppen enthalten, wie in 2b gezeigt. Die Spitzen zwischen 1200 und 1650 cm −1 gehören zu den Streckmethoden von CN-Heterocyclen, und die breiten Peaks liegen im Bereich von 3000~3500 cm −1 werden der Streckschwingung der N-H-Gruppe zugeschrieben [49]. Mit steigender hydrothermaler Temperatur werden die beiden Peaks bei 1650 cm −1 (C=C) und 3350 cm −1 (O-H) sind aufgrund von DA auf g-C3 . deutlicher zu erkennen N4 . Nach der Hochtemperaturkarbonisierung verbleiben nur drei schwache Peaks für NC-120 bei 1600 cm −1 , 1260 cm −1 , und 3450 cm −1 (Abb. 2c), die der C-C- und C-N-Schwingung zugeschrieben werden. Dies weist darauf hin, dass die Hochtemperatur-Karbonisierung O-H-, N-H- und andere chemische Bindungen zerstört, während C-N-Bindungen stabil sind, wodurch die effektive Dotierung von Stickstoffelementen gewährleistet wird.
Raman-Spektroskopie wird verwendet, um die strukturelle Entwicklung von NC-T zu bewerten. Abbildung 2d zeigt die Raman-Spektren von NC-120, NC-140 und NC-160 und die Peaks bei 1350 und 1580 cm −1 entsprechen der D- bzw. G-Bande [50, 51]. Mit steigender hydrothermaler Temperatur wird das Intensitätsverhältnis von I D /Ich G sinkt von 2,34 auf 2,08, was den erhöhten Graphitisierungsgrad mit steigender Temperatur anzeigt.
XPS-Charakterisierung
XPS wird verwendet, um die elementare Zusammensetzung der Proben zu untersuchen, wie in Abb. 3 gezeigt. Im Vergleich zu g-C3 N4 , drei g-C3 N4 /PDA-T-Proben weisen aufgrund der karbonisierten DA-Beschichtung auf g-C3 . einen erhöhten Sauerstoffgehalt auf N4 (Zusatzdatei 1:Tabelle S1). Mit steigender Hydrothermaltemperatur von 120 auf 160 °C sinkt der N-Gehalt (Abb. 3a). Für C-bezogene Peaks nehmen die Intensitäten der C-C/C=C- und C-O-Peaks zu, während der Peak von N-C=C mit steigender Hydrothermaltemperatur allmählich abnimmt, wie in 3b gezeigt. Nach einem früheren Bericht [24] könnte die wünschenswerte elektrochemische Leistung durch Proben mit einem hohen effektiven N-Dotierungsgehalt erreicht werden. Basierend auf den XPS-Spektren von NC-T steigt der C-Gehalt nach einer 900 °C-Wärmebehandlung mit dem Anstieg der hydrothermalen Temperatur (Zusatzdatei 1:Abbildung S6). Tabelle 1 gibt den effektiven N-Gehalt der drei Proben an. Das NC-T zeigt die Anwesenheit von Pyridin N (398,5 eV) und Graphit N (401,1 eV) [25]. Wenn die hydrothermale Temperatur auf 160 °C erhöht wird, nimmt der N-Gehalt deutlich ab. Abbildung 4 zeigt hochauflösende N 1 s XPS-Spektren von NC-T-Proben. Der Prozentsatz von Pyridin-N und Graphit-N als Funktion der Hydrothermaltemperatur ist in Fig. 4d gezeigt. Der N-Gehalt nimmt mit steigender hydrothermaler Temperatur allmählich ab.
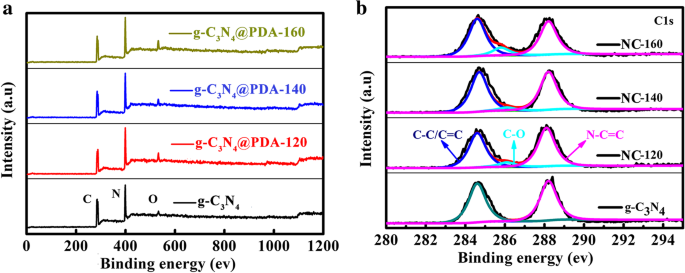
a XPS-Umfrage und b C1s XPS-Spektren von g-C3 N4 @PDA-T, hergestellt bei einer anderen HT als g-C3 N4 bzw. 120 °C, 140 °C bis 160 °C
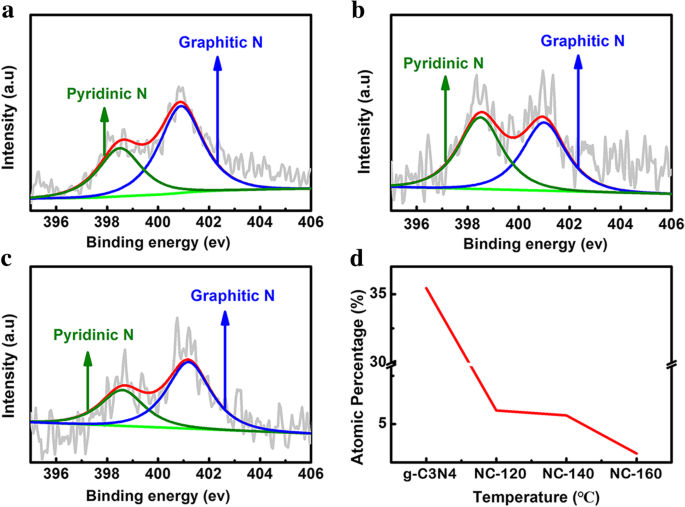
Hochauflösende XPS-Spektren von NC-T a 120 °C, b 140 °C und c 160 °C; d Die Änderung des absoluten Atomgehalts von dotiertem N bei unterschiedlicher Temperatur
Brunauer-Emmett-Teller (BET) Charakterisierung
Die katalytische Aktivität hängt von der spezifischen Oberfläche und der Porenstruktur ab.
Die BET-spezifischen Oberflächen der Proben werden durch N2 . bestimmt Adsorptionsisothermentest bei 77 K, und alle Proben zeigen Typ-IV-Kurven [19]. Dies impliziert, dass die Proben Mikroporen und mesoporöse Strukturen aufweisen, wie in Zusatzdatei 1:Abbildung S5 gezeigt. Die spezifischen Oberflächen von NC-120, NC-140 und NC-160 betragen 954, 824 und 517 m 2 g −1 , die deutlich höher sind als die des ursprünglichen g-C3 N4 (85 m 2 g −1 ). Die Ergebnisse zeigen, dass eine niedrigere Temperatur zur Bildung einer großen spezifischen Oberfläche und Porengröße beiträgt. Für den ORR-Katalysator sind die Vorteile der Schichtstruktur, der hohen spezifischen Oberflächen und des hohen Stickstoffgehalts von großer Bedeutung. Die REM- und TEM-Bilder von g-C3 N4 /PDA-T zeigte, dass die drei Proben eine ähnlich geschichtete Struktur mit makellosem g-C3 . haben N4 (Zusatzdatei 1:Abbildung S1). NC-120 weist die größte große spezifische Oberfläche auf (954 m 2 g −1 ) und hat eine geeignete mesoporöse Struktur (≈ 5 nm). Die große spezifische Oberfläche trägt dazu bei, die Kontaktfläche mit den Reaktanten zu erhöhen und die Reaktion zu beschleunigen [52].
Elektrokatalytische Leistung und Diskussion
Aus den obigen Ergebnissen konnte geschlossen werden, dass NC-120 die größte spezifische Oberfläche und den höchsten Stickstoffgehalt hat, was für die ORR sehr vorteilhaft ist [46]. Die elektrochemischen Eigenschaften der Proben werden mittels Cyclovoltammetrie (CV) untersucht und mit kommerziellen Pt/C-Katalysatoren verglichen. Die Ergebnisse sind in Abb. 5 und Tabelle 2 gezeigt. Bei allen Proben wurde unter Stickstoffsättigung kein Peak der Sauerstoffreduktion beobachtet (Abb. 5a und Zusatzdatei 1:Abbildung S8). Für sauerstoffgesättigte Bedingungen gibt es einen offensichtlichen Sauerstoffreduktionspeak, der mit abnehmender hydrothermaler Temperatur deutlicher wird. Die Ergebnisse legen nahe, dass das CV-Verhalten mit der Struktur von Katalysatoren zusammenhängt. In O2 -gesättigten 0,1 M KOH-Lösungen zeigt die NC-120-Probe die beste Leistung, die nahe an Pt-basiertem Katalysator liegt und ihr Halbpeak-Potential beträgt 0,224 V und ihre endgültige Stromdichte beträgt 5,04 mA cm -1 (Zusätzliche Datei 1:Abbildung S7). Abbildung 5b ist die lineare Scan-Voltammogramm (LSV)-Kurve, die die Grenzstromdichte und die Onset-Potentiale der NC-T-Proben zeigt. Mit abnehmender Hydrothermaltemperatur werden die Spannungs- und Stromdichte erhöht und die Leistung des Katalysators wird allmählich verbessert. Aus Fig. 5c ist ersichtlich, dass nach der Zugabe von Methanol eine kleine Bewegung dieser Kurve festgestellt wird, was darauf hindeutet, dass NC-120 eine ausgezeichnete Toleranz gegenüber Methanol aufweist. In Abb. 5(e) zeigte der NC-120 gute Sauerstoffreduktionseigenschaften, was auf die große spezifische Oberfläche und den Stickstoffgehalt zurückzuführen sein könnte (Zusatzdatei 1:Abbildung S7). Für NC-120 (Abb. 5d, f) wird die Zahl der Elektronenübertragungen im Prozess der Sauerstoffreduktion mit 3,9–4,1 berechnet, was darauf hinweist, dass die Sauerstoffreduktionsreaktion des katalytischen NC-120 aus vier elektronischen Prozessen besteht. NC-120 hat die beste elektrochemische Leistung, was der effektiven N-Dotierung nach der gegenwärtigen Strategie zugeschrieben wird.
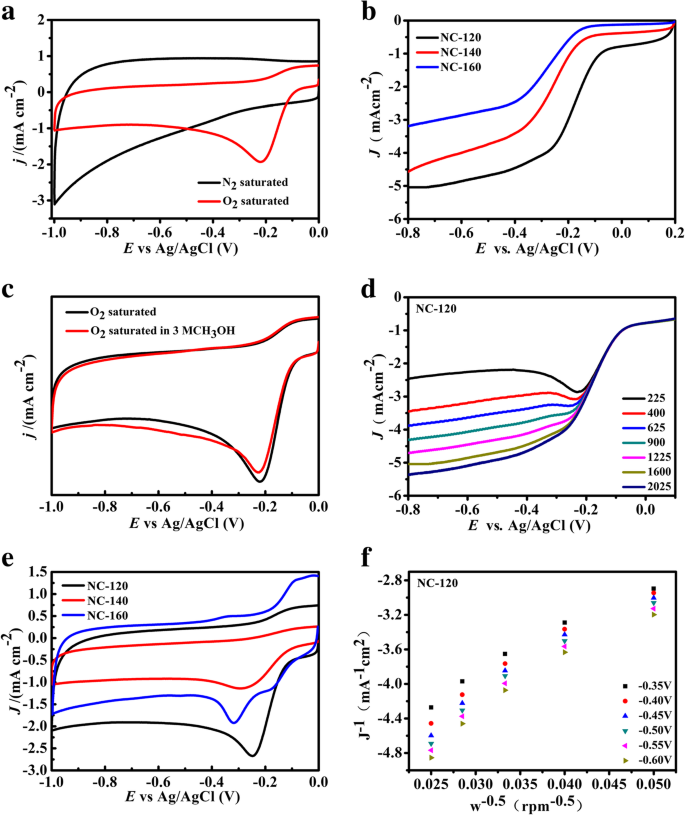
a CV-Kurven von NC-120 in N2 und O2 gesättigte wässrige 0,1 M KOH-Lösung mit einer Scanrate von 100 mV s −1 . b LSV-Kurven von NC-T bei 1600 U/min Rotationsgeschwindigkeiten. c Lineare Polarisationskurven von NC-120 mit unterschiedlichen Rotationsraten bei einer Sweep-Rate von 5 mV s −1 in O2 -gesättigte 0,1 µM KOH. d K-L-Plots bei verschiedenen Potentialen basierend auf den Ergebnissen von c . e Lebensläufe von NC-120 in O2 -gesättigte 0,1 M KOH-Lösung mit 3 M CH3 OH. f CV-Kurven von NC-T in O2-gesättigter wässriger 0,1 M KOH-Lösung mit einer Abtastrate von 100 mV s −1
Wie in Schema 1 gezeigt, wird DA als Kohlenstoffquelle und g-C3 . verwendet N4 Nanosheet wird als Templat und Stickstoffquelle verwendet. Es gibt drei Gründe für diese Strategie:Erstens g-C3 N4 kann eine mehrschichtige Struktur bereitstellen und kann bei 900 ° C vollständig verschwinden. Zweitens kann DA ein Kohlenstoffatom bereitstellen und karbonisiertes DA könnte beide Seiten von g-C3 . bedecken N4 . PDA wurde auf der Vorlage von g-C3 . gebildet N4 in einem hydrothermalen Verfahren unter Verwendung von DA als Kohlenstoffquelle. Bei hydrothermalen Verfahren kann PDA stark an der Substratoberfläche organischer oder anorganischer Materialien haften, indem starke kovalente und nicht-kovalente Bindungen auf der Oberfläche des Substrats gebildet werden. Nach der Bildung des Beschichtungsmaterials führt die Pyrolyse unter Stickstoffbedingungen zur Bildung von porösen Kohlenstoffmaterialien mit großer spezifischer Oberfläche. Schließlich das zerlegte g-C3 N4 würde N-Atome zum Dotieren der Kohlenstoffstruktur bereitstellen, wodurch die aktiven Zentren für ORR effektiv erhöht würden. In früheren Berichten haben Liu et al. vorbereitet g-C3 N4 @PDA-Verbundstoffe durch direktes Eintropfen der DA-Lösung in g-C3 N4 Lösung unter Rühren zur Verbesserung des photokatalytischen H2 . mit sichtbarem Licht Produktionsaktivität, die vielversprechende Ergebnisse zeigt [37]. In der vorliegenden Arbeit haben wir, wie oben diskutiert, eine neue Strategie entwickelt, um N-dotierte poröse Kohlenstoffstrukturen mit hoher spezifischer Oberfläche (954 m 2 g −1 ) und hoher N-Gehalt (5,71%) mit g-C3 N4 als Templat und N-Quelle gleichzeitig. Die erworbenen Verbundwerkstoffe weisen eine vergleichbare ORR-Aktivität, überlegene Haltbarkeit und Methanoltoleranz gegenüber dem Pt/C-Referenzelektrokatalysator auf.
Schlussfolgerung
Zusammenfassend haben wir eine Strategie zur Synthese von N-dotierten Kohlenstoffstrukturen entwickelt. Der erste Schritt ist hauptsächlich der hydrothermale Prozess und der zweite Schritt ist der Wärmebehandlungsprozess. Mit g-C3 N4 als Templat und DA als Kohlenstoffquelle konnten poröse Kohlenstoffnetzwerke mit hohem N-Dotierungsgehalt erreicht werden. Die resultierenden Netzwerkstrukturen können die spezifische Oberfläche des Katalysators erhöhen und bieten somit ausgezeichnete elektrochemische Eigenschaften, einschließlich einer guten Methanoltoleranz und Stabilität im Vergleich zu Pt/C-Katalysatoren. Die Leistung dieser ausgezeichneten Elektrokatalyse kann den folgenden Gründen zugeschrieben werden:(1) Eine N-dotierte C-Schichtstruktur mit einem hohen Gehalt an Graphit-N- und Pyridin-N-Spezies liefert ein hochaktives Zentrum für die Sauerstoffreduktionsreaktion. (2) Die hohe spezifische Oberfläche (954 m 2 g −1 ) koexistiert mit hohem graphitischem Kohlenstoff und amorphem Kohlenstoff und trägt zur Elektronenleitung der ORR bei. (3) Die porösen Strukturen beschleunigen den Elektronentransfer und fördern die volle Ausnutzung der aktiven Zentren. All diese Vorteile bestimmen die gute katalytische Wirkung dieses Materials. Darüber hinaus ist die derzeitige Methode zur Herstellung von N-dotierten kohlenstoffbasierten Nanomaterialien wirtschaftlich, umweltfreundlich und effizient, sodass sie in Zukunft in Brennstoffzellen weit verbreitet verfügbar sind.
Verfügbarkeit von Daten und Materialien
Die in der aktuellen Studie verwendeten bzw. analysierten Datensätze sind auf begründete Anfrage beim entsprechenden Autor erhältlich.
Abkürzungen
- WET:
-
Bunauer–Emmett–Teller
- Lebenslauf:
-
Zyklische Voltammetrie
- DA:
-
Dopamin
- g-C3 N4 :
-
Graphit-Kohlenstoff-Nitrid
- GCE:
-
Glaskohleelektrode
- LSV:
-
Linearscan-Voltammogramm
- ORR:
-
Sauerstoffreduktionsreaktion
- SEM:
-
Rasterelektronenmikroskop
- TEM:
-
Transmissionselektronenmikroskop
- XPS:
-
Röntgenphotoelektronenspektroskopie
Nanomaterialien
- Aktivkohlefasern mit hierarchischer Nanostruktur aus Baumwollhandschuhabfällen als Hochleistungselektroden für Superkondensatoren
- Monodisperse Kohlenstoff-Nanosphären mit hierarchischer poröser Struktur als Elektrodenmaterial für Superkondensatoren
- Magnetische Kohlenstoff-Mikrosphären als wiederverwendbares Adsorptionsmittel zur Entfernung von Sulfonamid aus Wasser
- Ein einfacher Ansatz zur Synthese von fluoreszierenden Kohlenstoffquantenpunkten aus Tofu-Abwasser
- Funktionelles poröses Polymer auf Triphenylphosphin-Basis als effizienter heterogener Katalysator für die Synthese cyclischer Carbonate aus CO2
- Selbstdotierter hochporöser Kohlenstoff mit hohem Graphitgehalt für die Elektrokatalyse von Sauerstoffreduktionsreaktionen
- Sauerstoffreduktionsreaktion auf PtCo-Nanokatalysator:(Bi)Sulfat-Anionenvergiftung
- Hochaktive und stabile Fe-N-C-Sauerstoffreduktions-Elektrokatalysatoren aus Elektrospinnen und In-situ-Pyrolyse
- Carbon Dots @ Platin-Porphyrin-Composite als theranostischer Nanowirkstoff für eine effiziente photodynamische Krebstherapie
- Eine hochgradig nanoporöse Stickstoff-dotierte Kohlenstoff-Mikrofaser aus Bioressourcen als neue Art von ORR-Elektrokatalysator



