Maßgeschneiderte Festpolymerelektrolyte von Montmorillonit mit hoher Ionenleitfähigkeit für Lithium-Ionen-Batterien
Zusammenfassung
Feste Polymerelektrolyte (SPEs) auf Basis von Polyethylenoxid (PEO) haben eine wichtige Bedeutung für die Entwicklung wiederaufladbarer Lithium-Ionen-Batterien der nächsten Generation. Eine starke Koordination zwischen Lithiumionen und PEO-Ketten führt jedoch dazu, dass die Ionenleitfähigkeit normalerweise niedriger ist als erwartet. In dieser Studie wird Submikron-Montmorillonit als Lewis-Base-Zentrum in die PEO-Rahmen eingebaut, wodurch die Lithiumionen der Zurückhaltung der PEO-Ketten entkommen können. Nach Einbeziehung von Montmorillonit (MMT) in die SPEs beträgt die Ionenleitfähigkeit der SPEs 4,7 mS cm − 1 bei 70 °C, was einen vergleichbaren Wert mit dem von Flüssigelektrolyt aufweist. Als Kopplung mit LiFePO4 Material liefert der Akku eine hohe Entladekapazität von 150,3 mAh g − 1 und eine hervorragende Ratenleistung mit einer Kapazität von 111,8 mAh g − 1 bei 0,16 C und behält 58,2 mAh g − 1 . bei bei 0,8 C. Diese Studie legt nahe, dass der maßgeschneiderte Einbau von Lewis-Basismaterialien eine vielversprechende Lösung für die Erzielung eines Hochleistungs-Festkörperelektrolyten auf PEO-Basis sein könnte.
Einführung
Die Anforderungen an Energiespeichergeräte für tragbare elektronische [1], Kommunikationsgeräte [2] und hybride Elektrofahrzeuge werden immer stärker [2,3,4]. Typischerweise werden die Speichergeräte mit Lithium-Ionen-Batterien (LIBs) vorgeschlagen, die eine hohe spezifische Energie aufweisen, ein geringes Gewicht haben und einfach zu transportieren und schnell einzurichten sind, als Energiequellen, um diese Felder zu erfüllen [5,6,7,8 ,9,10,11]. Bei den kommerziellen Lithium-Ionen-Batterien sind die Flüssigelektrolytsysteme jedoch aufgrund der Entflammbarkeit und der Wirkung eines Giftes enorm gefährdet [5, 12, 13]. Beispielsweise beträgt der Siedepunkt von Ethylacetat, Dimethylcarbonat, Diethylcarbonat und Ethylencarbonat nur 77 °C, 90 °C, 127 °C bzw. 243 °C [5]. Noch wichtiger ist, dass das Material der kommerziellen Separatoren Polyethylen (PE) oder Polypropylen (PP) ist, das sich bei Temperaturen von bis zu 60 ° C verformt [14]. Sobald die Betriebstemperatur (> 60 °C) die kritische Temperatur überschreitet, schrumpft die Struktur der Separatoren, was zu einem inneren Kurzschluss aufgrund der verlorenen Funktion zur physikalischen Trennung von Kathode und Anode führt [14, 15]. Im Vergleich dazu sind Festelektrolyte zu erwarten, da sie aufgrund ihrer thermischen Stabilität, chemischen Beständigkeit und elektrochemischen Kompatibilität die wettbewerbsfähigsten Strategien zur Bekämpfung der oben genannten Probleme aufweisen [16,17,18,19].
Die anorganischen Festelektrolyte wie Sulfide (z. B. Li10 GeP2 S12 [20], Li9,54 Si1.74 P1.44 S11.7 Kl0,3 (25 mS cm − 1 ) [21], Li11 Si2 PS12 [22]), Oxide (z. B. Li7+2x−y (La3−x Rbx )(Zr2−y Tay )O12 (0 ≤ x ≤ 0.375, 0 ≤ y ≤ 1) [23] und Li7 La3 Zr2 O12 [18]), zeigen eine außergewöhnlich hohe Leitfähigkeit. Einige Forscher berichteten, dass die Lithiumionenleitfähigkeit bis zu 25 mS cm − 1 . erreichen kann , die weit höher ist als die Leitfähigkeit von flüssigem Elektrolyt (~ 10 − 3 S cm − 1 ) [21]. Bei anorganischen Festelektrolyten zeigen sie jedoch die schlechten mechanischen Eigenschaften mit niedrigem Young-Modul und einer großen Anzahl von Korngrenzen im Inneren des Festelektrolyten [24], was dazu führt, dass die Produktion im Maßstab nicht möglich ist [1].
Anorganischer Festelektrolyt in Kombination mit ionenleitfähigem Polymer-Polyethylenoxid (PEO) hat aufgrund der einzigartigen Eigenschaften, dass PEO eine ausgezeichnete mechanische Stabilität, zuverlässige Filmbildungsfähigkeit und insbesondere die gute Verträglichkeit aufweist, weit verbreitete Bedenken hinsichtlich Festpolymerelektrolyten (SPEs) auf sich gezogen, um die oben genannten Probleme zu überwinden mit der Lithium-Metall-Anode [17, 25, 26]. Aufgrund der Lewis-Base-Leistung von PEO neigen Lithiumionen jedoch dazu, sich an den PEO-Ketten festzusetzen, was zu einer geringen Lithiumionenleitfähigkeit führt [17, 27, 28, 29].
In dieser Arbeit führen wir eine kleine Menge Submikro-Montmorillonit als Lewis-Base-Zentrum in die SPEs ein, wo der Montmorillonit die Koordination mit Lithiumionen bilden kann, da der Montmorillonit als Konkurrent zu den Lithiumionen dient [30]. Als Ergebnis liefern die vorgeschlagenen SPEs eine hohe Ionenleitfähigkeit (4,7 mS cm − 1 ) bei 70 °C und der vorbereiteten vollfesten Lithium-Ionen-Akku-Kupplung LiFePO4 als Kathode trägt eine Entladekapazität von 150,3 mAh g − 1 . bei mit dem LiFePO4 Belastung von 2 mg cm − 2 , weit über dem Festelektrolyt auf PEO-Basis (119,1 mAh g − 1 .) ) bei einer Stromdichte von 0,08 C (1 C = 0,170 mAh g − 1 ).
Experimentelle Methoden
Materialien und Chemikalien
Für die Herstellung von Festpolymerelektrolyten werden 500 mg PEO (Aladdin) und 250 mg Lithiumbis(trifluormethansulfonyl)imid (LITSFI, Aladdin) in 10 ml Acetonitril (Aladdin) gelöst und dann 150 mg Li6.4 La3 Zr1.4 Ta0,6 O12 (LLZTO, Tai’an Faraday Energy Technology Co., Ltd) wird unter schnellem Rühren bei 70 °C in die PEO-Lösung gegeben, um eine gleichmäßige Verteilung zu gewährleisten. Schließlich wird die Aufschlämmung auf die Oberfläche des Teflonfilms gegossen und bei 80ºC unter einer Ar-Atmosphäre getrocknet. Zum Vergleich:Der Festelektrolyt auf MMT-Basis wird nach dem gleichen Verfahren hergestellt, außer dass zusätzlich Montmorillonit (Aladdin) mit einer Massenbeladung von 100 mg hinzugefügt wird.
Charakterisierung
Thermogravimetrische (TG, Netzsch STA 449F3) Analyse wird auf thermische Stabilität mit einer Heizrate von 10 °C min − 1 . durchgeführt bei Ar-Atmosphäre. Die Kristallstruktur wird durch Röntgenbeugungsmuster (XRD) bei Raumtemperatur unter Verwendung eines UltimaIV-Diffraktometers mit CuKα1-Strahlung (λ = 1,4506 Å) und einen positionsempfindlichen Detektor. Die Oberflächenmorphologien und die entsprechende energiedispersive Röntgenstrahlung (EDX) der SPEs werden mit einem Rasterelektronenmikroskop (REM, FEI NANOSEI 450) beobachtet.
Elektrochemische Messungen
Alle elektrochemischen Tests werden mit einer Standard-Knopfzelle (CR 2025) durchgeführt. Die AC-Impedanzspektroskopie wird durch eine elektrochemische Workstation (CHI660E, Chenhua Instruments Co., China) in einem Frequenzbereich von 0,1 Hz–100 MHz durchgeführt. Lineare Sweep-Voltammetrie (LSV, 2,5 bis 6,0 V mit einer Abtastrate von 10 mV − 1 ) und zyklische Voltammetrie (CV, − 0.5 bis 6.0 V mit einer Abtastrate von 10 mV − 1 ) werden auf der elektrochemischen Workstation (CHI660E, Chenhua Instruments Co., China) mit einem Edelstahl als Arbeitselektrode und Li-Metall als Referenz- und Gegenelektrode durchgeführt. Die Zyklen werden mit einem CT2001A-Zelltestgerät (Wuhan LAND Electronic Co, Ltd) durchgeführt. Für die Lithium-Ionen-Leitfähigkeit, die nach Gl. (1).
$$ \upsigma =\frac{d}{\mathrm{RA}} $$ (1)wobei σ die Leitfähigkeit ist, d ist die Dicke von SPEs, R ist der Widerstand gemäß Nyquist-Plots und A ist die Querschnittsfläche. Alle Festkörper-Lithium-Ionen-Batterien sind mit LiFePO4 . bestückt Kathodenkopplung mit Lithium-Metall-Anode. Normalerweise LiFePO4 , Acetylenruß und Polyvinylidenfluorid (7:2:1) werden mit N-Methyl-2-pyrrolidon (NMP) vermischt. Die Mischung wird auf die Aluminiumfolie aufgetragen und über Nacht bei 60 °C im Vakuum getrocknet. Das LiFePO4 Ladung in der Kathode beträgt 2 mg cm − 2 .
Ergebnisse und Diskussion
Um die Beziehung der Lithiumionen-Diffusionsgrade in einer Lewis-Base-Umgebung zu veranschaulichen, ist das Designkonzept in Abb. 1a gezeigt, bei dem eine kleine Menge Montmorillonit als Lewis-Base-Zentrum in die PEO-Rahmen hinzugefügt wird. Basierend auf der Lewis-Säure-Base-Theorie kann der Montmorillonit als Konkurrent mit der PEO-Kette fungieren, um die Selbstkonzentration des Lithiumions (Lewis-Säure) auf der Oberfläche des Montmorillonits aufgrund der hohen Absorptionsenergie zu ermöglichen [14]; somit können die Lithiumionen der Zurückhaltung der PEO-Ketten entkommen. Darüber hinaus kann die niedrige Lithium-Ionen-Diffusions-Energiebarriere (0,15 eV) auf der Oberfläche von Montmorillonit die Lithium-Ionen-Migration ungehindert ermöglichen, da die Strategien zur Erleichterung des Ionentransports, wie z hoch notwendig [30]. Wie in Abb. 1b dargestellt, kann gemäß den aus seiner XRD-Kurve abgeleiteten Ergebnissen ein hügelartiger Peak beobachtet werden, was darauf hindeutet, dass die Kristallinität von PEO bis zu einem gewissen Grad verringert wurde, was die Fähigkeit von Montmorillonit bestätigt, die Lithiumionenkoordination mit . zu schwächen PEO-Ketten. Weiter getragen wird die Ionenleitfähigkeit mittels AC-Impedanzspektroskopie getestet, bei der Knopfzellen die SPEs zwischen zwei Edelstahlelektroden eingelegt werden. Wie in Abb. 1c gezeigt, zeigen die Ergebnisse deutlich den Vorteil nach dem Einbau von Montmorillonit, dass die Ionenleitfähigkeit von SPEs stark verbessert werden konnte. Insbesondere die Ionenleitfähigkeit (4,7 mS cm − 1 ) von SPEs mit Montmorillonit-Einbau bei 70 °C ist vergleichbar mit der von Flüssigelektrolyt und würde zu einem schnellen Transport von Lithiumionen führen.
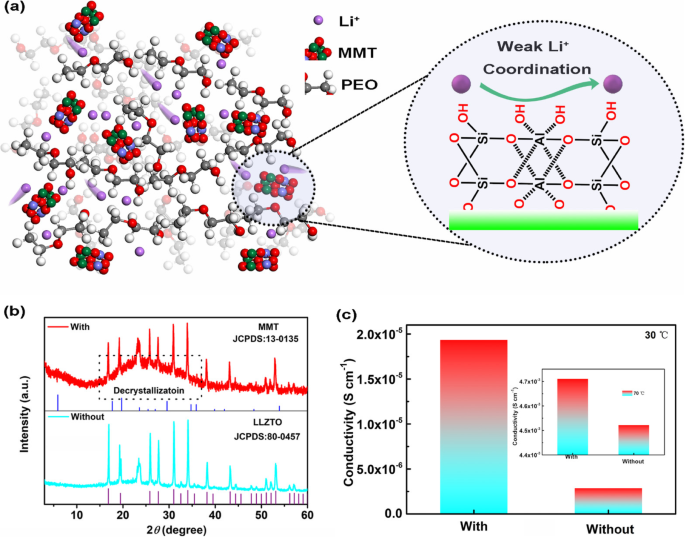
Charakterisierung von SPEs mit Montmorillonit-Dotierung:a Das Designkonzept, dass Lithiumionen entlang der Oberfläche von Montmorillonit schnell diffundieren können. b , c Die XRD- und FTIR-Ergebnisse von SPEs mit bzw. ohne Montmorillonit-Partikel
Abbildung 2 zeigt die typischen Oberflächenmorphologien der vorbereiteten SPEs. Wie in Abb. 2a gezeigt, weisen die SPEs ohne Montmorillonit einheitliche Oberflächen auf. Die Integrität von SPEs wurde jedoch in verschiedene unregelmäßige Bereiche unterteilt, die durch die Verdunstung des Lösungsmittels verursacht werden können. Dadurch erhöht diese Struktur die interne Kristallgrenzfläche von SPEs und verlangsamt den Transport von Lithiumionen. Im Gegensatz dazu wurde diese Situation nach der Beteiligung von Montmorillonit stark optimiert. Die Ergebnisse zeigen, dass die Lücken zwischen segmentierten SPEs aufgrund der Dekristallisation gefüllt wurden, dargestellt in Abb. 1b. Darüber hinaus bestätigte die Merkmalselementkartierung von Si und Al die homogene Verteilung von Montmorillonit-Partikeln, die in die PEO-Matrix eingebettet sind (Abb. 2c). Abbildung 2d zeigt die Hochtemperaturleistung von SPEs mittels thermogravimetrischer Analyse. Bei niedrigen Temperaturen (< 150 °C) beobachteten wir einen leichten Gewichtsverlust, möglicherweise durch das Verdampfen des restlichen Lösungsmittels. Offensichtlich weisen beide SPEs mit oder ohne Montmorillonit eine ausgezeichnete thermische Stabilität bis zu 370 °C auf.
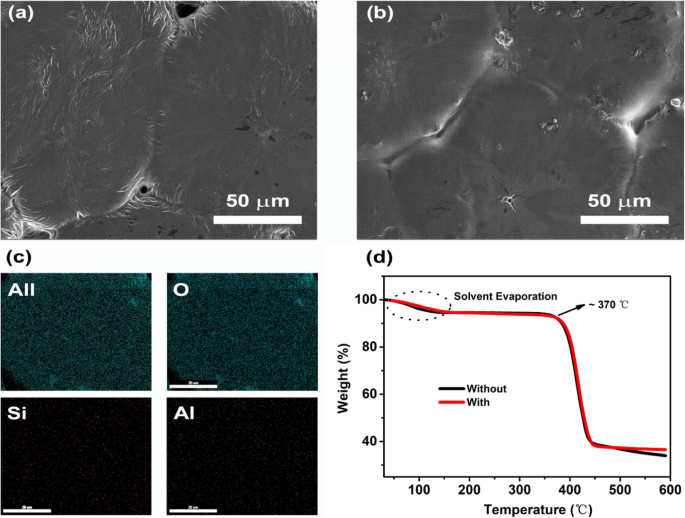
REM-Bilder von SPEs ohne (a ) und mit (b ) Montmorillonit-Dotierung. c Die Elementkartierung von SPEs mit Modifikation von Montmorillonit. d TGA-Kurve von SPEs von 30 bis 600 °C bei einer Rate von 10°C min − 1
Abbildung 3 zeigt die Untersuchung der elektrochemischen Leistung von SPEs. Wie in Abb. 3a gezeigt, wird lineare Sweep-Voltammetrie verwendet, um das elektrochemische Fenster von SPEs vor und nach dem Einbau von Montmorillonit zu untersuchen. Ohne Montmorillonit beginnt der Oxidationsprozess bei 3,9 V. Während der Sweep im Fall nach dem Einbau von Montmorillonit ohne offensichtlichen Strom auf 4,6 V ausgedehnt werden kann. Die erhöhte elektrochemische Stabilität ist auf die durch den Montmorillonit entfernten Verunreinigungen wie Wasser aus der Grenzfläche zurückzuführen [31]. Dementsprechend wird die verbesserte elektrochemische Stabilität durch Cyclovoltammetrie (CV)-Scans weiter bestätigt, die zeigen, dass die SPEs mit Montmorillonit einen vernachlässigbaren Redoxstrom von 2,5 bis 5 V liefern (Abb. 3b). Es wurde jedoch ein gegensätzliches Phänomen beobachtet, dass die SPEs ohne Montmorillonit den Oxidationsstrom erhöhen, was aus LSV-Ergebnissen besteht. Darüber hinaus sind die galvanostatischen Lade- und Entladezyklen von LiFePO4 Batterien werden bei 70 °C getestet, um die tatsächlichen Anwendungen von SPEs zu bestätigen. Wie in Abb. 3c gezeigt, beträgt die spezifische Entladekapazität 150,3 mAh g − 1 . mit einem hohen Coulomb-Wirkungsgrad von fast 100 % bei 0,08 C, was 88 % des theoretischen Werts entspricht (170 mAh g − 1 ). Dementsprechend sind die typischen Potentialplateaus von LFP bei 3,39 V und 3,44 V entsprechend Entladung und Aufladung deutlich zu erkennen. Wenn die Stromdichten auf 0,16, 0,4, 0,6 und 0,8 C erhöht werden, verringern sich die spezifischen Entladekapazitäten auf 111,8, 85,9, 75,2 und 58,2 mAh g − 1 , bzw. Ohne Montmorillonit konnte eine geringere Entladekapazität von nur 119,1 mAh g − 1 . gefunden werden bei 0,08 C, was 70 % des theoretischen Wertes entspricht. Mit zunehmender Stromdichte sinken die spezifischen Entladekapazitäten schnell auf 92,8, 75,4, 63,4 und 55,5 mAh g − 1 entsprechend 0,16, 0,4, 0,6 bzw. 0,8 C. Daher zeigen alle Ergebnisse noch einmal deutlich die Vorteile von Montmorillonit, alle Festkörperelektrolyte mit hoher Ionenleitfähigkeit für die tatsächliche Anwendung von Lithium-Ionen-Batterien anzupassen.
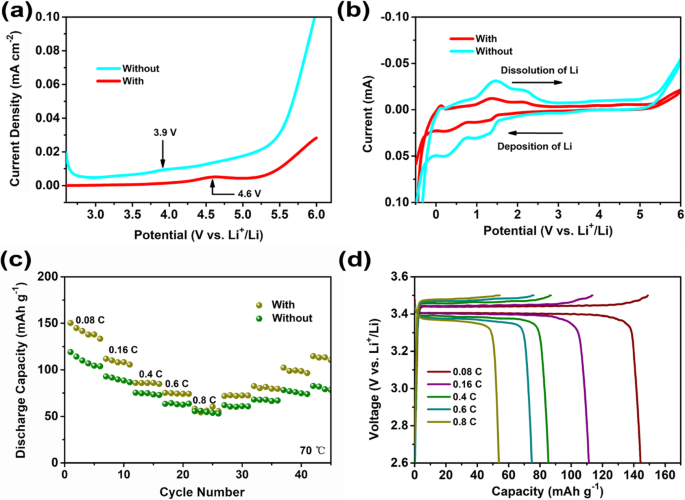
Die elektrochemische Leistung von SPEs:LSV-Profile (a ), Radfahrleistung (b ), Leistung bewerten (c ) und Spannungsprofile von SPEs nach Montmorillonit (d )
Schlussfolgerungen
Zusammenfassend lässt sich sagen, dass eine kleine Menge Montmorillonit als Lewis-Base-Zentrum in die PEO-Gerüste aufgenommen wird, um SPEs zu ermöglichen, eine hohe Ionenleitfähigkeit zu erreichen. Die gleichmäßige Verteilung von Montmorillonit ermöglicht ein verbessertes elektrochemisches Fenster von SPEs von 3,9 auf 4,6 V. Diese vorgeschlagene Strategie weist eine ausgezeichnete elektrochemische Leistung auf, die das hergestellte LiFePO4 Akku liefert eine hohe Entladekapazität von 150,3 mAh g − 1 mit einer Belastung von 2 mg cm − 2 bei 70 °C, weit über der Kontrollprobe (119,1 mAh g − 1 .) ) bei einer Stromdichte von 0,08 C. Alle Ergebnisse deuten darauf hin, dass die vorgeschlagene Strategie basierend auf der Lewis-Säure-Base-Theorie eine vielversprechende Methode sein könnte, um Lithium-Ionen-Batterien mit hoher Kapazität und hoher Rate zu erhalten.
Verfügbarkeit von Daten und Materialien
Alle Daten sind uneingeschränkt verfügbar.
Abkürzungen
- Lebenslauf:
-
Zyklische Voltammetrie
- EDX:
-
Energiedispersive Röntgenstrahlung
- LIBs:
-
Lithium-Ionen-Akkus
- LITFSI:
-
Bis(trifluormethansulfonyl)imid
- LLZTO:
-
Li6.4 La3 Zr1.4 Ta0,6 O12
- LSV:
-
Lineare Sweep-Voltammetrie
- MMT:
-
Montmorillonit
- NMP:
-
N-Methyl-2-pyrrolidon
- PE:
-
Polyethylen
- PEO:
-
Polyethylenoxid
- PP:
-
Polypropylen
- SEM:
-
Rasterelektronenmikroskop
- SPEs:
-
Festpolymerelektrolyte
- TG:
-
Thermogravimetrisch
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Erneuerbare PVDF-Qualitäten für Lithium-Ionen-Batterien
- Mechanischer Verbund aus LiNi0.8Co0.15Al0.05O2/Kohlenstoff-Nanoröhren mit verbesserter elektrochemischer Leistung für Lithium-Ionen-Batterien
- Elektrogesponnene Polymer-Nanofasern, dekoriert mit Edelmetall-Nanopartikeln für die chemische Sensorik
- Synthese und elektrochemische Eigenschaften von LiNi0.5Mn1.5O4 Kathodenmaterialien mit Cr3+ und F− Verbunddotierung für Lithium-Ionen-Batterien
- MoS2/Acetylene Black Composite mit wenigen Schichten als effizientes Anodenmaterial für Lithium-Ionen-Batterien
- Na4Mn9O18/Carbon Nanotube Composite als elektrochemisches Hochleistungsmaterial für wässrige Natrium-Ionen-Batterien
- Eingebetteter Si/Graphen-Verbundstoff, hergestellt durch thermische Magnesiumreduktion als Anodenmaterial für Lithium-Ionen-Batterien
- Umweltfreundliche und einfache Synthese von Co3O4-Nanodrähten und ihre vielversprechende Anwendung mit Graphen in Lithium-Ionen-Batterien
- Eine nanokristalline Fe2O3-Filmanode, hergestellt durch gepulste Laserabscheidung für Lithium-Ionen-Batterien
- Stabile Polymertinte mit hoher Leitfähigkeit



