Doppelte Morphologie von Co9S8 beschichtet mit N,S-codotiertem Kohlenstoff als effiziente Anodenmaterialien für Natrium-Ionen-Batterien
Zusammenfassung
Co9 S8 ist aufgrund seiner hohen Natriumspeicherleistung, leichten Zugänglichkeit und Thermostabilität ein potenzielles Anodenmaterial. Die Volumenausweitung ist jedoch ein großes Hindernis für seine Entwicklung. Hierbei handelt es sich um einen Verbundstoff, der Co9 . enthält S8 Nanofasern und hohles Co9 S8 Nanokugeln mit N, S codotierter Kohlenstoffschicht (Co9 S8 @NSC) wird erfolgreich durch einen einfachen solvothermalen Prozess und eine Hochtemperaturkarbonisierung synthetisiert. Aufgrund der Kohlenstoffbeschichtung und der großen spezifischen Oberfläche können starke Volumenspannungen effektiv gemildert werden. Insbesondere mit N- und S-Heteroatomen, die in die Kohlenstoffschicht eingeführt wurden, was der Na + . förderlich ist Adsorption und Diffusion an der Kohlenstoffoberfläche, Co9 S8 @NSC kann einen kapazitiveren Natriumspeichermechanismus ausführen. Als Ergebnis kann die Elektrode eine günstige reversible Kapazität von 226 mA h g −1 . aufweisen bei 5 A g −1 und eine günstige Kapazitätserhaltung von 83,1% bei 1 A g −1 nach 800 Zyklen. Das einzigartige Design bietet einen innovativen Gedanken zur Verbesserung der Natriumspeicherleistung.
Einführung
Mit der rasanten Entwicklung von Gangreservesystemen in Elektrofahrzeugen und tragbaren elektronischen Produkten sind Natrium-Ionen-Batterien (SIBs) aufgrund des ähnlichen Lade-Entlade-Verhaltens wie LIBs zu einem starken Konkurrenten für Lithium-Ionen-Batterien (LIBs) geworden , und riesige Naturschutzgebiete [1,2,3]. Und das elektrochemische Potenzial von Na (− 2,71 V gegenüber der Standard-Wasserstoffelektrode, SHE) ist mit 330 mV höher als das von Li (− 3,04 V), was es SIBs ermöglicht, den Energiespeicherbedarf im großen Maßstab zu decken [4,5, 6]. Die größte Herausforderung bei SIBs ist jedoch die große Volumenausdehnung während des Sodiationsprozesses, die von der großen Dehnung herrührt, die sich aus dem größeren Radius von Na + . ergibt (1,02 Å) als Li + (0,76 Å) [7, 8]. Dies führt zu einer starken Pulverisierung und Abblätterung aktiver Materialien von der Kupferfolie und führt außerdem zu einer schlechten Zyklenleistung. Daher ist ein rationales Design von Anodenmaterialien ein bevorstehendes Anliegen.
Für ihre hohe theoretische Kapazität wurden verschiedene Anodenmaterialien beschrieben, wie Übergangsmetallsulfide (TMS) [9,10,11,12,13,14], Übergangsmetalloxide (TMOs) [15,16,17,18 ], Phosphide [19,20,21,22] und Kohlenstoffverbundstoffe [23,24,25,26]. Darunter kobaltbasierte MS (wie CoS, CoS2 , Co3 S4 , und Co9 S8 ) haben wegen ihrer metallnahen Leitfähigkeit und leichten Zugänglichkeit große Aufmerksamkeit auf sich gezogen [27,28,29]. Insbesondere kubisches Co9 S8 zieht viel Aufmerksamkeit für seine große Thermostabilität auf. Leider wird es immer noch durch die starke Lautstärkeschwankung behindert, langsames Na + Diffusionsrate und schlechte Leitfähigkeit [30,31,32]. Es wurden große Anstrengungen unternommen, um die Mängel von Co9 . zu beheben S8 .
Bisher konzentrierten sich die meisten Studien auch auf die Entwicklung neuartiger Kohlenstoffmaterialien mit heteroatomdotierten (N, P, S, B), wie z. B. sandwichartige Strukturen mit N, S-dotiertem RG O[33, 34], nanoflower-like /CoS 2[35], Co9 S8 beschichtet mit N-dotierten Kohlenstoff-Nanosphären [36, 37] und N,S-dotierten Nanofasern [38, 39]. Eine Kohlenstoffbeschichtung kann nicht nur die Leitfähigkeit von TMSs erhöhen, sondern auch die durch die Volumenausdehnung entstehenden Spannungen abbauen. Insbesondere durch die Heteroatomdotierung kann die elektronische Struktur des Kohlenstoffs modifiziert werden, um die physikalischen und chemischen Eigenschaften zu verbessern, indem extrinsische Defekte erzeugt, der Zwischenschichtabstand vergrößert und ein zusätzlicher Elektronentransferweg angeboten wird, wenn Heteroatome an Kohlenstoffatome gebunden sind [40,41, 42,43,44].
Hier synthetisieren wir die doppelte Morphologie von Co9 S8 , enthaltend Nanofasern und hohle Nanokugeln, beide beschichtet mit N, S co-dotiertem Kohlenstoff (bezeichnet als Co9 S8 @NSC) für hochstabile SIBs. Die nanofaserartige Struktur bietet einen kontinuierlichen Elektronentransport über lange Reichweiten, während die hohlen Nanokügelchen die Infiltration des Elektrolyten verbessern. Die mit N, S kodotierte Kohlenstoffschicht kann mehr freie Elektronen bereitstellen, was der Adsorption von Na + . zugute kommt auf der Oberfläche und erhöhen die integrale Leitfähigkeit. Aufgrund der Härte der Kohlenstoffbeschichtung und des 3D-Netzwerks kann die Volumenvariation während der Einfügung/Extraktion von Natriumionen auf atomarer und 3D-Ebene gut gemildert werden. Und die hohe spezifische Oberfläche kann die Kapazität des Pseudo-Kapazitätsbeitrags verbessern, was zu einer hervorragenden Ratenleistung führt. Dadurch werden SIBs mit Co9 S8 @NSC kann eine stabile Kapazitätserhaltung von 318 mA h g −1 . liefern nach 800 Zyklen bei 1 A g −1 mit einer Coulomb-Effizienz von ~ 100 %, was sie zu einer vielversprechenden Anode für groß angelegte SIBs macht.
Experimentelle Methoden
Synthese von Co9 S8 @NSC
In einem typischen Verfahren wurden die Verbundstoffe durch koaxiales Elektrospinnen nach einem alkoholthermischen Verfahren und Karbonisierung hergestellt.
Vorbereitung von elektrogesponnenen Nanofasern
0,74 g PAN (Sigma-Aldrich, MW =150.000) und 9 ml DMF wurden über Nacht gerührt, um die homogene äußere Lösung zu bilden, während 1,8 g Cobalt(II)acetylacetonat (Co(acac)2 , Aladdin, Reinheit ≥ 99%) und 0,74 µg PAN (Macklin, MW =150000) wurden mit 9 µl DMF vermischt und gleichzeitig mit der dunkelroten Innenlösung gerührt. Dann wurden die beiden Arten von Lösungen durch koaxiales Elektrospinnen durchgeführt (Nadelgröße:innen 17 G, außen:22 G). Der Abstand zwischen der Nadel und dem Al-Folienkollektor betrug 15 cm, und die Temperatur wurde bei 65 °C gehalten. Dann wurde ein elektrisches Potenzial bei 15 kV mit einer Flussrate von zwei Spritzen angelegt, beide bei 1,5 ml h −1 . Die fertigen Vorläuferfasern wurden 24 Stunden lang bei 60 °C im Vakuum getrocknet
Schwefelung und Karbonisierung
Die erhaltenen Nanofasern wurden zunächst mit 50 ml Ethanol enthaltend Thioacetamid (TAA, Aladdin, Reinheit ≥ 99%) in 100 ml Teflon-ausgekleidetem Edelstahlautoklaven bei 120°C für 6 h durch Solvothermalverfahren gemischt. Das Endprodukt wurde durch Karbonisieren bei 700°C für 1 h mit einer Heizrate von 5 °C min −1 . erhalten und natürlich abkühlen. Zum Vergleich wurde auch eine Probe ohne Kobalt (N, S co-dotierter Kohlenstoff, bezeichnet als NSC) unter Verwendung des gleichen oben erwähnten Verfahrens ohne Zugabe von Co(acac)2 . hergestellt .
Strukturelle Charakterisierung
Die Morphologie und Struktur des Co9 S8 @NSC wurden durch Rasterelektronenmikroskopie (REM, ZEISS Gemini 500) und Transmissionselektronenmikroskopie (TEM, JEM-2100HR) charakterisiert. Es wurde ein Test zur thermischen Schwerkraftanalyse (TGA) durchgeführt, um den Gehalt an Co9 . zu bewerten S8 von Netzsch STA449. Die kristallinen Strukturen und Oberflächenvalenzzustandsanalysen wurden durch Röntgen-Photoelektronen-Spektroskopie (XPS, ESCALAB 250Xi), Röntgen-Pulverdiffraktion (XRD, Bruker D8 Advance) und Raman-Spektren nachgewiesen. Die spezifische Oberfläche und die Porengrößenverteilung wurden mit dem Analysegerät Brunauer-Emmett-Teller (BET, Micromeritics ASAP-2020) aufgezeichnet.
Elektrochemische Messungen
Schlämme wurden durch Mischen von Aktivmaterialien, Poly(vinylidenfluorid) (PVDF) und Super P (Gewichtsverhältnis von 8:1:1) mit N-Methylpyrrolidon (NMP) erhalten. Dann wurde die Arbeitselektrode hergestellt, indem die Aufschlämmungen gleichförmig auf eine vorgeschnittene Kupferfolie (Durchmesser 12 mm) aufgetragen und bei 60 °C in Luft bzw. Vakuum über Nacht getrocknet wurden. Die Knopfzellen vom CR2032-Typ wurden mit Natriummetall als Referenzelektrode, einer Glasfasermembran als Separator und der so hergestellten Kupferfolie als Anode zusammengebaut. Der Elektrolyt war 1 M NaClO4 in EC/DMC (EC:DMC =1:1, im Volumen) mit 5,0% FEC. Die Montageverfahren wurden alle in einer Ar-gefüllten Handschuhbox (O2 <0,1 ppm, H2 O <0,1 ppm). Die Ergebnisse der zyklischen Voltammetrie (CV) und der elektrochemischen Impedanzspektroskopie (EIS) wurden von einer elektrochemischen Workstation (CHI660E, Shanghai Chen Hua Instruments Ltd.) erhalten. Und die galvanostatischen Entladungs-Ladungstests wurden in einem NEWARE-Batterietestsystem durchgeführt.
Ergebnisse und Diskussion
Der Syntheseprozess von Co9 S8 @NSC ist in zusätzlicher Datei 1 dargestellt:Schema S1, einschließlich koaxialem Elektrospinnen, solvothermaler Sulfurierung und Karbonisierung. Die Kristallinität von Co9 S8 @NSC und NSC nach diesen Prozeduren sind in Fig. 1a gezeigt. Die XRD-Kurve von Co9 S8 @NSC zeigt typische charakteristische Beugungspeaks in Übereinstimmung mit dem kubischen Co9 S8 Phase (JCPDS Nr. 86-2273), während NSC nur Spitzen von hartem Kohlenstoff aufweist. Der breite Peak bei 24,8° entspricht der (111)-Ebene von amorphem Kohlenstoff. Auffallend ist, dass er niedriger ist als der Standardwert von 26,6°, was auf einen erweiterten Zwischenschichtabstand und eine geringere Graphitisierung hindeutet, die von N,S-codotierten Stellen in den Kohlenstoff abgeleitet wird [41]. Auch die Raman-Spektren (Abb. 1b) bestätigen die Existenz und Zusammensetzung von Kohlenstoff in den Verbundwerkstoffen. Co9 S8 @NSC und NSC zeigen beide zwei offensichtliche Peaks von 1308 cm −1 und 1513 cm −1 , die die D-Bande bzw. die G-Bande von Kohlenstoff darstellen. Außerdem Co9 S8 @NSC besitzt einen schwachen typischen Peak bei 671 cm −1 , entsprechend dem Co9 S8 . Im Detail wird die D-Bande den Strukturdefekten des amorphen Kohlenstoffs zugeschrieben, während die G-Bande auf die E zurückzuführen ist 2g Vibrationsmodus von Sp 2 Bindung zwischen graphitischen Kohlenstoffatomen [45]. Das etwas größere ID /IG von Co9 S8 @NSC (1.31) als NSC (1.14) zeigt an, dass in den Verbundwerkstoffen mehr Defekte vorhanden sind, die aus der N-Dotierung und S-Dotierung resultieren.
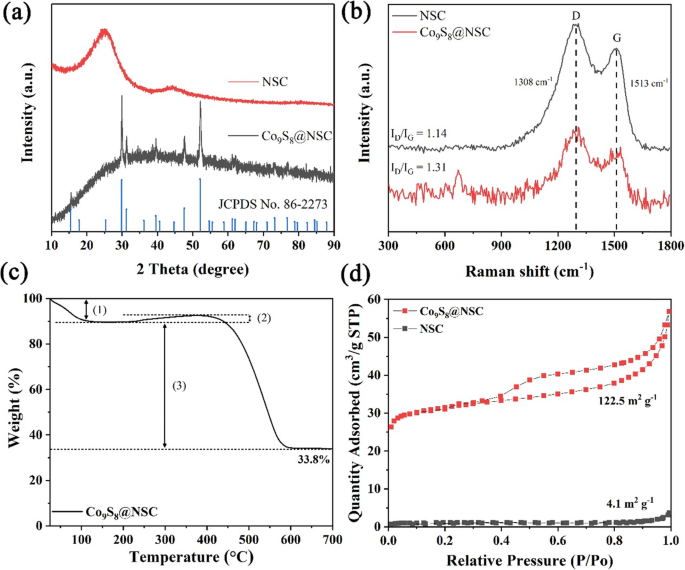
a Röntgenbeugung (XRD) von Co9 S8 @NSC und NSC. b Raman-Spektren von Co9 S8 @NSC und NSC. c TG von Co9 S8 @NSC. d N2 Adsorptions- und Desorptionsisothermen von Co9 S8 @NSC und NSC
Das Gewichtsverhältnis von Co9 S8 wird durch thermogravimetrische Analyse (TGA) gemessen, wie in Fig. 1c gezeigt. Nach dem Erhitzen auf 700°C in Luft mit 10 °C min −1 , ist eine mehrstufige Reaktion mit dem Endprodukt als Co3 . beteiligt O4 , die zugeschrieben werden kann auf:(1) die Verdampfung von Spurenwasser (unter 100°C), (2) die Oxidation von Co9 S8 zu CoSOx (von 200 bis 400°C) und (3) die Zersetzung von Kohlenstoff und die kontinuierliche Oxidation von CoSOx (über 400°C). Gemäß diesen Reaktionen ist der Gehalt an Co9 S8 in den Verbundwerkstoffen wird mit 40,1 % berechnet. Co9 S8 @NSC weist typische Isothermenkurven vom Typ IV auf, die auf die mesoporöse Struktur hinweisen, während die NSC mikroporös ist (Abb. 1d). Die spezifische Oberfläche von Co9 S8 @NSC (122,5 m 2 g −1 ) ist viel größer als NSC (4,1 m 2 .). g −1 ), was die Infiltration von Elektrolyt für eine schnelle Einführung/Extraktion von Na + . fördern kann und die starke Lautstärkeänderung aufgeben. Die Poren von Co9 S8 @NSC mit einer durchschnittlichen Größe von 8,6 nm (gezeigt in Zusatzdatei 1:Abbildung S1) stammen aus der Pyrolyse chemischer Gruppen von Polyacrylnitril, Auflösung von Co(acac)2 aus den Nanofasern und die Bildung von hohlem Co9 S8 Nanokugeln.
Röntgen-Photoelektronenspektroskopie (XPS) wird durchgeführt, um die chemische Zusammensetzung von Co9 . zu bestimmen S8 @NSC. Die Signale im Vermessungsspektrum stimmen mit den fünf Elementen C, N, O, S und Co in Abb. 2a überein. Das Vorhandensein von O sollte darauf zurückzuführen sein, dass die Probe der Luft ausgesetzt wurde, wobei etwas Sauerstoff an der Oberfläche adsorbiert war. Das hochauflösende Spektrum von C 1s (Abb. 2b) zeigt vier Peaks, die bei 284,6 eV (CC/C=C), 285,0 eV (CN), 285,8 eV (CS) und 288,6 eV (C=N ) [46]. Das Co 2p-Spektrum wurde in Abb. 2c gezeigt. Peaks bei 786,1 eV und 803 eV können an die Satellitenpeaks von Co 2p3/2 . angepasst werden und Co 2p1/2 , bzw. Außerdem gehören Peaks von 778,5 eV und 793,6 eV und zwei weitere Peaks bei 781,4 eV und 797,2 eV zu Co 2+ und Co 3+ , bzw. [36]. Darüber hinaus passt das S 2p-Spektrum (Abb. 2d) in vier Peaks, bestehend aus 162,45 eV (S-Co), 163,7 eV (S-C), 165 eV (S-C) und 168,2 eV (Sulfat) [47]. Und N 1s-Spektren (zusätzliche Datei 1:Abbildung S2) enthalten drei Peaks bei 398,4 eV, 400,1 eV und 401,0 eV, die Pyridin-N, Pyrrol-N bzw. Graphit-N entsprechen [48]. Im Vergleich zu reinen Kohlenstoffmaterialien kann die Einführung von N,S-codotierten Kohlenstoffzentren mehr freie Elektronen liefern, was der Adsorption von Na + . zugute kommt an der Oberfläche und erhöht die integrale Leitfähigkeit [41]. Die Ergebnisse aller XPS-Spektren bestätigen das Vorhandensein von N, S-Co-Dotierung in Co9 S8 @NSC.
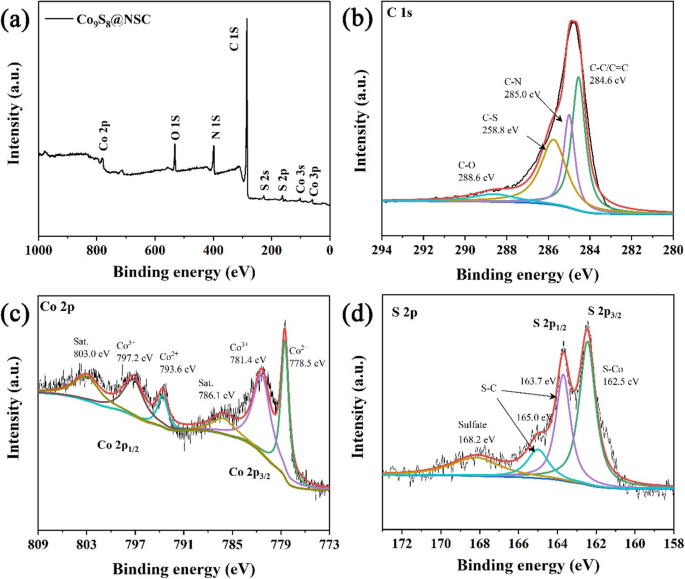
a XPS-Umfragespektrum. b C 1s. c Co 2p und d S 2p von Co9 S8 @NSC
Die interessanten Morphologien und detaillierten internen Strukturen von Co9 S8 @NSC und NSC werden durch SEM und TEM gemessen. Abbildung 3a–c zeigt das Co9 S8 @NSC besteht aus zwei Arten von Strukturen, einschließlich hohler Nanokugeln und Nanofasern. Diese Nanofasern werden durch Karbonisierung von PAN-Fasern aufgebaut. Die Bildung von Nanokügelchen, die auf den Nanofasern haften, kann auf die Zersetzung und Schwefelung von Co(acac)2 . zurückgeführt werden welches aus dem Inneren von PAN-Elektrospinnfasern gelöst wurde. Und die Komposite besitzen die deutlich raue Oberfläche, die die Benetzbarkeit des Elektrolyten verbessern kann. Zusätzliche Datei 1:Abbildung S3a–c zeigt die NSC-Morphologie mit nur glatten Nanofasern, die ohne Nanokugeln aneinander zementiert sind, was auf das Fehlen einer Co-basierten Verbindung und der Schmelze von PAN-Nanofasern beim Karbonisierungsprozess zurückzuführen sein kann. Die elementare Zusammensetzung wird durch EDS-Mapping bestätigt (Zusatzdatei 1:Abbildung S4), wobei sich C-, N-, Co- und S-Elemente gleichmäßig in den Kompositen verteilen. Und dies zeigt weiter die erfolgreiche Dotierung des N,S-Elements.

a –c SEM und d –f TEM von Co9 S8 @NSC bei unterschiedlicher Vergrößerung. (Der Einsatz von (f ) ist der SAED von Co9 S8 @NSC.)
Wie in Abb. 3d–f gezeigt, zeigen TEM-Bilder die internen Details der Morphologien von Co9 S8 @NSC. Abbildung 3d und e zeigen die Co9 S8 Nanopartikel sind in Kohlenstoff-Nanofasern und Nanohohlkugeln eingebettet, was den oben vorgeschlagenen Punkt über die Bildung der Nanohohlkugeln bestätigt. Abbildung 3f zeigt den interplanaren Abstand von 0,308 nm, der gut mit den (311)-Ebenen von Co9 . übereinstimmt S8 , während der NSC in Zusatzdatei 1:Abbildung S3d–f den traditionellen Charakter von Hartkohlenstoff manifestiert. Co9 S8 Nanopartikel mit einer Größe von alle bis zu 50 nm verteilen sich gleichmäßig im Verbund, und die Dicke der Kohlenstoffbeschichtung wird zwischen 3 und 5 nm gemessen (Abb. 3f). Aufgrund der rauen Oberfläche, der hohlen Struktur und der Kohlenstoffbeschichtung können starke Pulverisierung und Abblätterung aktiver Materialien aufgrund von Volumenschwankungen effektiv gemildert werden.
Um die elektrochemische Leistung von Co9 . zu untersuchen S8 @NSC, Knopfzellen vom Typ 2032 werden für elektrochemische Tests montiert. Wie in Fig. 4a gezeigt, sind die CV-Kurven von Co9 S8 @NSC zeichnet die ersten fünf Zyklen mit einer Abtastrate von 0,1 mV s −1 . auf . Der erste Zyklus unterscheidet sich stark von den nachfolgenden Zyklen mit einem breiten Peak bei 0.476 V im kathodischen Durchlauf, der der Bildung eines Festelektrolytgrenzflächenfilms (SEI) und einer irreversiblen Einlagerung von Na + . zugeschrieben wird , und die schrittweise Umwandlung von Co9 S8 zu Co und Na2 S [49]. Im ersten anodischen Durchlauf können zwei Oxidationspeaks von 0.375 V und 1.682 V der mehrstufigen Reaktion von Co zu CoSx . zugeschrieben werden [36]. Die folgenden CV-Kurven von Co9 S8 @NSC überlappen sich allmählich, was auf die hohe elektrochemische Reversibilität hindeutet. Zum Vergleich:CV-Kurven von NSC in Zusatzdatei 1:Abbildung S5a zeigt die typischen charakteristischen Peaks von Kohlenstoff, die die Adsorption und Insertion von Na + . darstellen in Kohlenstoff-Nanofasern. Abbildung 4b und Zusatzdatei 1:Abbildung S5b zeigt die Lade-/Entladekurven für verschiedene Zyklen von Co9 S8 @NSC und NSC mit einer anfänglichen Coulomb-Effizienz (CE) von 54,1 % bzw. 28,3 %. Der relativ niedrige CE wird durch die irreversible Bildung von SEI-Film und Elektrolytverbrauch verursacht [7]. Die Kurven dieser beiden Proben zeigen eine charakteristische Spannungsplattform von Co9 S8 und Kohlenstoff, die mit den Ergebnissen von CV-Tests übereinstimmen (Abb. 4a und Zusatzdatei 1:Abbildung S5a).
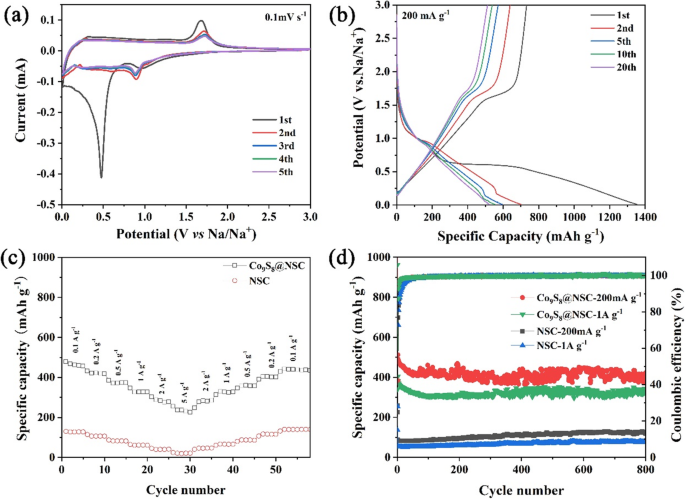
CV-Kurven (a ) und Lade-Entlade-Profile (b ) mit verschiedenen Zyklen von Co9 S8 @NSC. Ratenfähigkeit (c ) und Radfahrleistung (d ) von Co9 S8 @NSC im Vergleich zu NSC
Die Ratenleistung ist in Fig. 4c gezeigt. Die Kapazität von Co9 S8 @NSC kann 226 mAh g −1 erreichen bei 5 A g −1 , während NSC nur 21 mAh g −1 . aufrechterhalten kann . Und dann, wenn sich die Stromdichte auf 100 mAh erholt, g −1 , kann die Kapazität gut auf 440 mAh g −1 . zurückgeführt werden . Abbildung 4d zeigt die Zyklenleistung von Co9 S8 @NSC. Die Entladekapazitäten von Co9 S8 @NSC halten bei 423 mAh g −1 bei 200 mA g −1 und 318 mAh g −1 bei 1 A g −1 nach 800 Zyklen mit anfänglicher Coulomb-Effizienz von 42,3% bzw. 37,4%. Dies kann durch die Umwandlung des Reaktionsmechanismus von Interkalation/Deinterkalation bei niedriger Stromdichte zu Adsorption/Desorption von Na + . erklärt werden bei hoher Stromdichte [2]. Offenbar sind die Kapazitäten von Co9 S8 @NSC sind alle höher als die von NSC, was auf die aktiveren Zentren zurückzuführen ist, die von Co9 . abgeleitet sind S8 und N,S-Co-Dotierung. Darüber hinaus die Kapazitätserhaltung von 87,4 % bei 200 mA g −1 und 83,1 % bei 1 A g −1 nach 800 Zyklen zeigen die stabile Zyklenleistung und die gutartige Reaktionsreversibilität von Co9 . an S8 @NSC.
Um die Grenzflächeneigenschaften und inneren Widerstände von Co9 . zu verstehen S8 @NSC und NSC, elektrochemische Impedanzspektren (EIS) wurden durchgeführt. Wie in Zusatzdatei 1 dargestellt:Abbildung S6a, die Nyquist-Plots von Co9 S8 @NSC zeigt nach verschiedenen Zyklen typische Halbkreise im Hochfrequenzbereich (Ladungsübergangswiderstand, R ct ) und eine schräge Linie im Niederfrequenzbereich (Warburg-Widerstand, W ). Vor dem Anfangszyklus ist der größte R ct (ca. 1600 Ω) von Co9 S8 @NSC wird durch unzureichende Elektrolytinfiltration verursacht. Nach 5 Zyklen ist der R ct wird mit 153 Ω sehr klein für die Bildung eines SEI-Films und einen guten Kontakt mit dem Elektrolyten. Darüber hinaus ist die Abnahme des R ct kann auch auf den Aktivierungsprozess des Co9 . zurückgeführt werden S8 @NSC-Elektrodengrenzfläche. Nach 10 Zyklen hält es fast den gleichen Wert, was auf die hervorragende Stabilität hinweist. Zum Vergleich wird das EIS von NSC auch in Zusatzdatei 1 untersucht:Abbildung S6b–e. Das anfängliche R ct von NSC ist kleiner als Co9 S8 @NSC, was die höhere elektrische Leitfähigkeit von NSC anzeigt. Während der Zyklus weitergeht, wird der R ct von Co9 S8 @NSC wird aufgrund der größeren spezifischen Oberfläche und ausreichender Elektrolytinfiltration allmählich kleiner als die von NSC. Diese oben genannten Ergebnisse unterstützen die gutartige Zyklen- und Ratenleistung von Co9 S8 @NSC.
Um weitere Einblicke in die Elektrochemie von Co9 . zu erhalten S8 @NSC-Elektrode wird eine kinetische Analyse durchgeführt. Die CV-Kurven bei verschiedenen Sweep-Raten von 0,1 bis 0,9 mV s −1 gesammelt und in Abb. 5a dargestellt. Abweichend von der üblichen Ionendiffusion ist der Spitzenstrom (I , mA) ist nicht vollständig linear abhängig von v 1/2 (v ist die Abtastrate, mV s −1 ), was auf die Koexistenz von nicht-faradischem und faradischem Verhalten hinweist [35, 50]. Und die Ergebnisse können durch die Beziehung zwischen log(I ) und log(v ), gemäß der Gleichung von log(I ) =b log(v ) + log(a ). Wenn der Wert von b 0,5 oder 1 erreicht, weist darauf hin, dass der Reaktionsmechanismus vollständig durch Ionendiffusion bzw. kapazitives Verhalten kontrolliert wird [51, 52]. Wie in Abb. 5b gezeigt, sind die berechneten Werte von b sind 0,7518 (kathodischer Peak) und 0,7792 (anodischer Peak), was ein stärkeres kapazitives Verhalten bedeutet.
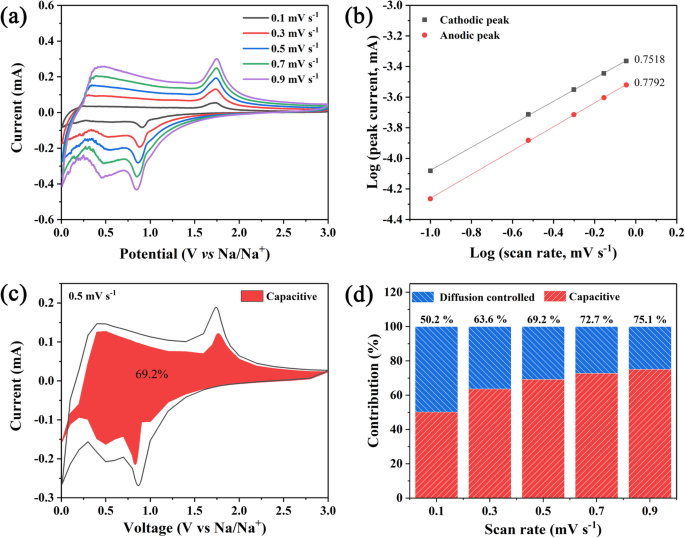
a CV-Kurven von Co9 S8 @NSC bei verschiedenen Scanraten. b Die lineare Beziehung zwischen log (v ) und logge (Ich ). c Kapazitiver Beitrag (rot) in der CV-Kurve. d Beitragsverhältnis der kapazitiven Kapazität bei verschiedenen Abtastraten
Darüber hinaus kann der Beitrag des kapazitiven Verhaltens aus der Gleichung erhalten werden:i (V) =k 1 v + k 2 v 1/2 [42], wobei i (V) ist der Strom bei einer festen Spannung, v ist die Sweep-Rate und k 1 v und k 2 v 1/2 die kapazitive Kapazität bzw. die Ionendiffusionskapazität darstellen. Bei einer Sweep-Rate von 0,5 mV s −1 , erreicht der Beitragsanteil der kapazitiven Kapazität 69,2 % (Abb. 5c). Für unterschiedliche Sweep-Raten zeigt Fig. 5d eine offensichtliche Tendenz, dass das Verhältnis der kapazitiven Kapazität mit der Scan-Rate von 0,1 auf 0,9 mV s −1 . ansteigt . Der zunehmende kapazitive Beitrag kann auf eine hohe spezifische Fläche und reichlich aktive Zentren zurückgeführt werden, die außerdem für die hervorragende Geschwindigkeitsleistung des Co9 . verantwortlich sein können S8 @NSC-Elektrode. Alle diese Ergebnisse zeigen eine schnelle Kinetik von Co9 S8 @NSC, das aus dem kapazitiven Effekt resultierte.
Nach Abb. 5a ist das Na + Diffusionskoeffizienten (D Na+ ) kann aus dem stärksten Spitzenstrom (I p ) und Sweep-Raten (v ) nach Randles-Sevick-Gleichung [32]:
$$ {I}_p=2,69\times {10}^5{n}^{3/2}A{D}_{Na+}^{1/2}{v}^{1/2}C $$wo n , A , und C repräsentieren die Anzahl der übertragenen Elektronen im Prozess von Na + Interkalation/Deinterkalation, die Oberfläche und die molare Konzentration von Na + , bzw. Das D Nein + von Co9 S8 @NSC ist proportional zur Steigung der linearen Beziehungen zwischen I p und v 1/2 (Zusätzliche Datei 1:Abbildung S7). Als Ergebnis sind die Steigungswerte des anodischen Peaks und des kathodischen Peaks von Co9 S8 @NSC sind viel positiv bzw. negativ als die von NSC, was bedeutet, dass das D Nein + von Co9 S8 @NSC ist im Prozess von Na + . viel höher als NSC Interkalation/Deinterkalation. Im Detail kann dies der günstigen Infiltration des Elektrolyten und der stark exponierten aktiven Zentren aufgrund der größeren spezifischen Oberfläche von Co9 . zugeschrieben werden S8 @NSC.
Schlussfolgerungen
Zusammenfassend lässt sich sagen, dass eine neuartige Doppelmorphologie von Co9 S8 , enthaltend hohle Nanokugeln und Nanofasern, mit Beschichtung N, S co-dotierte Kohlenstoffschicht wurde erfolgreich unter Verwendung von koaxialem Elektrospinnen nach Sulfurierung durch Solvothermalverfahren und Carbonisierung synthetisiert. Aufgrund der größeren spezifischen Oberfläche und der Kohlenstoffbeschichtung ist Co9 S8 @NSC kann die Volumenänderung während des Lade-/Entladevorgangs berücksichtigen. Gleichmäßiger, aktive Zentren, die von Co9 . abgeleitet sind S8 und N, S co-dotierte Position kann nicht nur mit viel mehr Elektrolyt in Kontakt treten, sondern auch die Diffusion von Na + . beschleunigen und reversible Reaktion zwischen Na + und Co9 S8 @NSC. Als Anodenmaterial verwendet, Co9 S8 @NSC kann eine hohe reversible spezifische Kapazität von 318 mAh g −1 . liefern nach 800 Zyklen bei 1 A g −1 wobei die Coulomb-Effizienz nahezu 100 % bleibt, während die große Oberfläche und reichlich N,S-codotierte Stellen zu einer hervorragenden Ratenfähigkeit führen können. Die Studie bietet mehr Möglichkeiten von Kobaltsulfiden bei der Entwicklung effektiver Anodenmaterialien für SIBs.
Verfügbarkeit von Daten und Materialien
Alle in diesem Manuskript verwendeten Daten sind auf Anfrage erhältlich.
Abkürzungen
- WET:
-
Brunauer-Emmett-Teller-Analyse
- CE:
-
Coulomb-Effizienz
- Co(acac)2 :
-
Cobalt(II)acetylacetonathydrat
- Lebenslauf:
-
Zyklische Voltammetrie
- DMC:
-
Dimethylcarbonat
- EC:
-
Ethylencarbonat
- EIS:
-
Elektrochemische Impedanzspektroskopie
- LIBs:
-
Lithium-Ionen-Akkus
- NSC:
-
N, S codotierter Kohlenstoff
- SIBs:
-
Natrium-Ionen-Batterien
- TGA:
-
Thermische Schwerkraftanalyse
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Materialien:Glas- und kohlenstofffaserverstärktes PP für die Automobilindustrie
- S, N codotierte Graphen-Quantenpunkt/TiO2-Komposite für eine effiziente photokatalytische Wasserstofferzeugung
- Einfache Synthese von auf MWNT verankerten SiO2@C-Nanopartikeln als Hochleistungsanodenmaterialien für Li-Ionen-Batterien
- MoS2/Acetylene Black Composite mit wenigen Schichten als effizientes Anodenmaterial für Lithium-Ionen-Batterien
- Auswirkung verschiedener Bindemittel auf die elektrochemische Leistung einer Metalloxidanode für Lithium-Ionen-Batterien
- Na4Mn9O18/Carbon Nanotube Composite als elektrochemisches Hochleistungsmaterial für wässrige Natrium-Ionen-Batterien
- Eingebetteter Si/Graphen-Verbundstoff, hergestellt durch thermische Magnesiumreduktion als Anodenmaterial für Lithium-Ionen-Batterien
- Eine nanokristalline Fe2O3-Filmanode, hergestellt durch gepulste Laserabscheidung für Lithium-Ionen-Batterien
- Synthese und Untersuchung von CuGeO3-Nanodrähten als Anodenmaterialien für fortschrittliche Natrium-Ionen-Batterien
- Mesoporöse Silizium-Mikrokügelchen, hergestellt aus in situ magnesiothermischer Reduktion von Siliziumoxid für Hochleistungs-Anodenmaterial in Natrium-Ionen-Batterien



