Graphen-induzierter Ferromagnetismus bei Raumtemperatur in mit Kobalt-Nanopartikeln dekoriertem Graphen-Nanohybrid
Zusammenfassung
Die Kontrolle über die magnetischen Wechselwirkungen in magnetischen Nanopartikeln (MNPs) ist ein entscheidendes Thema für die zukünftige Entwicklung nanometergroßer integrierter „Spintronik“-Anwendungen. Hier haben wir eine Nanohybridstruktur entwickelt, um Ferromagnetismus bei Raumtemperatur über eine einfache, effektive und reproduzierbare solvothermale Synthesemethode zu erreichen. Der Plan wurde auf Cobalt(Co)-NPs angewendet, bei denen das Wachstum von Co-NPs auf der Oberfläche von Nanoplättchen aus reduziertem Graphenoxid (rGO) die magnetischen Wechselwirkungen bei Raumtemperatur von superparamagnetisch auf ferromagnetisch umschaltet. Das Einschalten des Ferromagnetismus in diesem Nanohybrid kann auf die Hybridisierung zwischen ungesättigtem 2pz . zurückzuführen sein Orbitale von Graphen und 3d-Orbitale von Co, die die ferromagnetische Fernordnung fördern. Das ferromagnetische Verhalten von Co-rGO-Nanohybrid macht es zu einem hervorragenden Material im Bereich der Spintronik, Katalyse und Magnetresonanztomographie.
Einführung
In den letzten zehn Jahren haben magnetische Nanopartikel (MNPs) aufgrund ihrer potenziellen Anwendungen in der Spintronik, Katalyse und Biologie das beträchtliche Interesse der Wissenschaftler auf sich gezogen [1, 2]. In verschiedenen Metall-NPs (Fe, Co, Ni) wurden Co-NPs aufgrund ihrer potentiellen industriellen Anwendungen eingehend untersucht. Heutzutage hat sich gezeigt, dass Co-NPs aufgrund ihrer großen Anisotropie und größeren Protonenrelaxation eine hervorragende Alternative zu Eisen-NPs darstellen [3]. Diese interessanten Eigenschaften von Co-NPs machen sie zu einem idealen Kandidaten für Anwendungen in der Katalyse, Magnetresonanztomographie (MRT), Wirkstoffabgabe und therapeutischen [4,5,6].
In 2D-Kohlenstoffmaterialien hat sich Graphen aufgrund seiner großen Oberfläche, seines geringen Gewichts, seiner geringeren Toxizität und seiner hydrophilen Natur als perfektes Trägermaterial für Halbleiter- und Metalloxid-Nanopartikel erwiesen [7]. Die hervorragenden und einzigartigen Eigenschaften von 2D-Graphen kommen von seinen dicht gepackten Kohlenstoffatomen, die ein sp 2 . bilden -hybrides Netzwerk in einem Wabengitter. Beim Metall-NPs-Graphen-Hybrid sind die NPs durch eine starke kovalente Bindung mit der Oberfläche des Graphenblatts verbunden, wodurch die Verdampfung und Migration von NPs weiter verhindert wird. Darüber hinaus hat Graphen ungesättigte pz Orbital- und Null-Bandlücken, diese beiden Eigenschaften sind nützlich für die elektronische Wechselwirkung mit dem 3d-Orbital von Übergangsmetall-NPs [8]. Darüber hinaus kann das resultierende Hybridmaterial aufgrund begrenzter feiner Wechselwirkungen und kleiner Spin-Bahn-Kopplung einzigartige Eigenschaften von Graphen aufweisen, wie lange Spinkohärenzlängen und -zeiten [8]. Graphen ist daher ein vielversprechendes Material, um die elektronische Bandstruktur magnetischer NPs effizient zu alternieren und die ferromagnetischen Wechselwirkungen bei Raumtemperatur zu fördern.
Für die Synthese von MNPs-Graphen-Nanokomposit wurden vom Forscher verschiedene Methoden erforscht, darunter Sol-Gel-Methode, elektrochemische Abscheidung, grüne Synthesemethode, In-situ-Assembly-Methode und Solvothermal-Methode [9,10,11,12,13] . Abhängig von den erforderlichen Anwendungen kann man eine geeignete Art und Weise auswählen, um MNPs-Graphen-Nanokomposit zu synthetisieren, da die oben beschriebenen Verfahren ihre Vor- und Nachteile haben. In einer aktuellen Studie haben Xu et al.. [14] synthetisierten Co-rGO-Nanokomposit durch die einstufige Solvothermalmethode und fanden dieses Komposit als ausgezeichneten Katalysator für die Reduktion von Cr (VI) zu Cr (III). Athinarayanan et al. [12] haben Co3 . vorbereitet O4 -rGO Nanokomposit unter Verwendung von Dattelpalmenfruchtsirup und bewertet seine biologischen Eigenschaften an menschlichen mesenchymalen Stammzellen.
In dieser Arbeit haben wir Co-rGO-Nanohybrid durch eine einfache und effektive solvothermale Synthesemethode entworfen. In Co-rGO-Nanohybrid wurde Graphen als Trägermaterial verwendet, das eine große Oberfläche und Monodispersität für Co-NPs bietet und auch deren Oxidation und Aggregation verhindert. Die detaillierten mikrostrukturellen experimentellen Ergebnisse zeigen die erfolgreiche Bildung von Co-rGO-Nanohybrid. Darüber hinaus wurden die magnetischen Eigenschaften von Co-NPs und Co-rGO-Nanohybrid durch die Magnetometertechnik mit vibrierenden Proben untersucht, wobei die M-H-Kurve bei Raumtemperatur superparamagnetisches Verhalten für Co-NPs zeigt. Darüber hinaus haben wir durch Dekoration von Co-NPs auf der Oberfläche von Graphen ferromagnetisches Verhalten bei Raumtemperatur beobachtet.
Methoden
Materialien
Kobalt(III)acetylacetonat (99,99%, Sigma Aldrich), Oleylamin (> 50,0% (GC), TCI), Ethanol (99,9%, Merc). Ethylenglycol (Fisher Scientific), wasserfreies Natriumacetat (98,5%, Fisher Scientific), Ethylendiamin (99%, Merc), zweifach destilliertes Wasser (99%, Merc). Schwefelsäure (H2 .) SO4 , Fisher Scientific), Salpetersäure (HNO3 , Fisher Scientific), Salzsäure (HCl, Fisher Scientific), Kaliumchlorat (KClO3 , Fisher Scientific).
Synthese von Graphitoxid
Graphitoxid wurde nach der Staudenmaier-Methode mit leichten Modifikationen hergestellt [13, 15, 16]. In einen 500-ml-Becher wurden 180 ml Schwefelsäure und 90 ml Salpetersäure unter einem Eisbad gegeben. Ferner wurden 5 µg Graphitpulver zu der Mischung gegeben und durch magnetisches Rühren vermischen gelassen. Dann wurden 55 µg Kaliumchlorat innerhalb von 2 Stunden zu den Reaktionsmischungen gegeben. Danach wurde das Eisbad entfernt und die Reaktionsmischung 5 Tage lang ziehen gelassen. Schließlich wurde die Lösung gut mit HCl und destillierter Wasserlösung (10-mal) gewaschen und das erhaltene Produkt wurde im Vakuumofen bei 80 °C getrocknet.
Synthese von Kobalt-Nanopartikeln
Die Synthese von Co-NPs wurde durch ein einstufiges solvothermales Verfahren durchgeführt [17]. Kurz gesagt wurden 1,8 ml (641,26 mg) Kobalt(III)acetylacetonat zu 75 ml Oleylamin in einem Becherglas zugegeben. Die Reaktionsmischung wurde unter magnetischem Rühren etwa 1 h auf 100 °C erhitzt. Weiterhin wurde die Mischung in einen 100 ml Autoklaven überführt und 20 h auf 220 °C erhitzt. Schließlich wurde die Lösung mit Ethanol gereinigt und der erhaltene Niederschlag in einem Vakuumofen bei 60 °C getrocknet.
Synthese von Co-rGO Nanohybrid
Co-rGO-Nanohybrid wurde durch eine einfache solvothermale Synthesemethode synthetisiert, wie sie von unserer Gruppe in der vorherigen Studie beschrieben wurde [13, 15, 16]. In einem typischen Syntheseprotokoll wurden 80 ml Ethylenglykol, 15 ml Ethylendiamin, 6 g Natriumacetat, 200 mg Graphitoxid und 50 mg wie synthetisierte Kobalt-Nanopartikel in einem Becherglas 3 h lang beschallt. Außerdem wurde die dispergierte Lösung in einen 100 ml-Autoklaven überführt und 12 h lang auf eine Temperatur von 200°C erhitzt. Schließlich ließ man das Reaktionsgemisch auf Umgebungstemperatur abkühlen, reinigte es mehrmals mit Ethanol und trocknete das erhaltene Produkt in einem Vakuumofen bei 60 °C.
Rigaku MiniFlex Tisch-Röntgendiffraktometer (XRD) mit Cu Kα (λ =1,54 ) wurde verwendet, um ein XRD-Muster von wie synthetisierten Pulverproben zu erhalten. Die Größe und Form der so hergestellten Proben wurden von einem JEOL-2100F-Elektronenmikroskop erfasst. Für diese Charakterisierung wurde eine Beschleunigungsspannung von 120 kV verwendet, und die Proben wurden durch Tropfenkalkulation der dispergierten Probe auf einem 300-mesh-kohlenstoffbeschichteten Kupfergitter hergestellt. Die Oberflächenmorphologien und die Elementarkartierung der so synthetisierten Proben wurden mit einem SEM, einem Zeiss EVO 40-Mikroskop, bei einer Betriebsspannung von 20 kV bestimmt. Die Raman-Spektroskopie wurde mit einem Wi-tech alpha 300 RA-Raman-Spektrometer mit einem Argon-Laser mit einer Wellenlänge von 532 nm durchgeführt. Magnetische Eigenschaften von Co-NPs, rGO und Co-rGO-Verbundstoffen wurden durch die Vibrationsproben-Magnetometer-(VSM)-Technik mit PPMS cryogenics limited, USA, erhalten.
Ergebnisse und Diskussion
Abbildung 1 veranschaulicht den Synthesemechanismus von Co-rGO-Nanohybrid. Wie in der Abbildung dargestellt, wurden zunächst Graphitoxid (GO), Co-NPs, Ethylendiamin (EDA), Ethylenglykol (EG) und Natriumacetat (NaAc) in einen Becher gegeben und in einem Beschallungsgerät beschallt, um die Mischung richtig zu verteilen. Hier wurde NaAc als elektrostatischer Stabilisator verwendet, der die Partikelagglomeration stoppen kann; EDA und EG dienen als Lösungsmittel für die richtige Dispersion von Co-NPs. Nach der richtigen Dispergierung wurde die Mischung 12 h in einen Ofen bei 200 °C überführt. Bei dieser solvothermalen Reaktion spielt EDA eine bedeutende Rolle bei der Entwicklung von Co-rGO-Nanohybrid, und EG wirkt als Reduktionsmittel, das zur Reduktion von GO zu rGO beiträgt [15, 16].
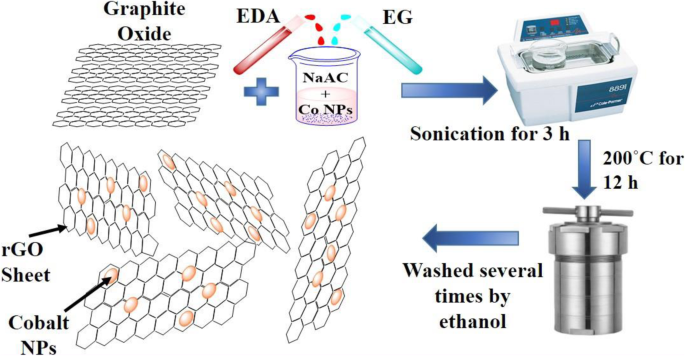
Schematische Darstellung des Synthesemechanismus von Co-rGO-Nanohybrid
Die Größe, Form und Ungleichheit der hergestellten Co-NPs wurden mit dem Transmissionselektronenmikroskop (TEM) untersucht. Wie in Abb. 2a zu sehen ist, haben die meisten Co-NPs eine nahezu sphärische Form mit einer durchschnittlichen Größe von 15–20 nm. Abbildung 2b ist das TEM-Bild von rGO-Nanoblättern, das zeigt, dass das rGO-Blatt mit einer zerknitterten papierähnlichen Oberfläche fast transparent ist. Außerdem sind Fig. 2 c und d TEM- bzw. HRTEM-Bilder von Co-rGO-Nanohybrid. Es ist gut dargestellt, dass Co-NPs erfolgreich über der Oberfläche der rGO-Schicht dekoriert werden. Der durchschnittliche Durchmesser der Co-NPs auf der Oberfläche des rGO-Blatts betrug 5–8 nm, was niedriger ist als der bei Co-NPs beobachtete Wert. Diese Änderung wird durch Graphen und Ethylenglykol beobachtet, die die Größe der Co-NPs bei solvothermalen Reaktionen begrenzen [14]. Darüber hinaus wurde aus dem HRTEM-Bild (Abb. 2d) der Interplanarabstand für rGO- und Co-NPs mit 0,36 bzw. 0,22 nm berechnet, was der (002)-Ebene beider Materialien entspricht. Die Oberflächenmorphologie von rGO- und Co-rGO-Nanohybrid wie synthetisiert wurde durch Rasterelektronenmikroskop (REM) untersucht. Abbildung 2 e ist eine typische REM-Aufnahme von rGO-Nanoblättern. Es veranschaulicht, dass rGO eine flauschige Morphologie mit einer lamellaren Struktur aufweist. REM-Aufnahme von Co-rGO-Nanohybrid ist in Abb. 2f gezeigt. Die weißlichen Flecken über der rGO-Schicht sind ein deutlicher Hinweis auf die gute Dispersion von Co-NPs. Es weist auch auf eine starke kovalente Bindung zwischen Co-NPs und dem rGO-Faltblatt durch elektronische Wechselwirkung hin. Daher spielt rGO eine entscheidende Rolle im Co-rGO-Nanohybrid, indem es die spezifische Oberfläche erhöht und die Disparität von Co-NP fördert, was die katalytische Aktivität synergistisch erhöht [14].

a –d TEM-Bilder a Co-NPs, b rGO-Nanoblätter, c und d Co-rGO-Nanohybrid. e – f REM-Bilder e rGO-Nanoblätter und f Co-rGO-Nanohybrid
Die energiedispersive Röntgenanalyse (EDX) wurde verwendet, um Informationen über lokalisierte Elemente innerhalb des Co-rGO-Nanokomposits zu untersuchen. Abbildung 3 zeigt die Elementaranalyse des Co-rGO-Nanohybrids, die die Existenz von C-, O- und Co-Elementen in der Probe deutlich zeigt. Das Nebenbild von Fig. 3 zeigt den Atomprozentsatz (at %) der konstituierenden Elemente in Co-rGO-Nanohybrid. Die Atomprozentsätze von Co, C und O betrugen 27,05, 67,77 bzw. 5,18 im Nanohybrid.
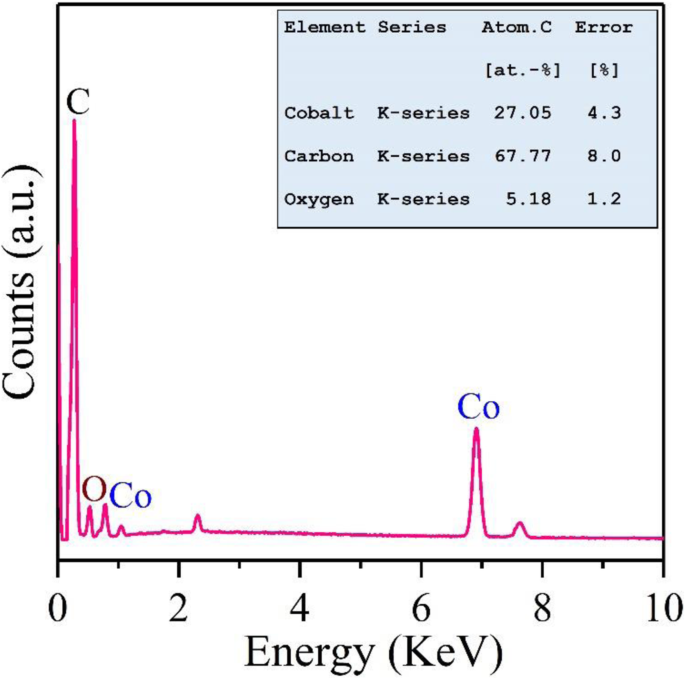
EDX-Spektrum von Co-rGO-Nanohybrid. Das eingefügte Bild zeigt die erhaltenen Elementar-Mapping-Ergebnisse der Co-rGO-Probe
Abbildung 4a zeigt das XRD-Muster der rGO-Nanoblätter. Es beschreibt die erfolgreiche Exfoliation von GO in rGO, da es Reflexion von (002)- und (100)-Ebenen bei 24,83° bzw. 43° enthält [15]. XRD-Muster von Co-NPs erfolgreich indiziert mit (100), (002), (101) und (110) Ebenen bei 41,63, 44,24, 47,37 bzw. 75,80° von Co (Abb. 4Ab) [14] . Diese Reflexionsebenen stimmen gut mit der hcp-Struktur von Co-NPs (JCPDS Nr. 05-0727) überein. Diese aufregende Phase wurde aufgrund der Umwandlung von Kobaltacetylacetonat [Co(acac)3 . beobachtet ] in metallisches Kobalt durch die solvothermale Reaktion. Weiterhin zeigt Fig. 4Ac das XRD-Muster von Co-rGO-Nanohybrid. Zusätzlich zu den in rGO beobachteten Reflexionsebenen {(002), (100) bei 24.83° bzw. 43°} enthält das XRD-Muster alle Reflexionsebenen, wie sie im Fall von Co-NPs gefunden werden. Dieses Ergebnis weist auf eine ordnungsgemäße Phasenbildung von Co-NPs auf der Oberfläche von rGO-Nanoblättern hin. Aus 4Ac ist auch ersichtlich, dass die relative Intensität der Co-Peaks mit der Bildung des Co-rGO-Nanohybrids zunahm. Dies könnte auf eine Verbesserung der Kristallinität und Orientierung von Co-NPs aufgrund von rGO zurückgeführt werden. Xuet al. beobachteten ähnliche Eigenschaften im Fall von Co-rGO-Nanokomposit [14].
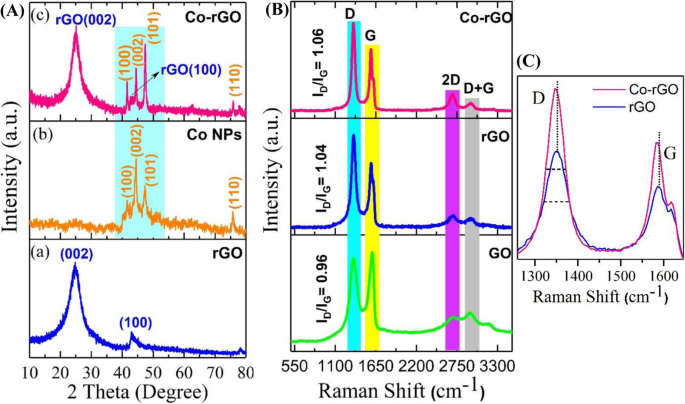
(A ) XRD-Muster a rGO-Nanoblätter, b Co-NPs und c Co-rGO-Nanohybrid (B) Raman-Spektren von GO, rGO und Co-rGO-Nanohybrid (von unten nach oben). (C) Raman-Spektren von rGO und Co-rGO, die Veränderungen der D- und G-Peaks zeigen
Abbildung 4b zeigt die Raman-Spektren von GO-, rGO- und Co-rGO-Nanohybriden. Alle drei Materialien enthalten vier Bänder, nämlich D, G, 2D und D + G, mit einer leichten Änderung ihrer Wellenzahl. Die G-Bande von rGO und Co-rGO Nanohybrid erscheint bei 1586 cm −1 und 1585 cm −1 während die G-Bande von GO bei 1600 cm −1 . beobachtet wird [15, 16]. Im Vergleich zu GO verschiebt sich die G-Bande von rGO und Co-rGO zu einer niedrigeren Wellenzahl, was die Reduktion von GO zu rGO anzeigt [15]. Im Allgemeinen wird als Ursprung der D-Bande eine Störung der Kohlenstoffatome sowie ein Defekt in der graphitischen Struktur angesehen, während die G-Bande als sp 2 . bezeichnet wird Hybridisierung geordneter Kohlenstoffatome in E2g Vibrationsmodus [18, 19]. Außerdem ist das Intensitätsverhältnis des D- und G-Bandes (ID /IG ) berechnet grob das Defektausmaß und den Graphitisierungsgrad von Kohlenstoffatomen. Das ID /IG Werte für rGO und Co-rGO wurden mit 1,04 bzw. 1,06 gefunden, die höher sind als der ID /IG Wert von GO (0,96). Darüber hinaus ist aus 4c ersichtlich, dass die D- und G-Bänder des Hybrids zu einer niedrigeren Wellenzahl verschoben sind (Rotverschiebung) und seine Halbwertsmaxima über die gesamte Breite im Vergleich zu rGO ebenfalls geändert sind. Diese Ergebnisse weisen auf die Hybridisierung von rGO- und Co-Orbitalen hin und bestätigen eine starke elektronische Wechselwirkung zwischen rGO und Co in der Hybridstruktur [8, 20] Die Aufspaltung im G-Band von sowohl rGO- als auch Co-rGO-Hybrid (Abb. 4c) ergab, dass die rGO-Schichten sind nicht mehr als dreischichtiges Graphen [21].
Abbildung 5a zeigt die feldabhängige Magnetisierungskurve (M-H) bei Raumtemperatur für rGO, Co-NPs und Co-rGO-Nanohybrid. Es zeigt, dass das rGO-Nanoblatt wie erwartet nichtmagnetisch reagiert. Andererseits zeigen Co-NPs superparamagnetisches Verhalten (minimale Koerzitivfeldstärke, HC 115 Oe) [22, 23]. Dieses Verhalten wurde aufgrund der kleineren Größe der Co-NPs (unter 20 nm) beobachtet [24]. In diesem Zustand wird die thermische Energie mit anisotroper magnetischer Energie vergleichbar und führt in kurzer Zeit zum Umdrehen der Spins (Abb. 6 linkes Feld). Die magnetische Anisotropieenergie E (ϴ ) pro Teilchen ist definiert als „die Energie, die erforderlich ist, um das magnetische Moment in einer bestimmten Richtung zu halten“ und kann ausgedrückt werden als
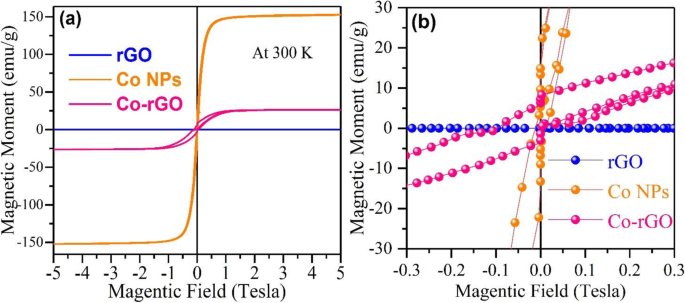
a Raumtemperatur-M-H-Diagramm von rGO, Co-NPs und Co-rGO-Nanohybrid. b M-H-Diagramm im unteren Feldbereich (− 0.3 T bis + 0.3 T).
E (ϴ ) = K eff V Sünde 2 ϴ
Hier, K eff ist die Anisotropiekonstante, V ist das Teilchenvolumen und ϴ ist der Winkel zwischen Magnetisierung und leichter Achse [22]. Die magnetische anisotrope Energiebarriere, die die beiden Spins trennt, d. h. Spin-up- und Spin-down-Zustand, ist proportional zu K eff V . Wenn die Größe des NC ausreichend abnimmt, wird die Energiebarriere kleiner als die thermische Energie (KB T), was zum Umdrehen von Spins führt. Dieses Verhalten wird als superparamagnetisch bezeichnet und Material wird als Superparamagnet bezeichnet. Ein solches Material hat ein massives magnetisches Moment in einem kleinen Magnetfeld ohne jegliche Hysterese. Aus der M-H-Schleife wird der berechnete Wert der Koerzitivfeldstärke (HC ), remanente Magnetisierung (MR ) und Sättigungsmagnetisierung (MS ) für Co-NPs und Co-rGO-Nanohybrid sind in Tabelle 1 aufgeführt.
Darüber hinaus veranschaulicht die M-H-Kurve des CO-rGO-Nanohybrids, wie in Fig. 5 gezeigt, das ferromagnetische Verhalten, da seine Magnetisierung mit hohem HC fast gesättigt ist und MR Werte 650 Oe bzw. 5,90 emu/g. Trotzdem ist der MS Wert des Co-rGO-Nanohybrids signifikant auf 26 emu/g im Vergleich zu seinem Bulk-MS . reduziert Wert (168 emu/g) [24]. Dies liegt an den nichtmagnetischen rGO-Nanoblättern und der geringeren Größe der Co-NPs. Es wird angenommen, dass der Ursprung des Ferromagnetismus (FM) in Co-rGO-Nanohybrid auf die Hybridisierung von pz . zurückzuführen ist -Orbital von rGO mit d-Orbital von Co-NPs (Abb. 6 rechtes Feld). Dies führt zu einem partiellen Elektronentransfer von rGO zum Co-d-Orbital, was die elektronischen Zustände des Nanohybrids weiter modifiziert und die ferromagnetische Wechselwirkung fördert. Wie bereits erwähnt, zeigt das Raman-Spektrum von Hybriden eine starke elektronische Wechselwirkung zwischen Co und rGO, was diesen Ladungstransfer zwischen Co und rGO bestätigt. Sun et al. beobachteten ähnliche Eigenschaften im Fall von mit rGO gerappten Co-dotierten ZnO (Co:ZnO)-Quantenpunkten [8]. Sie haben vorgeschlagen, dass rGO Co 2+ . bilden kann -VO Komplex im Co:ZnO aufgrund des Ladungstransfers von rGO zu Co:ZnO. Dies führt zu Veränderungen des Fermi-Niveaus und führt zur Beobachtung von Ferromagnetismus bei Raumtemperatur in der Hybridstruktur.
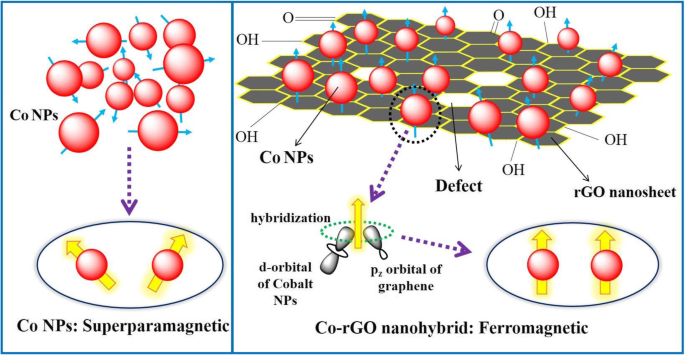
Schematisches Modell für SPM- und FM-Verhalten in Co-NPs bzw. Co-rGO-Nanohybrid
Somit wandelte sich die superparamagnetische Wechselwirkung zwischen Co-NPs mit der Bildung des Co-rGO-Hybrids in eine weitreichende ferromagnetische Wechselwirkung um. Auch die anderen mikrostrukturellen Parameter wie Morphologie, Eigenspannung und Orientierungsfehler können den Koerzitivfeldstärkewert erhöhen [25, 26]. Die Magnetisierungsergebnisse der vorliegenden Arbeit wurden mit einigen MNPs-rGO-Nanokompositen verglichen und in Tabelle 2 aufgelistet.
Schlussfolgerungen
Wir haben eine einstufige solvothermale Methode zur Herstellung von Kobalt-Nanopartikeln und reduziertem Graphenoxid und seinem Derivat zur Bildung von Co-rGO-Nanohybriden verwendet. XRD-, TEM-, SEM- und EDX-Charakterisierungstechniken wurden verwendet, um die korrekte Bildung von Co-rGO-Nanohybrid zu bestätigen. Signifikante Veränderungen im Raman-Spektrum des Co-rGO-Nanohybrids weisen auf eine intensive elektronische Wechselwirkung zwischen rGO und Co im Nanohybrid hin. Die Beobachtung des Ferromagnetismus bei Raumtemperatur im Co-rGO-Nanohybrid könnte das Ergebnis einer elektronischen Wechselwirkung zwischen rGO und Co-NP sein, die die magnetische Wechselwirkung durch Fernordnung weiter fördert. Somit eröffnet diese Studie eine Möglichkeit, ferromagnetisches Co-rGO-Nanohybrid zu synthetisieren, was für zukünftige Spintronik-, Katalyse- und MRT-Anwendungen von Vorteil sein könnte.
Verfügbarkeit von Daten und Materialien
Die verwendeten Datenblätter und Materialien sind auf begründete Anfrage beim entsprechenden Autor erhältlich.
Abkürzungen
- NPs:
-
Nanopartikel
- MNPs:
-
Magnetische Nanopartikel
- Ko:
-
Kobalt
- Fe:
-
Bügeleisen
- Ni:
-
Nickel
- GO:
-
Graphitoxid
- rGO:
-
Reduziertes Graphenoxid
- MRT:
-
Magnetresonanztomographie
- 2D:
-
Zweidimensional
- M-H:
-
Feldabhängige Magnetisierung
- XRD:
-
Röntgendiffraktometer
- SEM:
-
Rasterelektronenmikroskop
- EDX:
-
Energiedispersive Röntgenstrahlung
- TEM:
-
Transmissionselektronenmikroskop
- HRTEM:
-
Hochauflösendes TEM
- VSM:
-
Vibrations-Probenmagnetometer
- bei %:
-
Atomprozentsatz
- SPM:
-
Superparamagnetismus
- FM:
-
Ferromagnetismus
- Ö:
-
Oersted
- T:
-
Tesla
- MS :
-
Sättigungsmagnetisierung
- MR :
-
Remanente Magnetisierung
- HC :
-
Zwang
Nanomaterialien
- Weltweit erster ultraschneller volloptischer Raumtemperaturtransistor
- Biokompatible FePO4-Nanopartikel:Wirkstofftransport, RNA-Stabilisierung und funktionelle Aktivität
- Elektrogesponnene Polymer-Nanofasern, dekoriert mit Edelmetall-Nanopartikeln für die chemische Sensorik
- Mit Titanat-Nanoröhren dekorierte Graphenoxid-Nanokomposite:Vorbereitung, Flammhemmung und Photoabbau
- Ein neuer intelligenter oberflächenverstärkter Raman-Streusensor basierend auf pH-reaktiven Polyacryloylhydrazin-beschichteten Ag-Nanopartikeln
- Modifiziertes hyperverzweigtes Polyglycerin als Dispergiermittel zur Größenkontrolle und Stabilisierung von Goldnanopartikeln in Kohlenwasserstoffen
- Bewertung von Graphen/WO3- und Graphen/CeO x -Strukturen als Elektroden für Superkondensatoranwendungen
- Temperaturabhängigkeit von Raman-aktiven E2g-Phononen in der Ebene in geschichteten Graphen- und h-BN-Flocken
- Graphenoxid-basierte Nanokomposite, dekoriert mit Silbernanopartikeln als antibakterielles Mittel
- Poly(γ-Glutaminsäure) fördert die verstärkte Dechlorierung von p-Chlorphenol durch Fe-Pd-Nanopartikel



