In-situ-Elektrospinnen von Jod-basierten Fasernetzen für antibakterielle Wundverbände
Zusammenfassung
Für die effektive Anwendung von Elektrospinnen und elektrogesponnenen Fasergeweben in Wundverbänden haben wir in situ elektrogesponnenen Poly(vinylpyrrolidon)/Jod (PVP/I), PVP/Poly(vinylpyrrolidon)-Jod (PVPI)-Komplex und Poly(vinylbutyral) ) (PVB)/PVPI-Lösungen in faserige Membranen durch ein tragbares Elektrospinngerät. Die Morphologien der elektrogesponnenen Fasern wurden durch SEM untersucht, und die Hydrophobie, Gasdurchlässigkeit und antibakteriellen Eigenschaften der wie gesponnenen Netze wurden ebenfalls untersucht. Die Flexibilität und Durchführbarkeit des In-situ-Elektrospinnens von PVP/I-, PVP/PVPI- und PVB/PVPI-Membranen sowie die hervorragenden Gasdurchlässigkeiten und antibakteriellen Eigenschaften der wie gesponnenen Netze versprachen deren potenzielle Anwendungen bei der Wundheilung.
Hintergrund
Dank der Vorteile der einfachen Großserienproduktion, des großen Oberfläche-zu-Volumen-Verhältnisses, der hohen Porosität und der abstimmbaren inneren Strukturen [1,2,3,4] haben elektrogesponnene Fasergewebe in verschiedenen Bereichen großes Interesse geweckt B. Filtration [5, 6], medizinische Versorgung [7,8,9,10,11,12] und Energie [13, 14]. Elektrogesponnene Fasermembranen eignen sich aufgrund ihrer nanoskaligen Strukturen, die die Kollagenfibrillen der nativen extrazellulären Matrix und menschlicher Organe nachahmen, für die Wundversorgung [9, 11], und die so gesponnenen Netze können die Wunde nicht nur physikalisch vor Verunreinigungen schützen und Infektionen, sondern bieten auch ein ideales Umfeld für die Hautregeneration durch Aufrechterhaltung eines ausreichenden Gasaustausches sowie Förderung der Hämostasephase und Vermeidung von Narbeninduktion [9, 11, 12].
Unter den Tausenden geeigneter elektrogesponnener Materialien sind Poly(vinylpyrrolidon) (PVP) und Poly(vinylbutyral) (PVB) zwei wichtige Polymere wegen ihrer ausgezeichneten Biokompatibilität, Ungiftigkeit, guten Löslichkeit in Alkohol usw. [15,16,17 ,18]. Folglich wurden die Fasermaterialien aus PVP und PVB im versponnenen Zustand häufig für Wundverbände verwendet [18, 19, 20]. Darüber hinaus bildet PVP in Kombination mit Jod einen Komplex namens PVP-Jod (PVPI) und ist ein hochwirksames und weit verbreitetes Desinfektionsmittel wegen seiner geringen Stimulation, geringen Toxizität, Lichtverschmutzung, bakteriziden Breitbandwirkung und Nichtresistenz der Mikroorganismen für sogar lange Zeit mit [21,22,23,24]. Dennoch wird PVPI nicht zur Langzeitanwendung oder bei komplexen Wunden empfohlen [25]. Elektrogesponnene PVP-I-basierte Fasern können eine hilfreiche Lösung sein und wurden von mehreren Gruppen beschrieben [26,27,28,29,30,31,32,33]. Ignatovaet al. hatten PVPI- oder Poly(ethylenoxid) (PEO)/PVP-I-Fasern durch direktes Elektrospinnen von PVPI- oder PEO/PVP-I-Lösungen oder durch Vernetzen von PVP und PEO/PVP-Matten und Behandeln mit Joddampf oder Jodlösung hergestellt [26]. Wang hatte PVPI-Nanofasern durch Elektrospinnen von PVP-, Jod- und absoluten Ethanollösungen hergestellt, und die Charakterisierung von Fasern im gesponnenen Zustand aus Infrarotspektren, Raman-Spektren und Röntgenbeugung stellt die Bildung des PVPI-Komplexes sicher [27]. Uslu et al. haben über eine Reihe von PVPI-basierten elektrogesponnenen Fasern berichtet, wie Poly(vinylalkohol) (PVA)/PVPI [28], PVA/PVPI/Poly(ethylenglycol) (PEG)-Fasern, die (Hydroxypropyl)methylcellulose (HPMC) und Aloe Vera enthalten [29], PVA/PVPI-Nanofasern mit zusätzlichem Chitosan und Poloxamer 188 [30] und PVA/Poly(acrylsäure) (PAA)/PVPI-Fasern [31]. Von all diesen PVPI-Fasern war bekannt, dass sie potenzielle Anwendungen in der Wundversorgung zeigen, jedoch hauptsächlich auf die Morphologien und die thermische Stabilität der Fasern/Netze im gesponnenen Zustand konzentriert. Honget al. haben PLLA/PVPI/TiO2 gemeldet ultradünne Mehrkomponenten-Faservliese durch Elektrospinnen und Joddampfbehandlung [32]. Es wurde festgestellt, dass die Existenz von PVPI dem Vlies Wasserabsorptionsfähigkeit, antimikrobielle Aktivität, Haftfähigkeit und Umwandlungseigenschaften von Hydrophilie in Nicht-Hydrophilie verleiht. Sebeet al. haben PVP/Poly(vinylpyrrolidon-vinylacetat)/Iod-Nanofasern mit unterschiedlichen Polymerverhältnissen durch eine Hochgeschwindigkeits-Rotationsspinntechnik hergestellt. Neben der detaillierten morphologischen Analyse wurden auch die supramolekulare Struktur und antimikrobielle Aktivität der erhaltenen Matten untersucht, was auf mögliche Anwendungen in der Wundauflage hindeutet [33]. Für praktische Anwendungen können diese PVPI-Elektrospinnfasern jedoch nur anhand von vorgefertigten Modellen hergestellt und dann auf die Wunde des Patienten implantiert werden, was zu zweiten Wundverletzungen führen kann. In-situ-Elektrospinnen könnte dieses Problem lösen.
In diesem Artikel haben wir PVP- und PVB-Lösungen auf Jodbasis in situ mit einer tragbaren Elektrospinnvorrichtung zu Fasernetzen elektrogesponnen. Die Morphologie, Hydrophobie, Gasdurchlässigkeit und antibakterielle Eigenschaft der wie gesponnenen Netze wurden untersucht. Darüber hinaus wurden auch die Auswirkungen der Jodkonzentration auf diese Eigenschaften untersucht. Darüber hinaus wurde die Flexibilität und Machbarkeit von in situ elektrogesponnenen jodbasierten Fasermatten vorgestellt, und dann kann die Anwendung zur Wundauflage erwartet werden.
Methoden/Experimental
Materialien
Polyvinylpyrrolidon (PVP, 250 kDa, Sinopharm Chemical Reagent Co., Ltd., China) wurde in Ethanol (Sinopharm Chemical Reagent Co., Ltd., China) zu 13 Gew.-% gelöst. Poly(vinylbutyral) (PVB) (100 kDa, Sinopharm Chemical Reagent Co., Ltd., China) wurde in Ethylalkohol zu 10 Gew.-% gelöst. Jod (analytisches Reagenz, Sinopharm Chemical Reagent Co., Ltd., China) wurde PVP/Ethanol-Lösungen in einer Konzentration von 1 Gew.-%, 2 Gew.-% bzw. 5 Gew.-% zugesetzt. Der Poly(vinylpyrrolidon)-Iod-Komplex (PVPI, Sinopharm Chemical Reagent Co., Ltd., China) wurde in den PVP/Ethanol- und PVB/Ethanol-Lösungen zu 1 Gew.-%, 2 Gew.-% bzw. 5 Gew.-% gelöst. Die Komplexlösungen wurden vor dem Elektrospinnen mindestens 24 h bei Raumtemperatur unter ständigem Rühren gerührt. Modifizierte simulierte Körperflüssigkeit (SBF) wurde von Sinopharm Chemical Reagent Co., Ltd., China, bezogen.
Elektrospinning-Prozess
Die vorbereiteten Lösungen wurden in eine 5-ml-Spritze mit einer Düse mit einem Durchmesser von 0,1 mm gegeben und dann in das tragbare Elektrospinngerät (HHE-1, Qingdao Junada Technology Co., Ltd) geladen, wie in gezeigt Abb. 1a. Die Hochspannung dieses Gerätes beträgt fest etwa 10 kV [34, 35]. Beim in-situ-Elektrospinnverfahren kann man zunächst das Gerät bedienen und dann mit dem Finger auf die Spritze drücken. Die Fasern im gesponnenen Zustand können hergestellt und dann auf dem Kollektor abgelegt werden, wie in Fig. 1b vorgeschlagen. Die Elektrospinnstrahlen dieses Geräts können von einer Hochgeschwindigkeitskamera erfasst werden, die in Abb. 1c gezeigt ist. Für die weiteren Untersuchungen der in situ elektrogesponnenen Fasergewebe haben wir diese Fasern auch in situ elektrogesponnen auf einen Aluminiumfolienkollektor im Abstand von 8 cm. Die gesammelten Maschen wurden zur weiteren Charakterisierung von der Aluminiumfolie freigelegt.

Das tragbare Elektrospinngerät (a ) und der In-situ-Elektrospinnprozess (b ). Die Elektrospinndüsen sind von der Spinndüse aus zu sehen (c )
Charakterisierung
Die Morphologie und das energiedispersive System (EDS) der gesponnenen Fasern wurden mit einem Rasterelektronenmikroskop (REM, Phenom ProX, Phenom Scientific Instruments Co., Ltd., China) bei 10 kV untersucht, und alle Proben wurden mit Gold beschichtet 30 s lang vor der Analyse. Die Spektren der Fourier-Transformations-Infrarotspektroskopie (FTIR) wurden mit einem Thermo Scientific Nicolet iN10-Spektrometer gemessen. Der simulierte Kontaktwinkel der Körperflüssigkeit (SBF) wurde mit einem Contact Angle Analyzer (JY-PHb, China) mit einem 2-μl-SBF-Tröpfchen untersucht. Basierend auf dem Standard ASTM D 737 wurde die Luftdurchlässigkeit bei einem Druckabfall von 200 Pa mit einem Luftdurchlässigkeitstester (Textest FX3300) getestet. Die Porengrößen der Fasergewebe im gesponnenen Zustand wurden mit PSM 165 (Deutschland, Topas GmbH, PSM 165) bei einem Druck von 200 Pa untersucht. Die antibakteriellen Eigenschaften der Gewebe im gesponnenen Zustand wurden gegen Escherichia coli . untersucht (E. coli , ATCC 10536) und Staphylococcus aureus (S. aureus , ATCC 25923) Bakterien. Bakterienzellen von E. coli (ATCC 10536) und S. aureus (ATCC 25923) wurden 24 Stunden lang auf einem Schüttler bei 37 °C und 100 U/min gezüchtet.
Ergebnisse und Diskussion
Morphologien elektrogesponnener Fasern
Durch die HHE-1-Vorrichtung, wie in Fig. 1 gezeigt, können die hergestellten PVP/I-, PVP/PVPI- und PVB/PVPI-Lösungen bequem zu Fasern elektrogesponnen werden. Die Morphologien der Fasern im Rohzustand konnten aus den in Abb. 2 gezeigten REM-Bildern ermittelt werden. Aus den REM-Bildern kann man offensichtlich erkennen, dass die elektrogesponnenen Fasern glatte Oberflächen aufwiesen, während die Durchmesser der Fasern wie gesponnen unterschiedliche Verteilungen zeigten, weil der verschiedenen Materialien und Konzentrationen. Durch die umfassende Kombination von SEM-Bildern und den Daten in Tabelle 1 wird gezeigt, dass bei PVP/I-Fasern mit zunehmender Jodkonzentration der durchschnittliche Durchmesser der Fasern im gesponnenen Zustand offensichtlich abnimmt, was möglicherweise auf die höhere Leitfähigkeit der Lösungen zurückzuführen ist B. Jod zugesetzt wird [36]. Während bei PVP/PVPI und PVB/PVPI die durchschnittlichen Durchmesser der Fasern im gesponnenen Zustand mit einer höheren PVPI-Konzentration erhöht wurden, was aus der Erhöhung der Viskositäten der gemischten Lösungen resultieren kann [37].

SEM-Bilder der PVP/I (a1–a4), PVP/PVPI (b1–b4), PVB/PVPI (c1–c4) Fasern mit I- oder PVPI-Konzentrationen von 0 %, 1 %, 2 % und 5% bzw.
EDS und FTIR
Um die antibakteriellen Eigenschaften zu erreichen und dann der Wundheilung zugute kommen zu können, spielte Jod bei den elektrogesponnenen Fasern die entscheidende Rolle. Um die Existenz von Jod zu verifizieren, wurde EDS im Modell der Vollspektrumanalyse untersucht. Wie in Abb. 3 gezeigt, haben wir die Fasern im gesponnenen Zustand mit höheren Konzentrationen von I/PVPI, beispielsweise 5 %, gewählt, und die Bilder zeigten, dass bei jeder Art von elektrogesponnenen Fasern, mit Ausnahme der hauptsächlich Kohlenstoff (Abb. 3 ( a1), (b1) und (c1)) und Sauerstoff (Abb. 3 (a2), (b2) und (c2)) Elemente in den Polymeren wurde auch zusätzliches Jodelement beobachtet (Abb. 3 (a3), (b3) und (c3)). Darüber hinaus zeigte das den PVP-Lösungen zugesetzte Jod direkt eine hohe Konzentration an Jod, das sich von dem zugesetzten PVPI unterscheidet. Obwohl das Jod in den EDS-Bildern gefunden werden konnte, kann man aus Abb. 3 offensichtlich erkennen, dass der Jodgehalt im Vergleich zu anderen Elementen gering ist. Dieselbe Schlussfolgerung kann aus den FTIR-Spektren in Abb. 4 gezogen werden.

Verschiedene Elemente von EDS-Bildern der PVP/I (a–a3), PVP/PVPI (b–b3), PVB/PVPI (c–c3) Fasern mit 5% I/PVPI Dotierung
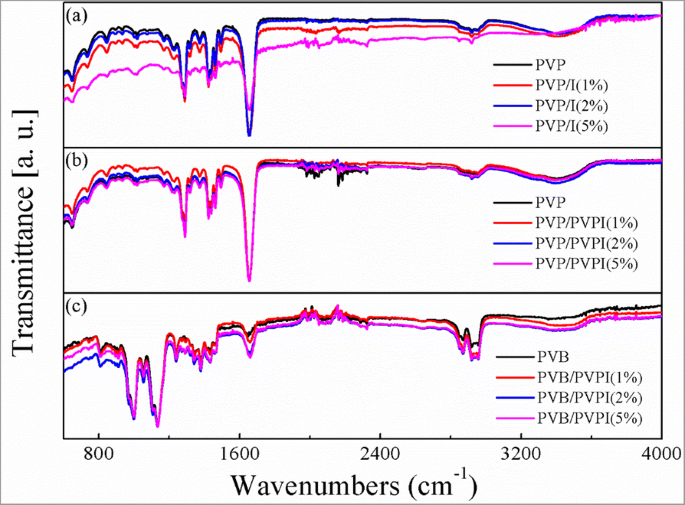
FTIR-Spektren der gesponnenen Fasern PVP/I (a ), PVP/PVPI (b ), PVB/PVPI (c )
Abb. 4a–c zeigten die FTIR-Spektren der Fasern im gesponnenen Zustand mit unterschiedlichen Konzentrationen verschiedener Zugaben. Wie aus Abb. 4 ersichtlich ist, ändern die Zugaben von Jod oder PVPI die chemischen Strukturen der Polymere offensichtlich nicht, was möglicherweise auf die geringe Menge der Zugaben zurückzuführen ist. Die unveränderten Polymere stellten auch die Stabilität der Polymere für die Wundheilung sicher, ohne weitere Unsicherheiten.
Benetzbarkeit
Darüber hinaus wurde angenommen, dass ein idealer Wundverband einige Vorteile aufweisen sollte, wie die Aufrechterhaltung der Wundhydratation und die Absorption von überschüssigem Wundexsudat, was die Benetzbarkeit des entworfenen Wundverbands erfordern kann [5, 7,8,9]. Folglich untersuchten wir auch die Hydrophilie der Fasernetze im gesponnenen Zustand durch Messung ihrer SBF-Kontaktwinkel. Wie in Abb. 5 angedeutet, zeigten alle drei Arten von elektrogesponnenen Fasermembranen mit steigender Jod- und PVPI-Konzentration eine gute Hydrophilie. Bei Netzen auf PVP-Basis bildeten die elektrogesponnenen Fasernetze aufgrund der Hydrophilie des Polymers auch kleine SBF-Kontaktwinkel, und der Winkel erhöhte sich für PVP/I auf 19,5°, wie in Abb. 5 (a–a3) und ( b–b3). Die erhöhten SBF-Kontaktwinkel können aus der zunehmenden Oberflächenrauheit dieser Netze resultieren. Bei PVB-basierten Netzen war der Fall jedoch anders. In unserer vorherigen Studie wurde darauf hingewiesen, dass elektrogesponnene PVB-Fasernetze aufgrund ihrer ungleichen Strukturen Hydrophobie aufweisen [38]. In Abwesenheit von PVPI zeigten die elektrogesponnenen PVB-Netze einen ähnlichen Kontaktwinkelfall, wie in Abb. 5(c) zu sehen ist. Da PVPI in PVB dotiert ist, nahm der SBF-Kontaktwinkel ab und ging mit PVPI von mehr als 2% schnell auf null, was darauf hinwies, dass PVPI die Hydrophilie der wie gesponnenen Fasernetze erhöhte. Die gute Hydrophilie dieser Fasernetze gewährleistet die Fähigkeit, überschüssiges Wundexsudat zu absorbieren und wäre dann für Wundauflagen von Vorteil.

SBF-Kontaktuntersuchung der gesponnenen Fasern PVP/I (a–a3), PVP/PVPI (b–b3), PVB/PVPI (c–c3) mit unterschiedlichen Jod-/PVPI-Konzentrationen
Luftdurchlässigkeit
Ein idealer Wundverband erfordert auch eine gute Luftdurchlässigkeit, um ein positives Umfeld für die Wundheilung zu schaffen [9, 11,12,13]. Hier haben wir auch die Luftdurchlässigkeit dieser Arten von joddotierten Fasergeweben untersucht, wie in Tabelle 2 gezeigt. Wie in Tabelle 2 zu sehen ist, wurde mit der zunehmenden Dotierung von Jod in PVP auch die Luftdurchlässigkeit von 59,92 auf . erhöht 324,3 mm s −1 , was aus dem verringerten Durchmesser und der erhöhten Porosität resultieren kann, während die Luftdurchlässigkeit von Fasergeweben mit PVPI dotiert in PVP und PVB keine offensichtlichen Trends zeigt. Trotzdem zeigen die mit 5% dotierten Polymere eine bessere Gasdurchlässigkeit als die reinen Polymere. Zum Vergleich haben wir auch die Luftdurchlässigkeit von zwei auf dem Markt gekauften traditionellen Wundauflagen (TWD) getestet. Es ist klar, dass die entwickelten elektrogesponnenen faserigen Wundverbände eine bessere Luftdurchlässigkeit aufweisen als die auf dem Markt erhältlichen.
Zur weiteren Untersuchung der Luftdurchlässigkeit testeten wir die Porengröße und Porenverteilung der gesponnenen Netze. Wie in Tabelle 3 gezeigt, wurden die durchschnittlichen Porengrößen der Netze im gesponnenen Zustand aufgelistet. Im Allgemeinen gilt:Je größer die durchschnittliche Porengröße, desto besser die Luftdurchlässigkeit, verglichen mit den Daten in Tabelle 2. Darüber hinaus waren die Porengrößen der wie gesponnenen Fasergewebe hauptsächlich einheitlich, wobei der größte Anteil bei den mittleren Größen liegen kann, die zu finden in Zusatzdatei 1:Abbildung S1. Die Porengrößen dieser elektrogesponnenen Netze lagen im Bereich von 1,936–9,152 μm, was der Größe der menschlichen Gewebezellen entsprach, was für die Wundheilung von Vorteil wäre. Aufgrund der Instrumentenpräzision waren die Porengrößen des TWD jedoch zu klein, um getestet zu werden, was zu einer schlechten Luftdurchlässigkeit führen kann.
Antibakterielle Aktivität
Eine weitere Voraussetzung für einen idealen Wundverband ist Asepsis und sogar Antibiose zur Vorbeugung und Behandlung von Wundinfektionen [11,12,13]. In dieser Arbeit sollen die Jod- und PVPI-Dotierung zu Recht dies erreichen. Die antibakteriellen Aktivitäten der Fasergewebe im gesponnenen Zustand wurden gegen typische pathogene Bakterien wie E. coli und S. aureus , wie in Fig. 6 dargestellt. Aus Fig. 6 kann man entnehmen, dass für reines PVP oder PVB kein bakteriostatischer Kreis gebildet wurde. Nachdem das Polymer mit Jod oder PVPI dotiert war, zeigten die wie gesponnenen Fasermembranen nach 24 Stunden-Intervallen deutliche Hemmzonen für die beiden Bakterienstämme. Darüber hinaus zeigte das mit Jod dotierte PVP die besten antibakteriellen Eigenschaften sowohl gegen E. coli und S. aureus , wobei das PVPI-dotierte PVP den zweiten und PVB/PVPI den letzten Platz belegt. Die guten antibakteriellen Eigenschaften sorgten dafür, dass die elektrogesponnenen Fasergewebe auf Jodbasis zur Wundheilung gegen bakterielle Infektionen der Wunde eingesetzt werden konnten. Darüber hinaus ist zu erwarten, dass die antibakteriellen Eigenschaften der Netze umso besser sind, je höher die Konzentration der zusätzlichen antibakteriellen Mittel ist. Folglich kann man leicht bessere antibakterielle Eigenschaften erzielen, indem man seinen Lösungen mehr Jod oder PVPI hinzufügt.
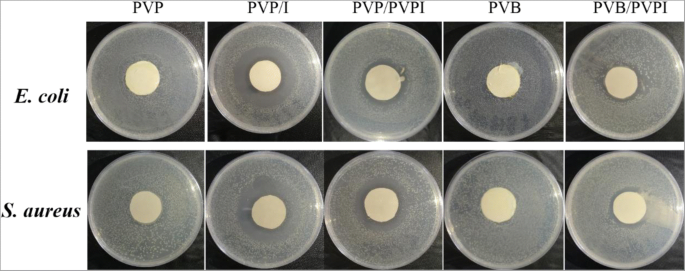
Die antibakterielle Aktivität der frisch gesponnenen Membranen gegen E. coli und S. aureus
In-Situ-Anwendungen
Es wird davon ausgegangen, dass der In-situ-Wundverband durch zusätzliche Überlegenheit, wie z. Folglich wird das In-situ-Elektrospinnen als sinnvolles Konzept angesehen, um unabhängig von Wundgröße und -tiefe geeignete Ersatzstoffe für die Gewebereparatur und Wundheilung direkt an der Läsion des Patienten herzustellen [18, 34, 35, 40, 41]. Wie in Abb. 7a, b gezeigt, können die jodbasierten Fasernetze in situ mit dem HHE-1-Gerät auf die „verletzte Hand“ elektrogesponnen werden und bilden einen dünnen Film auf der Hautoberfläche wie eine zweite Hautschicht gegen elektrostatische Anziehungskräfte. Die elektrogesponnene PVP-I-Fasermembran weist eine gute Flexibilität und Kompaktheit auf und kann bei Bedarf leicht entfernt werden [siehe Abb. 7c, d). Die anschaulicheren Details zum In-situ-Elektrospinnen des PVP-I-Wundverbands finden Sie in Zusätzliche Datei 1:Video S1 und S2 und Abbildung S2.
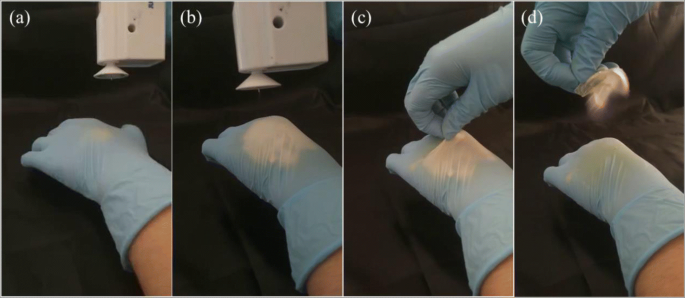
In-situ-Anwendungen des Handgeräts und der elektrogesponnenen Fasermatten auf Jodbasis. Mit dem HHE-1 kann man leicht in situ ein jodbasiertes PVP/I-Netz auf die „verletzte Hand“ (a –b ) lassen sich die Elektroschleudermatten leicht aus dem „Wundbett“ entnehmen (c –d )
Schlussfolgerungen
Zusammenfassend haben wir in situ PVP/I, PVP/PVPI und PVB/PVPI durch eine handgehaltene Elektrospinnvorrichtung zu faserigen Membranen elektrogesponnen. Diese elektrogesponnenen Netze zeigen einheitliche Durchmesser und eine bessere Hydrobilität bei Dotierung mit Jod oder PVPI. Darüber hinaus gewährleistet die gute Luftdurchlässigkeit der Mischungen aus PVP/I-, PVP/PVPI- und PVB/PVPI-Elektrospinngeweben ihre Anwendung in Wundverbänden. Die erhöhten Konzentrationen von Jod und seinem Komplex begünstigen die antibakteriellen Eigenschaften dieser Netze und verbessern dann die Wirkung als Wundauflage. Darüber hinaus kommt das in-situ-Elektrospinnverfahren auch dem Elektrospinnverfahren und den wie gesponnenen Fasergeweben für die Wundheilung zugute.
Abkürzungen
- E. coli :
-
Escherichia coli
- EDS:
-
Energiedispersives System
- FTIR:
-
Fourier-Transformations-Infrarotspektroskopie
- HPMC:
-
(Hydroxypropyl)methylcellulose
- PAA:
-
Poly(acrylsäure)
- PEG:
-
Poly(ethylenglycol)
- PEO:
-
Poly(ethylenoxid)
- PVA:
-
Poly(vinylalkohol)
- PVB:
-
Poly(vinylbutyral)
- PVP:
-
Poly(vinylpyrrolidon)
- PVP/I:
-
Poly(vinylpyrrolidon)/jod
- PVPI:
-
Poly(vinylpyrrolidon)-jod
- S. aureus :
-
Staphylococcus aureus
- SEM:
-
Rasterelektronenmikroskop
- WCA:
-
Wasserkontaktwinkel (WCA)
Nanomaterialien
- Nanodiamanten für magnetische Sensoren
- Nano-Heterojunctions für Solarzellen
- Elektrogesponnene Polymer-Nanofasern, dekoriert mit Edelmetall-Nanopartikeln für die chemische Sensorik
- In-Situ-Aufzeichnungsgerät mit Ladungsteilung (CSIR) zur Echtzeit-Untersuchung des Plasma-Ladeeffekts in FinFET-BEOL-Prozessen
- Herstellung und Charakterisierung eines neuen anodischen Tio2-Kohlenstoff-Nanofaser-Verbundkatalysators für eine Direkt-Methanol-Brennstoffzelle mittels Elektrospinnverfahren
- Antibakterielle Aktivität einer in situ hergestellten Lösung aus Chitosan/Silber-Nanopartikeln gegen Methicillin-resistente Stämme von Staphylococcus aureus
- Entwicklung von elektrogesponnenem Chitosan-Polyethylenoxid/Fibrinogen-Biokomposit für potenzielle Wundheilungsanwendungen
- Hochaktive und stabile Fe-N-C-Sauerstoffreduktions-Elektrokatalysatoren aus Elektrospinnen und In-situ-Pyrolyse
- Verbesserung des photoelektrischen Umwandlungswirkungsgrads der flexiblen faserigen farbstoffsensibilisierten Solarzellen
- Elektrisch feldunterstützte präzise In-situ-Abscheidung von elektrogesponnenen γ-Fe2O3/Polyurethan-Nanofasern für magnetische Hyperthermie



