Rolle der Schlacke in der Konverterstahlerzeugung
Rolle der Schlacke in der Konverterstahlerzeugung
Das Sauerstoffkonverterverfahren ist das primäre Stahlherstellungsverfahren zur Herstellung von unlegierten und niedriglegierten Stählen. Das Verfahren ist im Wesentlichen ein oxidierendes Verfahren zur Veredelung des kohlenstoffreichen Roheisens (HM) zu kohlenstoffarmem Flüssigstahl. Der Oxidationsprozess wird durch Einblasen von Sauerstoff in den Konverter durchgeführt. Dadurch bilden flüssiges Eisen und die anderen in der flüssigen Schmelze im Konverterbad vorhandenen metallischen und nichtmetallischen Verunreinigungen Oxide, die leichter als der flüssige Stahl sind und an die Badoberfläche schwimmen. Der allgemeine Name dieser Oxide ist „Schlacke“. Einige Oxide sind von Natur aus sauer und können mit den basischen feuerfesten Materialien des Konverters reagieren, und daher wird gewöhnlich eine basische Schlacke unter Verwendung von Kalk und kalziniertem Dolomit hergestellt, um die feuerfesten Materialien des Konverters zu schützen. Der Sauerstoff kann auch mit Kohlenstoff reagieren, um ein Gas zu erzeugen, das Blasen zum Aufschäumen der flüssigen Schlacke und zum Bereitstellen chemischer Energie bereitstellt, die während der Stahlherstellung benötigt wird.
Bei der Stahlherstellung ist die Schlacke überwiegend eine Mischung aus Oxiden mit geringen Mengen an Sulfiden und Phosphiden. Die Oxide sind entweder saurer oder basischer Natur. Schlacke entsteht beim Frischen von Roheisen, bei der Si zu SiO2, Mn zu MnO, Fe zu FeO und P zu P2O5 usw. oxidiert, und Zugabe von Oxiden wie CaO (Kalk), MgO (gebrannter Dolomit), Eisenoxid, und andere. Die Zugabe von Oxiden erfolgt, um die gewünschten physikalisch-chemischen Eigenschaften der Schlacke wie Schmelzpunkt, Basizität, Viskosität usw. zu erhalten.
Es gibt vier Hauptquellen für die Schlacke während des Stahlerzeugungsprozesses im Konverter. Dies sind (i) Oxidation metallischer Elemente im flüssigen Stahl (z. B. Silizium, Mangan, Aluminium, Titan, Chrom und Vanadium usw.), (ii) aufgrund des Vorhandenseins von Nichtmetallen im flüssigen Bad (z. B. Schwefel und Phosphor), (iii) Flussmittelzusätze (z. B. Kalk, kalzinierter Dolomit und Flussspat) und gelöste feuerfeste Materialien (z. B. MgO und CaO + MgO).
Eine saure Schlacke erodiert die Konverterauskleidung, da die Auskleidungssteine basisch sind. Die saure Schlacke enthält hohe Mengen an SiO2, Al2O3, die die Schlacke dünner machen können. Eine basische Schlacke enthält Oxide wie MgO und CaO, wodurch die Schlacke dicker wird. FeO ist der wichtigste Bestandteil der Schlacke, da es Kalk bei niedrigeren Temperaturen auflösen lässt, was als „Fluxen“ bezeichnet wird. Da die Schmelztemperatur von CaO 2570 °C und MgO 2800 °C beträgt, ist ersichtlich, dass es schwierig ist, ohne FeO den Schmelzpunkt zu senken, Kalk oder Magnesia in Lösung zu bringen, wenn die Stahlabstichtemperaturen im Allgemeinen unter 1650 °C liegen.
Die Rolle, die die Schlacke im Sauerstoffkonverter-Stahlherstellungsprozess spielt, ist sehr wichtig. Kalk ist für die Stahlherstellung von entscheidender Bedeutung. Die Wissenschaft, wie Kalk mit den verschiedenen Komponenten interagiert, die während der Stahlherstellung entstehen, ist die Grundlage für das Verständnis des alten Satzes „Mache die Schlacke und der Stahl wird sich selbst machen“. Schlacke ist ein Gattungsname und in der Stahlerzeugung meist eine Lösung aus Oxiden und Sulfiden im flüssigen Zustand und den multikristallinen Phasen im festen Zustand. Schlacke ist eine andere Phase als flüssiger Stahl, da sie (i) leichter als der flüssige Stahl ist und (ii) mit dem flüssigen Stahl nicht mischbar ist. Die wichtigen Rollen, die Schlacke während der Stahlherstellung spielt, sind unten aufgeführt.
- Es fungiert als Senke für Verunreinigungen während der Stahlveredelung.
- Es steuert das Oxidations- und Reduktionspotential des Bades während der Raffination durch den FeO-Gehalt. Ein höherer FeO-Gehalt der Schlacke bewirkt, dass die Schlacke oxidiert, während ein niedrigerer FeO-Gehalt die Schlacke reduziert.
- Es hilft bei der Entphosphorung und absorbiert etwas Schwefel.
- Es verhindert den Durchgang von Stickstoff und Wasserstoff aus der Atmosphäre in den flüssigen Stahl im Bad.
- Es absorbiert Oxid-/Sulfideinschlüsse.
- Es isoliert das Flüssigkeitsbad und reduziert Wärmeverluste. Es bildet eine thermische Barriere und verhindert so eine Wärmeübertragung vom flüssigen Stahl in die Umgebung.
- Es schützt den flüssigen Stahl vor Reoxidation.
- Es emulgiert das heiße Metall und fördert die Kohlenstoffoxidation.
Die oben angegebenen Funktionen der Schlacke erfordern, dass die Schlacke bestimmte chemische Eigenschaften (Basizität, Oxidationspotential) sowie physikalische Eigenschaften (Dichte, Schmelzpunkt, Viskosität) besitzt. Beide Eigenschaften werden durch die Zusammensetzung und die Struktur der Schlacke gesteuert.
Vom Standpunkt der Schlackenbildung gibt es zwei einschränkende Blaspraktiken, nämlich (i) weiches Blasen mit hoher Lanzenposition ohne Inertgasbodenrührung und gekennzeichnet durch eine niedrige Eisenbadmischintensität, und (ii) hartes Blasen mit niedriger Lanzenposition und mit Bodenrührung (in kombinierten Blaskonvertern), gekennzeichnet durch intensivere Durchmischung des Eisenbades und tiefere Wechselwirkung des Sauerstoffstrahls mit dem Flüssigkeitsbad. Beim sanften Abblasen ist die Wechselwirkung des Sauerstoffstrahls mit dem Eisenbad oberflächlich, der Stofftransport aus dem Badinneren ist durch schwache Durchmischung langsam, Eisen wird zuerst oxidiert und verschlackt. Beim harten Blasen ist die Wechselwirkung zwischen dem Sauerstoffstrahl und dem Bad sowie der Stoffaustausch vom Badinneren zu den Oberflächenschichten intensiver und die Störelemente des Bades werden zuerst oxidiert. Die Hauptwirkungen des sanften Blasens sind unten angegeben.
- Die Schlackenbildungsrate steigt an
- Es führt zu einem höheren FeO-Gehalt in der Schlacke
- Es führt zu einer Sauerstoffübersättigung des flüssigen Stahls
- Es begünstigt das Aufschäumen von Schlacke
- Es fördert die Entphosphorung zumindest bei einem hohen Kohlenstoffgehalt
- Es erhöht die Oxidationsrate von Mn und anderen Verunreinigungen
- Es erhöht den Verschleiß der feuerfesten Materialien
- Es erhöht die Wahrscheinlichkeit, dass Schlacke verschüttet wird
Es gibt vier Prinzipien bei der Kontrolle von Schlacke in der Stahlherstellung. Diese sind (i) Kontrolle der Schlackenbasizität, die das Verhältnis der basischen Oxide und der sauren Oxide ist, (ii) Sättigung der Schlacke mit MgO, (iii) Schlackenschaumkontrolle, auch bekannt als Schlackenviskositätskontrolle, und (iv) Gleichgewicht von Stahl und Schlacke im Stahlherstellungsprozess zum Erreichen eines „Gleichgewichtszustands“.
Der Begriff Schlackenbasizität ist ein Mittel, mit dem bestimmt wird, wie sauer oder wie basisch eine Schlacke im Verhältnis zu dem im Konverter verwendeten basischen feuerfesten Material ist. Wenn die Schlacke saurer ist, erodiert sie die Ziegel, ist sie basischer, schützt sie die Ziegel. Die Basizität der Schlacke wird normalerweise durch die Menge an zugegebenem Kalk und kalziniertem Dolomit, die Silizium- und Aluminiumgehalte des zugeführten Roheisens und Stahlschrotts sowie Ferrolegierungen festgelegt. Der niedrigere Wert des Verhältnisses zeigt an, dass die Schlacke sauer ist, und wenn das Verhältnis zunimmt, wird die Schlacke immer basischer.
Neben der Basizität ist auch der MgO-Gehalt der Schlacke wichtig. Die Schlacke enthält gelöste Calciumverbindungen und saure Verbindungen, die bewirken, dass sich MgO aus den feuerfesten Steinen der Ausmauerung in die Schlacke löst. MgO löst sich in der Schlacke basierend auf Beziehungen von FeO-Gehalt, Basizität und Temperatur. Je niedriger die Basizität der Schlacke ist, desto höher ist der MgO-Bedarf für die Schlacke. Eine Erhöhung von FeO und Temperatur erhöht auch den MgO-Bedarf der Schlacke. Die Auswirkungen auf MgO sind in Abb. 1 zu sehen.
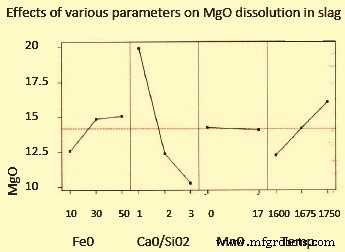
Abb. 1 Auswirkungen verschiedener Parameter auf die MgO-Auflösung in Schlacke
Die Schaumhöhe im Konverter ist eine Funktion der Blaszeit. Die maximale Schaumhöhe ist erreicht, wenn sich die Schlackenmasse 70 % der Endschlackenmenge nähert. Der reaktive Konverterstaub ist eine Quelle von Eisenoxiden und unterstützt die schnelle Bildung von Schaumschlacke, selbst wenn das Einblasen mit einer niedrigen Lanze, d. h. einer harten Einblaspraxis begonnen hat. Die aufschäumende Schlacke verringert das Nachverbrennungsverhältnis und erhöht die Wärmeübertragungseffizienz zum Bad.
Mehrere Faktoren beeinflussen die Schaumneigung der flüssigen Schlacke. Diese sind unten angegeben
- FeO-Gehalt in der Schlacke. Schlacke muss FeO enthalten und in ausreichender Menge vorhanden sein, um mit Kohlenstoff zu reagieren und CO-Blasen zu bilden.
- Richtige Viskosität oder Konsistenz, um die Blasen so lange wie möglich zu halten.
- Ausreichend MgO, um den feuerfesten Verschleiß zu minimieren und die Schaumbildung zu fördern.
Kohlenstoff aus flüssigem Eisen im Bad erzeugt CO-Blasen, um die Schlacke aufzuschäumen. Die Schlackenviskosität wird durch das Verhältnis der Schlackenkomponenten bestimmt und wie diese Komponenten die Schlacke dünn oder dick machen. Es ist das Gleichgewicht dieser Komponenten, um die richtige Schlackenviskosität herzustellen, um die Blasen länger zu halten. SiO2, FeO und Al2O3 machen die Schlacke dünner, während CaO und MgO die Schlacke dicker machen.
Eine grobe Schätzung für die Dichte der Konverterschlacke, die aus CaO, SiO 2 , FeO und MnO usw. besteht, innerhalb typischer Zusammensetzungs- und Temperaturbereiche des Sauerstoffkonverterprozesses beträgt 2,8 bis 3 Tonnen/m³. Wenn das Massenverhältnis von Schlacke zu Stahl am Ende eines Konverterstoßes innerhalb von 0,08 bis 0,1 variiert, steigt das Volumenverhältnis von Schlacke zu Stahl von nahezu Null zu Beginn des Stoßes auf 0,20/0,25 gegen Ende des Stoßes an>
Im Allgemeinen wird angenommen, dass Schlacke Metallauswürfe (Spucken) und Staubbildung aus dem Konverter während des Einblasens dämpft. Wird ein Konverter mit sehr geringer Schlackenmenge betrieben, kann es zu Schwermetallauswürfen und Schädelbildung kommen. Die Eigenschaften der Schlacke sind jedoch von größter Bedeutung. Flüssige, stark oxidierende Schlacke ist günstig für Oxidationsreaktionen, kann aber dazu führen, dass Schlacke aus dem Konverter herausschwappt. Slopping tritt häufig auf, wenn die Schlackenbildung aus irgendeinem Grund verzögert wird und eine große Menge Sauerstoff in die Schlacke durch sanftes Blasen, Erz-/Staubzugabe usw. „geladen“ wird. Eine intensive CO-Bildung führt ohnehin zur Bildung einer Schlacke-Metall-Emulsion, Die Schlackenbildung beginnt, sekundäre und tertiäre Oxidationsreaktionen finden heftig statt und eine verstärkte Gasbildung führt zu starkem Schwappen. Die richtige Kontrolle der Schlackenbildung und Schaumbildung ist eine zentrale Maßnahme zur Vermeidung von Slopping.
FeO in der Schlacke ist proportional zum im Stahl gelösten Sauerstoff. Bei allen Schlacke/Metall-Reaktionen gibt es ein Verhältnis zwischen der Menge einer Sache im Stahl und der Menge in der Schlacke. Dies wird als „Teilungsverhältnis“ bezeichnet. Stahl und Schlacke im Konverter müssen so ausbalanciert werden, dass sie sich im Gleichgewichtszustand befinden. Es gibt auch eine Beziehung zwischen dem Kohlenstoffgehalt im Stahl, der den Sauerstoffgehalt des Stahls steuert. Kohlenstoff beeinflusst den Sauerstoffgehalt im Stahl. Bei niedrigem Kohlenstoffgehalt reagiert Sauerstoff mit Eisen zu FeO, wodurch die Schlacke dünner wird und Ausbeuteverluste beeinträchtigt werden.
Der SiO2-Gehalt der Schlacke bestimmt, wie viel Kalk während der Stahlherstellung benötigt wird. Es senkt auch den Ertrag. Alle Stoffe, die unter oxidierenden Bedingungen in das Konverterbad gelangen, beeinflussen die Anforderungen an die Schlacke und die Kosten dieser Zugaben sowie Ausbeuteverluste. Roheisen und Schrott zusammen beeinflussen den SiO2-Gehalt der Schlacke. Jedes Kilogramm Silizium, das mit Sauerstoff reagiert, erzeugt 2,17 Kilogramm SiO2. Dieses SiO2 muss mit Kalk und kalziniertem Dolomit neutralisiert werden, um eine basische Schlacke zu bilden. Diese basische Schlacke verursacht einen Verlust von 5 kg Eisen als FeO in die Schlacke. Der Grund dafür ist, dass das Schlackenvolumen zunimmt, indem die Menge an saurem Material erhöht wird, das durch ein basisches Material wie Kalk ausgeglichen werden muss.
Der chemische Verschleiß der feuerfesten Auskleidung hängt unter anderem von ihrer Wechselwirkung mit Schlacke/Emulsion, flüssigem Metall und Gasphase einschließlich O2-Blasen ab. Der wichtigste Mechanismus ist die Auflösung des Futters in die Schlacke. Ein entscheidender Punkt ist die schnelle Schlackenbildung, um das im Blasanfang entstehende saure SiO2 zu binden und zu neutralisieren. Stark oxidierende heiße Schlacke löst Magnesia- oder Dolomitauskleidungen leicht auf. Die Verwendung von kalziniertem Dolomit kann die Lebensdauer der Auskleidung erheblich verbessern. In letzter Zeit ist das Verspritzen von Schlacke zu einer etablierten Praxis geworden, um die Lebensdauer des Konverters zu verlängern. Die Restschlacke im Konverter wird nach dem Abstich auf chemische Zusammensetzung und Temperatur konditioniert und durch einen heftigen Stickstoffstrom um die Konverterwand gespritzt. Das Verfahren selbst sowie die Folgen für den Konverterprozess sind ziemlich komplex und die Schlacke sollte für die Behandlung streng angepasst werden.
Schlacke soll während des Stahlherstellungsprozesses im Sauerstoffkonverter mehrere Aufgaben erfüllen. Es wird in erster Linie spontan durch die bei der Oxidation von Eisen entstehenden nichtflüchtigen Oxide und die Nebenbestandteile des Roheisens (SiO2, MnO, P2O5 und FeO) gebildet. Um die Störoxide zu fluxen und eine niedrigschmelzende flüssige Schlacke zu bilden, werden Kalk und kalzinierter Dolomit (ein Gemisch aus CaO und MgO) und ggf. Flussspat (CaF2) in den Konverter chargiert. Zweitens stellt flüssige Schlacke eine Reaktionsumgebung für die Entfernung von Schwefel und Phosphor durch die Prozesse der Entschwefelung und Entphosphorung bereit, obwohl mit der Entwicklung der Sekundärmetallurgie die Bedeutung dieser Reaktionen im Sauerstoffkonverter nicht mehr vorhanden ist. Schlacke spielt bei der Bildung einer Emulsion mit Kohlenmonoxid (CO) und flüssigen Stahltröpfchen (Schlackenschäumen) offensichtlich eine gewisse Rolle bei der Nachverbrennung von CO zu Kohlendioxid (CO2) und beeinflusst die Strahlungswärmeübertragung vom gebildeten „Hot Spot“. in der Sauerstoffstrahl-Flüssigkeitseisen-Prallkammer, wodurch die Temperaturverteilung im Konverter ausgeglichen wird. Schaumschlacke verringert auch deutlich die Rate der Stauberzeugung, indem sie einen Teil des Staubs absorbiert.
Die Schlackenbildung beginnt mit der Auflösung von Sauerstoff in flüssigem Eisen und gleichzeitiger Oxidation von Eisen und anderen Badbestandteilen in der Sauerstoffstrahl-Aufprallzone. Da die Temperatur des Flüssigkeitsbades in der Auftreffzone des Sauerstoffstrahls sehr hoch ist (mehr als 2000 °C), kann eine große Menge Sauerstoff (bis zu 1 %) durch das Eisen gelöst werden. In dieser primären Oxidationszone wird Eisenoxid gebildet und das flüssige Eisen mit hohem Sauerstoffgehalt dringt in das Bad ein und kommt mit frischem flüssigem Eisen im Bad in Kontakt, das einen höheren Gehalt an Kohlenstoff und anderen Bestandteilen hat, die es oxidieren. Ein Teil der primären Reaktionsprodukte wird in die Schlacke- und Ofenatmosphäre gespritzt.
Eisenoxid und andere nichtflüchtige Oxidationsprodukte wie SiO2, MnO und P2O5 usw. vermischen sich mit der vorhandenen Schlacke und mehr Kalk und gebrannter Dolomit wird in der flüssigen Schlacke gelöst. Schlacke entsteht dementsprechend durch eine komplexe Reaktionskette. Die Schlackenbildungsreaktionen sind unten angegeben.
[Si] + 2[O] =SiO2 |
[Mn] + [O] =MnO |
[Fe] + [O] =FeO |
[P] + 5[O] =P2O5 | + CaO + (CaO + MgO) => Schlacke
Diesen Reaktionen folgen sekundäre Oxidations-Reduktions-Reaktionen, insbesondere eine Entkohlung, die auf der Oberfläche von flüssigen Eisentröpfchen stattfindet, die in der Schlacke zirkulieren.
[FexOy] + y C =x Fe + y CO (g)
In der Anlaufphase eines Konverterabblasens, wenn die Badtemperatur niedrig ist, ist die Schlacke normalerweise mit Di-Calcium-Silikat (2CaO.SiO2) gesättigt, aber mit fortschreitender Oxidation des heißen Metalls weicht die Schlackenzusammensetzung von dem Di-Calcium ab Silikat-"Nase" kehrt in der späteren Phase des Schlags dorthin zurück und führt es in den Sättigungsbereich von Tricalciumsilikat (3CaO.SiO2) oder sogar in den Sättigungsbereich von Kalk. Die Bewertung des Schlackenwegs, der die Hochtemperatur-Liquidusoberflächen wie die 2CaO.SiO2-Nase oder die Liquidusoberflächen von 3CaO.SiO2 oder Kalk passiert, und die entsprechende Ausfällung fester Phasen aus dem Flüssigkeitsbad, wird durch die Tatsache, dass Schlacken aus mehreren Komponenten bestehen, etwas verdeckt Phasen und die Schlackentemperaturen liegen Berichten zufolge sogar um mehrere hundert Grad über der Durchschnittstemperatur des flüssigen Eisenbades.
Lokale Affinitäten an Phasengrenzen (Schlacke/Bad, Schlacke/Tröpfchen, Bad/Gas Schlacke/Gas etc.) steuern den Ablauf ähnlicher Reaktionen der Komponenten in der gleichen Lösungsphase (Eisenschmelze oder Schlacke). Die Größe der Reaktionsaffinität hängt von der Standardaffinität und den Aktivitäten (chemischen Potentialen) von Reaktionskomponenten in Lösungsphasen ab. Die lokalen Reaktionsaffinitäten, die die Sauerstoffverteilung zwischen der Oxidationsreaktion von Nebenelementen im Eisenbad und Eisen steuern, d. h. das gegenseitige Fortschreiten der Oxidationsreaktionen, ändern sich mit der Zeit und der Temperaturentwicklung des Prozesses. Auf die gleiche Weise steuern die lokalen Affinitäten sekundärer Oxidationsreaktionen durch Eisen (und andere Oxide in Schlacke, wie Manganoxid) den Fortschritt der Entkohlung gegenüber der Oxidation anderer Nebenbestandteile von Eisentröpfchen in der Schlackenumgebung. Diese thermodynamische Steuerung der Oxidationsreaktion erklärt, warum Eisen oxidiert und bei weichem Schlag verschlackt wird. Ein schwaches Mischen im Eisenbad führt zu einem langsamen Transport kleinerer Badbestandteile (Si, Mn, C usw.) aus dem Badinneren zu den Oberflächenschichten, wo die Oxidation stattfindet und aus denen Eisentröpfchen spritzen oder in die Schlacke platzen. Diese Schichten sind das Auslaufen kleinerer Elemente, ihre Aktivitäten in der Metallphase und dementsprechend sind die Reaktionsaffinitäten relativ zu Eisen verringert. Die Eisenoxidation wird somit thermodynamisch günstig.
Denn die Entphosphorungsschlacke spielt bei der Sauerstoffkonverterstahlerzeugung eine wichtige Rolle. Das Gleichgewicht der Sauerstoffaktivität in Stahl und Schlacke kann in der Oxidationsphase sowie Materialien, die zur Entphosphorung verwendet werden, in Beziehung gesetzt werden. Die Gleichung zum Entfernen von Phosphor aus dem Stahl lautet einfach ausgedrückt wie folgt.
2P + CaO + 5FeO => P2O5.CaO + 5 Fe Temperatur <1640 °C
2P + CaO + 5FeO <=P2O5.CaO + 5 Fe Temperatur> 1640 °C
All dies zeigt, dass zur Entfernung von Phosphor aus dem Stahl Kalk (CaO) und Sauerstoff (FeO) benötigt werden, um das Produkt P2O5.CaO zu erzeugen und in der Schlacke einzufangen. Wenn die Temperatur jedoch über 1640 °C steigt, wird die Reaktion umgekehrt und es findet eine Rephosphorisierung statt. Daher muss zur Entfernung von Phosphor P2O5.CaO-haltige Schlacke durch Entschlackung des Konverters während des Abblasens entfernt werden oder es muss mehr Kalk hinzugefügt, die Hitze stärker heruntergeblasen (Sauerstoffaktivität) oder gehalten werden Kühler.
Herstellungsprozess
- Liquid Crystal Display (LCD)
- Hochofenschlacke und ihre Rolle beim Ofenbetrieb
- Einschlüsse in der Stahl- und Sekundärstahlerzeugung
- Grüne Stahlerzeugung
- Induktionsofen und Stahlerzeugung
- Kombinierter Blasprozess in der Konverterstahlerzeugung
- CAS-OB Prozess der Sekundärstahlerzeugung
- Die Rolle von Präzisionsschläuchen in Flüssigkeitsabgabesystemen:Teil 3 von 3
- Die Rolle von Präzisionsschläuchen in Flüssigkeitsabgabesystemen:Teil 2 von 3
- Die Rolle von Präzisionsschläuchen in Flüssigkeitsabgabesystemen:Teil 1



