Einfache sonochemische Synthese in einem Schritt und photokatalytische Eigenschaften von Graphen/Ag3PO4-Quantenpunkt-Kompositen
Zusammenfassung
In dieser Studie wurde ein neuartiges Graphen/Ag3 PO4 Quantenpunkt (rGO/Ag3 PO4 QD)-Komposit wurde erstmals erfolgreich über eine einfache einstufige photoultraschallunterstützte Reduktionsmethode synthetisiert. Die Verbundstoffe wurden durch verschiedene Techniken analysiert. Gemäß den erhaltenen Ergebnissen ist Ag3 PO4 QDs mit einer Größe von 1–4 nm wurden gleichmäßig auf rGO-Nanoblättern dispergiert, um rGO/Ag3 . zu bilden PO4 QD-Verbundwerkstoffe. Die photokatalytische Aktivität von rGO/Ag3 PO4 QD-Komposite wurden durch die Zersetzung von Methylenblau (MB) bewertet. Unterdessen wurden auch die Auswirkungen der Tensiddosierung und der rGO-Menge auf die photokatalytische Aktivität untersucht. Es wurde festgestellt, dass rGO/Ag3 PO4 QDs (WrGO :WKomposit = 2,3 %) der Verbundwerkstoff zeigte eine bessere photokatalytische Aktivität und Stabilität mit einem Abbau von 97,5 % der MB innerhalb von 5 Minuten. Die verbesserten photokatalytischen Aktivitäten und Stabilitäten waren hauptsächlich auf den synergistischen Effekt zwischen Ag3 . zurückzuführen PO4 QDs und rGO mit hoher spezifischer Oberfläche, die zu einem effizienten Grenzflächentransfer photogenerierter Elektronen und Löcher auf beiden Materialien führten. Darüber hinaus mögliche Bildung und photokatalytische Mechanismen von rGO/Ag3 PO4 QDs wurden vorgeschlagen. Das erhaltene rGO/Ag3 PO4 QDs-Photokatalysatoren hätten großes Potenzial in der Abwasserbehandlung und Wasserspaltung.
Hintergrund
In letzter Zeit hat die Synthese von Photokatalysatoren mit hoher Effizienz die Aufmerksamkeit der Forscher aufgrund ihrer potenziellen Anwendungen bei der Entfernung organischer Schadstoffe und der Wasserstoffproduktion auf sich gezogen [1,2,3]. Aufgrund der hohen Aktivierung und effizienten Trennung der photoangeregten Elektronen (e − ) und Löcher(h + ) [4], Ag3 PO4 Halbleiter-Photokatalysatoren erhielten von Forschern auf dem Gebiet der Photokatalyse große Aufmerksamkeit. Leider gibt es mehrere Faktoren, die die photokatalytische Leistung von Ag3 . beeinflussen PO4 , wie unregelmäßige Morphologie, schlechte Löslichkeit, Instabilität, hohe Kosten usw., die eine breite Anwendung behinderten [5]. Daher ist es notwendig, die Photoaktivität und Photostabilität von Ag3 . zu verbessern PO4 .
Frühere Untersuchungen haben gezeigt, dass die photokatalytische Leistung durch die effiziente Trennung von photogeneriertem e − . deutlich verbessert werden kann -h + Paare [6,7,8]. Nach der Gleichung τ = r 2 /π 2 D , wobei τ stellt die durchschnittliche Diffusionszeit der photogenerierten Ladungsträger dar, r steht für den Partikelradius und D bezieht sich auf den Trägerdiffusionskoeffizienten [9], eine verringerte Partikelgröße kann für die effiziente Unterdrückung der Ladungsträgerrekombination von Vorteil sein, wodurch die photokatalytische Aktivität der Photokatalysatoren verbessert wird. Aus dieser Sicht lässt sich ableiten, dass die Anwesenheit von Quantenpunkten (QDs) die photokatalytische Aktivität verstärken könnte [10, 11]. Da die Tensidbedeckung den gegenseitigen Kontakt zwischen QD-Oberfläche und Schadstoffen behindern kann, wird selten berichtet, dass QDs unabhängig als hocheffizienter Photokatalysator eingesetzt werden. Um diesen Mangel auszugleichen, wurden QDs normalerweise auf einen Träger mit großer Oberfläche geladen, um die Aggregation in Abwesenheit jeglicher Stabilisatoren zu verringern, was QDs mit der verbesserten photokatalytischen Aktivität verleiht.
Aufgrund der besseren Elektronentrennung und des Elektronentransfers in Heterostrukturen wurde rGO als Träger für das Ag3 . ausgewählt PO4 QDs. rGO hat eine zweidimensionale (2D) Kohlenstoffstruktur mit hervorragenden elektronischen, mechanischen und thermischen Eigenschaften [12], hoher spezifischer Oberfläche und hoher Trägermobilität [13,14,15,16].Diese Eigenschaften machen es zu einem guten Substrat für Ag3 PO4 Photokatalysator, da er die e − . effektiv fördern könnte -h + Paartrennung und erleichtern den Ladungstransfer zwischen den Heteroübergängen, um die photokatalytische Aktivität und Stabilität zu verbessern. Darüber hinaus könnte rGO durch ein chemisches Oxidations- und Reduktionsverfahren hergestellt werden [17]. Die Methoden der Graphenoxid (GO) in rGO umfassen die chemische Gasphasenabscheidung (CVD) Reduktion [18, 19], chemische Reduktion [20] und hydrothermale Reduktion [21, 22]. Die obigen Verfahren haben jedoch einige intrinsische Nachteile, wie beispielsweise ein komplexes Verfahren und eine sekundäre Verschmutzung. Daher ist es notwendig, einen grünen Weg zur Herstellung von rGO zu entwickeln. Kürzlich wurde über die neuen umweltfreundlichen Methoden der photounterstützten [23, 24] und ultraschallunterstützten [25] Reduktionsmethode berichtet.
Die Photoreduktion von GO zur Herstellung von rGO ist eine milde und umweltfreundliche Methode; außerdem können photochemische und photothermische Reduktionsmechanismen einzeln oder gleichzeitig in den Prozessen ablaufen [26,27,28]. Darüber hinaus kann die Selbstphotoreduktion von GO zu rGO das Vorhandensein von Lochfängern in der Lösung verstärken [24]. Ultraschall wird häufig für die Materialsynthese und Abwasserbehandlung verwendet [29, 30]. Ultraschallbestrahlung kann lokalisierte Hotspots mit einem Druck von etwa 20 MPa, Temperaturen von etwa 5000 K und einer hohen Abkühlgeschwindigkeit von etwa 10 10 . bieten Ks − 1 , die durch akustische Kavitation erzeugt werden [31]. Bei der Ultraschallbestrahlung können in den Flüssigkeiten durch akustische Kavitation verschiedene physikalische und chemische Effekte erzeugt werden, und unter diesen extremen Bedingungen kann eine einzigartige chemische Reaktionsumgebung bereitgestellt werden [31, 32]. Nach unserem besten Wissen die Synthese von rGO/Ag3 PO4 Über QD-Verbundwerkstoffe mit einer photoultraschallunterstützten Reduktionsmethode wurde noch nicht berichtet.
Hier berichten wir über das Design und die Entwicklung von rGO/Ag3 PO4 QD-Komposite mit hocheffizienter photokatalytischer Leistung, wobei das Ag3 PO4 QDs mit einer Größe von 1–4 nm wurden erstmals über eine einfache einstufige photoultraschallunterstützte Reduktionsmethode gleichmäßig auf rGO-Nanoblätter geladen. Die Verbundstoffe wurden durch verschiedene Techniken analysiert. Die photokatalytische Aktivität und Stabilität der erhaltenen Komposite wurden durch den Abbau von Methylorange (MO), Rhodamin B (RhB) und Methylenblau (MB) unter Bestrahlung mit sichtbarem Licht bewertet. In der Zwischenzeit wurden auch die Tensiddosierung und die Menge an rGO auf die photokatalytische Leistung diskutiert. Der mögliche photokatalytische Mechanismus von rGO/Ag3 PO4 QDs wurden basierend auf den Experimenten zum Einfangen freier Radikale analysiert. Dieses Papier wird eine einfache und umweltfreundliche Methode zur Herstellung mehrerer Metalloxid-QDs und effizienter funktioneller Materialien mit breiterer Anwendung im Bereich der Umweltreinigung bieten.
Experimenteller Abschnitt
Synthese von rGO/Ag3 PO4 QDs
GO wurde aus Naturgraphit nach der Hummers-Methode hergestellt [33]. In einem typischen Syntheseverfahren wurden 20 mg GO in 50 ml Wasser zugegeben und 30 Minuten lang beschallt, um eine einheitliche Suspension zu bilden, und dann wurden 2,2 mmol Natriumoleat in die obige Lösung gegeben und 60 Minuten lang beschallt. Danach 10 ml AgNO3 wässrige Lösung (0,6 mol/l) wurde zugegeben, die erhaltene Lösung wurde 4 h lang gerührt, um den Ionenaustausch abzuschließen, und dann 10 ml Na2 HPO4 wässrige Lösung (0,2 mol/l) wurde der Lösung tropfenweise unter Ultraschallbestrahlung zugesetzt. Nach 60 Minuten wurde das Präzipitat 5 Minuten lang zentrifugiert (5000 U/min) und mehrmals mit Hexylalkohol und absolutem Ethanol gewaschen, um GO/Ag3 . zu erhalten PO4 QD-Verbundwerkstoffe. Danach 0,3 g GO/Ag3 PO4 QDs wurde in 100 ml absolutem Ethanol gelöst und das Gemisch wurde 60 Minuten einer Bestrahlung mit sichtbarem Licht (CEL-S500, 300 W Xe-Lampe, 420 nm-Grenzfilter) und Ultraschall ausgesetzt. Die Ultraschallbestrahlung wurde mit einer hochintensiven Ultraschallsonde (Xinzhi Co., China, JY92-2D, 10 mm Durchmesser, Ti-Horn, 20 kHz) durchgeführt, die in das Reaktionssystem eingebracht wurde. Der Niederschlag wurde 5 min zentrifugiert (5000 U/min) und dann 12 h bei 60 °C getrocknet, um rGO/Ag3 . zu erhalten PO4 QD-Verbundwerkstoffe. Ag3 PO4 QDs wurden unter den gleichen Bedingungen ohne GO hergestellt. Um die optimale rGO-Beladungsmenge zu untersuchen, eine Reihe von Proben mit theoretischen Gewichtsverhältnissen von rGO zu rGO/Ag3 PO4 QD-Verbundwerkstoffe (WrGO :WKomposit = 1,5, 2,0, 2,3, 2,5 und 3,0 Gew.-%) erhalten. Das entsprechende rGO/Ag3 PO4 QD-Komposite wurden als R-1.5, R-2, R-2.3, R-2.5 und R-3 markiert.
Materialcharakterisierung
Ag3 PO4 QDs und rGO/Ag3 PO4 QD-Komposite wurden durch Röntgenbeugung analysiert (XRD, Cu-Ka, k = 1,5418 Å) im 2θ-Bereich von 10° bis 80°, FT-IR-Spektroskopie, TEM (JEOL JEM-2010), Raman-Spektrensystem (Horiba JY-T64000, Frankreich), XPS (PHI Quantera SXM)-Spektrometer und UV- vis-Spektrophotometer (U-3010, Hitachi, Japan). Photolumineszenzspektren wurden mit einem FL-Spektrophotometer (F-4500, Hitachi, Japan) erhalten.
Photokatalytische Aktivitätsmessung
Um die photokatalytischen Eigenschaften der Komposite zu messen, wurden 10 mg der vorbereiteten Proben zu 100 ml von 10 ppm MB hinzugefügt. Die Mischung wurde 30 Minuten lang im Dunkeln magnetisch gerührt, um ein Absorptions-Desorptions-Gleichgewicht sicherzustellen. Ein Filter (λ ≥ 420 nm) wurde auf das Becherglas gelegt und dann mit einer 300 W-Xenon-Lichtquelle (CEL-S500, China) bestrahlt. Am Anfang wurden die Proben alle 1 Minute gesammelt, bis 6 Minuten, und dann wurden die Proben alle 2 Minuten entnommen. Ein UV-Vis-Spektrophotometer wurde verwendet, um die Absorptionseigenschaften der gesammelten Lösung zu analysieren. Die Photokatalysatoren wurden vor den UV-Vis-Messungen durch Zentrifugation (12.000 U/min, 3 Minuten) entfernt.
Nachweis aktiver Arten
Das Einfangexperiment wurde in ähnlicher Weise mit dem photokatalytischen Abbauexperiment durchgeführt. Drei verschiedene Radikalfänger, darunter (Konzentration etwa 1 mM) Isopropanol (IPA, OH·-Scavenger), Dinatriumethylendiamintetraacetat (EDTA, Lochfänger) und p-Benzochinon (BQ, O2 .) · − Scavenger) wurden jeweils verwendet, um die wichtigsten aktiven Spezies zu untersuchen, die beim Photoabbauprozess erzeugt werden.
Ergebnisse und Diskussion
Materialcharakterisierung
Abbildung 1 zeigte die XRD-Muster von GO, rGO, Ag3 PO4 QDs und R-2.3. Die XRD-Ergebnisse von GO und rGO zeigten einen charakteristischen Reflexionspeak bei 2θ = 10,7° bzw. 25° (entsprechend einem d-Abstand von 0,83, 0,36 nm) (Abb. 1a, b) [34]. Alle XRD-Peaks von Ag3 PO4 kann auf die kubisch-raumzentrierte Phase von (JCPDS Nr. 06-0505) indiziert werden (Abb. 1d). R-2.3 zeigte ein ähnliches XRD-Muster mit reinem Ag3 PO4 QDs und die breiteren Beugungspeaks wurden der geringen Größe von Ag3 . zugeschrieben PO4 QDs, die nach der Scherrer-Gleichung [35] zu etwa 3,7 nm berechnet wurde. In den Kompositen konnten keine GO und rGO zugeordneten Beugungspeaks beobachtet werden (Abb. 1c), was auf die geringe rGO-Menge im Komposit zurückgeführt wurde [36]. Um die Wirkung von GO auf die Bildung von Ag3 . zu untersuchen PO4 QDs, das XRD-Muster von reinem Ag3 PO4 QDs wurde gemessen. Die Beugungspeaks von reinem Ag3 PO4 QDs könnten auf kubisches Ag3 . indiziert werden PO4 . Die durchschnittliche Größe von reinem Ag3 PO4 QDs wurde mit der Scherrer-Gleichung zu etwa 5,1 nm berechnet, die größer war als die von rGO/Ag3 PO4 Verbundstoffe. Die obigen Ergebnisse zeigten, dass GO-Schichten die Bildung von Ag3 . beeinflussen könnten PO4 QDs.
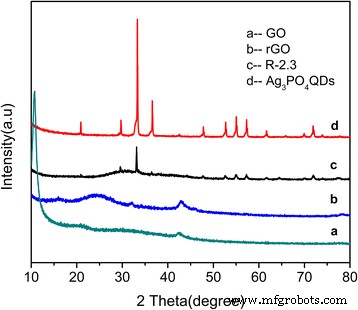
XRD-Muster von a LOS, b rGO, c R-2.3 und d Ag3 PO4 QDs
Abbildung 2 zeigt die TEM-Bilder von R-2.3-Kompositen. Ag3 PO4 QDs mit einer relativ engen Größenverteilung mit einem Durchmesser von 2,81 ± 1,2 nm wurden gleichmäßig auf der rGO-Schicht dispergiert. Der Gitterabstand betrug 0,212 und 0,190 nm, was dem d-Abstand der kristallographischen Ebene (220) und (310) von Ag3 . entsprach PO4 , bzw. Um die Auswirkungen von Ultraschall zu untersuchen, wurde anstelle der Ultraschallbehandlung ein konventionelles Rühren durchgeführt. Die Ergebnisse wurden in der zusätzlichen Datei 1 angezeigt:Abbildung S1. Ag3 PO4 Partikel auf rGO, das durch ein konventionelles Rührverfahren gebildet wurde, zeigten keine einheitliche Struktur und die Größe von Ag3 PO4 größer wurde als die durch Ultraschallbehandlung gebildete. Die obigen Ergebnisse zeigten, dass die Ultraschallbehandlung beim Dispergieren und Kontrollieren der Größe von Ag3 . sehr effektiv war PO4 Partikel auf rGO-Schichten [37].
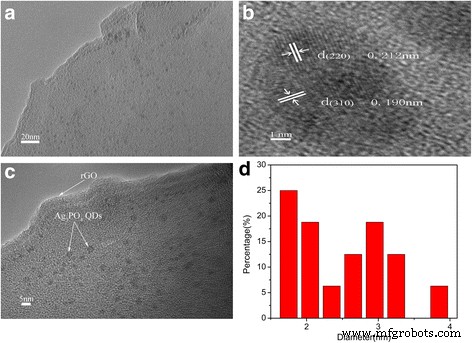
TEM-Bilder von R-2.3 (a , c ), HRTEM-Bild von R-2.3 (b ) und Partikelgrößenverteilung (d )
Die erfolgreiche ultraschallunterstützte Photoreduktion von GO zu rGO kann weiter durch XPS-Spektren von GO- und R-2.3-Kompositen bestätigt werden, wie in Abb. 3 gezeigt. Die Peaks bei 131,7, 284,2, 367,2 und 530,2 eV wurden auf die indiziert charakteristische Peaks von P2p, C1s, Ag3d bzw. O1s (Abb. 3a). Die starken Peaks bei 366,8 und 372,8 eV werden Ag + . zugeschrieben von Ag3 PO4 [38] (Abb. 3b). Die O1s-XPS-Spektren von R-2.3 können in zwei Peaks unterteilt werden, die O1s von Ag3 . zugeschrieben wurden PO4 (529,5 eV) und O1s von rGO (531,3 eV) [7, 39]. Der Peak von O1s von rGO (531,3 eV) hat sich im Vergleich zu dem von GO (531,8 eV) zu einer niedrigeren Bindungsenergie verschoben, was darauf hindeutet, dass eine chemische Wechselwirkung zwischen rGO und Ag3 . bestand PO4 QDs durch C=O-Bindung. Das C1s-Spektrum von GO wurde in drei verschiedene Peaks bei 284,8, 286,7 und 287,7 eV unterteilt, die C-C/C=C, C-O bzw. C=O zugeordnet wurden [40, 41] (Abb. 3c). Nach Reduktion durch sichtbares Licht unterstützt durch Ultraschallbestrahlung (Abb. 3d) zeigten die sauerstoffhaltigen Gruppen, insbesondere C-O, C=O bemerkenswert verringerte Peakintensitäten, was darauf hindeutet, dass die Reduktion von GO zu rGO erfolgreich verlief.
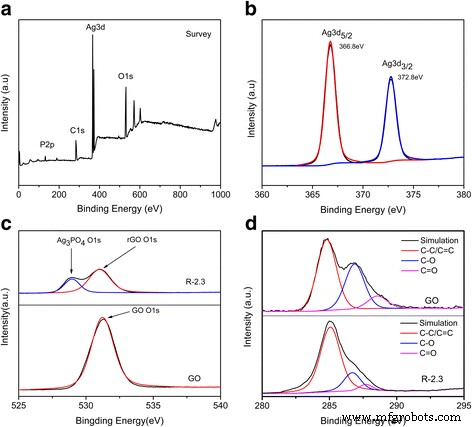
XPS von a Umfragespektrum, b Ag3d, c O1s und d C1s von GO und R-2.3
Abbildung 4a zeigt die FTIR-Spektren von GO, rGO, Ag3 PO4 QDs und R-2.3. Die charakteristischen Peaks bei 1725,6, 1056,5 und 1615,4 cm − 1 in GO wurden den Streckschwingungen von Carboxyl C=O, Alkoxy C-O bzw. C=C zugeschrieben [40, 42]. Der breite Peak bei 3000–3600 cm − 1 wurde der OH-Streckschwingung zugeschrieben [43]. Ag3 PO4 QDs und R-2.3-Komposite hatten ähnliche FT-IR-Peaks bei 552,1 und 970,2 cm − 1 , die den Schwingungen von P-O von PO4 . zugeordnet wurden 3− [44]. Dies deutete darauf hin, dass Ag3 PO4 QDs wurden auf rGO-Platten gebondet. Nach der photoultraschallunterstützten Reduktion auf rGO sind die charakteristischen Peaks (bei 1725,6, 1056,5 cm − 1 ) im Vergleich zu GO zu niedrigeren Wellenzahlen verschoben, was mit den Ergebnissen der XPS-Analyse übereinstimmte, was auf die Existenz einer Ladungswechselwirkung zwischen rGO und Ag3 . hinweist PO4 in den so hergestellten Kompositen.
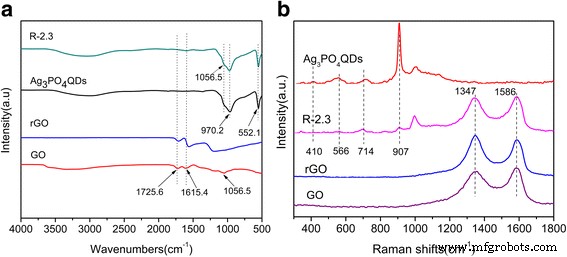
FT-IR-Spektren (a ) und Raman-Spektren (b ) von GO, rGO, Ag3 PO4 QDs und R-2.3
Abbildung 4b zeigt die Raman-Spektren von GO, rGO, Ag3 PO4 QDs und R-2.3. Das Raman-Spektrum von GO zeigte zwei charakteristische Peaks der D-Bande bei 1347 cm − 1 und G-Band bei 1586 cm − 1 . Der Wert von I D /Ich G in R-2,3 und in GO betrug etwa 1,039 bzw. 0,9056. Es war offensichtlich, dass das Komposit eine relativ hohe Intensität der D-Bande im Vergleich zu GO aufwies, was bestätigte, dass die GO-Faltblätter teilweise zu rGO reduziert wurden [37]. Die Raman-Spektren von Ag3 PO4 QDs und R-2.3 zeigten drei unterschiedliche Peaks bei 410, 566 und 714 cm − 1 , und diese Spitzen wurden den P-O-P-Bonds zugeschrieben. Der starke Peak bei 907 cm − 1 wurde durch die Bewegung der terminalen Sauerstoffbindungsschwingung in Phosphatketten hervorgerufen [23].
Vorbereitungsmechanismus von rGO/Ag3 PO4 QDs
Der Syntheseweg von rGO/Ag3 PO4 Ein QD-Komposit wurde vorgeschlagen und in Abb. 5 schematisch dargestellt. Die Synthesereaktionen wurden wie folgt beschrieben:
$$ {\mathrm{Ag}}^{+}+\mathrm{oleate}\ \mathrm{ionen}\to \mathrm{Ag}\hbox{-} \mathrm{oleate} $$$$ \mathrm{Ag }\hbox{-} \mathrm{oleate}+\mathrm{GO}\to \mathrm{GO}\hbox{-} \mathrm{Ag}\hbox{-} \mathrm{oleate} $$ (1) $ $ \mathrm{GO}\hbox{-} \mathrm{Ag}\hbox{-} \mathrm{oleate}+{{\mathrm{PO}}_4}^{3\hbox{-}}\to \mathrm {GO}\hbox{-} {\mathrm{Ag}}_3{\mathrm{PO}}_4\mathrm{QDs} $$ (2) $$ \mathrm{GO}\hbox{-} {\mathrm{ Ag}}_3{\mathrm{PO}}_4+\mathrm{h}\upsilon \to \mathrm{GO}\hbox{-} {\mathrm{Ag}}_3{\mathrm{PO}}_4\mathrm{ QDs}\left({\textrm{e}}^{\hbox{-} }+{\textrm{h}}^{+}\right) $$ (3) $$ {\textrm{H}}_2 \mathrm{O}\zu \cdotp\mathrm{OH}+\cdotp\mathrm{H} $$$$ \cdotp\mathrm{OH}+\cdotp\mathrm{OH}\zu {\mathrm{H}} _2{\mathrm{O}}_2 $$$$ \mathrm{GO}\hbox{-} {\mathrm{Ag}}_3{\mathrm{PO}}_4\mathrm{QDs}+{\mathrm{e }}^{\hbox{-}}\to \mathrm{rGO}\hbox{-} {\mathrm{Ag}}_3{\mathrm{PO}}_4\mathrm{QDs} $$ (4) $$ \mathrm{GO}\hbox{-} {\mathrm{Ag}}_3{\mathrm{PO}}_4\mathrm{QDs}+\cdotp\mathrm{H}\to \mathrm{rGO}\hbox{- } {\mathrm{A g}}_3{\mathrm{PO}}_4\mathrm{QDs} $$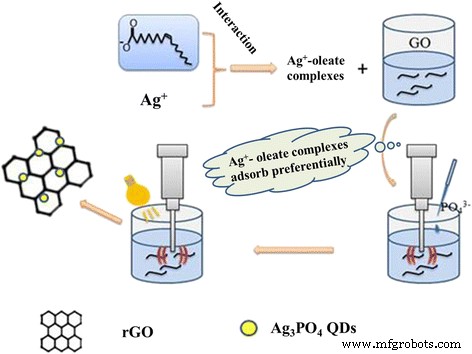
Illustration der Synthese von rGO/Ag3 PO4 QD-Verbundwerkstoffe mittels photo-ultraschallunterstützter Methode
Die Route der Totalsynthese kann in vier aufeinanderfolgende Stufen unterteilt werden. Erstens, Ag + und Oleationen wechselwirkten elektrostatisch, um Ag-Oleat-Komplexe zu bilden, Hydrolyse von Ag + Ionen könnten durch dieses Verfahren wirksam verhindert werden. Ag-Oleat-Komplexe interagierten mit dem Überschuss an Oleat-Ionen und verbesserten dessen hydrophile Eigenschaft, um sich in Wasser zu dispergieren. Sauerstoffgruppen auf der Oberfläche von GO lieferten hydrophile Eigenschaften. Wenn der wässrigen Agoleat-Lösung GO-Faltblätter zugesetzt wurden, adsorbieren die Ag-Oleat-Komplexe bevorzugt an diesen sauerstoffhaltigen funktionellen Gruppen (Gl. (1)). Zweitens Reaktionen zwischen Ag + und PO4 3− ging zur Gründung von Ag3 . über PO4 QDs auf der GO-Oberfläche (Gl. (2)). Drittens, wenn GO-Ag3 PO4 QDs wurden in Lösung beschallt, die ultraschallstimulierten Elektron-Loch-Paare aus Ag3 PO4 QDs bei GO-Ag3 PO4 QDs wurde mit sichtbarem Licht in Ethanollösung bestrahlt. Gleichzeitig ·H und H2 O2 wurden durch Ultraschallbestrahlung hergestellt. Letztendlich wurde GO durch ·H zu rGO reduziert und akzeptierte photogenerierte Elektronen aus dem Leitungsband (CB) von Ag3 PO4 . Als Ergebnis rGO/Ag3 PO4 QD-Komposit wurde durch Photoultraschall-unterstützte Reduktion erhalten.
Optische Eigenschaften der Photokatalyse
Die UV-Vis-Absorptionsspektren von Ag3 PO4 QDs und rGO/Ag3 PO4 QDs mit unterschiedlichem Massenverhältnis von rGO wurden in Abb. 6a gezeigt. Die Absorptionswellenlänge von reinem Ag3 PO4 QDs war kürzer als 530 nm; umgekehrt rGO/Ag3 PO4 Die QD-Verbundstruktur zeigte eine erweiterte Wellenlänge (> 530 nm) und ihre Intensität nahm mit steigendem rGO-Gehalt zu, was zuvor 2,3 % erreichte, und nahm danach ab. Dies kann darauf zurückgeführt werden, dass das Vorhandensein von Kohlenstoff in rGO/Ag3 PO4 QDs reduzieren die Lichtreflexion [45]. Mit der Kubelka-Munk-Funktion [46] erhalten wir die Bandlücken der Photokatalysatoren wie in Abb. 6b und Zusatzdatei 1:Abbildung S2 gezeigt; die Bandlücke von R-2.3 wurde mit 1,62 eV berechnet, was niedriger war als bei reinem Ag3 PO4 QDs (2.23 eV). Die relativ schmale Bandlückenenergie kann dem synergetischen Effekt zugeschrieben werden, dass die Summe des Gesamteffekts dem Einzeleffekt überlegen ist, nachdem verschiedene Arten von Dispersionen zwischen rGO und Ag3 . wechselwirken PO4 QDs [47], die zu einer Verbesserung der Nutzungseffizienz des Sonnenspektrums der Photokatalysatoren führen [36].
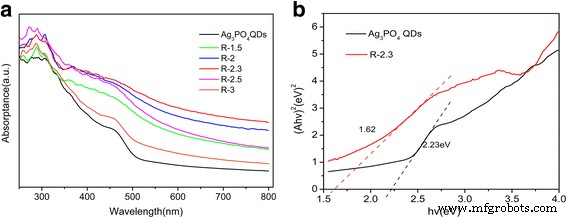
a UV-vis DRS-Spektren von Ag3 PO4 QDs, R-1.5, R-2, R-2.3, R-2.5, R-3 Composites und b die Plots von (αhν) 2 gegen zB
Photokatalytische Aktivität und Stabilität
Um die Einflussfaktoren auf den experimentellen Prozess auf die photokatalytische Aktivität zu verstehen, wurden die Auswirkungen unterschiedlicher Tensidmassen untersucht, wie in Zusatzdatei 1:Abbildung S3 gezeigt. Proben wurden hergestellt, wenn andere Bedingungen konstant blieben. Das Ergebnis zeigte, dass die photokatalytischen Aktivitäten mit zunehmender Tensidmasse zunahmen, aber nach mehr als 0,5 g abnahmen, wie in Zusatzdatei 1 gezeigt:Abbildung S3, was auf die übermäßigen Oleationen zurückgeführt werden kann, die Ag3 PO4 QDs-Größenverteilung auf der rGO-Oberfläche [35]. Dies führt zu einer Abnahme der photokatalytischen Aktivität. Im Vergleich zu reinem Ag3 PO4 QDs, die MB-Konzentration nahm für rGO/Ag3 rapidly schnell ab PO4 QD-Verbundwerkstoffe (Abb. 7a). Dieses Ergebnis deutet darauf hin, dass die photokatalytische Reaktion mit der Existenz aktiver Zentren zusammenhängt [48, 49]. Bei einem rGO-Gehalt von 2,3 % trat die höchste photokatalytische Aktivität auf und konnte MB 5 min lang um 97,46 % abbauen. Dies kann dem rGO-Halbleiter-Heteroübergang zugeschrieben werden, der den Ladungstransfer von rGO-Nanoblättern unter Bestrahlung mit sichtbarem Licht effektiv genutzt hatte [23]. Unter den gleichen Bedingungen hatten die Ergebnisse bei einer Erhöhung des rGO-Gehalts auf 3% die Tatsache bewiesen, dass eine übermäßige Beladung mit rGO die Farbstoff- und Photonenabsorption auf Ag3 . verringern kann PO4 [23]. Wichtig:rGO/Ag3 PO4 QD-Komposite zeigten eine bessere photokatalytische Leistung als reines Ag3 PO4 QDs und rGO-basiertes Ag3 PO4 Komposite [23, 50]. Die durch Licht angeregten Elektronen (e − ) könnte von der CB von Ag3 . übertragen werden PO4 QDs zu rGO und rGO in den Kompositen könnten als Autobahn für den Elektronentransfer fungieren, um das e − . zu unterdrücken -h + Rekombination, die für die bemerkenswert verbesserte Photokonversionseffizienz verantwortlich war [51]. Darüber hinaus könnte der Ladungstransfer an der Grenzfläche aufgrund der größeren Oberflächenfläche von rGO erleichtert werden [52, 53]. Darüber hinaus wurde die photokatalytische Abbaueffizienz von R-2.3-Komposit gegenüber verschiedenen organischen Farbstoffen untersucht, wie in Zusätzliche Datei 1:Abbildung S4 gezeigt.
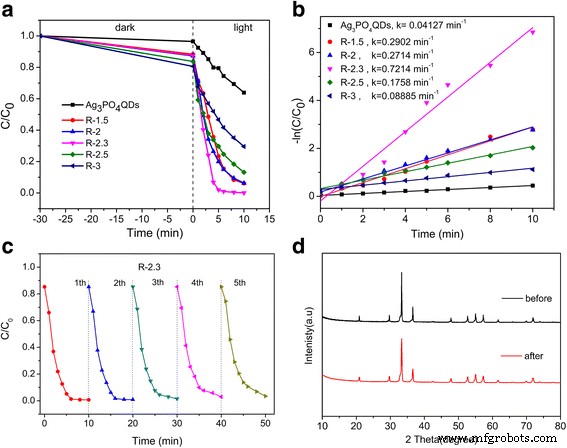
a Photokatalytischer Abbau von MB durch Ag3 PO4 QDs, R-1.5, R-2, R-2.3, R-2.5 und R-3 Composites, b entsprechende Geschwindigkeitskonstanten (k) von Proben für den photokatalytischen Abbau von MB, c Recyclingexperimente des R-2.3 zum Abbau von MB und d XRD-Muster vor und nach den Recyclingexperimenten
Um die Stabilität des R-2.3-Komposites zu testen, wurden die Zyklenexperimente des Komposits für MB durchgeführt (Abb. 7c). Die Ergebnisse zeigten, dass R-2.3-Verbundwerkstoffe nach fünf Zyklen eine höhere photokatalytische Stabilität aufweisen, wobei ihre Abbaueffizienz bis zu 90% beibehalten wurde, was auf die gute photokatalytische Stabilität hinweist. Und dies kann von dem effizienten fotogenerierten e − . profitieren -h + Trennung. Darüber hinaus ist das XRD-Muster von R-2.3, das für fünf Zyklen verwendet wurde, in 7d gezeigt, und es wird kein offensichtlicher Peak über Ag beobachtet. Dies kann darauf zurückgeführt werden, dass rGO den Elektronentransfer auf Ag3<. erleichtern könnte /sub> PO4 QDs und verringerte die Photokorrosion von Ag3 PO4 QDs [23].
Mechanismus der verbesserten photokatalytischen Leistung
Die oben genannten experimentellen Ergebnisse zeigten, dass die photokatalytische Leistung von Ag3 PO4 wurde durch die Kombination von Ag3 . verbessert PO4 mit rGO-Blättern, was der schnellen Übertragung und Trennung von photogeneriertem e − . zugeschrieben wurde -h + Paare in den Kompositen [23]. Die Photolumineszenz (PL)-Spektren wurden durchgeführt, um die e − -h + Paare Migrations-, Transfer- und Rekombinationsprozesse in Halbleitern [54, 55]. Abbildung 8a zeigt die PL-Spektren der Proben. Die PL-Spektren von rGO/Ag3PO4-QDs zeigten eine geringere Rekombinationsrate von photogeneriertem e − -h + Paare im Vergleich zu Ag3 PO4 QDs, was darauf hindeutet, dass mehr photogeneriertes e − und h + kann an der Reduktions- und Oxidationsreaktion teilnehmen; dies könnte zu einem Rückgang der Rekombination von photogeneriertem e − . führen -h + Paare in Ag3 PO4 bei den Kompositen. Daher rGO/Ag3 PO4 QD-Komposit zeigte eine überlegene photokatalytische Aktivität als die von Ag3 PO4 QDs.
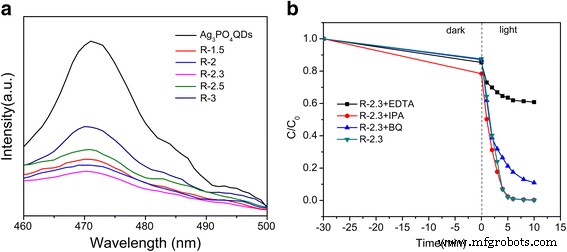
a Photolumineszenzspektren von Ag3 PO4 QDs, R-1.5, R-2, R-2.3, R-2.5 und R-3 und b die Wirkung verschiedener Quencher auf den photokatalytischen Abbau von MB
Zur weiteren Bestätigung der wichtigsten aktiven Spezies im Photokatalyseprozess über rGO/Ag3 PO4 QDs, MB wurde als Schadstoff verwendet. Die Ergebnisse sind in Abb. 8b dargestellt. Hier wird nach Zugabe von Isopropanol (als Hydroxylradikalfänger) [56] die katalytische Aktivität von rGO/Ag3 PO4 QDs war offensichtlich nicht betroffen; bei Zugabe von EDTA (als Hole Capture) [57] wurde der photokatalytische Abbau von MB stark gehemmt. Wenn jedoch p-Benzochinon (BQ, O2 · − Scavenger) hinzugefügt, die Deaktivierung von rGO/Ag3 PO4 QDs war nicht zu vernachlässigen. Die obigen Ergebnisse haben gezeigt, dass Löcher und O2 · − Radikale waren die wichtigsten aktiven Spezies im Photokatalyseprozess.
Der Mechanismus des photokatalytischen Abbaus organischer Farbstoffe durch rGO/Ag3 PO4 QDs ist in Abb. 9 dargestellt. Bei Belichtung mit sichtbarem Licht wird Ag3 PO4 QDs wurden photoangeregt, und Elektronen wurden vom Valenzband zum Leitungsband angeregt; danach konnten die Elektronen aufgrund der Wirkung des elektrischen Felds auf rGO übertragen werden, und dann wurden Elektronen auf die Oberfläche von rGO zurückübertragen, um an der photokatalytischen Reaktion teilzunehmen. rGO könnte e − . effizient trennen -h + Paaren, nutzten somit den Elektronentransfer [23] und führten zu der geförderten photokatalytischen Aktivität von rGO/Ag3 PO4 QD-Verbundwerkstoffe.
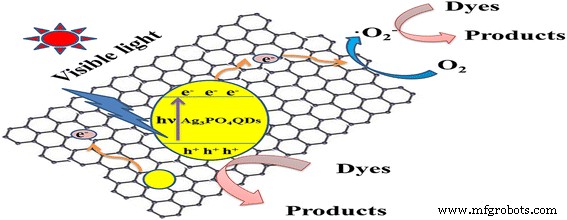
Der Mechanismus des photokatalytischen Abbaus organischer Farbstoffe auf der Oberfläche von rGO/Ag3 PO4 QD-Verbundwerkstoffe
Schlussfolgerungen
Ein neuartiges rGO/Ag3 PO4 QD-Komposit wurde über eine einfache photoultraschallunterstützte Reduktionsmethode hergestellt. Das erhaltene rGO/Ag3 PO4 QD-Komposite zeigten eine bessere photokatalytische Aktivität unter sichtbarem Licht und eine höhere als reines Ag3 PO4 QDs allein. Dies lag an der effizienten e − -h + Paartrennung und schneller Elektronentransfer in diesen Heteroübergängen. Die rGO-Blätter förderten effektiv die Trennung von e − und h + und schneller Elektronentransfer in den Heterostruktur-Photokatalysatoren. Experimente zum Einfangen freier Radikale zeigten, dass h + spielten eine wichtige Rolle beim photokatalytischen Abbau von Farbstoffen. Es war klar, dass die ultraschallunterstützte Methode ein einfacher und wirtschaftlicher Weg war, um auf sichtbares Licht reagierendes und hocheffizientes Ag3 . herzustellen PO4 QDs-basierte Verbundwerkstoffe.
Abkürzungen
- 2D:
-
Zweidimensional
- BQ:
-
p-Benzochinon
- CB:
-
Leitungsband
- Lebenslauf:
-
Chemische Gasphasenabscheidung
- EDTA:
-
Dinatriumethylendiamintetraacetat
- GO:
-
Graphenoxid
- IPA:
-
Isopropanol
- MB:
-
Methylenblau
- MO:
-
Methylorange
- QDs:
-
Quantenpunkte
- R-1.5, R-2, R-2.3, R-2.5 und R-3:
-
rGO-Gehalt in Verbundwerkstoffen 1,5, 2,0, 2,3, 2,5 und 3,0 Gew.-%
- rGO:
-
Graphen
- RhB:
-
Rhodamin B
- WKomposit :
-
Gewicht von Verbundwerkstoffen
- WrGO :
-
Gewicht von Graphem
Nanomaterialien
- Einfache Synthese und optische Eigenschaften kleiner Selen-Nanokristalle und -Nanostäbe
- S, N codotierte Graphen-Quantenpunkt/TiO2-Komposite für eine effiziente photokatalytische Wasserstofferzeugung
- Graphen- und Polymerverbundstoffe für Superkondensatoranwendungen:ein Rückblick
- Synthese von Pyridin-reichen N,S-codotierten Kohlenstoff-Quantenpunkten als wirksame Enzymnachahmer
- Einstufige Elektrospinnroute von SrTiO3-modifizierten Rutil-TiO2-Nanofasern und ihre photokatalytischen Eigenschaften
- Synthese wasserlöslicher Antimonsulfid-Quantenpunkte und ihre photoelektrischen Eigenschaften
- Einfache Synthese von Wurmloch-ähnlichem mesoporösem Zinnoxid durch verdunstungsinduzierte Selbstorganisation und die verbesserten Gassensoreigenschaften
- Eintopfsynthese von Cu2ZnSnSe4-Nanoplatten und ihre durch sichtbares Licht getriebene photokatalytische Aktivität
- Umweltfreundliche und einfache Synthese von Co3O4-Nanodrähten und ihre vielversprechende Anwendung mit Graphen in Lithium-Ionen-Batterien
- Einstufige Kugelmahlvorbereitung von nanoskaligem CL-20/Graphenoxid für deutlich reduzierte Partikelgröße und Empfindlichkeit



