Einfache In-situ-Herstellung und antibakterielle In-vitro-Wirkung von silberhaltigen Copolymer-Mizellen auf PDMAEMA-Basis
Zusammenfassung
Gut definierte Polymermizellen mit Kern-Schale-Struktur sind eine gute Transportplattform zur Stabilisierung von Silbernanopartikeln (AgNPs) im Bereich antimikrobieller Wirkstoffe gegen Krankheiten. Der rationale Aufbau der Polymerstruktur, ein effizienter, einfacher und grüner Herstellungsansatz und eine umfassende Untersuchung der abgeleiteten AgNPs sind erforderlich, wie Größe, Partikelstabilität, antibakterielle Aktivität und andere Eigenschaften. Hier haben wir die antimikrobielle In-vitro-Aktivität von AgNPs-dekorierten Copolymermizellen mit unterschiedlichen Copolymertopologien entworfen und bewertet. Zunächst wurden lineare oder vierarmige Stern-Triblockcopolymere mit ähnlichem Molekulargewicht und Polymerisationsgrad erhalten, die aus DMAEMA zur in-situ-Reduktion von Silberionen zu AgNPs ohne externes Reduktionsmittel bestanden. HEMA und PEGMA in einer mizellaren Hülle ergaben eine verbesserte Stabilität von AgNPs während der Blutzirkulation. Die Kombination von Computermodellen und experimentellen Ergebnissen zeigte, dass beide Micellentypen AgNPs mit monodisperser und sphärischer Morphologie herstellen können. Mit Sterncopolymermizellen stabilisierte AgNPs hatten eine geringere durchschnittliche Größe, bessere Stabilität und eine höhere antibakterielle Aktivität als solche mit linearer Struktur, was möglicherweise auf die höhere Stabilität der Micellen aus Sterncopolymeren zurückzuführen ist. Darüber hinaus zeigte der Zytotoxizitäts-Bewertungstest, dass die erhaltenen linearen oder sternförmigen Copolymer-Micellen-stabilisierten AgNPs eine gute Biokompatibilität aufwiesen. Diese Arbeit bietet einen einfachen und universellen Ansatz für das rationale Design von Micellen-stabilisierten AgNPs mit geeigneter Topologie zur Bekämpfung einer Vielzahl bakterieller Infektionen.
Einführung
In den letzten Jahrzehnten wurde eine Reihe traditioneller antimikrobieller Mittel in großem Umfang zur Behandlung von Infektionskrankheiten eingesetzt. Nach Angaben der Weltgesundheitsorganisation (WHO) ist das schnelle Auftreten multiresistenter Mikroorganismen zu einem immer ernsteren globalen Problem geworden, das in der Liste der größten Bedrohungen für die menschliche Gesundheit unter den Top 3 rangiert [1, 2, 3, 4, 5]. Daher ist es notwendig, neue antimikrobielle Mittel mit guter Sicherheit und wirksamer antibakterieller Fähigkeit zu entwickeln, ohne Bakterienresistenz zu erzeugen. Silbernanopartikel (AgNPs) als eines der besten antimikrobiellen Wirkstoffe seit der Antike wurden aufgrund ihrer überlegenen Leistung gegen verschiedene bakterielle und pilzliche Krankheitserreger, ihrer relativ geringen Toxizität für Säugerzellen und ihrer begrenzten bakteriellen Resistenz in Konsumgütern häufig verwendet [6,7, 8,9,10]. AgNPs sind in der Lage, die Membranpermeabilität von Bakterien zu verbessern, in das Zytoplasma einzudringen, bakterielle Proteine zu denaturieren und die Replikation von Bakterien zu stören, was zum Absterben von Bakterien führt [11,12,13]. Eine große Zahl von Silberformulierungen wurde verwendet, um die antibakterielle Aktivität von AgNPs aufzuklären [14,15,16,17], zum Beispiel ein Wundverband durch ein zwitterionisches Polycarboxybetain-Hydrogel zusammen mit antibakteriellen AgNPs als Kernkomponente, vorgeschlagen von Zhang et al.. [18], die von Moreno-Couranjou et al. vorgeschlagenen multifunktionalen Oberflächen durch Mehrkomponentenbeschichtung zur Co-Immobilisierung von AgNPs usw. [19].
Die große spezifische Oberfläche und die hohe Oberflächenenergie führten jedoch zur Aggregation von AgNPs, die zu einem großen Flaschenhals für ihre Anwendung geworden ist. Daher wird eine Polymermatrix oder ein externer Stabilisator benötigt, um die AgNPs zu stabilisieren. Polymermatrix ist bekanntlich die gebräuchlichste Methode, um das Aggregationsproblem zu lösen. Gegenwärtig wurden verschiedene Methoden verwendet, um AgNPs mit Polymermatrix zu stabilisieren, wie die chemische Reduktionsmethode, die elektrochemische Methode, die photochemische Methode und die Mikrowellenmethode. Unter diesen ist die chemische Reduktion eine übliche und wirksame Methode. Silbernitrat wird durch Zugabe von Reduktionsmitteln wie Hydrazinhydrat (N2 H4 ), Natriumborhydrid (NaBH4 ), Natriumcitrat und Ascorbinsäure in Lösung [20,21,22,23]. Hoda et al. hergestellte Polystyrol-Block-Polyacrylsäure (PS-b -PAA) Reverse Micellen, beladen mit den 20 nm AgNPs unter dem Einfluss des Reduktionsmittels N2 H4 , und die PS-Blöcke spielten die äußere Schicht in Toluol [24]. Lius Gruppe berichtete, dass selbstorganisierte Micellen-Nanotemplaten aus Poly(ε-caprolacton)-block-poly (Asparaginsäure) (PCL-b) hergestellt wurden -PAsp). Gut dispergierte AgNPs wurden mit AgNO3 . hergestellt als Vorläufer und NaBH4 als Reduzierstück [25]. Die oben genannten Methoden waren jedoch nicht umweltfreundlich, und die Zugabe übermäßiger Reduktionsmittel erzeugte Nebenprodukte, die die Reinigung von AgNPs erschwerten und ihre Anwendung von antimikrobiellen Mitteln gegen Infektionskrankheiten einschränkten.
Inzwischen wurde berichtet, dass Polymere mit Amingruppen sowohl als Reduktionsmittel als auch als Stabilisator verwendet werden könnten, um AgNPs in situ herzustellen. Lang et al. synthetisierten sechsarmige Sternpolymere bestehend aus PCL, 2-(Dimethylamino)ethylmethacrylat (DMAEMA) und Poly(ethylenglycol)methylethermethacrylat (PEGMA). Das System reduzierte Silbernitrat direkt zu AgNPs, ohne ein weiteres Reduktionsmittel in wässriger Phase zuzugeben [26]. Obwohl die oben erwähnten AgNPs eine leichte Oberflächenmodifizierung ohne zusätzlichen Reduktionsmittel zeigen, ist der Einfluss von Polymertopologien auf die Reduktion und Stabilität von Silbernanopartikeln zusammen mit ihrer Anwendung in der mizellenbasierten antibakteriellen Aktivität im Vergleich zu den Goldnanopartikeln [27, 28] geringer studiert.
In dieser Arbeit wurde ein milder, einfacher und grüner Ansatz entwickelt, um bakterielle Infektionen zu bekämpfen, wobei polymere Micellen genutzt werden, die sich aus linearen oder vierarmigen Stern-Triblock-Copolymeren mit ähnlichem Molekulargewicht und Polymerisationsgrad wie die Nanoplattform selbstorganisieren um AgNPs zu dekorieren (Schema 1). Bei diesem Ansatz konnten die Triblockcopolymere, bestehend aus DMAEMA, 2-Hydroxyethylmethacrylat (HEMA) und PEGMA, selbstorganisierte Micellen in wässrigem Zustand erzeugen, was ein gutes Templat für die Herstellung und Stabilisierung von AgNPs ist. Die PDMAEMA-Blöcke mit tertiären Amingruppen könnten leicht das Ag + . absorbieren Ionen durch Koordinationswechselwirkung und erzeugen dann in situ AgNPs ohne Reduktionsmittel. HEMA- und PEGMA-Blöcke mit hoher Hydrophilie könnten als Stabilisatoren in der Wasserphase verwendet werden, um die Stabilität von AgNPs weiter zu verbessern. Daher könnte Silbernitrat spontan an den Kern von selbstorganisierten Copolymermizellen koordinieren und desoxidieren, um AgNPs zu bilden. Sie waren in einen micellaren Kern eingebettet und könnten zur Zerstörung der Bakterienmembran führen. Hier wurde umfassend untersucht, wie lineare oder vierarmige Sterncopolymertopologien die maximale Absorptionswellenlänge, Morphologie, Partikelgröße, Zetapotential, Stabilität sowie die antibakterielle Wirksamkeit von AgNPs beeinflussen. Daher kann die Studie über die Beziehung zwischen Struktur und Eigenschaften eine eingehende Erklärung von Silber-Hybrid-Nanopartikeln zur Behandlung bakterieller Infektionen liefern. Darüber hinaus würde es Designideen und technische Grundlagen für die Herstellung von AgNPs mit stabilerer Struktur und kontrollierbarer Partikelgröße liefern.
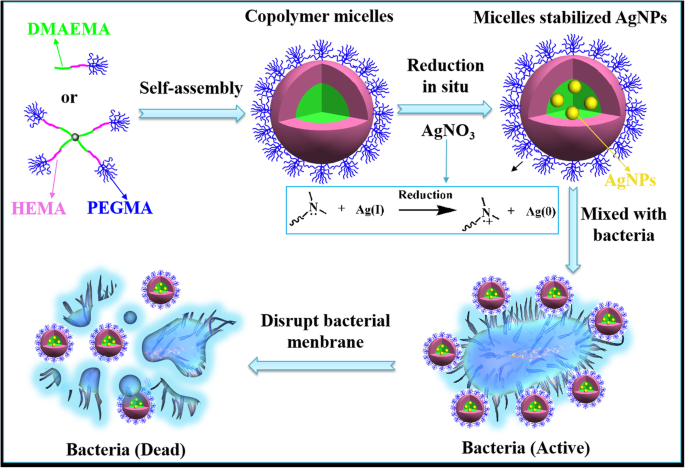
Schematische Darstellung der Bildung von linearen/Stern-Copolymeren Micellen stabilisierten AgNPs für ausgezeichnete antibakterielle Aktivität
Material und Methoden
Materialien
Pentaerythrit (J&K Scientific Ltd.) wurde vor der Verwendung 24 h bei reduziertem Druck getrocknet. 2-(Dimethylamino)ethylmethacrylat (DMAEMA,> 98%), 2-Hydroxyethylmethacrylat (HEMA, 99%) und Poly(ethylenglycol)methylethermethacrylat (PEGMA, M n =300 Da, 99%, alle von Aldrich, wurden durch Passieren durch eine neutrale Aluminiumoxid enthaltende Säule gereinigt, um den Inhibitor zu entfernen. Durch die Verwendung von Calciumhydrid (CaH2 ), Tetrahydrofuran (THF) und Toluol von Aldrich wurden getrocknet und dann vor der Verwendung im Vakuum destilliert. Ethyl-2-bromisobutyrat (EBiB, 98%, Alfa Aesar), 2-Bromisobutyrylbromid (BIBB, 98%, Alfa Aesar), 1,1,4,7,10,10-Hexamethyltriethylentetramin (HMTETA, 99%), Silbernitrat (AgNO3 , 99,9%), Kupfer(II)-bromid (CuBr2 .) ), Methanol, Triethylamin (TEA), Dichlormethan (DCM), Aceton, n -Hexan, Dimethylsulfoxid (DMSO), Zinnoctoat (Sn(Oct)2 ), Natriumcarbonat (Na2 CO3 ), Natriumbicarbonat (NaHCO3 ), Natriumchlorid (NaCl), Natriumsulfat (Na2 SO4 ) und alle anderen Reagenzien von J&K Chemical Company wurde wie erhalten verwendet.
Allgemeine Charakterisierung und Instrumentierung
Protonenkernmagnetische Resonanz ( 1 H-NMR)-Spektren der linearen oder vierarmigen Triblockcopolymere wurden in CDCl3 . nachgewiesen , und D2 O bei 25 °C durch ein Bruker ADVANCE 400 MHz Spektrometer (Madison, WI, USA). Fourier-Transform-Infrarotspektroskopie (FTIR)-Spektrenmessungen von linearen Copolymeren, Sterncopolymeren und ihren Micellen-stabilisierten AgNPs wurden mit einem FT-IR-Spektrophotometer (Nicolet Nexus für Euro, USA) mit einem Transmissionsmodus bei 25 °C durchgeführt. Granulare Proben wurden hergestellt, nachdem sie mit Kaliumbromid (KBr) gemahlen und dann komprimiert worden waren. Um ein Spektrum zu erhalten, wurden die Spektralbedingungen zuvor mit Wellenlängen von 4000 bis 400 cm −1 . eingestellt (32 Scans) und einer Auflösung von 8 cm −1 . Die Zeta-Potentiale von linearen und sternförmigen Copolymer-Micellen-stabilisierten AgNPs bei verschiedenen Molverhältnissen wurden mittels elektrophoretischer Messung mit dem Malvern Zetasizer Nano S-Instrument (Malvern, WR, UK) gemessen, wobei jede Probe dreimal bei 25 °C getestet wurde. Transmissionselektronenmikroskopie (TEM, FEI Tecnai-G20) bei 200 kV wurde durchgeführt, um die Morphologien von linearen und sternförmigen Copolymermizellen stabilisierten AgNPs bei verschiedenen Molverhältnissen zu beobachten. Der Herstellungsprozess des Produktes für TEM war wie folgt:10 µL Probelösung wurden zuerst auf ein mit Kohlenstoff beschichtetes Kupfergitter getropft und dann an der Luft getrocknet. UV-Vis-Spektren von linearen und sternförmigen Copolymermizellen stabilisierten AgNPs bei verschiedenen Molverhältnissen wurden unter Verwendung eines UV-Vis-Spektrophotometers (UV-2450, Shimadzu, Kyoto, Japan) bestimmt. Die thermogravimetrische Analyse (TGA) wurde auf einem NETZSCH (STA409PC, Deutschland)-Gerät durchgeführt. Alle getrockneten Pulverproben (lineare Copolymere, Sterncopolymere und ihre Micellen-stabilisierten AgNPs) wurden unter Stickstoffbedingungen mit einer Geschwindigkeit von 10 °C /min von 25 auf 600 °C erhitzt.
Synthese von PDMAEMA-b -PHEMA-b -PPEGMA
Die kontinuierlichen Aktivatoren, die durch radikalische Elektronentransfer-Atomtransfer-Polymerisation (AGERT ATRP) von DMAEMA, HEMA und PEGMA regeneriert wurden, wurden nach dem von Zhang et al. modifizierten Verfahren durchgeführt. [29, 30]. Kurz gesagt, nach der Zugabe von CuBr2 (10 mg, 0,045 mmol) wurde der 100 ml trockene Dreihalskolben evakuiert und dreimal mit Argon gespült. Mit Hilfe einer entgasten Spritze wurden wasserfreies Toluol (25 ml), EBiB (88 μl, 0,24 mmol), DMAEMA (5,15 ml, 30,5 mmol) und Ligand HMTETA (62 μl, 0,24 mmol) geordnet in den Behälter injiziert 10 Minuten Rühren. Nach der Injektion von Sn(Oct)2 (78 μL, 0.24 mmol) mit Toluol (2 mL) als Lösung wurde die Reaktion 8 h bei 70 °C im Ölbad durchgeführt. Der nachfolgende Block HEMA (2,32 ml, 18,4 mmol) wurde für die nächste 8-stündige Reaktion injiziert, nachdem die Lösung viel dicker wurde. Schließlich beobachteten wir unter Beteiligung des dritten Monomers PEGMA (8.89 g, 55.6 mmol) eine 72-stündige kontinuierliche Reaktion, bevor der Kolben auf fast Raumtemperatur abgekühlt wurde. THF (30 ml) wurde in den Behälter eingespritzt und die Reaktionsmischung wurde dann durch eine neutrale Aluminiumoxidsäule geleitet, um den Katalysator zu entfernen. Das Produkt PDMAEMA-b -PHEMA-b -PPEGMA wurde in einem zehnfachen Überschuss an kaltem n . ausgefällt -Hexan, filtriert und schließlich 48 h bei 35 °C unter Vakuum getrocknet.
Synthese von (PDMAEMA-b -PHEMA-b -PPEGMA)4
Sternförmiger bromterminierter Initiator (Br)4 wurde durch die Veresterung der endständigen Hydroxylgruppen des Pentaerythrits mit 2-Bromisobutyrylbromid unter Verwendung von THF als Lösungsmittel und TEA als Säurebindemittel synthetisiert. Typischerweise wurde der 100-ml-Dreihalskolben nach dem Befüllen mit Pentaerythrit (2,72 g, 2 mmol) evakuiert und dreimal mit Argon gespült, gefolgt von aufeinanderfolgender tropfenweiser Injektion von wasserfreiem THF (120 ml) und TEA (12,51 ml, 90 mmol) . Unter Eis/Wasser-Umständen wurde 2-Bromisobutyrylbromid (11,12 ml, 90 mmol) tropfenweise in die stark gerührte Lösung nach einer 4-stündigen Reaktion bei 0°C und dann 20 Stunden bei 25°C injiziert. Um das Produkt zu reinigen, wurde das Gemisch zunächst durch eine neutrale Aluminiumoxidsäule geleitet. Das Rohprodukt wurde nacheinander mit Wasser, 10 % Na2 . gewaschen CO3 , gesättigtes NaHCO3 , und gesättigtes NaCl, dann nacheinander durch Na2 . getrocknet SO4 über Nacht, filtriert und konzentriert, bevor es in den zehnfachen Überschuss an kaltem n . gegossen wird -Hexan, um das Produkt auszufällen, und schließlich 24 h unter Vakuum getrocknet, um das Produkt zu erhalten.
Die Synthesewege und Fütterungsmengen von (PDMAEMA-b -PHEMA-b -PPEGMA)4 wurde nach dem gleichen Verfahren wie PDMAEMA-b . durchgeführt -PHEMA-b -PPEGMA.
Herstellung von AgNPs mit linearen oder sternförmigen Copolymer-Mizellen
Das PDMAEMA-b -PHEMA-b -PPEGMA oder (PDMAEMA-b -PHEMA-b -PPEGMA)4 zunächst eine wässrige Lösung (pH 7,0) erhalten, zu der das AgNO3 Lösung wurde zugegeben, während die Reduktionsreaktion von DMAEMA mit Ag + . ausgelöst wurde um AgNPs in situ im micellaren Kern zu bilden. Bestimmung des Molverhältnisses von DMAEMA und AgNO3 gleich 9 als Beispiel, erstens PDMAEMA-b -PHEMA-b -PPEGMA oder (PDMAEMA-b -PHEMA-b -PPEGMA)4 mit der gleichen Menge an [DMAEMA] =4,8 mM in Aceton (5 ml) für 4 h gerührt, gefolgt von der Zugabe von destilliertem Wasser (20 ml) unter Rühren über Nacht, um stabile Micellen zu bilden. Dann AgNO3 Lösung (220 &mgr;l, 48 mM) wurde tropfenweise in die obige Lösung injiziert und bei 25°C im Dunkeln für 48 h gerührt. Schließlich wurden die mit linearen oder sternförmigen polymeren Micellen stabilisierten AgNPs durch Sammeln und Gefriertrocknen hergestellt, bevor sie für die folgenden Experimente bei − 20 °C gelagert wurden.
Antibakterieller Assay
Die antibakteriellen Untersuchungen an polymermizellenstabilisierten AgNPs wurden gegen Escherichia coli . durchgeführt DH5alpha (E . Coli DH5α)-Stämme unter Verwendung von Luria-Bertani (LB)-Medium als Träger, um verschiedene Konzentrationen der Polymermizellen-stabilisierten AgNPs-Lösungen durch Ultraschall herzustellen. Das monoklonale E . Coli DH5α wurden über Nacht in LB-Medium (5 ml) bei 37 °C auf einem Schüttler bei 200 U/min kultiviert, bevor die Bakteriensuspension auf 1 × 10 5 . verdünnt wurde KBE/ml pro LB-Medium. Nach Mischen eines gleichen Volumens verdünnter Bakterien mit unterschiedlichen Konzentrationen von Copolymermizellen oder Micellen-stabilisierten AgNPs und Inkubation bei 37 °C für 16 h wurde die Änderung der optischen Dichte bei der Wellenlänge von 600 nm mit einem Mikroplatten-Lesegerät (Multiskan Spectrum, Thermo Scientific, Vantaa, Finnland). Jeder Assay wurde sechsmal wiederholt.
Zelllebensfähigkeitsbewertung
Um die Lebensfähigkeit der Zellen zu bewerten, wurde der 3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazoliumbromid (MTT)-Assay mit Leber-Hepatozellulären Karzinomzellen (HepG2) durchgeführt. Vor der Zellaussaat wurden HepG2-Zellen zuerst in einer befeuchteten Atmosphäre von 5 % CO2 . inkubiert bei 37 °C in Dulbeccos modifiziertem Eagle-Medium (DMEM), ergänzt mit 10 % fötalem Rinderserum (FBS), Penicillin (100 μl/ml) und Streptomycin (0,1 mg/ml). Dann wurden HepG2-Zellen in einem frischen DMEM-Medium auf einer 96-Well-Platte mit einer Dichte von 1 × 10 4 . ausgesät pro Vertiefung und 1 Tag kultiviert. Nach Austausch des DMEM-Mediums in vorgefertigten Copolymermizellen oder Micellen-stabilisierten AgNPs-Lösungen (100 &mgr;l) in verschiedenen Konzentrationen wurden die Zellen für die nächsten 24 Stunden weiter kultiviert. Nach dreimaligem Waschen mit PBS-Puffer wurden 20 µl MTT-Reagenz (5 mg/ml) und 180 µl frisches DMEM zugegeben und weitere 4 h inkubiert. Schließlich wurde die Lösung in 200 µL DMSO gewechselt und die Platte 10 min leicht geschüttelt. Die Extinktion bei 570 nm wurde mit dem oben erwähnten Mikroplatten-Lesegerät gemessen. Die Daten von sechs parallelen Experimenten wurden gemittelt.
Dissipative Partikeldynamiksimulation
Um den Wachstumsprozess von AgNPs zu analysieren, wurde eine auf den grobkörnigen Modellen basierende dissipative Particle Dynamics (DPD)-Simulation mit dem Mesozit-Modul von Materials Studio 8.0 (Accelrys Inc., San Diego, CA, VEREINIGTE STAATEN VON AMERIKA). Wie in Zusatzdatei 1:Abbildung S1 gezeigt, bildeten sechs Arten von Kügelchen die Copolymere PDMAEMA-b -PHEMA-b -PPEGMA oder (PDMAEMA-b -PHEMA-b -PPEGMA)4 :Orange steht für das Zentrum, hellgrün für MAA1 (Methacrylat neben der Ethylamin-Seitenkette), grün für DMA (Aminoethyl-Seitenkette), pink für HEMA, hellblau für MAA2 (Methacrylat neben der PEG-Seitenkette) und blau für ANBINDUNG. Ein kleiner Cluster mit Elementarzellenkristall (Gitterlänge:3.87 ) bestand aus vier Silberatomen, markiert als Silberperle (goldene Farbe). Gleichzeitig enthielt jede Wasserperle (W) in schwarzer Farbe fünf Wassermoleküle. Gemäß unserer früheren Arbeit zeigt Zusatzdatei 1:Tabelle S1 das Ergebnis der rechnerischen Interaktionsparameter [31, 32]. A 30 × 30 × 30 r c 3 kubische Simulationsbox mit periodischen Randbedingungen wurde in alle Richtungen mit 100.000 Gesamtsimulationsschritten und 0,05 ns Integrationszeitschritt verwendet.
Statistische Analyse
Die statistische Analyse wurde unter Verwendung eines t .-Studenten-t . von zwei Stichproben durchgeführt Test mit ungleicher Varianz. p <0,05 wurde als statistisch signifikant angesehen.
Ergebnisse und Diskussion
Synthese und Charakterisierung von linearen/Stern-Copolymeren
Lineare Copolymere PDMAEMA-b -PHEMA-b -PPEGMA und Sterncopolymere (PDMAEMA-b .) -PHEMA-b -PPEGMA)4 wurden durch ARGET ATRP-Polymerisation von DMAEMA, HEMA und PEGMA mit CuBr2 . synthetisiert /HMTETA als Katalysator, Sn(Oct)2 als Reduktionsmittel und EBiB oder Pentaerythrit, das zuvor mit BIBB als Initiator in Toluol acyliert wurde (Schema 2). Die Struktur und Zusammensetzung der Zielpolymere wurden von 1 . bestätigt H-NMR. Polymermicellen wurden aus PDMAEMA-b . selbstorganisiert -PHEMA-b -PPEGMA oder (PDMAEMA-b -PHEMA-b -PPEGMA)4 mit dem DMAEMA als Funktionsblock, wobei das Ag + Ionen wurden angezogen und ohne zusätzliche Reduktionsmittel zu AgNPs reduziert. Die Auswirkungen topologischer Strukturen von Copolymeren auf AgNPs wurden diskutiert und anhand der physikalisch-chemischen Eigenschaften, antibakteriellen und krebsbekämpfenden Aktivitäten bewertet.
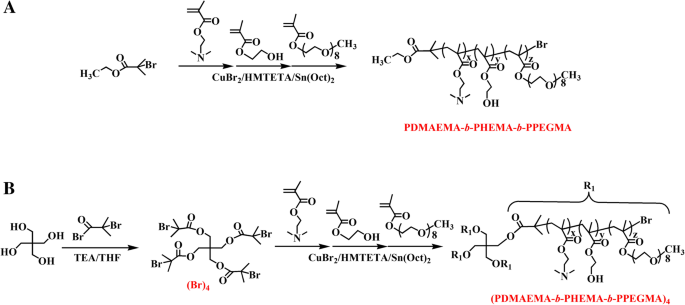
Synthesewege von a PDMAEMA-b -PHEMA-b -PPEGMA und b (PDMAEMA-b -PHEMA-b -PPEGMA)4
Die chemischen Strukturen von linearen/Stern-Copolymeren wurden durch 1 . bestätigt H-NMR. Zuerst wurden die endständigen Hydroxylgruppen von Pentaerythrit vollständig auf die endständige Bromgruppe (Br)4 . übertragen , wie in 1 . gezeigt H-NMR-Spektrum (Zusatzdatei 1:Abbildung S2). Der Peak bei 4,33 ppm wurde dem -CH . zugeschrieben 2 O- in Pentaerythrit, während das neue -(CH 3 )2 - Signal bei 1,94 ppm erschien. Und die Integrationsverhältniswerte der Peaks bei 1,94 ppm bis 4,33 ppm lagen bei etwa 3. Wie in Zusatzdatei 1:Abbildung S3 und S4 gezeigt, ist der Peak von -C(CH 3 )2 - erschien bei 1,94 ppm. Die Signale bei 1,83 ppm, 1,00 ppm wurden -CH . zugeordnet 2 - und -CCH 3 - jeweils in den Hauptketten von Methylmethacrylat. Die Peaks bei 2,58 ppm und 4,08 ppm gehörten zu den charakteristischen Resonanzen der koterminierten beiden Methylenprotonen -CH 2 CH 2 - im DMAEMA-Block, und der Peak bei 2,29 ppm wurde Methylprotonen -CH . zugeordnet 3 -, das an eine tertiäre Amingruppe gebunden war. Das Vorhandensein von -CH 2 CH 2 - Methylenprotonen, die mit der endständigen Hydroxylgruppe in der HEMA-Einheit verbunden waren, erschienen bei 4,08 ppm bzw. 3,57 ppm. Die charakteristischen PEG-Peaks von -OCH 2 CH 2 - und Terminal -CH 3 Protonen erschienen bei 3,67 bzw. 3,39 ppm. Doppelbindungspeaks bei 5,5–6,1 ppm verschwanden im 1 H-NMR-Spektren. Berechnet aus den Integrationsverhältniswerten von Signal (f) zu (a) (I f /Ich a ), Signal (g) zu (a) (I g /Ich a ) und signalisieren (h) an (a) (I h /Ich a ) bzw. PDMAEMA19.3 -b -PHEMA12.5 -b -PPEGMA24.6 und (PDMAEMA5.0 -b -PHEMA5.6 -b -PPEGMA5.0 )4 wurden erhalten.
Herstellung und Charakterisierung der mit Linear/Stern-Copolymer-Mizellen stabilisierten AgNPs
Der Bildungsprozess von AgNPs ist in Schema 1 gezeigt. Ein einsames Elektronenpaar am N-Atom, das zur tertiären Amingruppe in der PDMAEMA-Molekülkette gehört und die Fähigkeit zur Koordination und Reduktion besitzt, kann daher sowohl als Abfangreagens verwendet werden und ein Reduktionsmittel. Zuerst wurden Silberionen von PDMAEMA aufgrund der Komplexierung zwischen Ag + . eingefangen und N-Atom bilden (Ag + )-PDMAEMA-Komplex. Anschließend Ag + wurden in situ reduziert, um im Keimbildungsstadium Silberatome zu bilden. Danach setzte sich die Nukleation von Ag mit dem Wachstum des Ag-Kristalls fort, was zur Bildung von AgNPs führte [26]. Der hydrophile Block PPEGMA fungierte als mizellare Hülle, die eine stabile Schutzschicht bildete und die Stabilität der AgNPs weiter verbesserte. Der sterische Stabilisierungseffekt selbstorganisierter Micellen innerhalb des Systems wurde durch das thermodynamische Gleichgewicht der Micellen auf die Stabilisierung von AgNPs und die Agglomeration zwischen AgNPs bestimmt. Im Fall einer geringen Menge an AgNPs könnte die sterische Stabilisierung des Copolymers eine weitere Aggregation der AgNPs verhindern. Mit steigender Ag-Zahl würde die Stabilität der Micellen gegenüber den AgNPs geschwächt und dann würde die Möglichkeit von Kollisionen zwischen Partikeln steigen, was zu einem Größenwachstum der AgNPs führen würde. Die von uns hergestellten AgNPs nutzen die räumliche Stabilisierung von Micellen und haben eine kontrollierte Partikelgröße, die ein großes Potenzial für antibakterielle Anwendungen bietet.
Es wurde eine DPD-Simulation durchgeführt, um den Wachstumsprozess und die Verteilung von AgNPs zu untersuchen, mit den gleichen Konzentrationen des tatsächlichen Experiments (PDMAEMA/AgNO3 Molverhältnis =1/1, wobei die Volumenanteile der linearen Copolymere, Ag- und Wasserperlen jeweils 10 %, 0,23 % und 89,77 % betragen). Abbildung 1 zeigt, dass die Perlen von PDMAEMA-b -PHEMA-b -PPEGMA und AgNPs zeigten zunächst einen unregelmäßig verteilten Zustand in wässriger Lösung. Im Laufe der Zeit wurden schließlich acht selbstorganisierte Copolymermizellen gebildet und gleichmäßig dispergiert, während alle Ag-Kügelchen in die Mizellen geladen wurden. Es zeigte sich, dass AgNPs im Gleichgewicht in den Copolymermizellen ohne weitere Aggregation stabilisiert werden konnten, was darauf hindeutet, dass die selbstorganisierten Micellen die weitere Aggregation von AgNPs verhindern konnten und dann den Zweck erfüllten, ihre Partikelgröße und -verteilung zu kontrollieren.
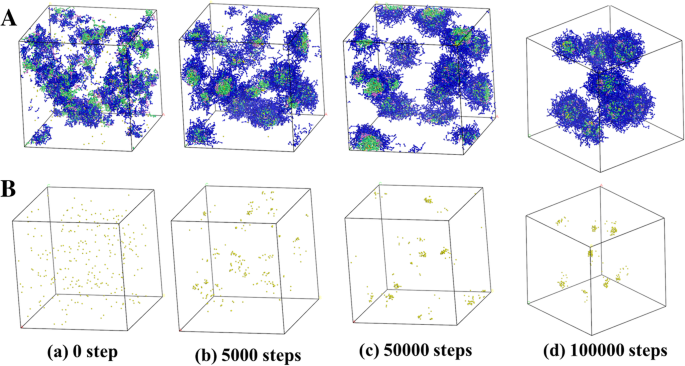
DPD-Simulation des Wachstumsprozesses und der Verteilung von AgNPs mit PDMAEMA-b -PHEMA-b -PPEGMA bei PDMAEMA/AgNO3 Molverhältnis =1/1 in unterschiedlicher Simulationszeit. a Die Wassermoleküle wurden aus Gründen der Übersichtlichkeit versteckt. b Es wurden nur die AgNPs gezeigt
Die FT-IR-Charakterisierung von linearen/Stern-Copolymeren und ihren Micellen-stabilisierten AgNPs wurde in Zusätzliche Datei 1 gezeigt:Abbildung S5. Offensichtlich ist die -COOR-Streckschwingung bei 1730 cm −1 . im Vergleich zu einfachen linearen/Stern-Copolymeren und die Biegeschwingung der C-N-Bindung in PDMAEMA bei 1457 cm −1 nach der AgNPs-Bildung verringert, was darauf hindeutet, dass die AgNPs erfolgreich auf Copolymermicellen geladen wurden. Die kristalline Natur von mit linearen/Stern-Copolymeren Micellen stabilisierten AgNPs wurde durch Röntgenbeugungsspektrum bestätigt (zusätzliche Datei 1:Abbildung S6). Die Beugungspeakwerte von 38,5°, 44,8°, 64,2° und 78,0° entsprachen den (111), (200), (220) und (311) Kristallflächen der kubisch-flächenzentrierten (fcc) Kristallstruktur von Ag-haltigen Nanopartikeln [33, 34]. Die Zeta-Potentiale von linearen/Stern-Copolymer-Micellen-stabilisierten AgNPs wurden gemessen. Wie in Abb. 2 gezeigt, lagen die Zeta-Potentiale dieser Copolymer-Micellen-stabilisierten AgNPs bei etwa 15.0–23.2 mV. Mit steigender AgNO3 .-Menge , das Zeta-Potenzial von Micellen-stabilisierten AgNPs aufgrund der Dekoration von mehr AgNPs bemerkenswert erhöht. Um die Dispersion von AgNPs und die stabilisierende Wirkung von Micellen auf AgNPs weiter zu untersuchen, wurden DPD-Simulationen von linearen/Stern-Copolymer-Micellen stabilisierten AgNPs bei verschiedenen PDMAEMA/AgNO3 Molverhältnisse wurden durchgeführt. Wie in Abb. 2 gezeigt, zeigten die Ergebnisse auch, dass die Größe der AgNPs proportional zu den Verhältnissen war, in denen die Anzahl der aggregierten kleinen AgNPs zunahm und der Abstand zwischen ihnen abnahm, was zu einer erhöhten Kollisions- und Agglomerationswahrscheinlichkeit führte.
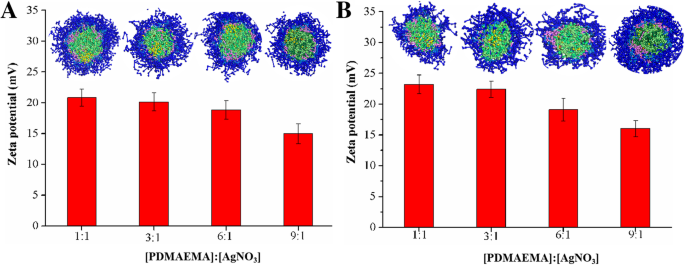
Die Zetapotentiale und die Querschnittsansichten von a linear und b Sterncopolymere Micellen stabilisierte AgNPs. Die Daten wurden mit verschiedenen PDMAEMA/AgNO3 . erhoben Molverhältnisse von (a) 1/1, (b) 3/1, (c) 6/1, (d) 9/1
Die Spektren für vier lineare Copolymer-Micellen-stabilisierte AgNPs zeigten einen geringfügigen Unterschied beim maximalen Absorptionspeak bei etwa 437 nm, der charakteristische Oberflächenplasmonenresonanz-(SPR)-Absorptionspeak von sphärischen/nahesphärischen AgNPs war, bezogen auf die Resonanzanregung und den Interband-Übergang von sie (Abb. 3a). Das Ergebnis zeigte, dass die tertiäre Amingruppe in den linearen Copolymeren mit Silbernitrat reagieren konnte und die Bildung von AgNPs kaum von der sterischen Hinderung der Micellen des linearen Copolymers abhing. Bei Sterncopolymeren mit ähnlichem Block- und Polymerisationsgrad unter den gleichen Bedingungen nahm die Partikelgröße der AgNPs ab, wenn PDMAEMA/AgNO3 Molverhältnis erhöht. Dies spiegelte sich in der hypsochromen Verschiebung in den UV-Vis-Spektren wider, wo die maximalen Absorptionspeaks bei 429 nm, 426 nm, 421 nm bzw. 414 nm lagen, aufgrund der unterschiedlichen Menge an AgNPs, die durch die Koordinationsreduktion am tertiären Amin gebildet wurden von Sterncopolymer-Mizellen (Abb. 3b). Mit anderen Worten, die sterische Stabilisierung der Sterncopolymere könnte die AgNPs besser stabilisieren und ihre weitere Aggregation bei geringen AgNP-Mengen verhindern. Im Gegensatz dazu schwächte die Zunahme der AgNPs den stabilisierenden Effekt, was mehr Möglichkeiten für die Kollision von AgNPs bot und schließlich zu größeren AgNPs führte. Vergleicht man Fig. 3a mit Fig. 3b, so zeigten die Absorptionspeaks bei 437 nm von AgNPs in linearen Copolymermizellen eine breitere Wellenlängenverteilung, während AgNPs in Sterncopolymermizellen bei etwa 422 nm lagen. Hier zeigte sich keine Blauverschiebung in den Spektren der linearen Copolymere, was dadurch erklärt werden könnte, dass die Blöcke der linearen Copolymer-Micellen einen schwächeren Einfluss auf die sterische Hinderung für AgNPs haben, was zu einer erhöhten Wahrscheinlichkeit einer Kollisionsagglomeration zwischen AgNPs.
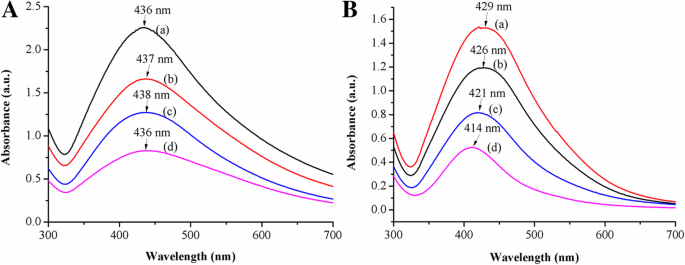
UV-Vis-Spektren von a linear und b Sterncopolymere Micellen stabilisierte AgNPs bei verschiedenen PDMAEMA/AgNO3 Molverhältnisse von (a) 1/1, (b) 3/1, (c) 6/1, (d) 9/1
Anschließend wurden TEM-Messungen durchgeführt, um die Größe, Größenverteilung und Morphologie der AgNPs zu bestimmen. Die TEM-Bilder von AgNPs hingen von AgNO3 . ab Fütterungsverhältnisse sind in Abb. 4 dargestellt. Wenn das PDMAEMA/AgNO3 die Molverhältnisse waren 6 und 1, berechnet mit der ImageJ-Software, die Partikelgröße von Micellen stabilisierten AgNPs mit linearen Copolymeren betrug 11,1 nm und 25,7 nm, während der Durchmesser von Micellen stabilisierten AgNPs mit Sterncopolymeren 3,7 nm bzw. 6,4 nm betrug. Der Anstieg von AgNO3 Der Gehalt führte zu mehr Silberatomen in Micellen, einer höheren Oberflächenenergie, und die Zahl der aggregierten AgNPs steigt entsprechend mit einer größeren AgNPs-Größe. Es war klar, dass Micellen-stabilisierte AgNPs monodispers und kugelförmig waren, mit etwas ungleichmäßigen von linearen Copolymer-Micellen-stabilisierten AgNPs. Die Größen der Micellen-stabilisierten AgNPs ergänzten die UV-Vis-Ergebnisse zusätzlich.

TEM-Bild von a , b lineare Copolymere und c , d Sterncopolymere Micellen stabilisierte AgNPs bei verschiedenen PDMAEMA/AgNO3 Molverhältnisse:a , c 6/1, b , d 1/1
Stabilität der linearen/Stern-Copolymere Micellen stabilisierte AgNPs
The stability of the linear/star copolymers micelles stabilized AgNPs is of great influence for the development of biomedical field. Obviously, the SPR peak in UV-Vis spectra (Fig. 5) of star copolymer micelles stabilized AgNPs did not display any significant changes for at least 1 month even after further diluted by one time, three times, and six times, indicating that the prepared AgNPs appeared well long-term colloidal stability within the experimental concentration range. However, the results of linear copolymer micelles stabilized AgNPs showed that the UV absorption wavelength decreased slightly as the increase of dilution ratios. And the micelles concentration of linear copolymer decreased after 1 month of placement may lead to insufficient provision of steric hindrances to stabilize AgNPs.
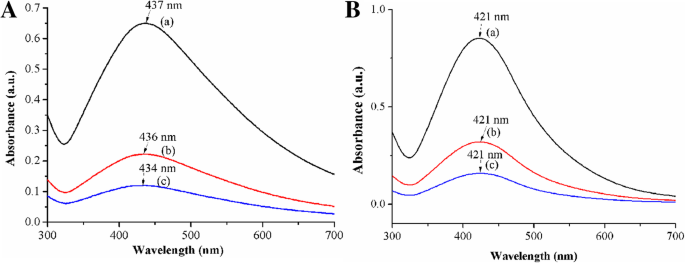
UV-Vis spectra of a linear copolymers and b star copolymers micelles stabilized AgNPs solution at PDMAEMA/AgNO3 molar ratio =6/1 after 1 month at the diluted times of 1 (a), 3 (b), and 6 (c), respectively
From the thermogravimetric analysis curves in Fig. 6, it was shown that the initial decomposition temperature (T onset ) of linear copolymers micelles was 217 °C, which shifted to 172 °C after silver loading, suggesting that the linear copolymer micelles stabilized AgNPs showed lower thermal stability than the pure linear copolymers micelles. It may be due to the fact that the chemical structure of PDMAEMA in the molecular chain changes and the catalytic effect of AgNPs in the thermal degradation process cannot be ignored [35]. As for star copolymers and their stabilized AgNPs, T onset were around 213 °C. The two Tonset of star copolymers micelles and their micelles stabilized AgNPs showed very few gaps, which could be speculated that the more stable star-shaped copolymers have better effect on stabilizing AgNPs than the linear copolymers. Combined the results of UV-Vis, TEM, and TGA measurements, it could be inferred that compared to the linear copolymers, the star copolymers have superior advantages in topology for stabilizing AgNPs, such as better stability, more uniform dispersion, slower nucleation rate during reduction, and the better product with a smaller and more uniform size of AgNPs.
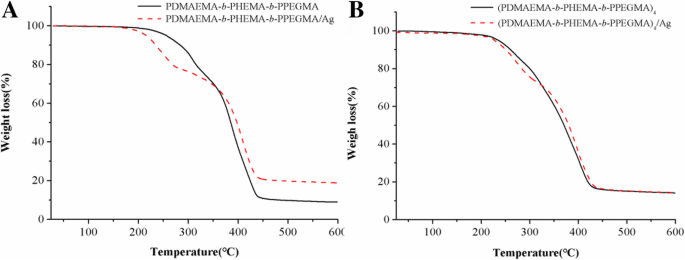
TGA curves of a linear copolymers and b star copolymers micelles and their micelles stabilized AgNPs at PDMAEMA/AgNO3 molar ratio =6/1
Antibacterial Activity and Cell Viability
To evaluate the antibacterial activities of the linear/star copolymers micelles stabilized AgNPs by optical density (OD600 ) measurements, E . coli DH5α was selected as the Gram-negative bacterial model. The absorbance at 600 nm after incubation was tested by incubating the bacteria with the eight different concentrations of micelles and micelles stabilized AgNPs at 37 °C. Results shown in Fig. 7a illustrated that the bacterial growth curves were highly correlated with the AgNPs concentration in the LB medium. The inhibition of linear/star copolymers micelles on the growth of bacteria was weak, which was not fatal to bacteria. However, as the concentration of linear/star copolymers micelles stabilized AgNPs increased, the survival rate of E . coli DH5α was significantly inhibited, indicating a strong antibacterial efficacy of AgNPs against E . coli DH5α. The concentrations of linear copolymers micelles stabilized AgNPs preventing the bacterial growth in the experiments were relatively higher than those of star copolymers micelles stabilized AgNPs, which might due to the fact that bigger size of AgNPs could lead to a lower antibacterial performance because of the inefficient exposure of bacteria to AgNPs and relatively slow release behavior of AgNPs.
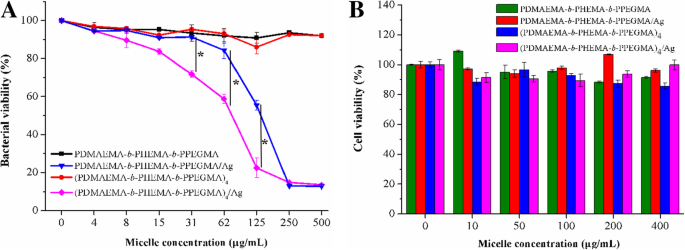
a Antibacterial activity and b cell viability of linear copolymers and star copolymers micelles stabilized AgNPs at PDMAEMA/AgNO3 molar ratio =6/1. *p <0.05, two-tailed Student t testen
Cancer is an uncontrollable disease of cell growth that can occur in any part of the body. The most common cancers are liver cancer, breast cancer, colorectal cancer, and lung cancer. Among them, the liver cancer has the much higher prevalence in both developed and developing countries. Therefore, the toxicity experiments of the linear/star copolymers micelles stabilized AgNPs on HepG2 cells were carried out, in which HepG2 cells were incubated with linear/star copolymers micelles stabilized AgNPs at different concentrations (10, 50, 100, 200, 400 mg/L, respectively) for 48 h and the cell viability with MTT assay was the most intuitive data to evaluate the biocompatibility of the composite material. As shown in Fig. 7b, the percentage of viable cells for the linear/star copolymers micelles stabilized AgNPs exhibited negligible cytotoxicity, and was about 90% viability even at the highest concentration applied (400 μg/mL) after 48-h incubation, indicating the advantageous cytocompatibility of the micelles stabilized AgNPs within a relatively wide range of concentration.
Conclusion
In conclusion, PDMAEMA-based linear and star copolymer micelles as effective delivery carriers for silver-bearing antimicrobials were developed, and their in vitro antimicrobial efficacy and cell viability were investigated. Being a reducing agent and a stabilizer simultaneously, the micellar PDMAEMA core acted as loading platform for AgNPs in situ translated from the precursor silver nitrate. In silico simulation and experimental results indicated that both types of the copolymer micelles could generate monodisperse and spherical AgNPs. Compared with linear copolymers sliver-bearing micelles, the fabricated star copolymers micelles stabilized AgNPs exhibited smaller average size, better stability against dilution and pyrogenic decomposition, and enhanced antibacterial activities against E . coli DH5α due to the serious damage of bacterial membrane caused by loaded AgNPs. Moreover, both types of copolymer micelles stabilized AgNPs possessed great cytocompatibility toward HepG2 cells. Therefore, these studies may provide some guidance for the construction of more effective AgNPs weapon with well-defined and feasible polymer topology for combating the multiple bacteria-induced infections.
Verfügbarkeit von Daten und Materialien
Die in der aktuellen Studie verwendeten und/oder analysierten Datensätze sind auf begründete Anfrage beim entsprechenden Autor erhältlich.
Abkürzungen
- AgNPs:
-
Silbernanopartikel
- DMAEMA:
-
2-(dimethylamino) ethyl methacrylate
- HEMA:
-
2-hydroxyethyl methacrylate
- PEGMA:
-
Poly (ethylene glycol) methyl ether methacrylate
- CuBr2 :
-
Cupric bromide
- 1 H NMR:
-
Proton nuclear magnetic resonance
- FTIR:
-
Fourier-Transformations-Infrarotspektroskopie
- KBr:
-
Potassium bromide
- UV-Vis:
-
Ultraviolet-visible
- MTT:
-
3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazoliumbromid
- HepG2:
-
Liver hepatocellular carcinoma
- DPD:
-
Dissipative particle dynamics
- SPR:
-
Oberflächenplasmonenresonanz
- XRD:
-
Röntgenbeugung
Nanomaterialien
- Herstellung und magnetische Eigenschaften von kobaltdotierten FeMn2O4-Spinell-Nanopartikeln
- Auf dem Weg zu TiO2-Nanofluiden – Teil 1:Vorbereitung und Eigenschaften
- Einfache Synthese und optische Eigenschaften kleiner Selen-Nanokristalle und -Nanostäbe
- Herstellung und verbesserte katalytische Hydrierungsaktivität von Sb/Palygorskit (PAL)-Nanopartikeln
- In-vitro-Studie zum Einfluss von Au-Nanopartikeln auf HT29- und SPEV-Zelllinien
- Biosicherheit und antibakterielle Wirkung von Graphen und Graphenoxid in vitro und in vivo
- Herstellung und photokatalytische Leistung von Hohlstruktur-LiNb3O8-Photokatalysatoren
- Magnetische Poly(N-isopropylacrylamid)-Nanokomposite:Einfluss des Herstellungsverfahrens auf die antibakteriellen Eigenschaften
- Eintopfsynthese von Cu2ZnSnSe4-Nanoplatten und ihre durch sichtbares Licht getriebene photokatalytische Aktivität
- Antibakterielle Aktivität einer in situ hergestellten Lösung aus Chitosan/Silber-Nanopartikeln gegen Methicillin-resistente Stämme von Staphylococcus aureus



