Organische Phosphor- und Kalziumquelle induzieren die Synthese von Mikrokügelchen aus Kalziumphosphat mit Eigelbhülle und hoher spezifischer Oberfläche:Anwendung bei der HEL-Adsorption
Zusammenfassung
Calciumphosphat-Mikrokügelchen mit Dotterschalenstruktur haben aufgrund ihrer hervorragenden physikalisch-chemischen Eigenschaften und ihrer Biokompatibilität ein großes Potenzial für medizinische Anwendungen. Die Entwicklung eines Calciumphosphats mit Dotterschalenstruktur und hoher Adsorptionsfähigkeit bleibt jedoch eine Herausforderung. Hierbei handelt es sich um eine poröse Eigelb-Schale-strukturierte Mikrosphäre (ATP-CG) aus Calciumphosphat mit hoher spezifischer Oberfläche [S WETTEN =143 m 2 g −1 , das ungefähr dreimal so hoch ist wie das von ATP-CL-Mikrosphären, die durch Ersetzen der Calciumquelle durch Calcium-L-Lactat-Pentahydrat (CL) synthetisiert wurden] erfolgreich unter Verwendung von Adenosin-5'-triphosphat-dinatriumsalz (ATP) als Phosphorquelle synthetisiert wurde und Calciumgluconatmonohydrat (CG) als Calciumquelle durch einen selbsttemperierenden Ansatz. Die Einflüsse des Molverhältnisses von Ca zu P (Ca/P), der hydrothermalen Temperatur und der Zeit auf die Morphologie von ATP-CG-Mikrokügelchen wurden ebenfalls untersucht. Es wurde festgestellt, dass die organische Calciumquelle und die organische Phosphorquelle eine entscheidende Rolle bei der Bildung der Dotterschalenstruktur spielen. Darüber hinaus wurde eine Reihe von Adsorptionsexperimenten untersucht, um den Adsorptionsmechanismus von zwei Arten von Mikrokügelchen mit Dotterschalenstruktur zu beleuchten, die mit unterschiedlichen Calciumquellen synthetisiert wurden. Die Ergebnisse zeigen, dass die Adsorptionskapazität von ATP-CG-Mikrokügelchen (332 ± 36 mg/g) etwa zweimal höher ist als die von ATP-CL-Mikrokügelchen (176 ± 33 mg/g). Darüber hinaus spielen die durch die Calciumquelle verursachte höhere spezifische Oberfläche und die einzigartigen chemischen Oberflächeneigenschaften für ATP-CG-Mikrokügelchen eine wichtige Rolle bei der Verbesserung der HEL-Adsorptionsfähigkeit. Die Studie weist darauf hin, dass die Mikrokügelchen mit Dotterschalenstruktur wie zubereitet vielversprechend für die Anwendung auf dem Gebiet der Wirkstoffabgabe sind und einen wirksamen Ansatz zur Verbesserung der Wirkstoffadsorptionsfähigkeit bieten.
Einführung
Calciumphosphat hat in den letzten Jahren aufgrund seiner hervorragenden Biokompatibilität [1], seiner hohen Beladungskapazität und seiner Liefereffizienz große Aufmerksamkeit erlangt. Mit Calciumphosphat verwandte Biomaterialien werden in verschiedenen biomedizinischen Bereichen wie Tissue Engineering [2], Knochenreparatur [3] und Wirkstoffabgabe [4] weit verbreitet eingesetzt. Um den Anwendungsbereich zu erweitern und die Leistung von Calciumphosphat-basierten Materialien zu verbessern, wurden verschiedene Calciumphosphat-Materialien mit einer Vielzahl von Morphologien und Mikrostrukturen verwendet, darunter Mikrokügelchen aus karbonisiertem Hydroxyapatit (HAp) [5], HAp-Mikroröhrchen [6], hohle HAp-Mikrokügelchen [7 ] wurden mesoporöse Yolk@cage-shell-Nanosphären aus amorphem Calciumphosphat (ACP) [8] berichtet.
Unter verschiedenen Morphologien haben Mikrokügelchen mit Dotterschalenstruktur immer mehr Aufmerksamkeit auf sich gezogen, da sie nicht nur die Materialwissenschaft der Vorreiter sind, sondern auch einzigartige morphologische Merkmale aufweisen. In Mikrokügelchen mit Dotterschalenstruktur kann der Hohlraum zwischen Dotterkern und Schale als Speicherreservoir für verschiedene Ladungen dienen und die porös strukturierte Schale kann einen Diffusionsweg für Gastmoleküle bieten, was ihnen ein großes Potenzial für verschiedene Anwendungen verleiht, darunter Katalyse [9], Lithium-Ionen-Batterien [10], Photokatalysator [11] und Biomedizin [12]. Traditionell sind Schablonenopfermethoden die primären Methoden, um Mikrokügelchen mit Dotterschalenstruktur herzustellen [13, 14]. Diese Template-Strategien haben große Erfolge bei der Anpassung von Struktur und Eigenschaften erzielt. Diese Ansätze weisen jedoch einige Nachteile auf. Zum Beispiel langwierige Verarbeitungsschritte und Tenside oder strukturdirigierende Reagenzien, die für den Menschen gesundheitsgefährdend sein können. Derzeit werden die selbsttemperierenden Methoden in großem Umfang in der Erforschung von Mikrokügelchen mit Dotterschalenstruktur verwendet [15, 16]. Im Gegensatz zu den traditionellen Templating-Ansätzen sind die Templates, die in Self-Templating-Ansätzen verwendet werden, nicht nur die Templates zum Bilden der Hohlräume, sondern auch die Vorläufer von Mikrokügelchen mit Dotterschalenstruktur. Selbsttemperierende Methoden sind daher bequeme Ansätze zur Herstellung von Mikrokügelchen mit Dotterschalenstruktur. Die Einführung von selbsttemperierenden Ansätzen zur Synthese von Calciumphosphat-Mikrokügelchen mit Dotterschalenstruktur bleibt jedoch eine interessante Herausforderung.
Darüber hinaus wurden Calciumphosphatmaterialien verwendet, um verschiedene Arten von Ladungen wie Proteine [17], DNA [18] und siRNA [19] zu transportieren. Die schlechte Arzneistoffadsorptionsfähigkeit von Calciumphosphat muss jedoch dringend behoben werden. Im Allgemeinen hängen die Ansätze zur Immobilisierung von Wirkstoffmolekülen über der Oberfläche des Trägers von den Oberflächeneigenschaften ab, die Oberflächenpotential [20], Hydrophobie/Hydrophilie [21], Wasserstoffbrückenbindung [22] und spezifische Oberfläche [23] enthalten. Daher ist die Verbesserung der Oberflächeneigenschaften und der spezifischen Oberfläche ein gültiger Ansatz zur Verbesserung der Wirkstoffadsorptionsfähigkeit des Trägers.
Hier haben wir eine Art poröser, dotterschalenstrukturierter Mikrokügelchen aus Calciumphosphat hergestellt, indem wir Adenosin-5'-triphosphat-Dinatriumsalz (ATP) als Phosphorquelle und Calciumgluconatmonohydrat (CG) als Calciumquelle durch einen selbsttemperierenden Ansatz verwendet haben. Ohne Zusatz von Templat weisen die präparierten Calciumphosphat-Mikrokügelchen mit Dotterschalenstruktur eine besonders hohe spezifische Oberfläche auf. Darüber hinaus wurde das Adsorptionsverhalten von Hühnerei-Lysozym (HEL) von ATP-CG-Mikrokügelchen im Vergleich mit den ATP-CL-Mikrokügelchen untersucht, die durch Ersetzen der Calciumquelle durch Calcium-L-Lactat-Pentahydrat (CL) hergestellt wurden. Die Ergebnisse zeigen, dass der durch die Calciumquelle verursachte Unterschied der spezifischen Oberfläche und die chemischen Oberflächeneigenschaften eine entscheidende Rolle bei der Verbesserung der HEL-Adsorptionsfähigkeit spielen.
Methoden
Materialien
Adenosin-5'-triphosphat-dinatriumsalz (ATP) wurde von Macklin Biochemical Co., Ltd (Shanghai, China) erhalten. Calciumgluconat-Monohydrat (CG) und Calcium(l)-Lactat-Pentahydrat (CL) wurden von Sangon Biotech Co., Ltd (Shanghai, China) erworben. Das Hühnerei-Lysozym (HEL, ~ 70000 U/mg) wurde von Sigma-Aldrich (Taufkirchen, Deutschland) bezogen.
Synthese und Charakterisierung von ATP-CG und ATP-CL Eigelb-Schale-strukturierten Mikrosphären
Die ATP-CG-Dotterschalen-strukturierten Calciumphosphat-Mikrokügelchen wurden wie folgt hergestellt:Kurz gesagt wurden 0,9 g CG in 20 ml Reinstwasser gelöst, um Lösung C bei 60 °C zu bilden, und 0,11 g ATP wurden in 5 ml . gelöst Reinstwasser, um Lösung P zu bilden. Dann wurde Lösung C auf Raumtemperatur abgekühlt und unter starkem Rühren mit Lösung P vermischt und der pH-Wert der Lösung wurde mit 2 M NaOH-Lösung auf 5 eingestellt. Das Endvolumen der Lösung betrug 30 ml mit der zusätzlichen Zugabe von Reinstwasser und das Molverhältnis von Ca zu P (Ca/P) betrug 3,3. Die endgültige Lösung wurde in ein Mikrowellenaufschlusssystem für die hydrothermale Mikrowellenreaktion überführt und bei 120°C für 15 Minuten behandelt. Die resultierenden Niederschläge wurden durch Zentrifugation (4500 UpM, 10 min) gesammelt, mit Reinstwasser gespült und 48 h lyophilisiert. Die ATP-CL-Mikrosphären wurden gemäß Literaturverfahren [24] hergestellt.
Die kristalline Phase der Mikrokügelchen wurde durch Röntgenbeugung charakterisiert (XRD, Cu Kα Quelle, λ =0,154). Die Morphologie der Mikrokügelchen wurde durch Rasterelektronenmikroskopie (REM), Transmissionselektronenmikroskopie (TEM) und hochauflösendes TEM (HRTEM) beobachtet. Die Zusammensetzungen der Mikrokügelchen wurden mit einem Fourier-Transform-Infrarot-Spektrophotometer (FTIR) untersucht. Die spezifische Oberfläche der Mikrokügelchen wurde nach Brunauer-Emmett-Teller (BET) bestimmt. Thermogravimetrieanalyse (TGA) wurde verwendet, um die thermischen Eigenschaften von Proben bei einer Heizrate von 10 °C/min in einer Stickstoffatmosphäre zu untersuchen.
HEL-Adsorption und Charakterisierung
Die HEL-Adsorptionsexperimente von zwei Arten von Mikrokügelchen wurden wie folgt durchgeführt:die bestimmten Mengen an Dotterschalen-Mikrokügelchen (ATP-CG, Ca/P =3,3, 120 °C, 15 min und ATP-CL, Ca/P =2,5, 120 °C, 30 min) wurden unter konstanter Ultraschallbehandlung für 10 min im Wasser dispergiert, um 1,5 mg/ml Mikrokügelchensuspension zu bilden. Dann wurden 0,5 ml wässrige Lösungen, die verschiedene Konzentrationen von HEL enthielten, sofort zu 1 ml der obigen Suspension gegeben und die Endkonzentrationen des Arzneimittels betrugen 1–7,5 mg/ml. Jede Lösung wurde 6 h bei 37 °C geschüttelt (200 U/min). Später wurden die Lösungen zentrifugiert und die HEL-Mengen in den Überständen wurden mit einem UV-Vis-Spektrophotometer bei 280 nm gemessen. Die Zetapotentiale und Zusammensetzungen der Mikrokügelchen vor und nach der Wirkstoffbeladung wurden mit einem Zetapotentialanalysator, einem FTIR-Spektrometer und einem thermogravimetrischen Analysator (TGA, Heizrate 10 °C min −1 , Stickstoffatmosphäre).
Adsorptionsisotherme
Um das Adsorptionsverhalten zu untersuchen, wurde in unserer Studie das Dubinin-Radushkevic-Isothermen-(D-R)-Modell durchgeführt. Das D-R-Modell basiert auf der Theorie der Mikroporenfüllung, die verwendet wird, um die nicht-ideale Sorption an einer heterogenen Oberfläche zu beschreiben sowie den Sorptionsmechanismus (physikalische Sorption oder chemische Sorption) zu unterscheiden. Das Modell wird durch die folgende Gleichung ausgedrückt:wobei Q eq ist die Adsorptionskapazität des Adsorptionsmittels im Gleichgewicht (mg/g), C eq ist die Adsorbatkonzentration in der wässrigen Phase im Gleichgewicht (mL/L). Q m ist die maximale Adsorptionskapazität. R ist die Gaskonstante 8,314 J/(mol k). T ist die absolute Temperatur. E stellt die mittlere freie Energie zum Schätzen der Art der Adsorption dar. Wenn das E Wert unter 8 kJ/mol, der Adsorptionstyp kann durch physikalische Adsorption erklärt werden, zwischen 8 und 16 kJ/mol, der Adsorptionstyp gehört zum Ionenaustausch und größer als 16 kJ/mol, der Adsorptionstyp kann durch chemische Adsorption beschrieben werden .
$$ {Q}_{\mathrm{eq}}={Q}_m\exp \left(-{K}_{\mathrm{DR}}\{\varepsilon}^2\right) $$ (1) $$ \varepsilon =\text{RT1n}(1+\frac{1}{{C}_\text{eq}}) $$ (2) $$ \mathrm{E}=\frac{1}{\ Quadrat{K_{\mathrm{DR}}}} $$ (3)Statistische Analyse der Arzneimitteladsorption
Die Daten wurden als Mittelwert ± Standardabweichung (SD) dargestellt. Signifikante Unterschiede (p <0,05) wurden statistisch zwischen verschiedenen Gruppen unter Verwendung der Einweg-ANOVA berechnet. Alle Experimente wurden dreifach durchgeführt und die Daten wurden mithilfe der DPS-Software analysiert.
Ergebnisse und Diskussion
Morphologie und chemische Charakterisierung von Mikrosphären
ATP-CG Eigelb-Shell-strukturierte Mikrosphären
REM-Bilder in Abb. 1 zeigen die Morphologien verschiedener Proben, die unter verschiedenen Reaktionsbedingungen erhalten wurden. Bei t =5 min oder 15 min, alle Produkte bestehen aus einheitlichen Mikrokügelchen. Wenn jedoch die Hydrothermalzeit weiter auf 30 min erhöht wird, wurden Nanoblätter mit selbstorganisierten Mikrokügelchen gebildet (wie in Abb. 1 f, i, l gezeigt). Inzwischen wird die Wirkung von Ca/P auf die Morphologie der Produkte auch bei t . beobachtet =30 Minuten Mit der Zunahme von Ca/P wurden die selbstorganisierten Mikrokügelchen der Nanoblätter allmählich gebildet (wie in Fig. 1 f, i, l gezeigt). Die Bildung von selbstorganisierten Mikrokügelchen aus Nanoblättern könnte durch die folgenden Gründe erklärt werden. Erstens könnten ATP-Moleküle unter dem hydrothermalen Mikrowellenprozess hydrolysieren, um Moleküle auf Adenosinbasis zu bilden, einschließlich Adenosindiphosphat (ADP), Adenosinmonophosphat (AMP) und Adenosin, und gleichzeitig Phosphationen (PO4 .) freisetzen 3− ). In der Zwischenzeit könnten CG-Moleküle hydrolysieren, um Gluconat und Calciumionen (Ca 2+ ). Dann würden Phosphationen mit Calciumionen reagieren, um primäre ACP-Kerne zu bilden [25]. Dann wachsen die anfänglichen ACP-Kerne und fügen sich zusammen, um ACP-Mikrokügelchen zu bilden. Wenn die Hydrothermalzeit weiter verlängert wird, werden die ATP- und CG-Moleküle in Lösung daher weiter hydrolysiert und setzen mehr PO4 . frei 3− und Ca 2+ Ionen, die die Bildung von selbstorganisierten Mikrokügelchen aus Nanoblättern bewirken, indem die Übersättigung des Systems und die Keimbildungsrate verbessert werden. Darüber hinaus wird durch die Erhöhung von Ca/P die lokale hohe Konzentration von Ca 2+ beschleunigt auch die Morphologieumwandlung von Produkten auf die gleiche Weise wie oben. Die obige Analyse zeigt, dass die Hydrothermalzeit und Ca/P einen wichtigen Einfluss auf die Morphologie der Produkte haben.

REM-Aufnahmen von ATP-CG-Mikrokügelchen, die mit der Mikrowellen-Hydrothermalmethode bei 120 °C hergestellt wurden
Als nächstes werden die FTIR-Spektren von Mikrosphären untersucht, die mit verschiedenen Ca/P bei 120 °C für 15 min synthetisiert wurden (Abb. 2). Die Peaks bei 1620 cm −1 , 1383 cm −1 , und 912 cm −1 auf die charakteristischen Peaks der C=O-, C–O- von CG- bzw. P–O-Gruppen von ATP zurückgeführt [26], was darauf hindeutet, dass nicht hydrolysierte CG- und ATP-Moleküle oder deren Derivate an der Oberfläche der Mikrokügelchen absorbiert werden. Der schwache charakteristische Peak des PO4 3− von HAp liegt bei 1035 cm −1 [27] und die Absorptionspeaks bei 1122 cm −1 und 567 cm −1 sind PO4 . zugeordnet 3− Ionen von ACP [28], was darauf hinweist, dass die Produkte aus ACP und HAp bestehen. Die FTIR-Ergebnisse deuten darauf hin, dass das Calciumphosphat erfolgreich hergestellt wird, indem ATP als Phosphorquelle und CG als Calciumquelle verwendet werden.
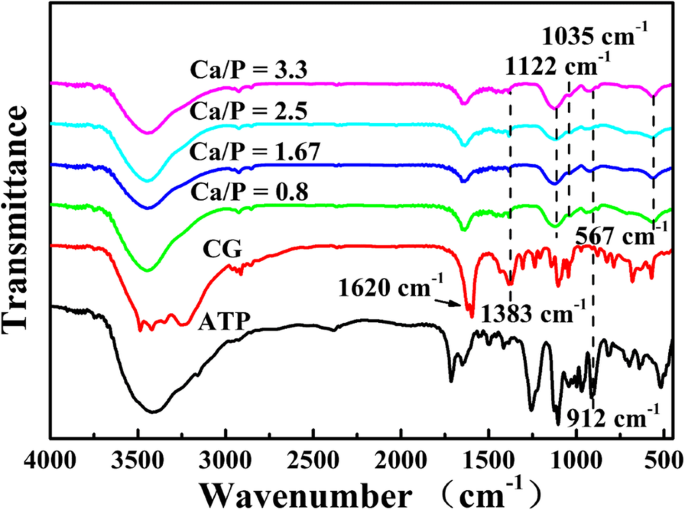
FTIR-Spektren von ATP-CG-Mikrosphären synthetisiert mit verschiedenen Ca/P bei 120 °C für 15 min
Darüber hinaus sind in Abb. 3 die SEM- und TEM-Bilder von Proben dargestellt, die mit verschiedenen Ca/P durch ein Mikrowellen-Hydrothermalverfahren bei 120 °C für 15 min synthetisiert wurden. Wenn Ca/P 0,8 oder 1,67 beträgt, bestehen die Proben aus porösen Mikrokügelchen ( Abb. 3b, d). Wenn Ca/P 2,5 beträgt, beginnt sich die Morphologie der Produkte in Mikrokügelchen mit Dotterschalenstruktur umzuwandeln (Fig. 3f). Wenn Ca/P weiter auf 3,3 ansteigt, bestehen die Produkte vollständig aus Mikrokügelchen mit Dotterschalenstruktur (Abb. 3h). Darüber hinaus werden einige gebrochene Kugeln und die freiliegenden Kerne der Dotter-Hülle-Mikrokugeln (Einsatz in Fig. 3g) nach dem mechanischen Aufbrechen beobachtet, was auf eine Hohlstruktur zwischen Dotter und Schale hindeutet. Basierend auf der obigen Beobachtung schlagen wir vorläufig den Bildungsmechanismus von Mikrokügelchen mit Dotterschalenstruktur vor, die mit verschiedenen Ca/P synthetisiert wurden. Wenn Ca/P niedriger ist, werden zuerst die porösen ACP-Mikrokügelchen gebildet, was der Hemmwirkung von ATP- und CG-Molekülen oder ihren Derivaten, die an der Oberfläche der Mikrokügelchen adsorbiert sind, zugeschrieben wird. Wenn dann Ca/P weiter erhöht wird, wächst das metastabile ACP weiter, was durch die hohe Übersättigung des Systems angetrieben wird. Schließlich werden die kristallinen HAps auf der äußeren Oberfläche gebildet, was durch das hochauflösende TEM (HRTEM)-Bild von Mikrokügelchen in Fig. 3i bestätigt wird (der Interplanarabstand von 0,308 nm kann auf (210) von HAp indiziert werden). Als Ergebnis werden die Hohlstrukturen zwischen Dotter und Schale aufgrund des Volumen- oder Dichteunterschieds zwischen HAp und ACP erzeugt [24]. Die entsprechende EDS-Kartierung zeigt, dass die Ca-, P- und O-Elemente gleichmäßig über die Mikrokügelchen verteilt sind. Die EDS-Spektren in Abb. 3k und XPS-Spektren in Abb. 3l zeigen, dass die chemischen Elemente der Mikrokügelchen hauptsächlich Ca, P und O umfassen, was mit dem Ergebnis von FTIR übereinstimmt (Abb. 2).

SEM- und TEM-Bilder von ATP-CG-Mikrokügelchen, die mit verschiedenen Ca/P synthetisiert wurden. a , b Ca/P =0,8. c , d Ca/P =1,67. e , f Ca/P =2,5. g , h Ca/P =3,3. ich HRTEM, j EDS-Mapping, k EDS-Spektren, l XPS-Spektren von ATP-CG-Mikrosphären mit Ca/P =3,3
Der Einfluss der mikrowellenunterstützten hydrothermalen Zeit und Temperatur auf die Morphologie von Mikrokügelchen, die mit Ca/P =3,3 synthetisiert wurden, wird weiter untersucht. Wie in Fig. 4a-b gezeigt, bestehen die Proben bei einer Hydrothermalzeit von 5 min aus porösen Mikrokügelchen. Wie oben besprochen, wenn t =15 Minuten besteht das Produkt ebenfalls aus Mikrokügelchen mit Dotterschalenstruktur (Abb. 4c-d). Wenn die Hydrothermalzeit auf 60 Minuten verlängert oder die Temperatur auf 160 o erhöht wird C, Platten- oder Stäbchengrenzen werden beobachtet (Abb. 4e-l). Die Morphologieumwandlung von porös zu Dotterschalen zu Blatt oder Stäbchen wird dem weiteren Wachstum von ACP mit der kontinuierlichen Hydrolyse von ATP- und CG-Molekülen in Lösung zugeschrieben. Darüber hinaus beschleunigt auch die Hydrolyse von ATP- und CG-Molekülen oder ihren Derivaten, die an der Oberfläche der ACP-Mikrokügelchen adsorbiert sind, das Wachstum von ACP. Ein interessantes Phänomen trat nach 60 Minuten oder 160 o auf C, diese Blätter oder Stäbchen werden ebenfalls aus ACP-Nanopartikeln entwickelt (wie in roten Kästchen gezeigt), was durch die DTA-Analyse in Abb. S1 bestätigt wird. In den DTA-Kurven [29, 30] wird ein exothermer Peak bei 650 °C beobachtet, der der ACP-Kristallisation zugeschrieben wird. Der exotherme Peak wird mit zunehmender Hydrothermalzeit oder Temperatur allmählich schwach, was darauf hindeutet, dass die Umwandlung von ACP in den Produkten in kristallines Calciumphosphat erfolgt.

SEM- und TEM-Bilder von ATP-CG-Mikrosphären synthetisiert mit Ca/P =3.3 unter verschiedenen experimentellen Bedingungen. a , b T =120 °C, t =5 Min. c , d T =120 °C, t =15 Min. e–h T =120 °C, t =60 Minuten ich–l T =160 °C, t =15 Minuten
Die chemische Konstitution und Struktur von Proben, die mit Ca/P =3.3 unter verschiedenen Hydrothermalzeiten oder -temperaturen synthetisiert wurden, werden mit FTIR und XRD untersucht. Wie in Fig. 5a gezeigt, sind die charakteristischen Peaks von PO4 3− Ionen von HAp befinden sich bei 1037 cm −1 und 603 cm −1 [27]. Der Peak bei 1122 cm −1 wird dem charakteristischen Peak von PO4 . zugeordnet 3− Ionen aus ACP. Die Absorptionspeaks bei 1620 cm −1 und 1383 cm −1 werden einem charakteristischen Peak der C=O- bzw. C–O-Gruppen von CG zugeschrieben. Der Absorptionspeak bei 912 cm −1 bezieht sich auf die asymmetrische P-O-Streckschwingung von ATP. Durch Erhöhen der Hydrothermalzeit oder -temperatur wird die Intensität der charakteristischen Peaks von CG und ATP allmählich verringert, was anzeigt, dass die ATP- und CG-Moleküle oder ihre Derivate, die an der Oberfläche der Mikrokügelchen adsorbiert sind, weiter hydrolysiert werden. Inzwischen ist die Intensität des charakteristischen Peaks von PO4 3− Ionen in HAp zeigen einen allmählich zunehmenden Trend mit der Abnahme der Intensität des charakteristischen ACP-Peaks, was die Umwandlung der kristallinen Phase der Produkte in die HAp-Phase beleuchtet.
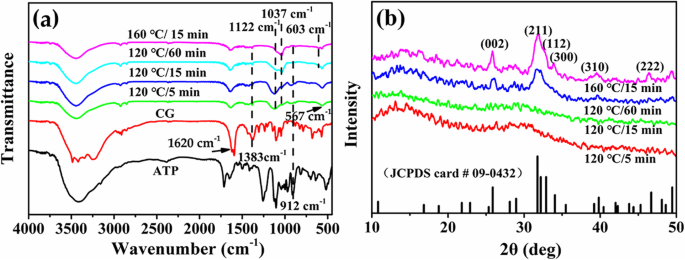
a FTIR-Spektren und b XRD-Muster von ATP-CG-Mikrokügelchen synthetisiert mit Ca/P =3.3 unter verschiedenen experimentellen Bedingungen
Abbildung 5b zeigt XRD-Muster verschiedener Proben. Ein charakteristischer Buckel aus amorpher Phase bei etwa 2θ =30° Mikrokügelchen, die nach 5 oder 15 min synthetisiert wurden, beobachtet. Wenn jedoch entweder die Hydrothermalzeit auf 60 min verlängert oder die Temperatur auf 160 °C erhöht wird, wandelt sich die kristalline Phase der Mikrokügelchen vollständig in HAp um, was als Standarddaten (JDCPS Nr. 09-0432) indiziert werden könnte. Die Verbesserung der relativen Intensität der (211), (300) und (002) Gitterebenen könnte die Zunahme der Kristallinität der Produkte weiter erklären. Somit bestätigen die XRD- und FTIR-Ergebnisse die kristalline Phasenumwandlung von Produkten mit zunehmender Hydrothermaltemperatur oder -zeit.
ATP-CL Eigelb-Shell-strukturierte Mikrosphären
Um das Arzneistoffadsorptionsverhalten zu vergleichen, wurden die anderen Mikrokügelchen mit Dotterschalenstruktur unter Verwendung von CL als organische Calciumquelle durch ein Mikrowellen-Hydrothermalverfahren hergestellt [24]. Morphologisch bestehen die Proben noch aus Dotterschalen-strukturierten Mikrokügelchen, was durch die gebrochenen Kügelchen (Einschub in Abb. 6a) und TEM-Aufnahmen (Abb. 6b, c) bestätigt wird. Das Ergebnis zeigt, dass die Änderung der Calciumquelle keinen signifikanten Einfluss auf die Morphologie der Produkte hat. Darüber hinaus zeigt die Elektronenbeugung im ausgewählten Bereich (SAED) die diskreten SAED-Flecken (Fig. 6d), was zeigt, dass gut kristallisierte Mikrokügelchen erhalten werden. Darüber hinaus zeigt das EDS-Mapping die gleichmäßige Verteilung von Ca-, P- und O-Elementen in Mikrokügelchen (Abb. 6e). Die entsprechenden EDS-Spektren bestätigen auch die Anwesenheit von Ca-, P- und O-Elementen in Mikrokügelchen (Abb. 6f), was darauf hindeutet, dass die Mikrokügelchen so hergestellt wurden, dass es sich um Calciumphosphat handelt.

a SEM. b , c TEM-Bilder. d S Elektronenbeugung im ausgewählten Bereich (SAED). e EDS-Mapping und f EDS-Spektren von ATP-CL-Mikrosphären
HEL-Adsorption und Adsorptionsmechanismus von Mikrosphären
Wie in Fig. 7 gezeigt, nimmt die Adsorptionskapazität von zwei Arten von Mikrokügelchen mit steigender Anfangskonzentration von HEL zu. Wenn die Anfangskonzentration von HEL auf 6,5 mg/ml ansteigt, erreicht die Adsorptionskapazität der ATP-CG-Mikrosphären ein Plateau und die maximale Adsorptionskapazität der Mikrosphären beträgt ungefähr 332 ± 36 mg/g (Abb. 7a), was ungefähr das Doppelte ist höher als bei ATP-CL-Mikrosphären (176 ± 33 mg/g, 6 mg/ml, Abb. 7b).
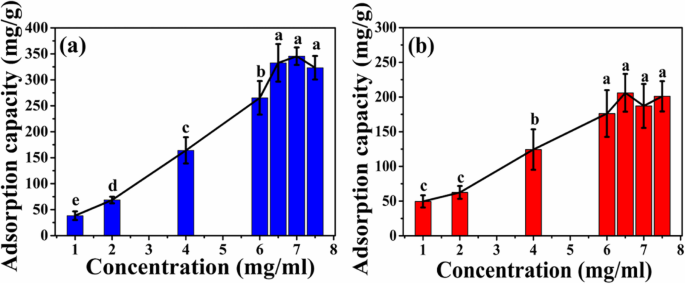
Adsorptionskurve von Mikrokügelchen bei unterschiedlicher Anfangskonzentration von HEL. a ATP-CG-Mikrosphären. b ATP-CL-Mikrosphären
Das HEL-Adsorptionsergebnis wird weiter durch die FTIR-Spektren und TG-Kurven gestützt. Wie in Abb. 8a, b gezeigt, liegen die Absorptionspeaks bei 1134 cm −1 (1139 cm −1 ) und 563 cm −1 (568 cm −1 ) dem charakteristischen Peak PO4 . zugeordnet 3− Ionen von ACP und 1039 cm −1 (1040 cm −1 ) dem charakteristischen Peak von PO4 . zugeordnet 3− Ionen von HAp werden in den HEL-adsorbierten Mikrokügelchen beobachtet, was darauf hinweist, dass die Einführung von HEL in Mikrokügelchen keine signifikante Änderung in der Struktur der Mikrokügelchen verursacht. Die Adsorptionspeaks bei 1542 cm −1 und 1545 cm −1 der Amidgruppe von HEL zugeschrieben werden, werden in HEL-adsorbierten Mikrokügelchen beobachtet, was bestätigt, dass HEL erfolgreich an den Mikrokügelchen adsorbiert wird. Die Adsorptionsbanden bei 2966, 2962, 2935 und 2927 cm −1 stammt aus –CH3 und –CH2 HEL-Gruppen werden auch in HEL-adsorbierten Mikrokügelchen nachgewiesen, was das Vorhandensein von HEL auf den Mikrokügelchen weiter bestätigt. Die TGA-Kurven zeigen, dass der Gewichtsverlust der ATP-CG-Mikrokügelchen vor und nach der HEL-Adsorption 11,3% bzw. 36,7% beträgt (Fig. 8c). Daher beträgt die HEL-Adsorptionskapazität von ATP-CG-Mikrosphären ungefähr 340 mg/g. Jedoch wird ein Gewichtsverlust von 21,1% von ATP-CL vor der HEL-Adsorption erhalten und 37% erscheinen auf den HEL-adsorbierten Mikrokügelchen (Fig. 8d). Somit beträgt die HEL-Adsorptionskapazität 189 mg/g für ATP-CL-Mikrosphären. Die TGA-Ergebnisse schließen sich an das Ergebnis aus Abb. 7 an.
FT-IR-Spektren und TGA-Kurven von Mikrokügelchen vor und nach der HEL-Adsorption. a FTIR-Spektren und c TGA-Kurven von ATP-CG-Mikrosphären, b FTIR-Spektren und d TGA-Kurven von ATP-CL-Mikrosphären
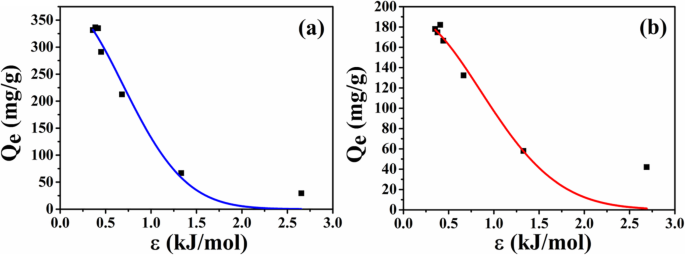
Um die Ursache der Adsorptionskapazitätsdifferenz zwischen zwei Arten von Mikrokügelchen zu untersuchen, werden die Gleichgewichtsadsorptionsdaten der Mikrokügelchen gemäß dem D-R-Isothermenmodell weiter analysiert. Die Anpassungskurven sind in Abb. 9 dargestellt und die Anpassungsparameter sind in Tabelle 1 aufgeführt. Aus den Anpassungsergebnissen geht hervor, dass der Korrelationskoeffizient von ATP-CG höher ist als der von ATP-CL, was darauf hindeutet, dass das D-R-Modell zur Beschreibung des Arzneimitteladsorptionsverhaltens von ATP-CG-Mikrokügelchen geeignet ist. Seit dem E Wert unter 8 kJ/mol liegt, ist die Adsorption von HEL an ATP-CG-Mikrosphären physikalische Sorption. Die maximale Kapazität (Q m ) von ATP-CG-Mikrokügelchen für HEL könnte bis zu 381 mg/g erreichen, was dem Ergebnis von Fig. 7a nahe kommt.

a Adsorptionsisothermenmodell von HEL auf ATP-CG-Mikrokügelchen. b Adsorptionsisothermen-Modell von HEL auf ATP-CL-Mikrosphären
Da die Adsorption von HEL auf den ATP-CG-Mikrokügelchen eine physikalische Sorption ist, wird das Oberflächenpotential der Mikrokügelchen untersucht. Wie in Abb. 10a gezeigt, beträgt der Zeta-Potentialwert von ATP-CG, ATP-CL-Mikrosphären und HEL in Reinstwasser – 17 mV, – 22 mV bzw. 20 mV. Nach der HEL-Adsorption ändert sich der Zeta-Potentialwert der ATP-CG- und ATP-CL-Mikrokügelchen auf 2,7 mV bzw. 1,5 mV, was darauf hinweist, dass die Adsorption von HEL-Molekülen auf der Oberfläche der Mikrokügelchen durch die anziehende elektrostatische Kraft erfolgt. Die elektrostatische Anziehungskraft ist jedoch nicht der Hauptgrund für den Unterschied in der Adsorptionskapazität zwischen zwei Arten von Mikrokügelchen, da es keinen signifikanten Unterschied in den Zeta-Potentialwerten (–17 mV und –22 mV) zwischen den Mikrokugeln gibt.
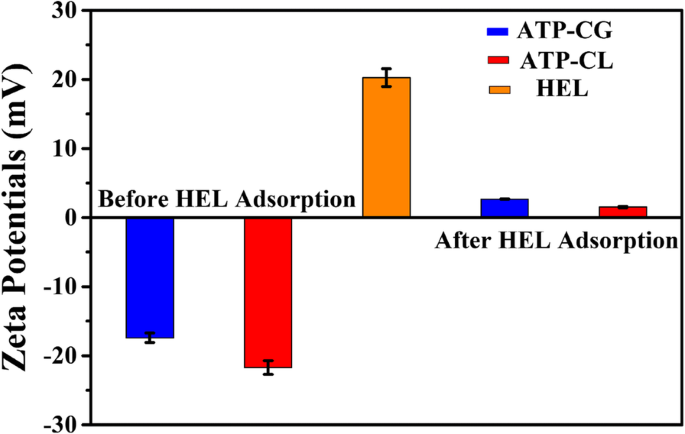
Zetapotentiale von HEL und Mikrosphären vor und nach der HEL-Adsorption
Um den Grund für den Unterschied in der Absorptionskapazität zwischen Mikrokügelchen weiter zu beleuchten, wird daher die spezifische Oberfläche der Mikrokügelchen untersucht. Wie in Abb. 11a gezeigt, ist die spezifische BET-Oberfläche (S WETTEN ) der ATP-CG-Mikrosphären beträgt 143 m 2 g −1 , das ungefähr dreimal so hoch ist wie die ATP-CL-Mikrosphären (55 m 2 g −1 , Tabelle 2). Somit kann die spezifische Oberfläche zum Unterschied der Absorptionskapazität zwischen Mikrokügelchen beitragen. Diese hohe spezifische Oberfläche von ATP-CG-Mikrosphären wird hauptsächlich der geringen Kristallinität zugeschrieben [31]. Aus 11b zeigen ATP-CG-Mikrokügelchen eine geringere Kristallinität als die von ATP-CL-Mikrokügelchen. Darüber hinaus ist der Kristallinitätsunterschied zwischen ATP-CG und ATP-CL hauptsächlich auf die unterschiedlichen Synthesebedingungen zurückzuführen. Im Allgemeinen nimmt die Produktkristallinität mit dem Hydrolyseausmaß der Reaktanten unter bestimmten Drücken und Temperaturen zu. Hier ist die Acidität von Gluconsäure (pKa =3,39) höher als die von 1-Milchsäure (pKa =3,86), was zu einer langsameren Hydrolysegeschwindigkeit und letztendlich zu einer geringeren Kristallinität führen würde. Als Ergebnis werden ATP-CG-Mikrokügelchen mit einer höheren spezifischen Oberfläche durch Wechseln der Kalziumquelle erhalten.
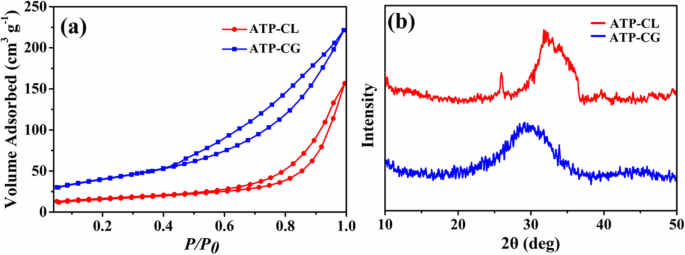
a Stickstoffadsorptions-Desorptions-Isothermen. b XRD-Muster von Mikrokügelchen
Schlussfolgerungen
Die ATP-CG-Dotterschalen-Mikrokügelchen wurden unter Verwendung von ATP als organische Phosphorquelle und CG als organische Calciumquelle durch ein mikrowellenunterstütztes hydrothermales Verfahren entwickelt. Die Mikrosphären weisen eine hohe spezifische Oberfläche und ein hohes Adsorptionsvermögen auf. Der Einfluss von Ca/P, hydrothermaler Temperatur und Zeit auf die Morphologie und Struktur von Mikrokügelchen wurde ebenfalls untersucht. Die Studie zeigt, dass eine organische Phosphorquelle und eine organische Calciumquelle einen signifikanten Einfluss auf die Bildung von Mikrokügelchen mit Dotterschalenstruktur haben. Darüber hinaus sind die hydrothermalen Bedingungen einschließlich Ca/P, Hydrothermal und Temperatur für die Bildung von Dotterschalen-Mikrokügelchen verantwortlich. Darüber hinaus stellen wir fest, dass die spezifische Oberfläche und die chemischen Oberflächeneigenschaften wie das Oberflächenpotential zwei Schlüsselfaktoren sind, die die Adsorptionskapazität von Mikrokügelchen beeinflussen, indem wir das HEL-Adsorptionsverhalten von zwei Arten von Mikrokügelchen vergleichen, die mit unterschiedlichen Calciumquellen synthetisiert wurden.
Verfügbarkeit von Daten und Materialien
Alle Daten, die die Schlussfolgerungen dieses Artikels unterstützen, sind im Artikel enthalten.
Abkürzungen
- WET:
-
Brunauer-Emmet-Teller-Messungen
- FTIR:
-
Fourier-Transformations-Infrarotspektroskopie
- TEM:
-
Transmissionselektronenmikroskopie
- XRD:
-
Röntgenbeugung
- TGA:
-
Thermogravimetrie-Analyse
- HRTEM:
-
Hochauflösendes TEM
- SAED:
-
Elektronenbeugung in ausgewählten Bereichen
Nanomaterialien
- Herstellung von ICA-beladenen mPEG-ICA-Nanopartikeln und ihre Anwendung bei der Behandlung von LPS-induzierter H9c2-Zellschädigung
- Ultraschmalbandiger perfekter Absorber und seine Anwendung als plasmonischer Sensor im sichtbaren Bereich
- Einfache Synthese von farbigen und leitfähigen CuSCN-Kompositen, die mit CuS-Nanopartikeln beschichtet sind
- Die Wirkung von Kontakt-Nichtgleichgewichtsplasma auf die strukturellen und magnetischen Eigenschaften von Mn Х Fe3 − X О4 Spinellen
- Auswirkung einer In-situ-Annealing-Behandlung auf die Mobilität und Morphologie von TIPS-Pentacen-basierten organischen Feldeffekttransistoren
- Abstimmung der Oberflächenmorphologien und -eigenschaften von ZnO-Filmen durch das Design der Grenzflächenschicht
- Abstimmung der tribologischen Leistung von geschichteten Zirkoniumphosphat-Nanoplättchen in Öl durch Oberflächen- und Zwischenschichtmodifikationen
- Synthese von ZnO-Nanokristallen und Anwendung in invertierten Polymersolarzellen
- Laser- und Transporteigenschaften von Poly[(9,9-dioctyl-2,7-divinylenfluorenylen)-alt-co-(2-methoxy- 5-(2-Ethylhexyloxy)-1,4-phenylen)] (POFP) für die Anwendung diodengepumpter organischer Festkörpe…
- Die Kopplungseffekte von Oberflächenplasmonpolaritonen und magnetischen Dipolresonanzen in Metamaterialien



