Wirkung von Alkalien auf den Eisenherstellungsprozess in einem Hochofen
Einfluss von Alkalien auf den Eisenherstellungsprozess in einem Hochofen
Eines der Hauptziele beim Betrieb eines Hochofens (BF) ist die Maximierung der Produktion von Roheisen (HM) der gewünschten chemischen Zusammensetzung bei minimalen Kosten. Voraussetzung dafür ist eine qualitativ hochwertige Rohstoffbasis und ein regelmäßiger, reibungsloser Betrieb des Hochofens. Die Qualität der Beschickungsmaterialien ist sehr wichtig, um Probleme im Prozess zu vermeiden, die durch unerwünschte Elemente verursacht werden, die in den Ofen gelangen. Auf diesem Gebiet muss auch auf den Gehalt an unerwünschten Elementen in der Eingangsladung geachtet werden. Diese unerwünschten Elemente verursachen eine Reihe von technologischen Problemen im BF. Außerdem beeinflussen sie die Produktionskosten des HM erheblich. Die wichtigsten unerwünschten Elemente in der Charge, die hinsichtlich der Entfernung und der Leistung des BF störend sein können, sind die Alkaliverbindungen der Metalle Kalium (K) und Natrium (Na).
Beim BF-Prozess ist bekannt, dass das Vorhandensein von Alkalien negative Einflüsse auf den Prozess hat. Alkalien verursachen eine höhere Reaktivität des Kokses, ein vorzeitiges Erweichen der Erzcharge, eine Zersetzung des Sinters, ein Aufquellen der Pellets und sind an der Bildung von Ablagerungen auf der feuerfesten Auskleidung des BF beteiligt, die den Verschleiß der Auskleidung beschleunigen. Die negativen Wirkungen von Alkalien beruhen auf der katalytischen Wirkung auf die Koksvergasung, der Zerstörung der Kohlenstoff(C)-Struktur durch das Einbringen von Alkali, Gerüstbildung und feuerfestem Angriff. Alkalien werden mit den Rohstoffen eingebracht und durch die Alkalizirkulation (Abb. 1) werden Alkalien auf dem Weg in die höhere Temperaturzone im BF aufgenommen.
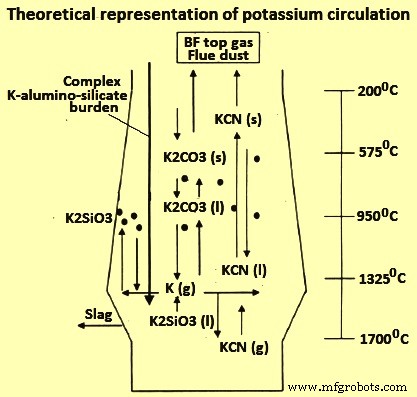
Abb. 1 Theoretische Darstellung der K-Zirkulation
Das Vorhandensein von Alkali führt zu einer geringeren Produktion und einem höheren Koksverbrauch in der BF, etwa 4,5 % bzw. 2,3 % für jedes kg/tSM Alkali, das mit der oberen Beschickung des Rohmaterials zugesetzt wird. Alkali verringert die Produktion aufgrund der Absenkung der Schwelle für die reversible Boudouard-Reaktion, C (s) + CO2 (g) =2 CO (g), erhöhtem Kokereigas und verringerter Stärke des Kokses. Die Gasdurchlässigkeit wird aufgrund des Koksabbaus verringert und es kann zu einer Gerüstbildung an den Wänden kommen, wodurch das Volumen des BF verringert wird.
Alkalireaktionen im BF
Bei allen in diesem Artikel angegebenen Alkalireaktionen kann K durch Na ersetzt werden. Die Reduktion von Alkalisilikaten durch C kann nach den reversiblen Reaktionen K2SiO3 (Schlacke) + C (s) =2K (g) + SiO2 (Schlacke) + CO (g) und K2SiO3 (Schlacke) + 3C (s) erfolgen. =2 K (g) + Si (HM) + 3 CO (g). Das Ausmaß dieser stattfindenden Reaktionen hängt von der Temperatur und dem Partialdruck von CO (Kohlenmonoxid) ab. Alkalioxide können entweder durch C im Koks oder durch das CO gemäß den reversiblen Reaktionen K2O + C (s) =2 K (g) + CO (g) und K2O + CO (g) =2 K (g) reduziert werden ) + CO2 (g).
Alkalien werden als Elemente verflüchtigt oder reagieren mit C und N2 (Stickstoff) in der Bosh-Region des BF und bilden Dämpfe von Kaliumcyanid (KCN) oder Natriumcyanid (NaCN) gemäß der reversiblen Reaktion 2K (g) + N2 (g) =2KCN (g). Die Brüden werden mit dem Ofengas hochgetragen und lösen sich nicht im HM oder in der Schlacke auf. Der Schmelzpunkt und der Siedepunkt für K betragen 63,4 °C bzw. 759 °C, während die entsprechenden Schmelz- und Siedetemperaturen für Na 97,7 °C bzw. 883 °C betragen. Die Schmelzpunkte von KCN und NaCN betragen 622 °C bzw. 562 °C, und die Siedepunkte betragen 1625 °C bzw. 1530 °C. Der Zustand dieser Verbindungen ist je nach Temperatur im unteren Schacht flüssig und im Laufbahn- und Herdbereich gasförmig. Das Gas wird von den sich schnell bewegenden Gasen im BF nach oben getragen.
Im Schacht, wo das Sauerstoffpotential (O2) ansteigt (bei etwa 1100 °C), sind K und KCN nicht mehr stabil und werden durch das Kohlendioxid (CO2) zu Alkalicarbonaten (K2CO3, Na2CO3) gemäß den Reaktionen 2K ( g) + 2CO2 (g) =K2CO3 + CO (g) und 2KCN (g) + 4CO2 (g) =K2CO3 (s) + N2 (g) + 5CO (g) bzw. und Alkalioxide durch das CO gemäß der reversible Reaktion 2KCN (g) + CO (g) =K2O + 3C + N2 (g). Die entstehenden Alkalicarbonate gehen in Form von weißem Feinanteil aus, der sich auf der Oberfläche des Möllers verteilt oder sich auf der Ausmauerung befindet.
An das Möllermaterial adsorbierte Alkalikomponenten und Koks bilden entsprechend ihrer relativen Stabilität neue Verbindungen. Kaliumcarbonat (K2CO3) und Natriumcarbonat (Na2CO3) sind bei Temperaturen unter 891 °C bzw. unter 851 °C fest. Die alkalihaltigen Verbindungen sinken mit den Beschickungsmaterialien ab und werden reduziert und wieder verdampft, wobei sie die Hochtemperaturzone erreichen, entsprechend der umkehrbaren Reaktion K2CO3(l) + 2C =2K (g) =3CO (g).
Der Großteil des Alkalis wird mit der Schlacke aus dem BF abgeführt. Ein Teil des Alkalis in der Schlacke wird jedoch reduziert, wobei Alkalidampf entsteht, der mit dem umgebenden Gas aufsteigt. Der Alkalidampf kondensiert im oberen Teil des BF, wo ein Teil mit dem Topgas austritt, während der Rest an den Innenwänden oder am Einsatzmaterial kondensiert. Aufgrund der Verflüchtigung und Kondensation des Alkalis in den verschiedenen thermischen Zonen neigt Alkali dazu, innerhalb des BF zu zirkulieren, was zu einer Akkumulation und Wechselwirkungen mit anderen Beschickungsmaterialien führt. Dies kann erhebliche Auswirkungen auf den Prozess haben, selbst wenn das Alkali in kleinen Mengen zugegeben wird, im Allgemeinen weniger als 5 Kilogramm pro Tonne Roheisen (kg/tSM). Eine vereinfachte Ansicht der Alkalizirkulation im BF ist in Abb. 2 dargestellt. Untersuchungen an ausgegrabenen BFs haben gezeigt, dass der Alkaligehalt dort am höchsten ist, wo die Temperatur über 1000 °C liegt, was bedeutet, dass im unteren Teil eine erhöhte Alkalikonzentration vorliegt der BF.
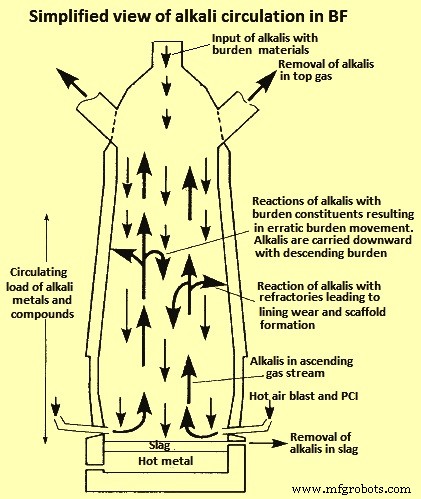
Abb. 2 Eine vereinfachte Ansicht der Alkalizirkulation im BF
Alkalikreislauf im BF
Alkalien gelangen normalerweise mit dem Eisenmaterial und mit dem Koks in Form von Silikaten in den BF. Für einen reibungslosen und effizienten BF-Betrieb ist es wünschenswert, die Alkalimenge auf etwa 1,5 kg/tSM bis 5 kg/tSM zu begrenzen, aber normalerweise liegt sie in verschiedenen Anlagen zwischen 2,5 kg/tSM und 7,5 kg/tSM. Von den beiden Alkalisubstanzen Na und K ist K normalerweise die Hauptverbindung, die in den BF eintritt. Die meisten Alkalien gehen mit der Schlacke aus, während einige Teil des Gichtgases werden und den Ofen mit dem Gichtgas verlassen. Rezirkulierendes Alkali kann entweder durch die Schlacke oder durch das Gas entfernt werden. K geht in höherem Maße in das Topgas über, da es flüchtiger ist als Na, das mehr mit der Schlacke austritt.
Alkalien gelangen in Form von Silikaten (K2SiO3) in den BF. Untersuchungen des Alkalikreislaufs haben gezeigt, dass die Silikate mit der Möllung absinken und der Kreislauf beginnt damit, dass das Alkalisilikat um das C des Kokses in der Schmelzzone gemäß der Gleichung K2SiO3 + C (s) =2 K (g) + reduziert wird SiO2 + CO (g). Die Reaktionen finden gemäß den thermodynamischen Daten für die Reaktionen bei etwa 1550 °C statt. Eventuell in den BF eingetragene oder gebildete Alkalioxide reagieren weiter oben im BF bei niedrigeren Temperaturen gemäß der Gleichung K2O + CO (g) =2K (g) + CO2 (g), da sie nicht stabil sind. K2O kann sich auch in der Primärschlacke auflösen.
Weiterhin reagieren die auf der Herdebene im BF erzeugten K-Dämpfe mit dem eingeblasenen Kohlenstaub und dem N2 des Heißluftstoßes gemäß der Gleichung 2K (g) + 2C (s) + N2 (g) =2KCN (g , l). Der Siedepunkt von KCN liegt bei 1625 °C, sodass sich das Kaliumcyanid (KCN), wenn es vom heißen Luftstrom aus den Blasdüsen weg aufsteigt, bei fallender Temperatur in eine flüssige Phase umwandelt. Die Zeit in der Blasdüsenzone ist aufgrund des hohen Gasflusses sehr kurz, so dass die Alkalicyanide Zeit haben, den BF nach oben zu bewegen, bevor sie sich in die flüssige Phase umwandeln. Weiter oben im BF reagieren die Alkalicyanide mit CO2 (Kohlendioxid) zu stabileren Carbonaten bei Temperaturen unter 1100 °C gemäß der Gleichung 2KCN (l) + 4CO2 (g) =K2CO3 + N2 (g) + 5CO ( g). Die Karbonate folgen entweder dem Topgas als Gas oder lagern sich auf der Möller ab, wenn sie unterhalb von 900 °C zu kondensieren beginnen.
Im Vergleich zu Alkalisilikaten sind Alkalicyanide instabil, so dass jegliches SiO2, das im Herdteil des BF vorhanden ist, mit den Alkalicyaniden reagieren kann, um wieder Alkalisilikate zu bilden. Als Alkalikreislauf wird der Prozess der Reduktion von Alkalisilikaten zu Alkalidämpfen bezeichnet, die im BF aufsteigen, mit dem Gichtgas austreten oder mit CO2 zu Carbonaten reagieren. Es gibt einige unterschiedliche Ansichten, die den Prozess leicht unterschiedlich zusammenfassen, indem sie sich darin unterscheiden, welche Reaktionen genau stattfinden. Es ist zweifelhaft, ob am oberen Rand des BF überhaupt Karbonate gebildet werden, da beim Abbau von BFs keine Karbonate gefunden werden. Über den Hauptprozess, dass Alkalicyanide entstehen und das Alkali im BF zirkuliert, herrscht jedoch Einigkeit in allen Ansichten.
Abb. 3 zeigt die Zirkulation von Alkalien im BF. Das geladene Material sinkt in die Hochtemperaturzone ab, bevor Alkalisilikate entweder zu Alkalidämpfen zerfallen oder von der primären Schlackenphase in Form von K2O oder Na2O absorbiert werden. Der Zyklus gibt auch an, wann der Alkalidampf mit Silikaten reagiert, um wieder Silikate zu bilden. Die Verteilung der Alkalidämpfe durch den BF hängt von den Gasströmungswegen und dem Ausmaß der zentralen Gasströmung ab. Gasströme haben einen großen Einfluss darauf, wie Wärme in einem BF verteilt wird. Zentralerer Fluss bedeutet mehr Schmelzen in der Mitte und weniger in der Peripherie des BF.
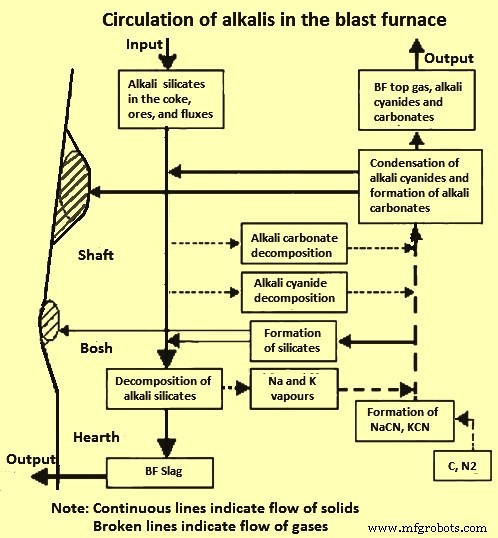
Abb. 3 Zirkulation von Alkalien im BF
Bildung von Ammoniak und Blausäure im BF
Es wird angenommen, dass Ammoniak (NH3) im BF gebildet wird. Grundreaktionen hinter der Bildung von NH3 und Cyanwasserstoff (HCN) im BF sind 2KCN + 3H2O =K2CO3 + 2NH3 + C und NH3 + CO =HCN + H2O. Das Verhältnis zwischen diesen Reaktionen hängt von mehreren Parametern ab, wie (i) der Menge an verfügbarer Feuchtigkeit, (ii) der Menge an verfügbarem KCN oben und (ii) der Temperatur während der Reaktionen. Die Temperaturschwelle für NH3 liegt bei etwa 600 °C und die NH3-Bildung nimmt kontinuierlich exponentiell bis 500 °C ab und wird danach nicht mehr erfasst. Weiterhin gebildetes NH3 wird entweder durch Fe2O3 oder CO2 oxidiert und die gebildete NH3-Menge nimmt ab. Die Oxidation von NH3 durch Fe2O3 oder MnO2 ist temperaturabhängig. Bei niedriger Temperatur ist MnO2 ein stärkeres Oxidationsmittel und bei höherer Temperatur ist Fe2O3 das stärkere Oxidationsmittel.
Da HCN und NH3 im Gichtgas zu finden sind, ist die Oxidationskinetik für NH3 nicht schnell genug, um es vollständig zu entfernen. Der höhere Wassergehalt im Topgas bedeutet, dass mehr NH3 gebildet wird, was gemäß der obigen Reaktion stattfinden kann. Die Bildung von NH3 im BF ist komplex, da mehrere Parameter, wie unten angegeben, seine Bildung beeinflussen.
Obere Gastemperatur – Die Topgastemperatur hängt vom Verhältnis zwischen endothermen / exothermen Reaktionen im BF ab. Die Temperatur beeinflusst den Feuchtigkeitsgehalt. Eine niedrigere Temperatur kann auch zu einer erhöhten Löslichkeit von NH3 in Wasser führen und HCN ist mit Wasser mischbar, sodass die Anwesenheit von Wasser seine Anwesenheit im Topgas verringern kann.
Flammentemperatur – Die Flammentemperatur hat einen geringen Einfluss auf die Menge des erzeugten Alkalidampfes und die Gesamtalkalibelastung. Eine hohe Temperatur ist erforderlich, um die Alkalisilikate zu Alkaligas zu reduzieren, das die Alkalizirkulation startet. Eine niedrigere Flammentemperatur führt daher dazu, dass mehr Alkali den BF durch die Schlacke verlässt.
Basizität – Eine niedrigere Basizität führt zu einer höheren Alkaliaufnahme in die Schlacke, daher gibt es weniger zirkulierendes Alkali im BF und es wird weniger NH3 produziert.
Feuchtigkeitsgehalt – Weniger Feuchtigkeit, die mit der Ladung oder auf andere Weise in den BF eingebracht wird, ergibt weniger Wasser für die NH3-Bildungsreaktion.
Einfluss von Alkali und Entfernung
Die Alkalikonzentration im Rohmaterial hat in den letzten Jahren aufgrund der geringeren Verfügbarkeit von hochwertiger Kokskohle zugenommen. Alkali ist für den BF-Betrieb schädlich, da es aufgrund der katalytischen Wirkung auf die Lösungsverlustreaktion (Boudouard-Reaktion) eine erhöhte Reaktivität von Koks verursacht.
Einer der größten negativen Effekte des Alkalis ist, dass es die reversible Boudouard-Reaktion katalysiert, indem es die Temperatur für die Reaktion von 900 °C auf 950 °C auf etwa 750 °C bis 850 °C senkt und die Koksreaktivität je nach Temperatur erhöht Koks Qualität. Es wirkt sich auch negativ auf die Koksstruktur aus. Die niedrigere Schwelle für die Boudouard-Reaktion bedeutet, dass mehr C in einer stark endothermen Reaktion im BF verbraucht wird. Daher ist eine Erhöhung der Kokszugabe in den BF erforderlich, um einen stabilen Betrieb mit 2 kg bis 10 kg Koks pro kg Alkali oder mit 6 kg bis 11 kg Koks je nach verwendeten Quellen aufrechtzuerhalten.
Alkali, das in die Koksstruktur eingedrungen ist, verringert die Koksfestigkeit im unteren Teil des BF aufgrund der erhöhten Reaktivität des Koks und somit des erhöhten Abbaus. Es hat sich gezeigt, dass die scheinbare Reaktionsgeschwindigkeit des Kokses auf der Höhe der Düse zehnmal so hoch ist wie die Reaktionsgeschwindigkeit des Beschickungskokses, was mit der Gesamtmenge an vorhandenem K zusammenhängt. Es ist bekannt, dass K die Reaktivität von Koks mit CO2 erhöht und resultieren kann beim Koksbruch durch Quellung der Kokskörner durch Einlagerung von K. Eine Erhöhung der Reaktivität kann vorteilhaft sein, da sie die BF-Betriebstemperatur, die Temperatur in der thermischen Reservezone und damit die Temperatur zur Reduktion von Eisenoxid senkt. Der Zweck von Koks besteht jedoch auch darin, als Beschickungsträger innerhalb des Ofens zu fungieren, und daher muss der Koksbruch minimiert werden.
Studien zum Eindringen von K-Dampf in Koks haben bestätigt, dass die Struktur von Koksmineralien aufgrund der Volumenausdehnung von alkalisierten Mineralien, insbesondere Kalsilit, aufgebrochen werden kann. Die Oberfläche zwischen den Mineralien und der C-Matrix vergrößert sich aufgrund des Bruchs der Mineralien im Koks. Dies erleichtert die Wechselwirkung von Mineralstoffen mit C- und BF-Gasen, was die Koksvergasung beschleunigt. Eine Expansion in Koks kann auch auftreten, wenn Alkalidämpfe in die Kristallschichten von Koks eindringen und Zwischenschichtverbindungen bilden. Die Koksstärke und -unterstützung des Möllers während des BF-Betriebs ist kritisch, da ein Zusammenbruch des Möllers die Gas- und Flüssigkeitsdurchlässigkeit verringert, was die Effizienz sowohl hinsichtlich der HM-Produktion als auch der erhöhten CO2-Emissionen verringert.
Kleine Kokspartikel unterschiedlicher Größe verkleinern die Hohlräume im Koksbett in der Nasszone und die Koksoberfläche vergrößert sich. Das Brechen von Koks fördert auch ein Überfluten, ein Verstopfen des Herds und ein erhöhtes Abbrennen von Blasdüsen und Schlackenkerben, die alle die Ofenleistung begrenzen. Die Neigung des aufsteigenden Gases, in die Nähe der Wände transportiert zu werden, nimmt zu, wenn die Permeabilität verringert wird, was die Ausnutzung des Gases verringert und somit die Koksrate erhöht.
Ein weiterer Effekt von Alkali ist die erhöhte Wahrscheinlichkeit einer Gerüstbildung im Schacht, da Alkali auf der Auskleidung kondensiert und das feine Material daran binden kann. Gerüste sind ein Aufbau aus festem Material an der Ofenwand und ragen in Richtung Ofenmitte. Gerüste können an jeder Stelle von der Mitte bis zum oberen Teil des Schachts auftreten. Die Gerüstbildung bewirkt, dass der Abstieg der Last verlangsamt oder unterbrochen wird und im Extremfall zum Hängen, Rutschen und unkontrollierten Aufladen führt. Die Gerüste reduzieren auch das Arbeitsvolumen des BF. Die Gasgeschwindigkeit wird in den nicht betroffenen Teilen im Schacht erhöht, was zu einer erhöhten Gichtgastemperatur und einer verringerten Ausnutzung des CO führt. Wenn sich die Gerüste von der Ofenwand lösen, entsteht häufig ein gekühlter Herd. Die Gerüste können durch vorübergehendes Erhöhen der Ofentemperatur entfernt werden oder werden entfernt, wenn ein Gasstrom mit hoher Temperatur den Bereich erreicht.
Das Möllermaterial kann auch durch kondensierte flüssige Cyanide und Karbonate verklebt werden, was die Bettdurchlässigkeit verringert. Darüber hinaus kann Alkali das feuerfeste Material angreifen, insbesondere feuerfeste Materialien auf C-Basis, die normalerweise im unteren Teil des Ofens verwendet werden. Alkaliverbindungen dringen in die C-Blöcke ein, die unter Bildung von Alkalidampf verbraucht werden. Dies führt zu einer kürzeren Lebensdauer der feuerfesten Auskleidung und zu einer häufigeren Neuauskleidung.
Die Entfernung von Alkali erfolgt hauptsächlich mit der Schlacke und wird am besten bei niedrigeren Basizitätswerten durchgeführt. Von dem entfernten Alkali werden über 90 % durch die Schlacke entfernt. Hier wird die Basizität als CaO/SiO2 betrachtet. Ergebnisse mehrerer Studien haben gezeigt, dass die niedrigere Basizität der Schlacke die Menge an Alkali in der Schlacke erhöht. Das Problem bei einer zu niedrigen Basizität besteht jedoch darin, dass ein höherer Gehalt an Schwefel (S) im HM verbleibt, da dem S durch in der BF-Schlacke vorhandenes CaO entgegengewirkt werden kann und CaO niedriger ist, wenn die Basizität niedriger ist. Die untere Grenze der Basizität, um die HM-Qualität unter Kontrolle zu halten, ist von Anlage zu Anlage unterschiedlich. Die Grenze ist abhängig von den BF-Parametern und der Qualität des verwendeten Rohmaterials. Ein Basizitätswert knapp über oder um 1 kann als Grenze angesehen werden, wenn Alkali entfernt werden soll und die HM-Qualität erhalten bleiben soll.
Um die Vergasung von Alkalisilikaten zu verhindern, muss der CO-Partialdruck hoch gehalten werden. Die hohe Temperatur für die Reaktion von 1550 °C bedeutet, dass auch eine niedrigere Flammentemperatur verwendet werden kann, um die Reduktion und Vergasung zu verlangsamen und somit die Alkalizirkulation zu verringern. Die Entfernung von Alkali erfordert eine verringerte Rezirkulation von alkalihaltigen Materialien zum BF, da Alkali sonst nur wieder in den BF eingeführt wird.
Eine Absenkung der katalysierenden Wirkung von Alkali auf die Koksvergasung kann durch Zusätze von Koksasche erfolgen, die das vorhandene Alkali in stabilerer Form binden kann. Es wurde zuvor mit bestimmten Mineralzusätzen versucht. Wenn Alkali durch den Koks diffundiert, kann eine Beschichtung mit Mineralienzusatz das Alkali an der Oberfläche des Kokses stabilisieren und es daran hindern, die inneren Teile des Kokses zu zersetzen.
Kontrolle der Alkalibelastung
Zur Steuerung der Alkalibelastung im BF ist der Alkalieintrag möglichst gering zu halten. Bei Schwankungen im Eingangsmaterial muss die Erzmischung gut gemischt werden, um das Risiko von Abschnitten mit hohem Alkaligehalt im BF zu minimieren. Eine weitere Vorsichtsmaßnahme besteht darin, die Rückführung von Flugstaub mit hohem Alkaligehalt zu vermeiden. Eine Möglichkeit, das Risiko der Gerüstbildung zu minimieren, besteht darin, die Festigkeit der Eisenbeschickung und des Kokses zu erhöhen, um die Bildung von Feinanteilen zu vermeiden.
Der BF kann mit zentraler Gasführung betrieben werden. Dadurch wird die Gichtgastemperatur im Zentrum so weit erhöht, dass ein Teil des Alkalis mit dem Gichtgas den Ofen als Dampf verlässt. Höhere Topgastemperaturen führen jedoch zu erhöhten Wärmeverlusten.
Das rezirkulierte Alkali kann verringert werden und stattdessen den BF über die Schlacke verlassen, indem der BF mit einer sauren Schlacke betrieben wird. Je niedriger die Basizität der Schlacke ist, desto leichter werden das basische K und Na in die Schlacke absorbiert, da Kalk (CaO) und Magnesia (MgO) die gleichen Stellen im Kieselsäurenetzwerk einnehmen wie Alkalioxide. Eine verringerte Basizität kann erreicht werden, indem die Basizität in der Eisenbeschickung und den Flussmittelzusätzen verringert wird. Eine geringere Basizität führt jedoch auch zu einem erhöhten Gehalt an S (Schwefel) im HM, da S in der Schlacke an Ca bindet.
Eine andere Möglichkeit, die Alkalibelastung zu verringern, besteht darin, das Schlackenvolumen zu erhöhen, was die Aktivität von Alkalioxiden in der Schlacke verringert und somit die Alkaliaufnahme und den Austrag durch die Schlacke erhöht, aber ein erhöhtes Schlackenvolumen erhöht auch die Koksrate. P>
Eine niedrigere Temperatur im BF führt zu einer verringerten Reduktion und Verdampfung von Alkali. Das Betreiben des BF mit niedrigerer Flammentemperatur führt zu einer verringerten Alkalibelastung, aber auch zu einer verringerten Produktivität und einer höheren Koksrate. Die Alkalibelastung kann auch verringert werden, indem der BF mit einem hohen CO-Partialdruck betrieben wird, da dies der Alkalivergasungsreaktion entgegenwirkt. Dies kann durch O2-Anreicherung des Strahls oder hohen Kopfdruck erreicht werden.
Herstellungsprozess
- Prozessautomatisierungs-, Mess- und Steuerungssystem für Hochöfen
- Verwendung von Nusskoks in einem Hochofen
- HIsmelt-Prozess der Eisenherstellung
- HIsarna-Prozess für die Eisenherstellung
- Hochofen Unregelmäßigkeiten während des Betriebs
- Kühlsystem für Hochöfen
- Chemie der Eisenherstellung im Hochofenverfahren
- Feuerfeste Auskleidung des Hochofens
- Hochofen und sein Design
- Eisenerzeugung durch Hochöfen und Kohlendioxidemissionen



